胃癌是全球范围内最常见的恶性肿瘤之一,根治性手术虽是主要治疗手段,但围手术期的应激反应、缺血再灌注损伤及禁食往往导致肠道黏膜屏障功能受损,进而引发肠道菌群移位和全身炎症反应。近年来,免疫营养素在改善患者预后方面的潜力备受关注,但其对肠道屏障的具体保护机制,尤其是通过肠道菌群介导的作用机制尚不明确。近期,一项发表在Biomedicines上的随机对照研究通过宏基因组测序技术,深入揭示了围手术期补充免疫营养素通过重塑肠道微生态、富集有益菌群、抑制致病菌及毒力因子,从而减轻胃癌患者术后肠道屏障损伤的潜在机制。
研究背景
胃癌患者由于疾病消耗及消化道梗阻等原因,营养不良的发生率极高。围手术期的肠外与肠内营养支持已在临床广泛应用。与传统标准营养配方相比,免疫营养素(如精氨酸、ω-3多不饱和脂肪酸、核苷酸)被认为具有抗炎、免疫调节及肠道保护潜力。既往研究提示,免疫营养素可能通过抑制核因子-κB(NF-κB)通路减少促炎因子的释放。
然而,现有证据多集中于孤立的炎症指标或营养指数,缺乏对肠道菌群结构、功能通路及肠道屏障生物标志物的系统性评估。此外,关于围手术期免疫营养素的高质量RCT研究相对有限,这也限制了其在临床指南中的推荐级别。
因此,本研究旨在通过测定血清肠道屏障标志物(二胺氧化酶、D-乳酸、内毒素)及免疫炎症参数,结合粪便宏基因组测序分析,探讨围手术期免疫营养素对比标准营养支持在改善胃癌患者肠道黏膜屏障功能及调节肠道菌群方面的优效性及其微生态机制。
研究方法
2.1 研究设计与受试者
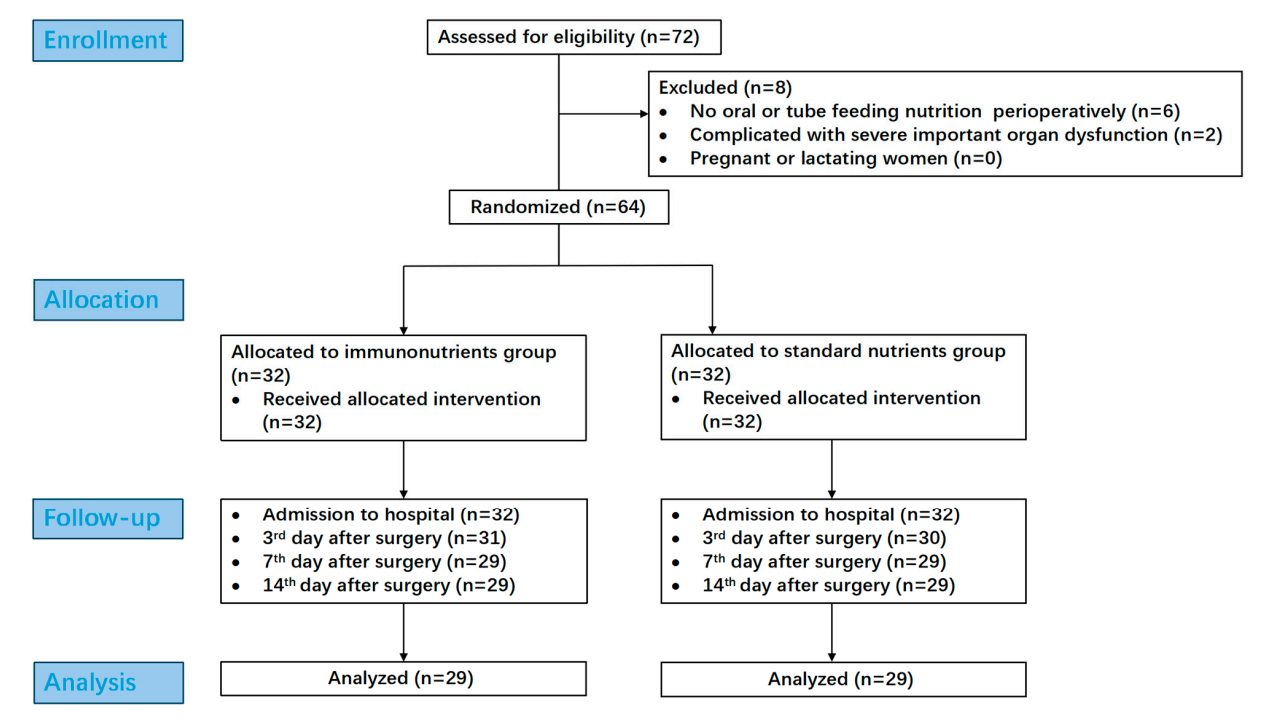
本研究为单中心、随机、平行对照临床试验。研究纳入了2023年6月至2024年12月期间在北京协和医院接受根治性胃切除术的58例胃癌患者。纳入标准包括年龄18-80岁、BMI 18.5-28 kg/m²。排除标准包括围手术期无法接受口服或管饲喂养、严重器官功能障碍、近期接受放化疗等。
2.2 分组与干预
患者被随机分为两组:免疫营养组(n=29):在标准营养基础上,每100千卡额外补充282 mg ω-3脂肪酸(EPA+DHA)、1.2 g精氨酸和128 mg核苷酸。标准营养组(n=29):接受等热量的标准营养配方。
干预方案涵盖术前3天至术后14天。术前3天每日口服补充20 kcal/kg/day;术后第3天起逐步恢复肠内营养,直至达到目标剂量并持续至术后第14天。
2.3 数据采集与检测
血液样本:于术前3天(基线)、术后第3、7、14天采集。检测指标包括免疫参数(WBC、淋巴细胞计数、CD3+/CD4+/CD8+ T细胞、IgG、hs-CRP)、营养参数(白蛋白、前白蛋白等)及肠道屏障标志物(二胺氧化酶DAO、D-乳酸、细菌内毒素)。
粪便样本:于术前3天及术后第14天采集。采用宏基因组测序技术(NovaSeq平台)分析菌群组成及功能通路。
研究结果
3.1 临床基线特征与术后恢复
两组患者在年龄、性别、BMI、TNM分期及手术相关参数方面基线平衡,无显著差异(P > 0.05)。术后并发症发生率在两组间无统计学差异(17.24% vs. 20.69%,P = 0.738)。
3.2 肠道屏障功能的改善
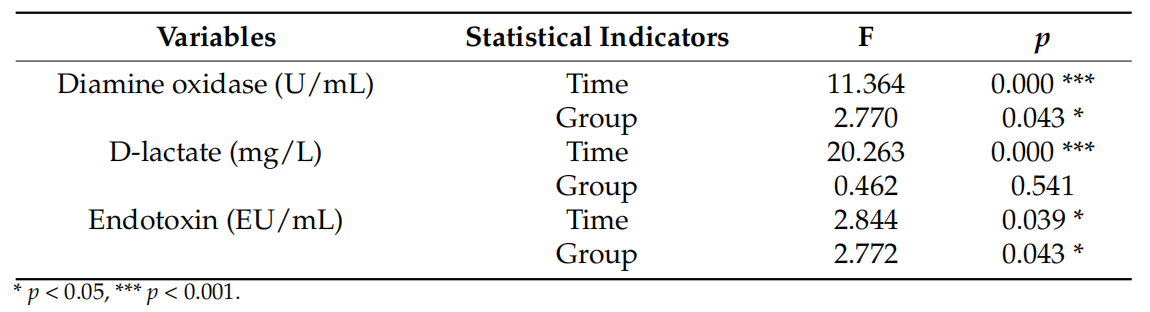
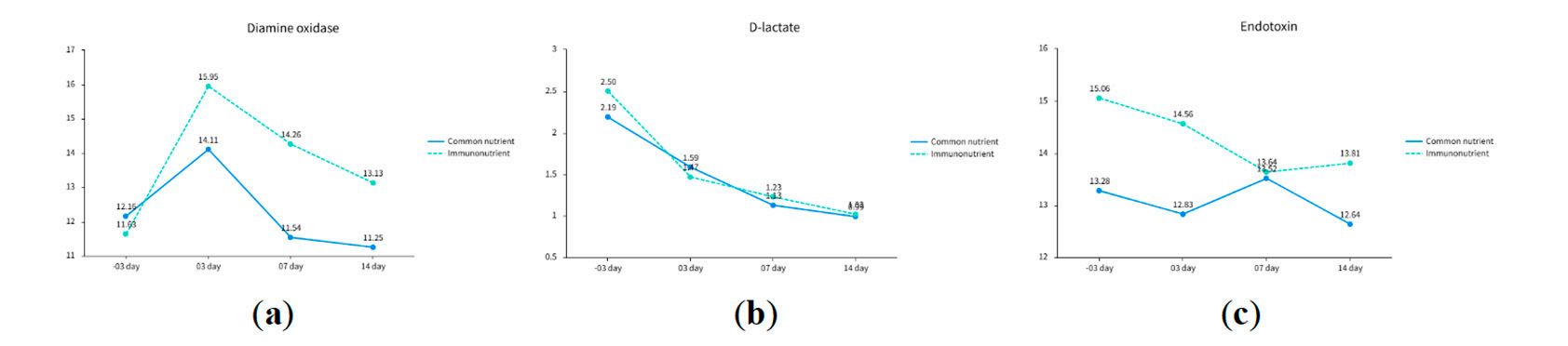
重复测量方差分析显示,免疫营养素对术后肠道屏障标志物具有显著的保护作用:
二胺氧化酶(DAO):免疫营养组术后DAO水平显著低于标准营养组(组间效应 F = 2.770, P = 0.043;时间效应 F = 11.364, P < 0.001)。DAO是反映肠黏膜完整性的关键指标,其水平降低提示黏膜损伤减轻。
细菌内毒素:免疫营养组术后内毒素水平显著更低(组间效应 F = 2.772, P = 0.043),表明免疫营养素有效减少了肠道细菌移位。
D-乳酸:虽表现出显著的时间效应(P < 0.001),但组间差异未达统计学显著性(P = 0.541)。
表1 两组间围手术期肠道屏障指标的比较及不同时点的差异分析
3.3 肠道菌群多样性的重塑
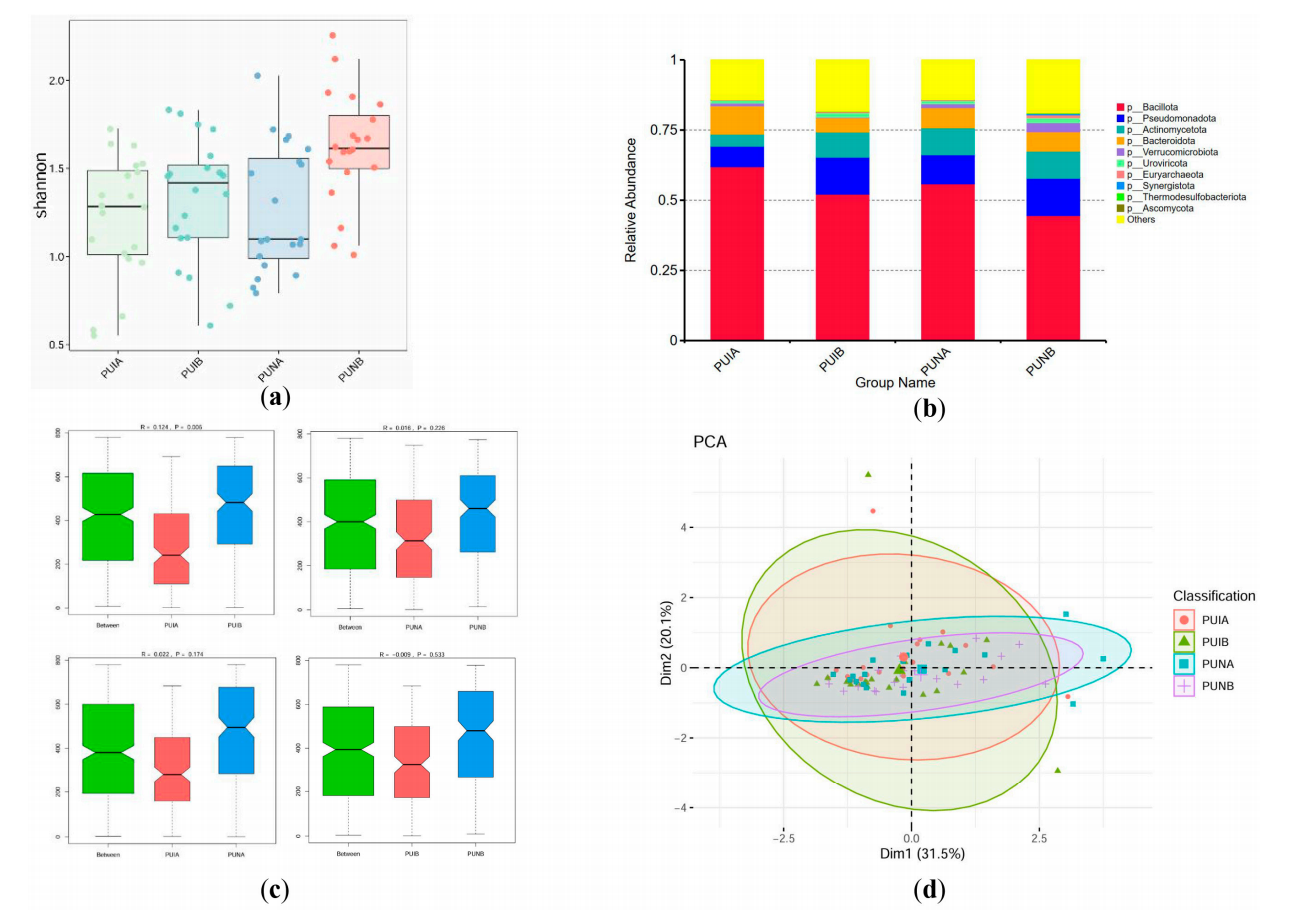
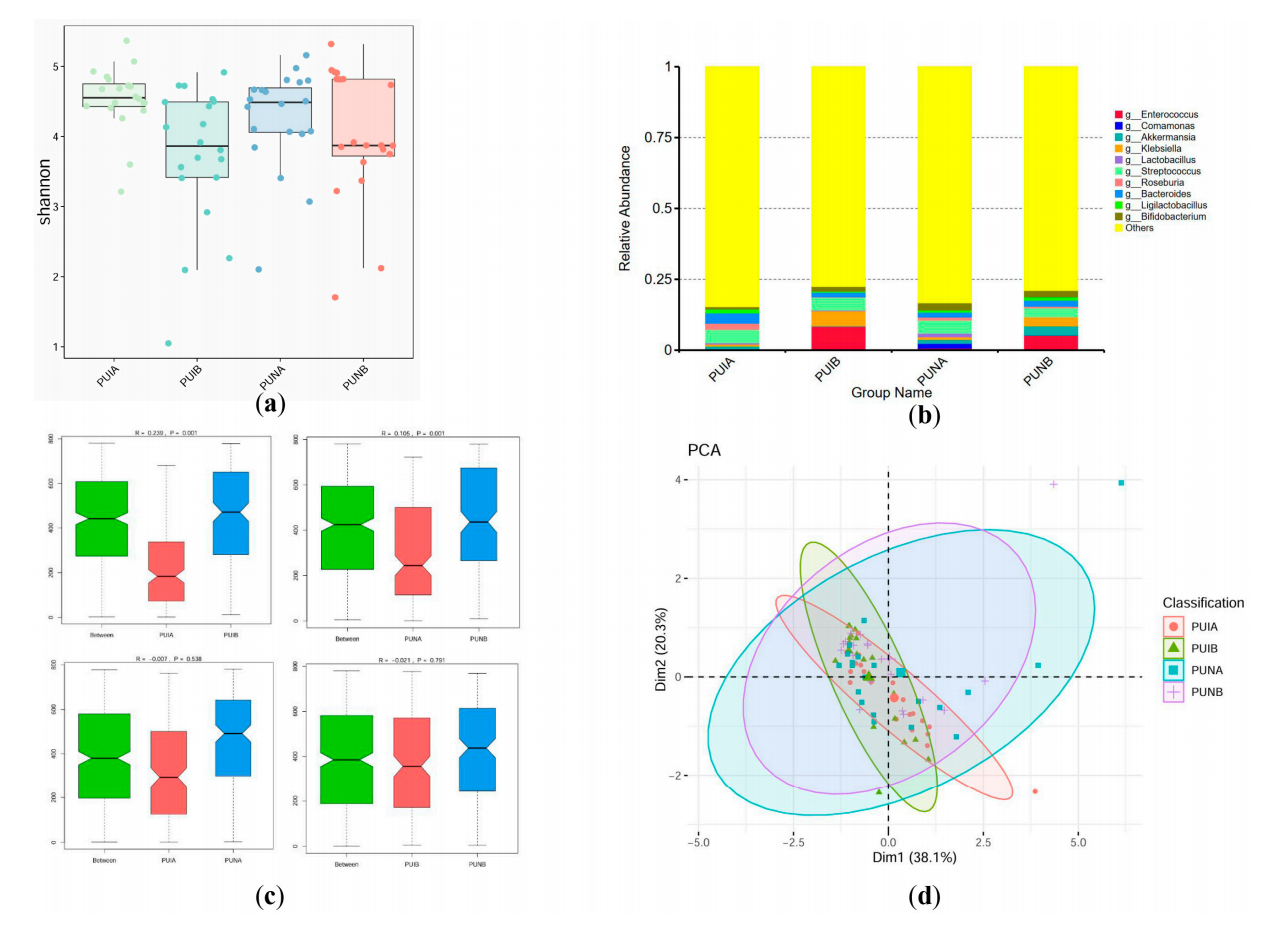
宏基因组测序结果显示,免疫营养素显著提升了术后肠道菌群的α-多样性:
Shannon指数:术后免疫营养组(PUNB)的Shannon指数显著高于术后标准营养组(PUIB),差异具有统计学意义(P = 0.0005)。
菌群结构稳定性:PCoA和ANOSIM分析(R = 0.124, P = 0.006)表明,标准营养组术后菌群结构发生了显著的病理性漂移,而免疫营养组的菌群结构与术前更为接近,提示其维持了微生态的稳定性。
3.4 关键菌属与物种的差异富集
LEfSe分析揭示了两组在属和种水平上的显著差异:
有益菌富集(免疫营养组):
嗜黏蛋白阿克曼氏菌:在免疫营养组中丰度高达3.26%,是标准营养组(0.23%)的近14倍。该菌通过降解黏蛋白刺激杯状细胞增殖,增厚黏液层,并可能通过AhR通路促进Treg分化,抑制过度炎症。
长双歧杆菌:丰度显著增加(2.31% vs 0.55%)。该菌可产生乙酸,降低肠道pH值,并分泌胞外多糖修复紧密连接蛋白(ZO-1)。
其他有益菌如Faecaliberium prausnitzii和Roseburia也显著富集,这些菌群与丁酸产生及抗炎功能密切相关。
致病菌抑制(免疫营养组):
标准营养组术后表现出机会性致病菌的显著增殖,包括粪肠球菌和产气克雷伯菌。
免疫营养组中,Enterococcus(5.27% vs 8.40%)和Klebsiella(3.17% vs 5.25%)的丰度均低于标准营养组,显示出对致病菌的抑制作用。
3.5 功能通路的改变
功能注释分析进一步证实了免疫营养素的代谢调节作用:
毒力因子:标准营养组富集了包括溶血素O(Streptolysin O, VF0353)和肠球菌表面蛋白Esp(VF0456)在内的毒力因子基因,这些因子促进细胞溶解和生物膜形成。
碳水化合物代谢:免疫营养组富集了与膳食纤维降解相关的糖苷水解酶家族(GH2, GH3),促进短链脂肪酸(SCFA)合成;而标准营养组则富集了降解宿主黏蛋白的酶系(GH1, GH4, GH73),这种“掠夺性”代谢可能加剧黏膜损伤。
结论
本研究通过严格的随机对照试验和宏基因组学分析,证实了围手术期补充含ω-3脂肪酸、精氨酸和核苷酸的免疫营养素对胃癌患者具有明确的临床获益。免疫营养素显著降低了术后二胺氧化酶和细菌内毒素水平(P < 0.05),客观反映了肠黏膜损伤的减轻和细菌移位的减少。同时,免疫营养素能够维持较高的菌群多样性(P = 0.0005),特异性富集Akkermansia和Bifidobacterium等下一代益生菌。其机制可能涉及促进有益菌发酵产生短链脂肪酸、增强黏液层屏障功能、抑制致病菌生长及其毒力因子表达,从而在“营养素-菌群-屏障”轴上发挥多重保护作用。
综上所述,免疫营养素可能通过调节肠道菌群多样性、富集有益分类群并抑制致病菌,从而减轻胃癌患者手术诱导的肠道屏障损伤。这一发现为围手术期免疫营养的应用提供了高质量的微生态学证据,支持在胃癌患者术后康复中推广这一营养支持策略。
Zheng Z, Liu G, Wang Y, et al. Perioperative Oral Immunonutrient Regulation of Intestinal Barrier and Gut Microbiota in Patients with Gastric Cancer, a Randomized Controlled Clinical Trial. Biomedicines. 2025;13(9):2163. Published 2025 Sep 5. doi:10.3390/biomedicines13092163
责任编辑:肿瘤资讯-Skye
排版编辑:肿瘤资讯-Vickey











 苏公网安备32059002004080号
苏公网安备32059002004080号


