全球范围内胃癌的发病率和死亡率都很高,中国胃癌疾病负担依然沉重[1]。中国超过 70% 的患者在确诊时已发展为局部进展期胃癌(LAGC),仅靠手术治疗对 LAGC 效果不佳,接受根治性 D2 手术的 LAGC 患者 5 年总生存率仍不足 50%。目前,胃癌新辅助治疗的最佳治疗方案、治疗时机、疗效评估及受益人群仍存在争议。胃癌患者易出现营养不良、代谢异常和免疫抑制,严重影响治疗效果和长期预后[2,3]。因此新辅助治疗过程中,精准有效的营养治疗是必不可少的一环。四川省肿瘤医院胃外科周达主治医师分享了一例局部晚期胃癌的诊疗过程,点评嘉宾为四川省肿瘤医院胃外科陈小东教授。该患者初诊时胃周合并巨大融合的肿大淋巴结(Bulky N),围术期在肿瘤特医食品全程营养支持下,通过化疗及免疫治疗联合,实现了术后病理完全缓解。
本期特邀点评专家——陈小东 教授
医学博士 主任医师
四川省肿瘤医院胃外科 支部书记 副主任(主持工作)
四川省肿瘤医院外科规培基地 教学主任
电子科技大学医学院 研究员 硕士生导师
国际胃癌学会(IGCA)会员
中国抗癌协会胃癌整合防筛专业委员会常务委员
本期特邀专家——周达 教授
医学博士 四川省肿瘤医院 胃外科 主治医师
以第一作者身份在 Redox Biology、Journal of cachexia sarcopenia and muscle等期刊上发表十余篇SCI论文
主持四川省肿瘤医院青年科学基金1项
四川省抗癌协会肿瘤营养专委会秘书
基本情况:
患者男性,66岁,ECOG PS评分0分。
主诉:
腹痛伴腹胀3月余。
现病史:
患者于3月前因饥饿出现上腹疼痛伴腹胀,进食后缓解,无呕吐腹泻,无胸闷气短,无头晕头痛。
患者于2024-06-26至当地医院行胃镜检查示:胃体上部小弯见巨大溃疡,污苔,质脆,易出血,侵及贲门口下缘及贲门部。术后病理报告示:(贲门)查见粘膜内腺癌。2024-07-02行CT检查示:胃底胃贲门区壁增厚,多系肿瘤性病变;胃底旁及肝胃间隙多发肿大淋巴结。2024-07-18当地医院会诊病理报告示:镜下见增生鳞状上皮及少量异型腺上皮;不排除腺上皮肿瘤形成。2024-07-30行CT示:胃底部、胃小弯前间隙见多发软组织密度肿块,大者大小约40mm*31mm。今为进一步治疗来我院就诊,门诊以"胃占位性病变"收入院。
查体:
身高:164cm 体重:59kg BMI:21.94kg/m² BSA DuBois:1.64m²。
实验室检查:
红细胞3.53*10^12/L,血红蛋白 88 g/L,CEA 5.48ng/ml,其余未见明显异常。
辅助检查:
2024-08-12 胸部CT增强^全腹CT增强:1.胃底、胃体小弯侧胃壁不均增厚(2.8cm),与邻近贲门分界不清,考虑胃癌可能,请结合临床及内镜检查。2.贲门左、胃小弯及肝胃间隙数个增大淋巴结(大者大小约4.6×3.1cm),多系转移,随诊。3.双肾囊肿。4.前列腺钙化。5.盆腔少量积液。部分腹膜稍厚。6.双肺少许炎性条索影。7.左侧第10、11后肋走行迂曲,考虑陈旧性骨折,请结合病史。
2024-08-12 上消化道内镜 :贲门-胃底-胃体巨大隆起型新生物,性质。
2024-08-13 消化系统病理 :贲门活检小组织:查见癌,腺癌待排,待免疫组化协助诊断。
分子标志物:
CerbB-2-Roche(1+)、MLH1(+)、MSH2(+)、MSH6(+)、PM S2(+)、EBER(原位杂交)(-)、Ki67(+,约80%)、Claudin18.2(1+:任何强 度百分比<40%或强度1+,任何百分比)、P40(-)、Syn(+),PD-L1 CPS=5。
腹腔镜检查:
2024-8-14 在全麻下行“腹腔镜下探查术”,术中发现“1、7组淋巴结肿大,约1-5cm大小”,术中留取腹腔冲洗液,术后病理示腹腔冲洗液查见较多淋巴细胞及间皮细胞,未见恶性细胞。
临床诊断
1.贲门腺癌(cT4aN1M0 Ⅲ期)1周期化疗及免疫治疗中 2.恶心和呕吐 3.低蛋白血症 4.重度营养不良伴消瘦 5.营养风险 6.疼痛 7.肝功能不全 8.缺铁性贫血 9.肾囊肿。
基线营养状况评估(2024年8月10日):NRS 2002评分为3分,存在营养风险。PG-SGA评分为9分,即合并重度营养不良。目前体重为59kg,BMI 21.94kg/m²,血红蛋白 88 g/L,白蛋白 33.7g/L。
治疗过程
经过科室MDT讨论,患者术前分期为cIII期,建议行新辅助治疗,同时行营养治疗,评估疗效后再行手术切除治疗。
新辅助治疗阶段
患者分别于2024年8月25日-2025年1月22日行6周期新辅助治疗,具体治疗方案:奥沙利铂 200mg ivgtt d1+ 卡培他滨 1500 mg po d1-14+替雷利珠单抗 200mg ivgtt d1/Q3W。
营养治疗方案
患者在新辅助化疗期间,根据MDT讨论中临床营养科的建议:使用富含精氨酸、n-3脂肪酸和核苷酸等免疫营养素的肿瘤特医食品速熠素,具体使用方法为小口慢饮,若无法耐受可适当温水稀释。待胃肠道逐渐耐受后,搭配日常饮食,作为口服营养补充增加至每日2瓶,能够额外增加710 kcal能量和43g蛋白质,满足病人日常能量和蛋白质需求。患者通过上述方式耐受后,每日口服2瓶肿瘤特医食品,持续口服至新辅助化疗结束时。
病灶及淋巴结变化
基线情况:2024-8-9全腹部CT提示胃底、胃体小弯侧胃壁不均增厚,病灶较厚处约2.8cm。贲门左、胃小弯及肝胃间隙数个增大淋巴结,大者大小约4.6×3.1cm。
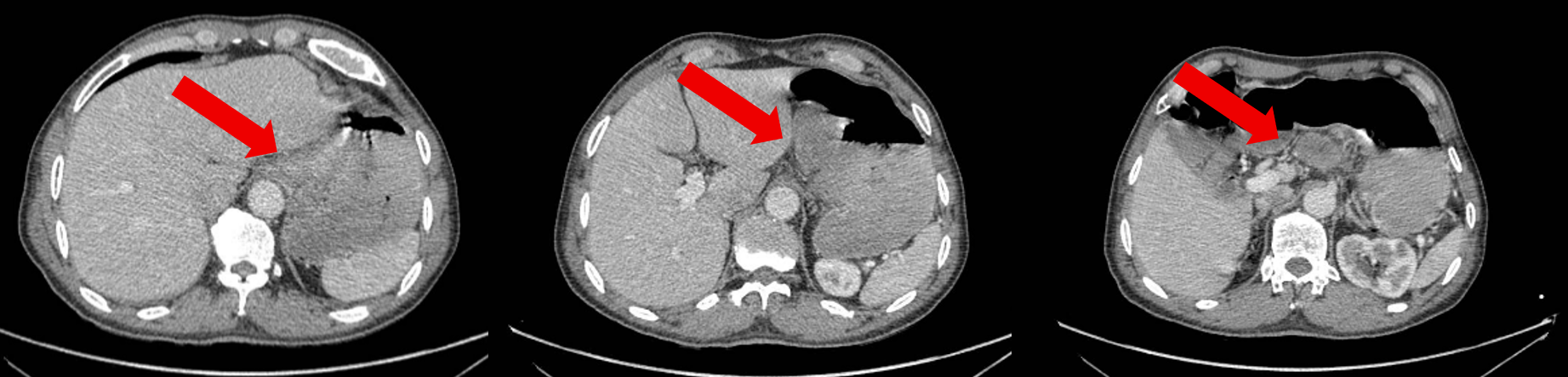
治疗2周期后患者于2024-10-20复查腹部CT:胃底、胃体小弯侧胃壁不均增厚,与邻近贲门分界不清,较前减轻,病灶较厚处约1.3cm。贲门左、胃小弯及肝胃间隙数个增大淋巴结,多系转移,多数较前缩小,大者大小约3.0×1.7cm。
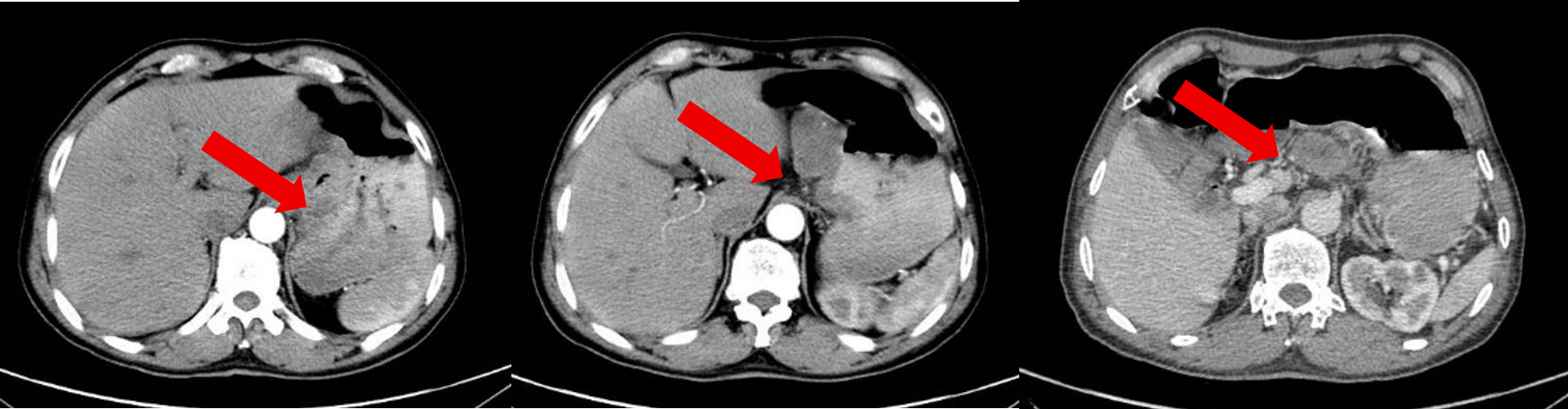
治疗4周期后患者于2024-12-27复查腹部CT:胃底、胃体小弯侧胃壁不均增厚,与邻近贲门分界不清,较前大致类似,病灶较厚处约1.3cm。贲门左、胃小弯及肝胃间隙数个增大淋巴结,多系转移,多数较前缩小,大者大小约2.6×1.6cm。
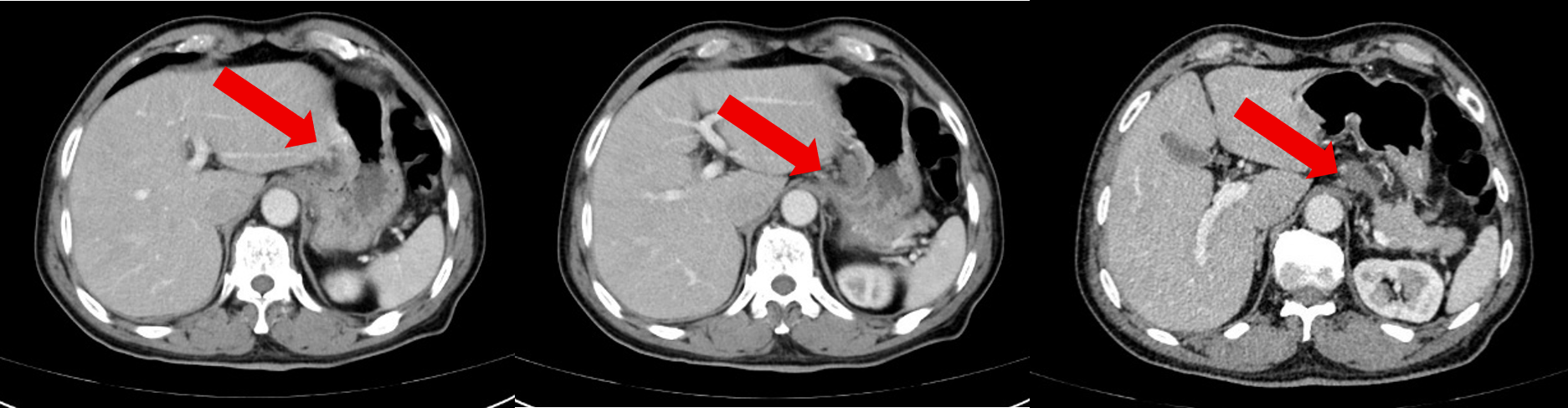
治疗6周期后患者于2025-3-6复查腹部CT:胃底、胃体小弯侧胃壁不均增厚,与邻近贲门分界不清,较前大致类似,病灶较厚处约 1.3cm。贲门左、胃小弯及肝胃间隙数个增大淋巴结,多系转移,部分较前稍缩小,大者大小约2.6×1.5cm。
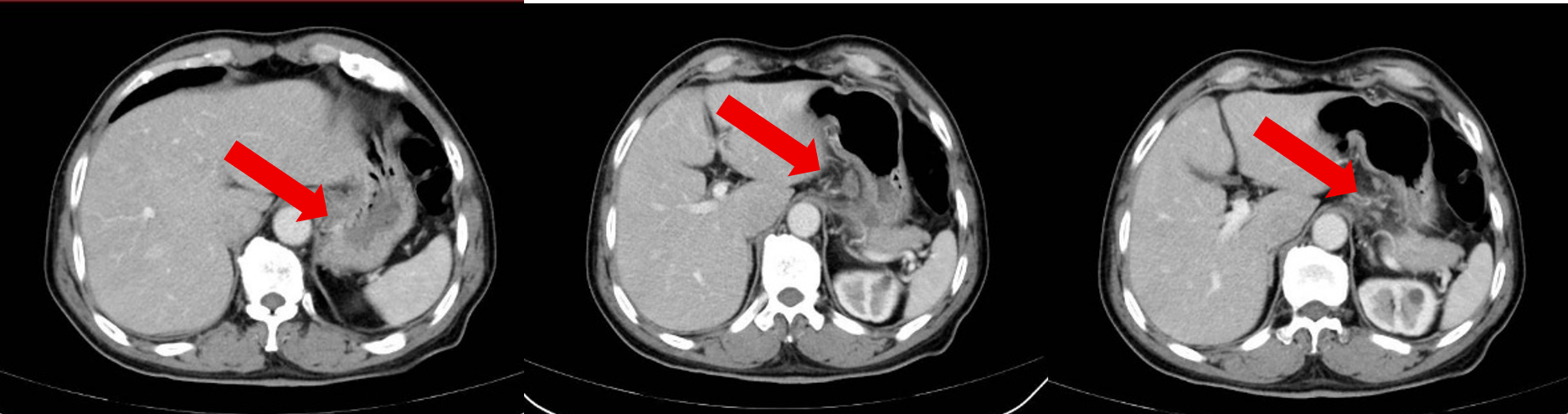
治疗6周期后患者于2025-3-7复查上消化道内镜:贲门-胃体上部小弯侧可见溃疡型新生物,底覆黄苔,周围粘膜充血肿胀。系贲门化疗后溃疡改变,较2024-8-12明显缩小。
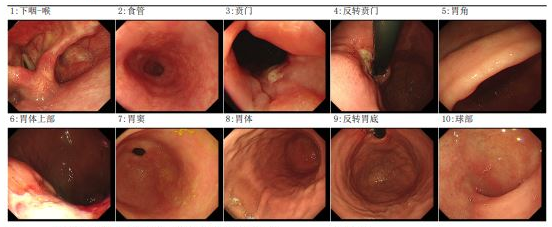
血清CEA变化:经过一个周期的治疗后,血清CEA就降至正常,之后都保持在正常水平。其余肿瘤标志物均未升高,在正常范围内。
经过上述系统的评估,病灶及周围淋巴结较前明显缩小,肿瘤标志物水平均在正常范围内,无新发病灶及远处转移,整体抗肿瘤疗效评估为PR。
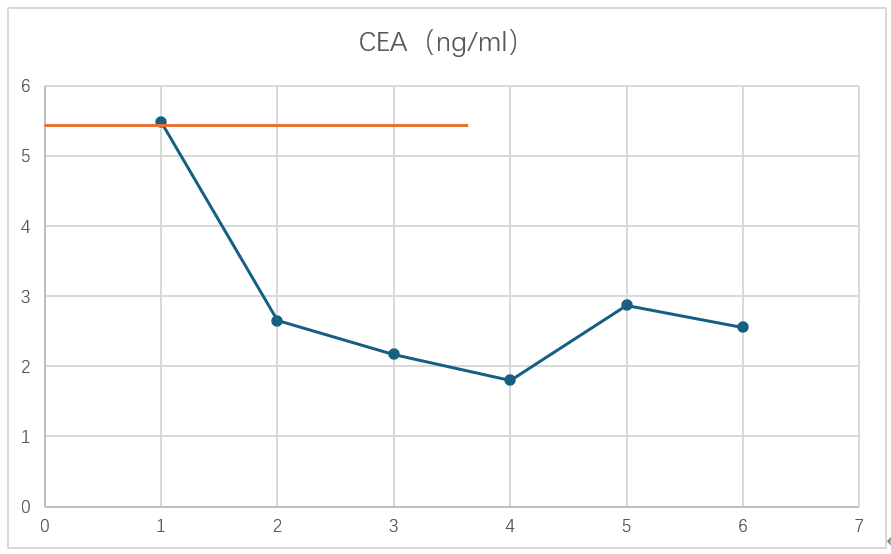
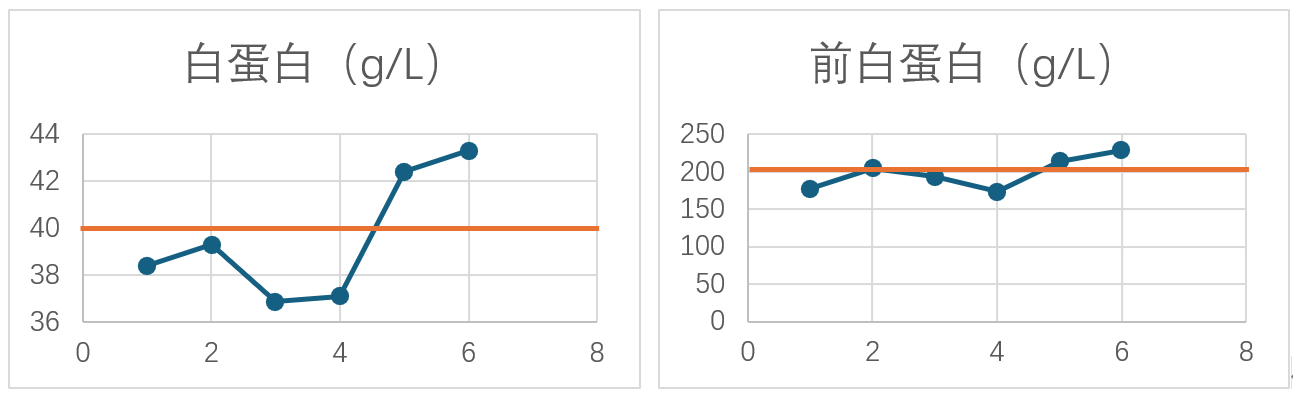
白蛋白及前白蛋白变化
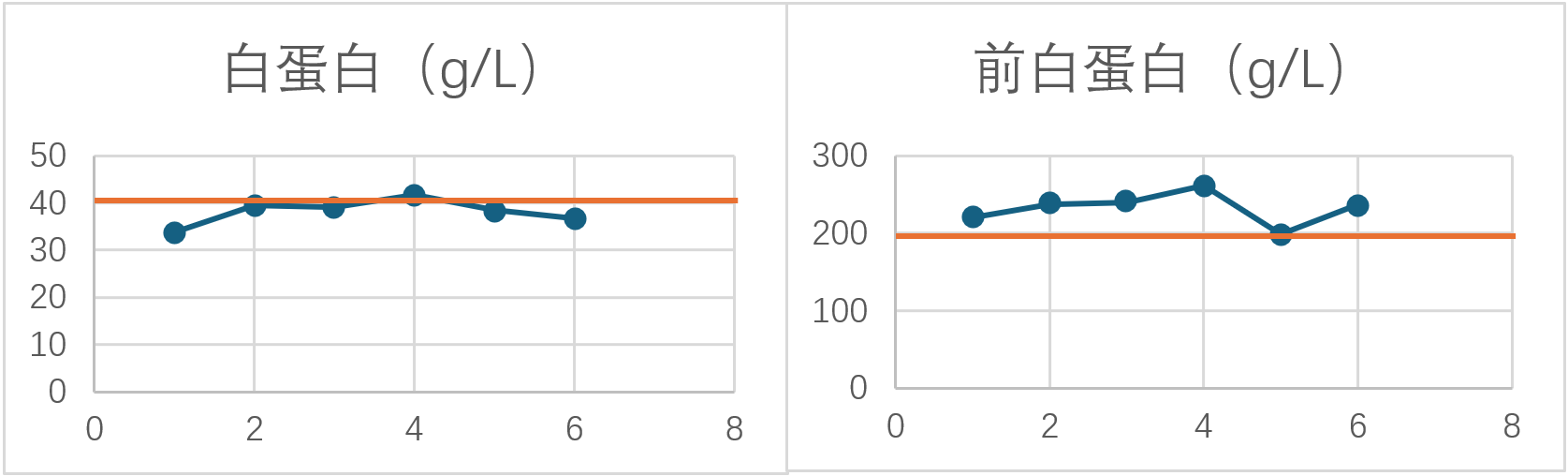
体重及血红蛋白变化
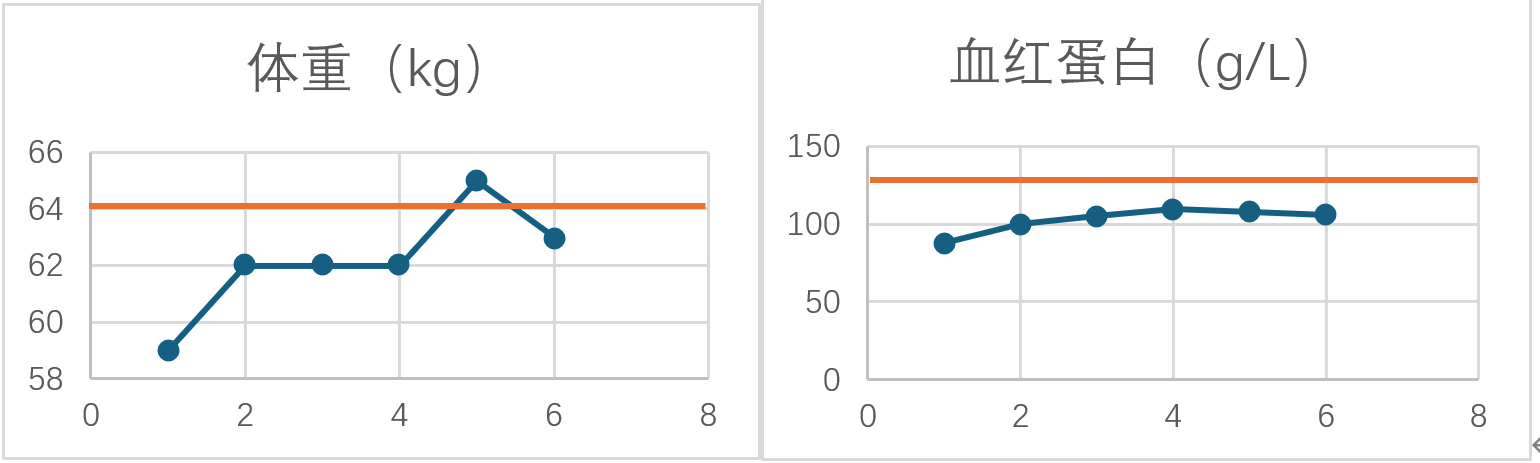
新辅助治疗期间不良反应
主要为胃肠道反应,腹痛、腹胀。无血液性毒性反应及免疫检查点抑制剂治疗相关不良反应。
手术治疗阶段
入院后患者完善相关检查,经科室MDT讨论,患者有手术指征,术前各项检查未见明显手术禁忌征,完善术前准备,于2025-03-11在手术室全麻下行腹腔镜贲门癌根治术(全胃切除术+D2淋巴结清扫术+食道-空肠(π型吻合)、空肠-空肠Roux-en-Y吻合术)+肠粘连松解术。
术中探查见无腹水,术区见肠粘连,腹盆腔腹膜、肝胆胰脾、大小肠及系膜外观、形态未见明显异常;肿瘤位于贲门小弯侧,外侵浆膜明显,局部小网膜组织受累皱缩,胃周Nos.3、7组淋巴结肿大融合,约1-1.5cm大小;切除后剖视标本见:食管胃结合部(EGJ)受侵犯约3mm,Borrmann II型,大小40mm×40mm。
手术顺利,术中未输血。术后第5天开始口服肿瘤特医食品速熠素,每天口服1瓶。无手术并发症发生,经过对症支持治疗后于术后第7天顺利出院。
术后病理示:全胃;大体类型:溃疡型;肿瘤大小:3cm×2cm×1cm;组织学类型:巨检“肿块”全部取材,未见确切恶性成分,结合病史,符合治疗后改变;淋巴结转移情况:第1组淋巴结(0/2);第2组淋巴结(0/1)伴治疗后改变;第3a组淋巴结(0/1);第3b组淋巴结、第4sa组淋巴结、第4sb组淋巴结、第4d组淋巴结、第7组淋巴结、第12a组淋巴结镜下为纤维脂肪组织;第5组淋巴结(0/1);第6组淋巴结(0/2);第8a组淋巴结(0/1);第9组淋巴结(0/5);第11组淋巴结(0/1);另送组织:查见纤维脂肪组织。
病理学分期:ypT0N0Mx(AJCC 8版);治疗反应:无肿瘤细胞残留(完全缓解,0分),达到病理完全缓解(pCR)。
辅助治疗方案
患者术后恢复尚可,经过科室MDT讨论,患者新辅助治疗效果佳,术后辅助化疗方案继续与新辅助治疗方案相同。分别于2025年4月24日和2025年6月12日行术后两周期化疗联合免疫治疗,后续采用免疫检查点抑制剂单药维持治疗。
术后营养治疗
患者出院后接受饮食指导及营养治疗,饮食指导为术后1周至1月以半流质饮食为主;术后1月以上可使用软质普通饮食。患者出院后在经口饮食的同时,补充肿瘤特医食品。从每天口服1瓶逐渐过渡并耐受每天口服2瓶,能额外提供710 kcal能量和43g蛋白质,患者持续口服至辅助治疗结束。
术后随访
体重及血红蛋白变化
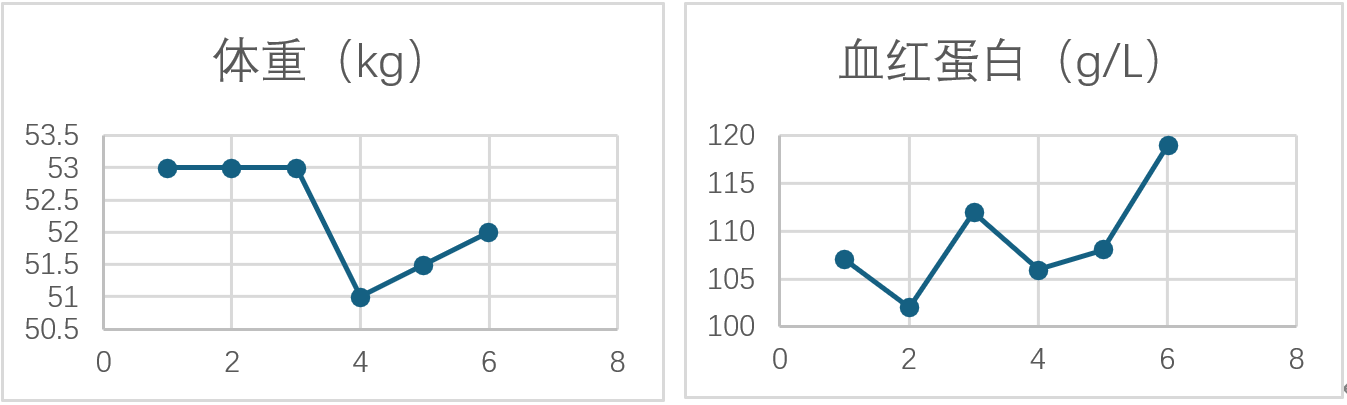
白蛋白及前白蛋白变化
CEA变化
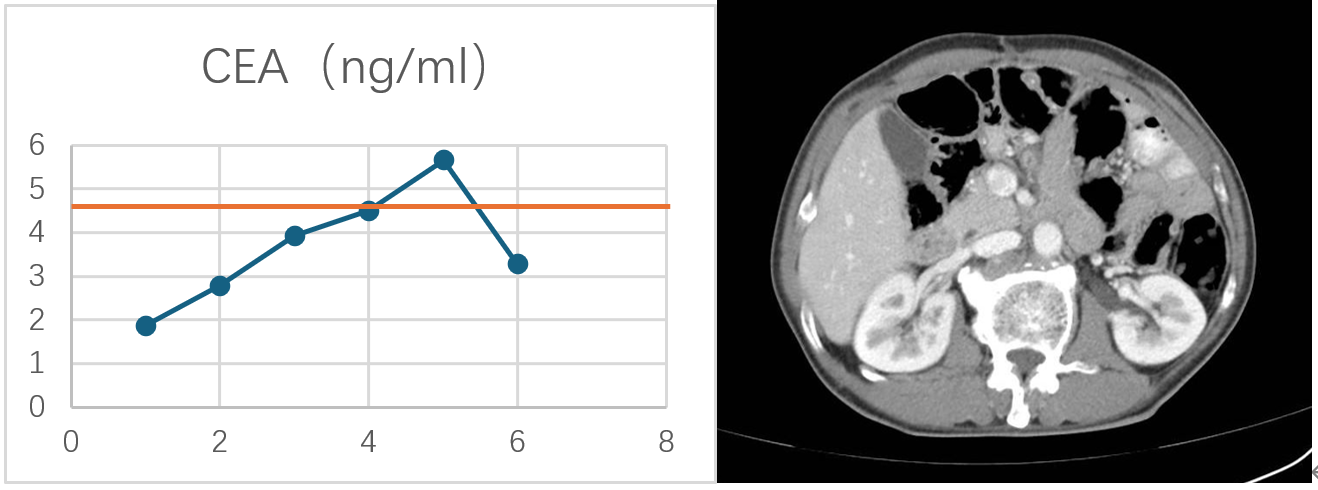
从术后第一周期化疗开始对患者进行定期随访,包括是否术后复发、化疗并发症、营养状况变化等。随访至今,患者并无复查。术后辅助化疗过程中偶有腹胀,余无其他化疗及免疫检查点抑制剂治疗相关不良反应。患者术后营养状况较好,体重维持稳定,血清白蛋白、前白蛋白、血红蛋白水平稳步提升,无营养不良的发生。
本病例为一名66岁男性局部晚期可切除伴随Bulky N的胃癌(III期)患者,初诊时合并重度营养不良。通过多疗程化疗联合免疫检查点抑制剂全身抗肿瘤治疗,并在新辅助治疗阶段、围术期及术后辅助治疗阶段,全程使用以肿瘤特医食品速熠素为核心的营养治疗方案,不仅极大改善了和维持了患者的营养状况,纠正代谢异常并重塑免疫,帮助患者实现病理完全缓解、术后零并发症、以及极大减少了围化疗期的不良反应,助力患者获得高质量的预后改善。
1. Nierengarten MB. Global Cancer Statistics 2022: The Report Offers a View on Disparities in the Incidence and Mortality of Cancer by Sex and Region Worldwide and on the Areas Needing Attention. Cancer (2024) 130(15):2568.
2. Zhao B, Zhang J, Zhang J, Zou S, Luo R, Xu H, et al. The Impact of Preoperative Underweight Status on Postoperative Complication and Survival Outcome of Gastric Cancer Patients: A Systematic Review and Meta-Analysis. Nutrition and cancer (2018) 70(8):1254-63.
3. Xu R, Chen XD, Ding Z. Perioperative Nutrition Management for Gastric Cancer. Nutrition (Burbank, Los Angeles County, Calif) (2022) 93:111492.
排版编辑:肿瘤资讯-李鑫











 苏公网安备32059002004080号
苏公网安备32059002004080号


