在胃癌的系统性治疗中,新辅助免疫联合化疗(nICT)近年来屡破僵局,为局部晚期胃癌患者带来了显著的生存获益(如NEOSUMMIT-01、MATTERHORN等大型临床试验)。然而,临床上仍有超过50%的患者无法从这种联合疗法中获益,甚至面临耐药和疾病进展的风险。究竟是谁在阻碍免疫系统的反击?我们又该如何精准筛选获益人群?
近日,中山大学肿瘤防治中心徐瑞华院士/袁庶强教授/赵齐研究员团队在国际顶级肿瘤学期刊Cancer Cell(IF 44.5)上发表重磅研究。该研究基于团队前期开展的NEOSUMMIT-01随机对照临床试验,通过对110例胃癌患者治疗前和治疗中的多组学配对样本进行深度剖析,不仅挖掘出了特异性预测nICT疗效的生物标志物,还首次揭示了由APOA1+肿瘤细胞与TREM2+巨噬细胞交织的免疫耐药新机制,并创新性地提出了指导临床的MOS三分型系统。

研究破局点:基于双臂设计的动态多组学追踪
该研究的最大优势在于其依托的NEOSUMMIT-01试验的双臂设计(nICT组 vs. 单纯化疗nCT组),并获取了治疗前与治疗中的配对样本。研究团队运用全外显子测序(WES)、RNA测序、蛋白质组学及单细胞RNA测序(scRNA-seq),呈现了胃癌在 nCT 和 nICT 治疗过程中肿瘤及免疫微环境动态的全面多组学特征分析,为发现高价值的特异性靶点奠定了坚实基础。
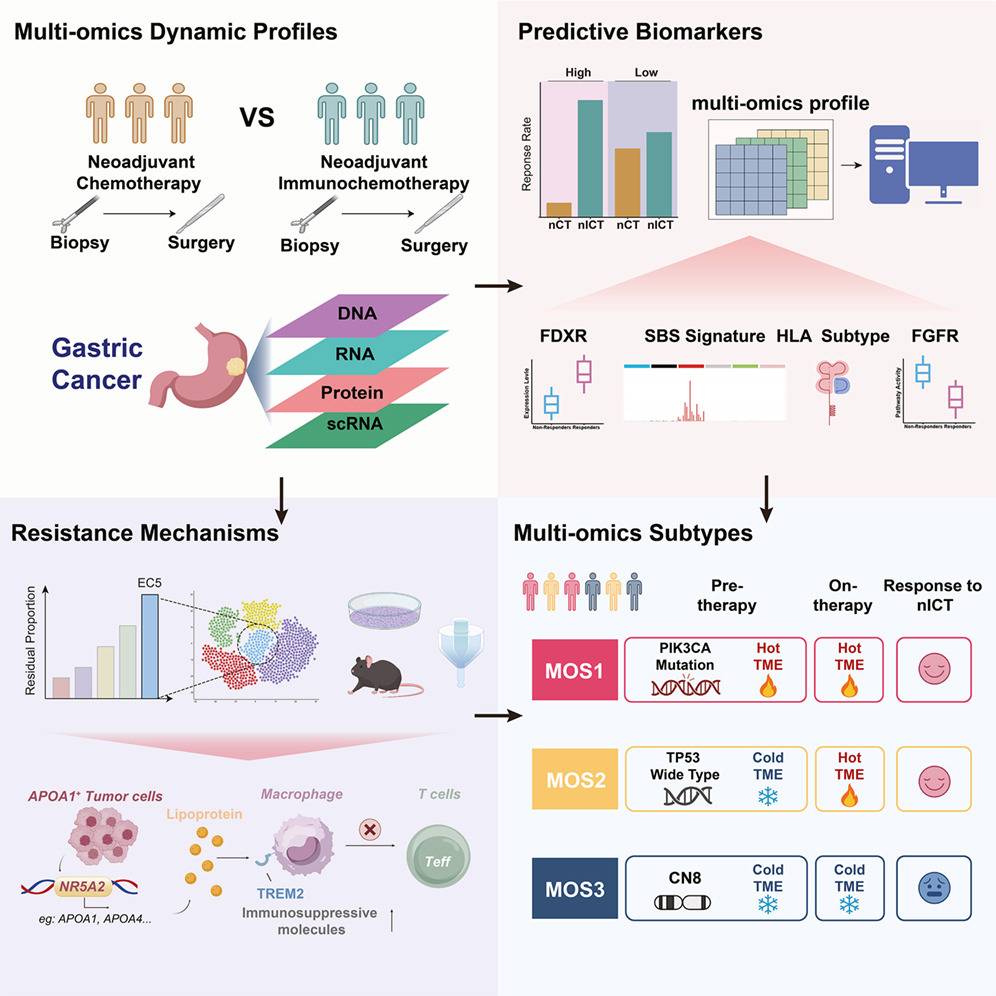
核心机制发现:从基因动态到微环境演化的多维度解码
锁定多维生物标志物:疗效预测的 "指南针"
以往的生物标志物研究往往缺乏对照组,难以区分标志物是“预测性”还是“预后性”。该研究利用双臂设计(nCT vs. nICT),通过整合分析,系统筛选出 nICT 的特异性疗效预测标志物:
获益标志物:携带LRP1B突变提示对nICT响应良好;此外,高表达的FDXR基因也是潜在的获益指标。
耐药(不利)标志物:HLA-B*15:02等位基因被明确为不利因素。研究发现,该HLA分型递呈突变多肽的能力较弱(亲和力低),导致肿瘤免疫原性下降;同时,特定突变特征SBS19以及高活性的FGFR通路也与nICT的耐药风险相关。
肿瘤微环境分析:五个不同的胃癌生态系统类型
研究团队通过scRNA-seq数据,将胃癌微环境聚类划分为5种具有高度异质性的生态型(Ecotypes, EC1-5):
·EC1(免疫激活生态型):对nICT响应率极高。富集效应免疫细胞亚群,以组织驻留记忆T细胞和细胞毒性T细胞富集为特征。
·EC2(三级淋巴结构生态型): 富含成熟 B 细胞及三级淋巴结构。nICT可以显著促进EC2中三级淋巴结构(TLS)的形成和B细胞的激活。
·EC3(血管正常化生态型):以促血管生成髓系细胞为标志,nICT可显著抑制其促血管生成作用,促进血管正常化。
·EC4(细胞外基质生态型):表现出中等程度的响应。以致密的基质成分和活跃的细胞外基质(ECM)重塑为特征,物理性地阻碍了免疫细胞进入肿瘤核心。
·EC5(代谢抑制生态型):这是该研究的最核心发现之一。以TREM2+巨噬细胞富集和脂质代谢活跃为特征,是导致免疫化疗彻底失效的核心“重灾区”。
揭秘耐药“元凶”:APOA1-TREM2细胞耐药轴
为什么EC5生态型的患者会对免疫化疗无动于衷?研究者将目光锁定在了EC5中特有的一群肠上皮样肿瘤细胞(APOA1+肿瘤细胞)。
·机制解析:这群APOA1+肿瘤细胞受到上游转录因子NR5A2的驱动,大量分泌脂蛋白(APOA1等)。这些脂蛋白作为配体,与巨噬细胞表面的TREM2受体结合,激活PI3K和SYK通路,诱导巨噬细胞向免疫抑制型极化。
·功能验证(惊艳的闭环):在小鼠胃癌类器官(mGCO)模型中,联合TREM2阻断可有效逆转APOA1过表达所介导的免疫化疗耐药,恢复抗肿瘤免疫应答。这一发现为克服胃癌免疫耐药提供了极具潜力的全新靶点。
临床转化:胃癌多组学分型(MOS)系统
为了将庞杂的多组学数据转化为临床可用的工具,研究团队整合了基因组、转录组及肿瘤微环境特征,创新性地构建了多组学分型(Multi-Omic Stratification, MOS)模型,将患者分为三种分子亚型,并规划了未来治疗策略。
MOS1(免疫激活型,约占30%):这类患者(常伴有PIK3CA突变、FDXR 高表达、基线免疫细胞浸润)是nICT的极佳获益人群,nICT响应率高达88%(vs化疗29%)。这一巨大的疗效差异充分说明了免疫治疗在这类患者中的重要价值。
MOS2(免疫可塑型,约占42%):呈现出初始的“免疫荒漠”特征,但免疫化疗能激发其内在潜力,显示出中度受益趋势。对于这类患者,治疗期间的动态监测至关重要。一旦证实微环境被成功重塑,患者即可斩获长期生存获益。
MOS3(免疫抑制型,约占28%):这类患者正是被APOA1+肿瘤细胞和TREM2+巨噬细胞主导的 "免疫抑制型",对 nICT 无显著获益。对于这部分难治性患者,常规免疫化疗犹如泥牛入海,是未来需要重点研发新药(如联合TREM2阻断剂)来攻克的人群。
该分型体系已在三个抗 PD-1 单药队列和两个单纯化疗队列中均显示出良好的预后预测价值和跨治疗场景的适用性。这一验证结果表明,MOS 分型系统不仅具有科学价值,更具有重要的临床应用前景。
结论
该研究解构了胃癌对新辅助免疫化疗响应的复杂网络,其揭示的HLA-B*15:02遗传劣势、APOA1-TREM2耐药轴以及MOS精准分型系统,为全球胃癌领域的后续新药开发和临床排兵布阵指明了方向。我们期待这些创新发现能早日走向临床,转化为患者实实在在的生存获益。
讨论与洞察:通往定制化治疗之路
本研究标志着胃癌新辅助治疗从“经验性盲选”向“多组学定制”迈出了关键一步。但研究存在一定的局限性,未来的研究方向应重点关注:
·不能仅凭治疗前的基线活检决定整个治疗周期的策略,动态的“治疗中”监测对于识别那些未能成功转化或产生获得性耐药的患者至关重要。
·MOS模型目前基于前瞻性临床试验的回顾性分析,未来需要更大规模的多中心、前瞻性随机对照队列来进一步校验其在真实世界中的效能。
·针对TREM2的小分子抑制剂或抗体药物有望与PD-1抑制剂联合,成为突破胃癌免疫耐药的关键策略。
·开发基于多组学的快速检测平台,实现临床快速分型。
Zhao Q, Huang R, Wang C, et al. Dissecting genetic and immune drivers of heterogeneous responses to neoadjuvant immunochemotherapy in gastric cancer. Cancer Cell. Published online February 19, 2026. doi:10.1016/j.ccell.2026.01.015.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


