胶质瘤是中枢神经系统最常见的原发性肿瘤之一,随着分子分型的精细化、靶向药物的涌现以及手术理念的更新,新的临床证据和研究成果层出不穷。对于相关领域的研究者与临床医生而言,及时、准确地把握国际前沿进展,是优化临床决策、推动学科发展的关键。
为此,脑医汇-神外资讯特别推出「胶研速递」项目,每月定期梳理与总结胶质瘤领域近期发表的重要文献,并邀请领域知名专家进行深度解读与点评。专家们将结合自身的临床经验与研究洞见,剖析研究的核心价值与临床意义,搭建一个连接全球前沿科研与本土临床实践的桥梁,共同推动中国胶质瘤诊疗水平的不断提升。
本期我们精选5篇在2025年12月份发表的胶质瘤领域文献,并邀请到重庆大学附属肿瘤医院神经外科杨海峰教授进行深入解读,欢迎各位同道阅读、分享。
Vorasidenib治疗IDH 1/2突变型低级别胶质瘤的随机、双盲、安慰剂对照III期临床研究(INDIGO):次要终点与探索性终点分析[1] (Lancet Oncology,IF:35.9)
在一项III期临床试验中,Vorasidenib(一种具有脑渗透性的口服IDH1/2突变抑制剂)在第二次中期分析时,显著改善了主要终点无进展生存期(PFS)和关键次要终点至下一次干预时间(TTNI),研究因此揭盲。本文报告了从第二次中期分析(2022年9月6日)至揭盲(2023年3月7日)期间额外6个月的双盲数据,并评估Vorasidenib对肿瘤体积生长速率、健康相关生活质量(HRQoL)、神经认知功能及癫痫控制的影响。
INDIGO是一项在加拿大、法国、德国、以色列、意大利、日本、荷兰、西班牙、瑞士、英国及美国共92家医院开展的随机、双盲、安慰剂对照III期试验。入组患者为年龄≥12岁的存在肿瘤残留或复发的IDH1/2突变型2级弥漫性胶质瘤,KPS评分≥80,既往至少接受过一次手术,且未接受过其他抗癌治疗。患者按1:1随机分组(根据当地判定的1p/19q共缺失状态和基线肿瘤大小分层),接受每日一次的口服Vorasidenib(40 mg)或安慰剂,连续28天为一个周期,直至疾病进展或出现不可耐受毒性。主要终点为盲态独立评审委员会评估的PFS,关键次要终点为TTNI。预设次要终点包括肿瘤生长速率(每6个月肿瘤体积变化率)和HRQoL(采用FACT‑Br量表评估)。预设探索性终点包括神经认知功能(采用认知评估量表)和癫痫发作情况(基于患者自我报告)。所有疗效分析采用全分析集(包括所有随机分组患者),安全性分析采用安全性分析集(包括所有至少接受一剂研究药物或安慰剂的患者)。试验已在ClinicalTrials.gov注册(NCT04164901),入组已完成,试验仍在进行中。
2020年1月9日至2022年2月22日期间,共331例患者入组并随机分配至Vorasidenib组(n=168)或安慰剂组(n=163)。其中男性187例(56%),女性144例(44%),白种人257例(78%)。中位随访时间为20.1个月(IQR 15.9-23.8)。额外6个月随访后,Vorasidenib组较安慰剂组在中位PFS(NR [95% CI 22.1-NE] vs 11.4个月[95% CI 11.1-13.9];HR 0.35 [95% CI 0.25–0.49])和TTNI(NE [95% CI NE-NE] vs 20.1个月[95% CI 17.5-27.1];HR 0.25 [95% CI 0.16–0.40])上仍有显著改善(NR:未达到;NE:无法估计)。Vorasidenib组肿瘤生长速率为‑1.3%(95% CI ‑3.2%–0.7%),安慰剂组为14.4%(95% CI 12.0%-16.8%),组间差异为15.9%(95% CI 12.6%–19.3%)。两组基线FACT‑Br总分相近(Vorasidenib组158.2 [SD 26.4],安慰剂组158.8 [23.3]),治疗结束时仍保持较高水平(154.2 [29.8] vs 153.2 [29.4])。从基线至治疗结束,两组在言语学习、执行功能、注意力、工作记忆和精神运动功能等神经认知维度上均无差异。Vorasidenib组癫痫年发生率低于安慰剂组(18.2次/人年 [95% CI 8.4-39.5] vs 51.2次/人年 [95% CI 22.9-114.8)。安全性方面,Vorasidenib组与安慰剂组最常见的≥3级治疗期间不良事件分别为:丙氨酸氨基转移酶升高(17例 [10%] vs 2例 [1%])、天冬氨酸氨基转移酶升高(8例 [5%] vs 0例)、癫痫发作(7例 [4%] vs 5例 [3%])及γ‑谷氨酰转移酶升高(5例 [3%] vs 2例 [1%])。Vorasidenib组的严重TEAEs发生率为12%(20例),安慰剂组为6%(10例),最常见为癫痫发作。未发生治疗相关死亡。
与安慰剂相比,Vorasidenib可降低肿瘤生长速率并改善癫痫控制,且未观察到对HRQoL或神经认知功能的负面影响。此外,延长随访进一步支持了Vorasidenib在IDH1/2突变型2级弥漫性胶质瘤患者中PFS和TTNI的稳健获益。这些结果支持对仅接受过手术、且无需立即放疗或化疗的IDH1/2突变型2级胶质瘤患者使用Vorasidenib。
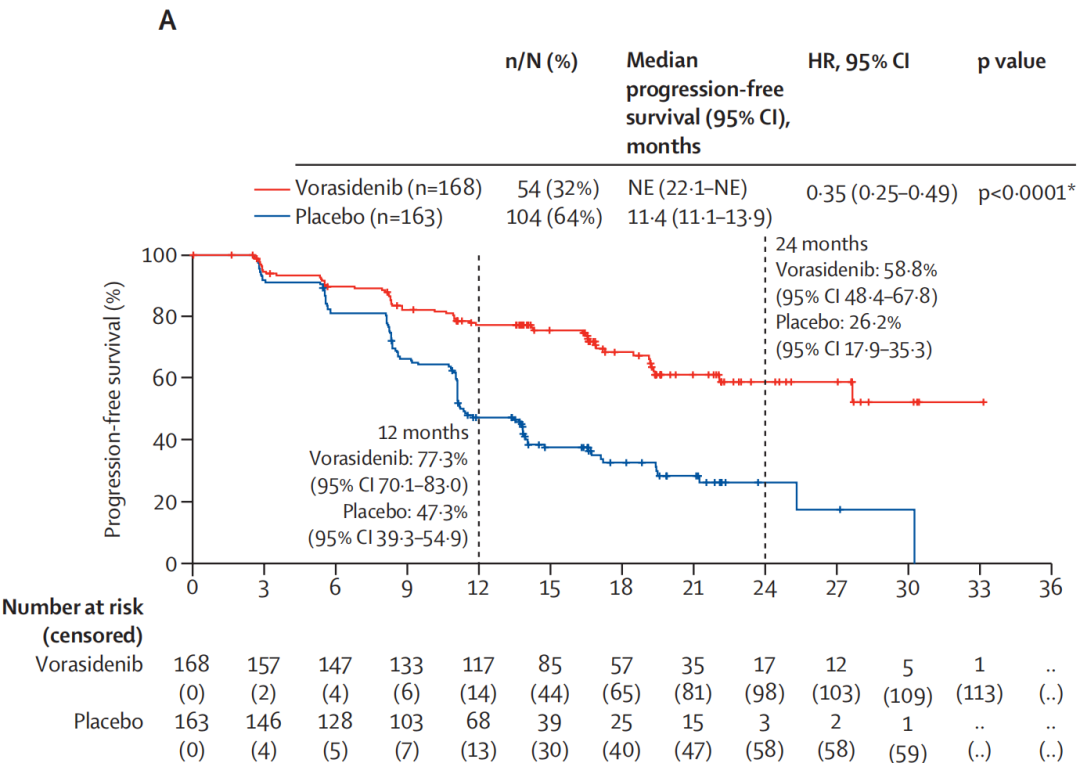
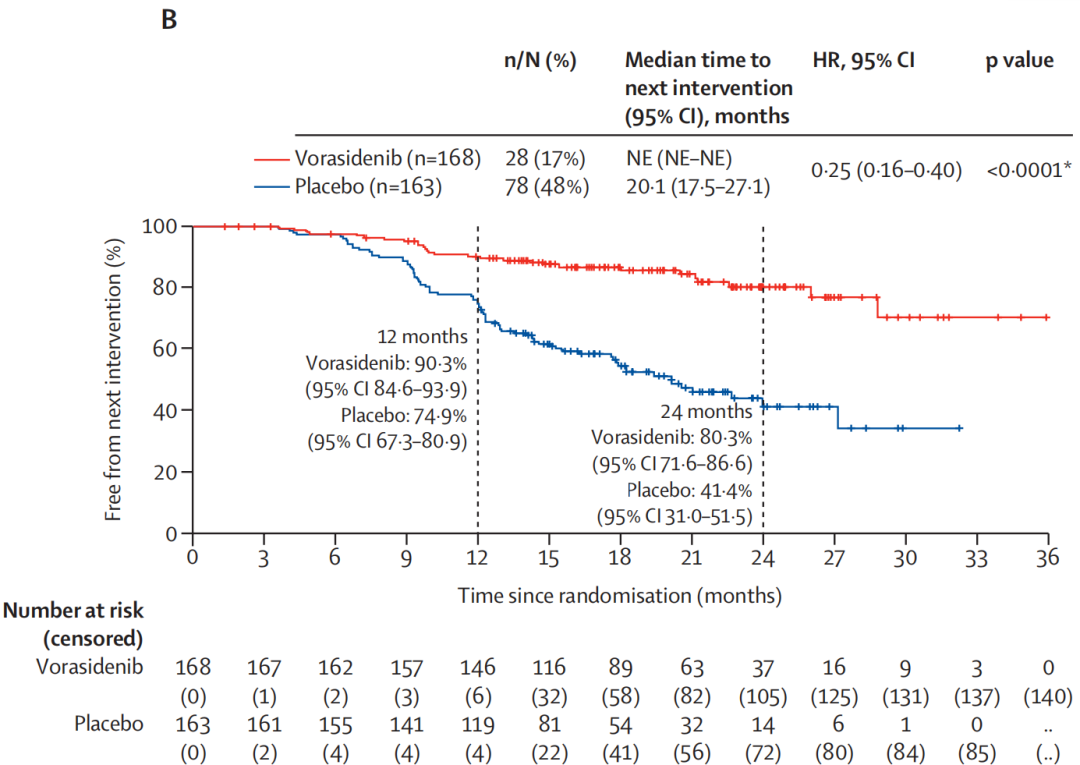 图1:研究揭盲前基于影像学的PFS和TTNI
图1:研究揭盲前基于影像学的PFS和TTNI
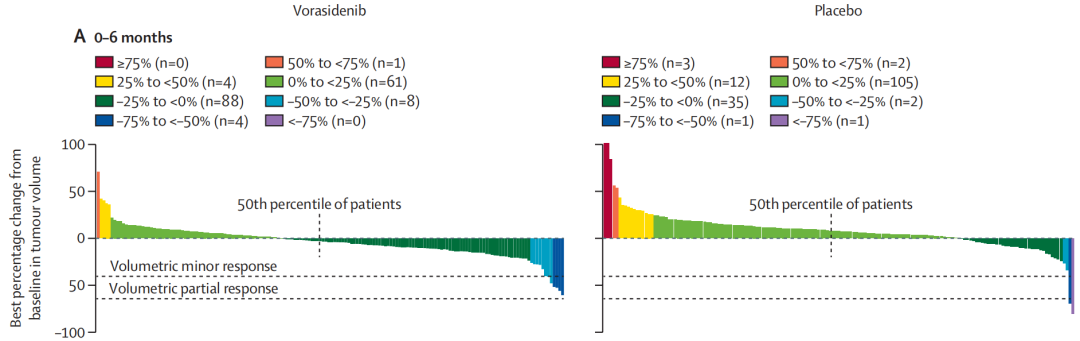
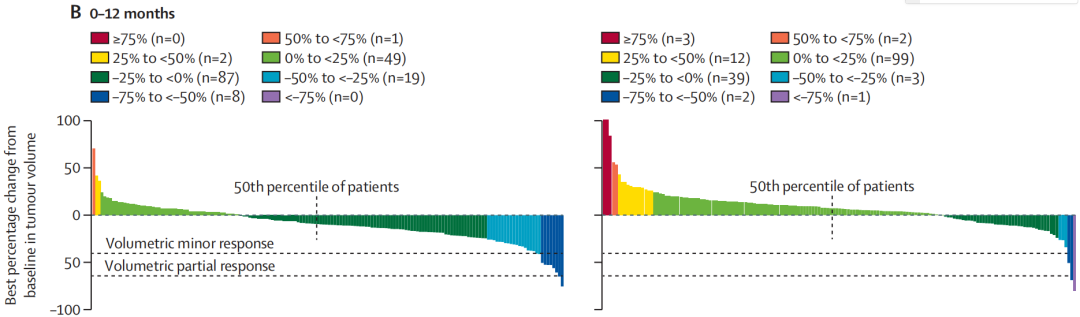
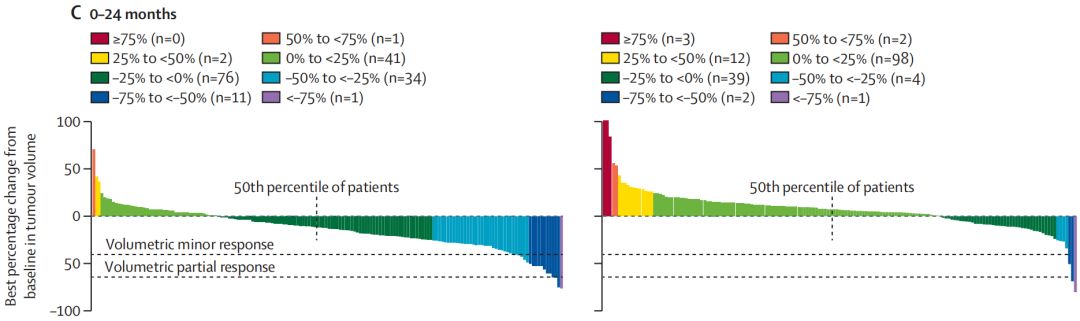 图2:肿瘤体积的最佳百分比变化
图2:肿瘤体积的最佳百分比变化
IDH突变型胶质瘤是一种具有弥漫性浸润生长特性的恶性肿瘤,难以治愈。这类疾病好发于中青年,患者中位年龄仅约40岁,这意味着疾病将给患者个人及家庭带来长期的生理、心理与社会负担。传统术后辅助放化疗虽能暂时控制疾病进展,但其长期毒性(如认知功能下降、内分泌紊乱等)会严重影响其生活质量与长期生存获益,因此亟需一种疗效确切、安全性良好、能延迟放化疗启动时间的精准治疗方案。而IDH突变作为这类肿瘤发生发展的早期核心驱动因素,会导致致癌代谢产物2-HG(2-羟基戊二酸)蓄积,进而促进肿瘤进展。因此,针对该靶点的精准治疗一直是胶质瘤领域的研究重点。Vorasidenib作为全球首个获批的高脑渗透性IDH1/2双重抑制剂,为这类患者提供了全新的治疗选择。
INDIGO研究是一项国际多中心、随机、双盲、安慰剂对照的III期临床研究,此次公布的是从第二次中期分析至研究揭盲这6个月的双盲期数据。结果显示,中位PFS在Vorasidenib组未达到,显著优于安慰剂组的11.4个月,疾病进展风险降低65%;Vorasidenib组的中位TTNI同样未达到,相比安慰剂组的20.1个月显著获益,显著延长了患者接受后续治疗的时间,尽管与NEJM首次报道的数据存在细微差异(如HR值略有降低、安慰剂组TTNI略有延长),但核心结论完全一致,均证实Vorasidenib能显著改善患者PFS并延迟后续干预时间,且获益具有良好的稳健性,排除了短期疗效波动的可能性。
尤其值得关注的是肿瘤生长速率这一指标:Vorasidenib组为-1.3%,而安慰剂组为14.4%,组间差异显著,证实Vorasidenib能有效抑制肿瘤生长,并使肿瘤体积呈现缩小趋势。进一步通过肿瘤体积变化瀑布图分析可见,Vorasidenib治疗后多数患者肿瘤体积呈持续下降趋势,且这种缩小效应具有时间依赖性:治疗初期6个月缩减幅度较温和,随治疗时长延长至12-24个月,缩减效果逐渐显著,与传统化疗的快速细胞杀伤模式存在明显差异,体现了靶向治疗的精准性与持续性,提示了Vorasidenib不仅延缓了无进展生存期,更直接改变了肿瘤的生长轨迹,使之脱离了增长曲线。更值得注意的是,从安慰剂组交叉至Vorasidenib组的患者,其肿瘤生长轨迹也得到明显纠正。此外,Vorasidenib在控制癫痫发作方面亦表现优异,发作率显著低于安慰剂组(18.2次/人年 vs. 51.2次/人年),考虑到IDH突变型胶质瘤很高的癫痫发作频率,对癫痫的控制作用具有很高的临床价值。
安全性方面,Vorasidenib耐受性亦良好,长期随访未出现新的安全信号,3级以上治疗相关不良事件发生率较低,主要为可管理的肝功能指标升高,无治疗相关死亡。
基于INDIGO研究的突破性结果,目前Vorasidenib已在多个国家获批上市。中国患者目前可通过海南博鳌乐城国际医疗先行示范区、北京天竺综合保税区等渠道实现临床用药可及。国内桥接研究及真实世界研究也正在推进,未来将为该药在中国患者中的应用提供更多依据。
IDH突变型2级胶质瘤切除范围的预后分类系统:一项包含外部验证的RANO切除组国际、多中心、回顾性研究[2](Lancet Oncology,IF:35.9)
对于IDH突变型2级胶质瘤,手术切除范围的疗效评估因各研究定义不一而存在争议。本研究旨在建立一套标准化的切除范围分类,并评估超全切除与不同分子亚型患者生存结局之间的关系。
本研究为一项国际多中心回顾性研究,从1993年9月1日至2024年5月10日期间,在美国、欧洲和亚洲16个中心的数据库中,纳入了年龄≥18岁、新诊断IDH突变型2级胶质瘤患者。研究采用Cox比例风险回归分析残余肿瘤与PFS及OS的关联。根据先前提出的一项基于残留肿瘤体积的分类系统对患者进行了分层。同时,研究使用加州大学旧金山分校(UCSF)在1998年2月16日至2017年11月14日期间确诊的患者队列进行地理和机构独立的外部验证。
研究共纳入1391例新诊断IDH突变型2级胶质瘤患者,中位随访81个月(95% CI 78-85)。其中728例患者(379例星形细胞瘤,349例少突胶质细胞瘤)术后未接受任何一线治疗,为评估单纯手术切除的疗效提供了条件。与T2-FLAIR次全切除(3类:残余体积5-25 cm³)或T2-FLAIR最小切除(4类:残余体积>25 cm³)相比,T2-FLAIR全切除(2类:残余体积0-5 cm³)的患者PFS和OS更优。三组患者的10年OS率分别为82%(95% CI 76%-87%) vs 75%(95% CI 62%-84%)vs 48%(95% CI 29%-65%; p<0.0001),5年PFS率分别为44%(95% CI 38%-50%)vs 25%(95% CI 16%-34%)vs 12%(95% CI 4%-24%; p<0.0001)。而超出T2-FLAIR边界的超全切除(1类)则带来进一步的生存获益,10年总生存率达98%(95% CI 92%-99%),5年无进展生存率达83%(95% CI 76%-88%)。生存获益与扩大切除范围的关联性在星形细胞瘤患者中于术后3年开始显现,而在少突胶质细胞瘤患者中,生存曲线的差异在术后6-8年出现。该四级分类的预后价值在多变量分析中得到验证,同时在625例接受一线化疗或放疗(联合或不联合化疗)的患者中,以及在包含381例IDH突变型2级胶质瘤患者的外部UCSF验证队列中均得到证实。
本研究提出的RANO手术切除范围分类可作为预后分层工具。尽管扩大切除对星形细胞瘤患者的生存改善显现更早,但超全切除同样能为少突胶质细胞瘤患者带来生存获益。
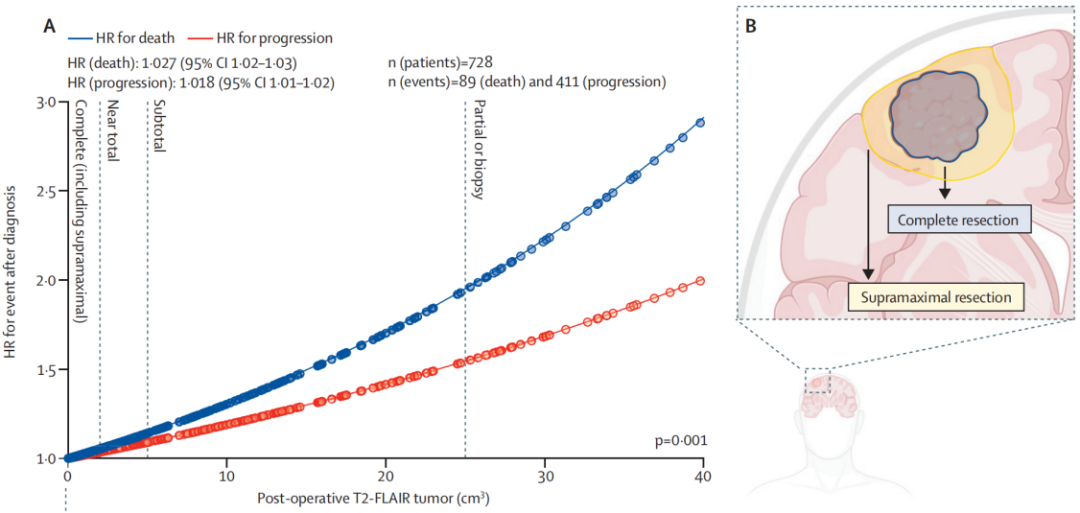
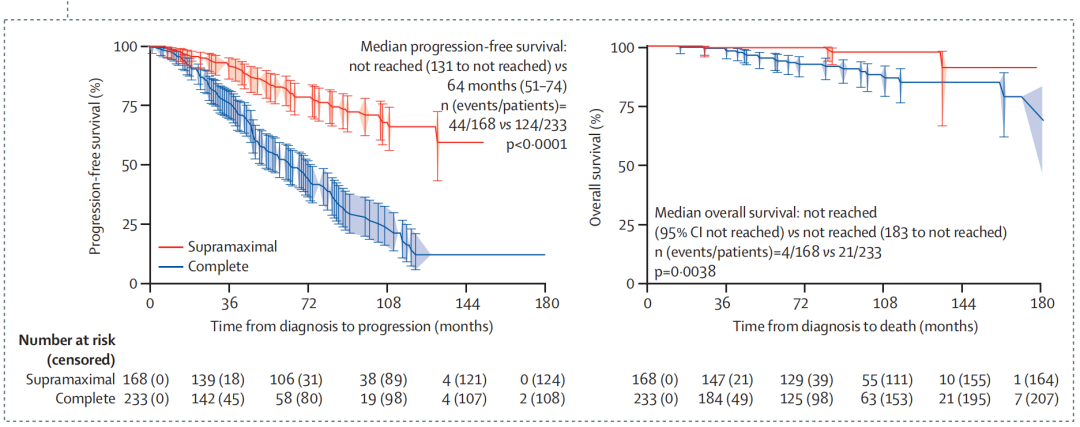 图3:残余T2-FLAIR肿瘤体积与超全切除的预后意义
图3:残余T2-FLAIR肿瘤体积与超全切除的预后意义
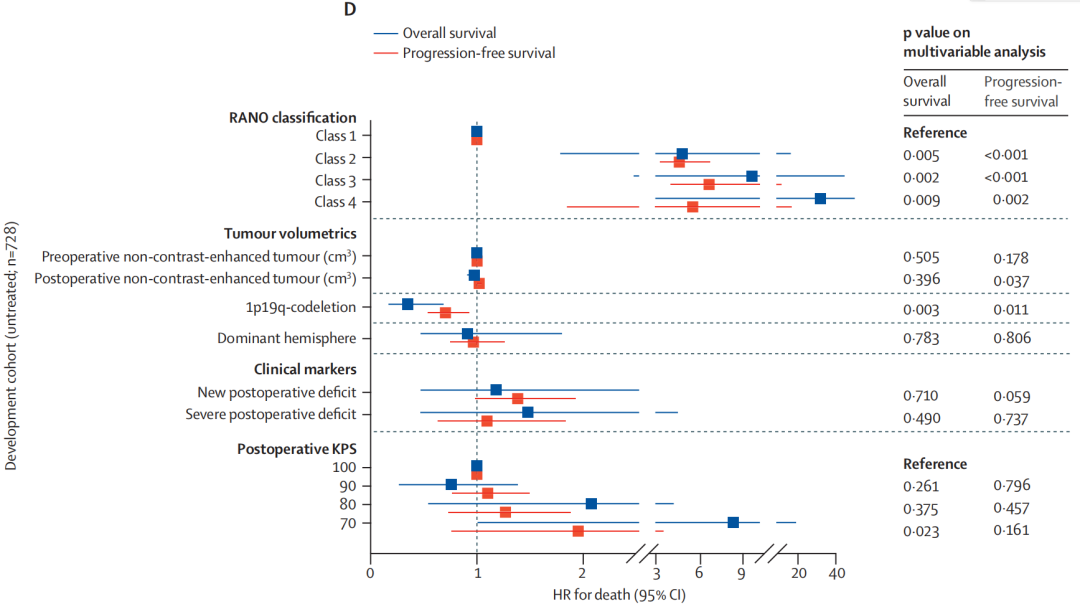 图4:新型RANO分类系统在2级胶质瘤中的验证
图4:新型RANO分类系统在2级胶质瘤中的验证
这篇由RANO切除组牵头开展的国际多中心回顾性研究,首次针对IDH突变型2级胶质瘤的切除范围提出了一套标准化的四级分类系统(RANO分类),并将其预后价值在外部独立队列中得到验证。该研究通过对1391例患者的分析,明确将切除程度分为:超全切除(切除超出T2-FLAIR边界,无残留)、全切除(残留≤5 cm³)、次全切除(残留5–25 cm³)和最小切除(残留>25 cm³)。研究结果显示,随着切除程度的提高,患者的无进展生存期和总生存期均显著改善,尤其是超全切除组(class 1)的10年生存率高达98%,显著优于仅达到影像学边界的“完全切除”。
结合最近发表在《Science》[3]上的一项研究成果:约40%的IDH突变胶质瘤患者的瘤周皮质中,存在携带IDH突变但尚未获得其他驱动事件的胶质祖细胞,这些细胞可能是肿瘤的“起源细胞”或“癌前克隆”。这意味着,手术中切除的不仅是影像学可见的肿瘤区域,还可能包括这些潜藏在“正常”脑组织中的早期恶性克隆。这一机制为RANO分类中倡导的超全切除提供了更强的理论依据:若能在保留功能的前提下,切除这些含有突变祖细胞的“肿瘤发生土壤”,理论上可更彻底地清除疾病根源,延缓甚至阻止肿瘤复发。
然而,这一机制也同时凸显了神经外科在临床决策中面临的矛盾:一方面,扩大切除可能带来更大的生存获益;另一方面,切除范围越大,损伤正常脑组织、导致神经功能缺损的风险也越高。是否值得为潜在的“土壤清除”冒较大的功能风险,仍需个体化权衡。未来,如何精准界定“该切除多少”以及“哪些区域真正含有高危克隆”,仍需更多影像‑基因组学整合研究及术中分子边界检测技术的支持。
依氟鸟氨酸联合洛莫司汀vs洛莫司汀单药治疗复发性3级星形细胞瘤的Ⅲ期、随机、开放标签研究(STELLAR)[4](Journal of Clinical Oncology:41.9)
STELLAR研究(ClinicalTrials.gov登记号:NCT02796261)是一项III期、随机、开放标签临床试验,旨在评估依氟鸟氨酸联合洛莫司汀对比洛莫司汀单药治疗复发性3级星形细胞瘤的疗效。
研究启动时,入组标准包括:年龄≥18岁;依据2016年WHO中枢神经系统肿瘤分类(WHO CNS4)确诊为间变性星形细胞瘤;放疗联合替莫唑胺(TMZ)治疗后首次复发≥6个月;KPS评分≥70;影像学表现不符合4级胶质母细胞瘤。按1:1随机分组,分层因素包括IDH突变状态、年龄、切除范围及地域。患者接受依氟鸟氨酸(2.8 g/m²,口服,每8小时一次,用药2周/停药1周)联合洛莫司汀(90 mg/m²,口服,每6周一次),或洛莫司汀单药治疗(110 mg/m²,口服,每6周一次)。主要终点为OS。
在8个国家74个中心随机入组的343例患者中,联合治疗组与单药组的OS无显著差异(中位OS:23.4个月 vs 20.3个月;HR=0.94)。随着2021年WHO CNS5分类标准更新,研究在揭盲前对2024年定义的IDH突变型3级星形细胞瘤亚组(n=196)进行了分析。结果显示,与洛莫司汀单药相比,联合治疗带来具有临床意义的中位OS延长(34.9个月 vs 23.5个月;HR=0.64)和中位PFS延长(15.8个月 vs 7.2个月;HR=0.57)。在CNS 4级肿瘤患者中未观察到差异。≥3级治疗相关不良事件主要为可逆性骨髓抑制(联合治疗组42% vs 单药组29%)和听力损害(24% vs 0%),未发现新的安全性信号。
STELLAR研究观察到具有临床意义的疗效改善。对于既往接受放疗联合TMZ治疗的复发性IDH突变型3级星形细胞瘤患者,依氟鸟氨酸联合洛莫司汀方案可使患者PFS延长1倍,并改善总体OS;但该方案对4级肿瘤患者无明显疗效。此结果与药物的细胞抑制作用机制一致。
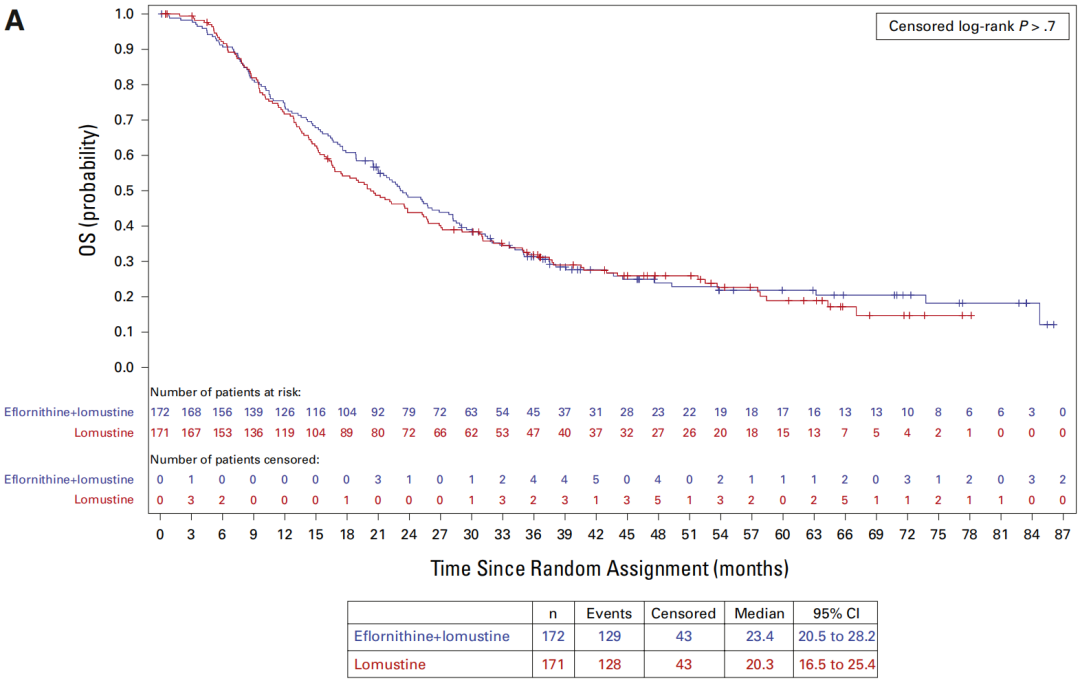
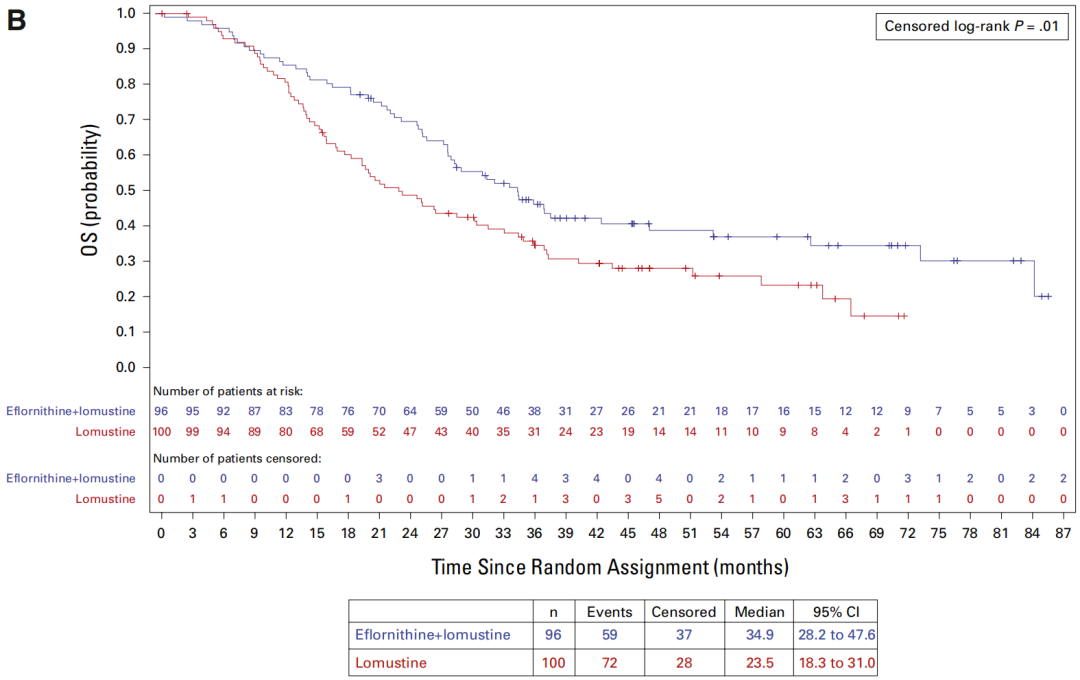 图5:意向治疗(ITT)人群和IDH突变3级亚组的OS Kaplan-Meier曲线
图5:意向治疗(ITT)人群和IDH突变3级亚组的OS Kaplan-Meier曲线
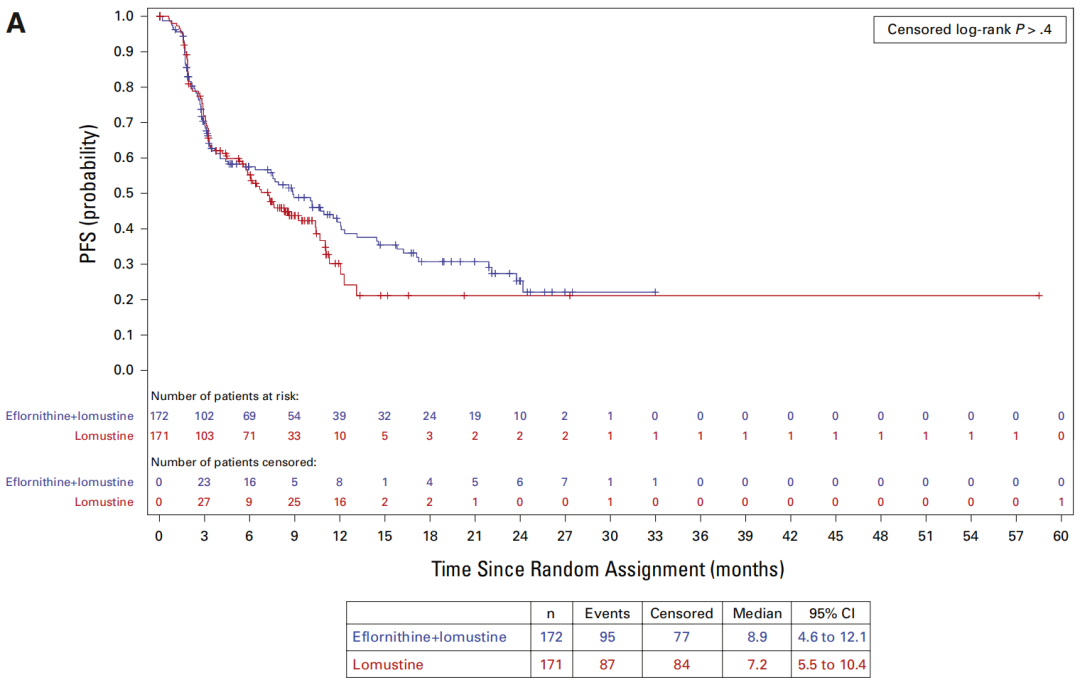
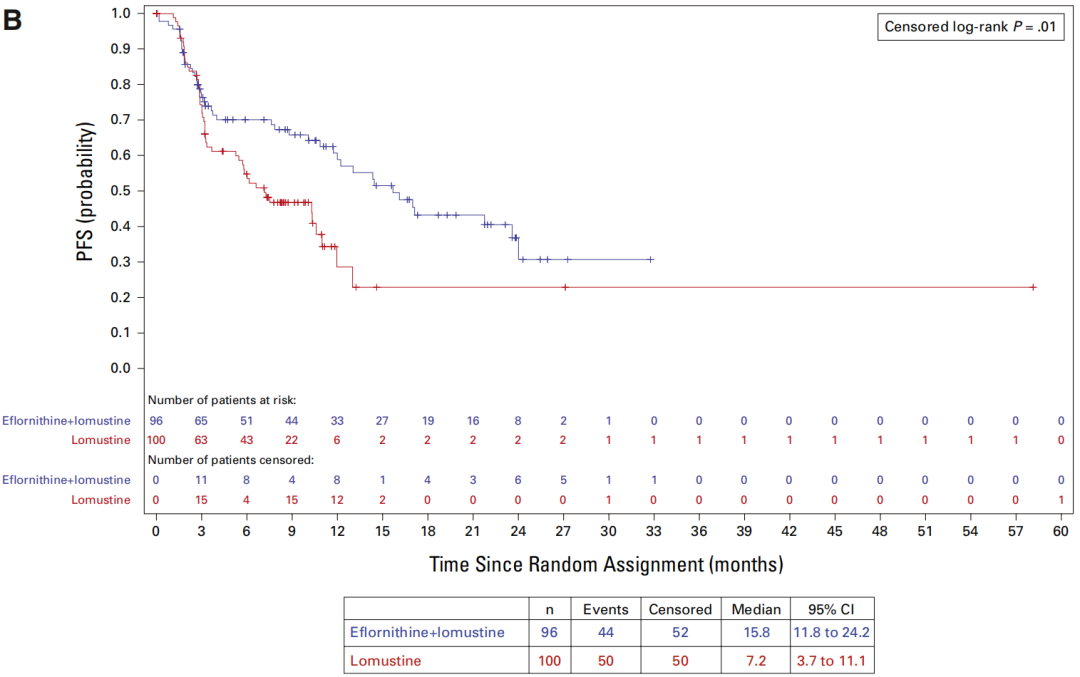 图6:意向治疗(ITT)人群和IDH突变3级亚组的PFS Kaplan-Meier曲线
图6:意向治疗(ITT)人群和IDH突变3级亚组的PFS Kaplan-Meier曲线
IDH突变型胶质瘤患者管理进展[5](Oncologist,IF:4.2)
IDH突变型胶质瘤是弥漫性胶质瘤中具有独特生物学行为和临床病程的一个亚型。过去十年间,随着分子分型、影像学及靶向治疗的进步,学界对此类肿瘤的认识已显著深化。本综述旨在全面概述当前IDH突变型胶质瘤的治疗格局。
本综述重点介绍了WHO 肿瘤分类中的关键分子特征与最新修订要点,以及磁共振波谱、液体活检等新型诊断工具。手术策略也已发生转变,强调在功能定位和先进神经影像引导下进行最大范围安全切除。在治疗方面,Vorasidenib等IDH抑制剂在特定患者人群中展现出良好应用前景,能够实现对疾病的长期控制。此外,放疗和化疗仍是关键治疗手段,多项临床试验正在探索其与靶向治疗的联合应用。最后,该文展望了未来方向,包括免疫治疗、PARP抑制剂及CDK4/6抑制剂在复发或难治性病例中的使用。
该综述强调,采用多学科协作的精准医疗策略对于优化IDH突变型胶质瘤患者的预后至关重要。
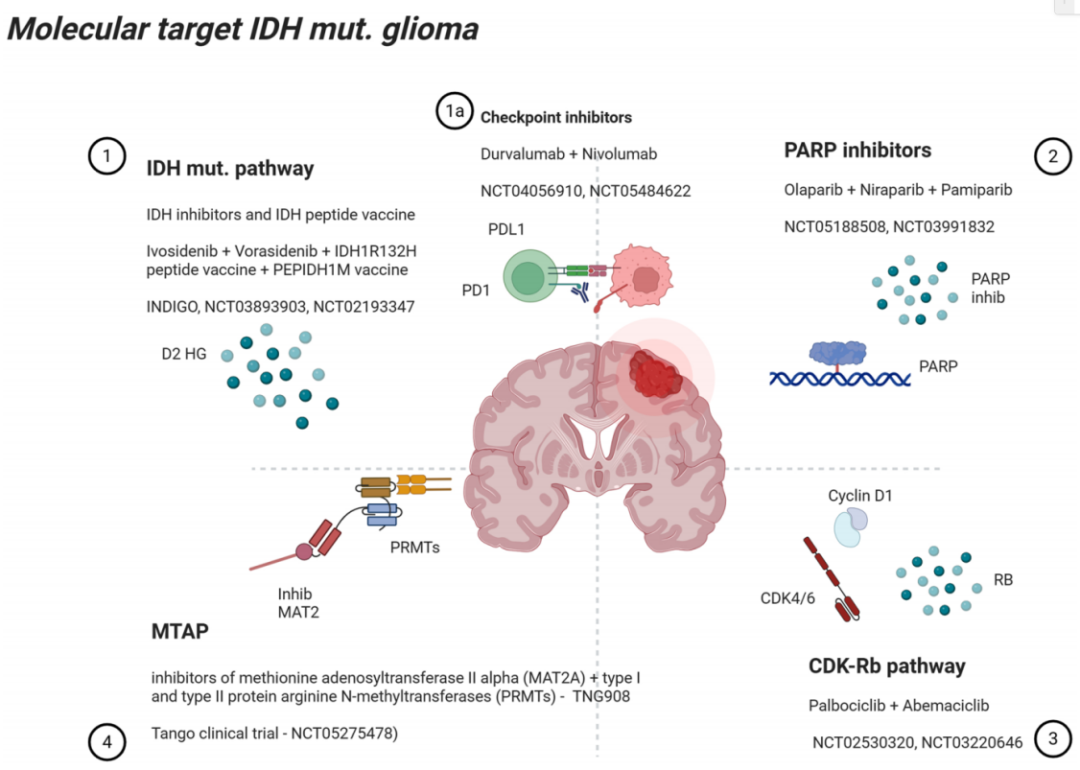 图7:IDH突变型胶质瘤中的新兴靶向治疗与分子改变
图7:IDH突变型胶质瘤中的新兴靶向治疗与分子改变
对比IDH抑制剂和丙卡巴肼-洛莫司汀-长春新碱(PCV)化疗方案治疗少突胶质细胞瘤 [6](Cancers,IF:4.4)
少突胶质细胞瘤是胶质瘤的少见亚型,其分子特征为IDH1/2突变伴1p/19q共缺失。标准治疗为最大范围安全切除后采用PCV方案进行辅助放化疗。尽管PCV方案能带来持久生存获益,但其治疗限制性毒性常见,常导致中断治疗。Vorasidenib等IDH抑制剂已展现出良好的疗效与耐受性,但不同疗法间缺乏比较数据,限制了最佳治疗决策的制定。
这项研究遵循PRISMA‑ScR指南,系统检索截至2025年3月7日的文献,并纳入年龄≥18岁、确诊为IDH突变伴1p/19q共缺失的少突胶质细胞瘤成人患者,接受PCV化疗或IDH抑制剂治疗且随访≥12个月。主要结局包括OS、PFS以及导致停药的≥3级不良事件(AEs)。
共28项研究符合纳入标准,涉及406例患者。这406例患者均为少突胶质细胞瘤;对于组织学类型混杂的研究队列,仅提取并分析其中少突胶质细胞瘤的特异性数据。在PCV队列中,不同研究报告的中位无进展生存期(PFS)差异较大,范围在24.3个月至8.4年之间;其中长期随访研究(如RTOG 9402和EORTC 26951)显示,患者的中位总生存期(OS)可长达14.7年。65-70%的患者因≥3级不良事件(主要为血液学或神经系统事件)停药。相比之下,III期INDIGO试验中Vorasidenib组患者的中位PFS为27.7个月(HR 0.39;95% CI 0.27–0.56;p<0.001),在14.2个月随访时中位OS尚未达到。≥3级不良事件发生率为22.8%,仅1-3%的患者因此停药,主要原因为无症状性转氨酶升高。来自扩大用药项目的早期真实世界数据同样支持其良好的耐受性。(附注:需要指出的是,不同研究间存在显著的异质性,其数据的绝对值不宜直接比较。具体而言,文献中PCV方案报告的长期生存数据主要基于PCV联合放疗的综合治疗模式;而关键IDH抑制剂研究[如INDIGO研究]的入组人群同时包含预后相对更差的IDH突变型星形细胞瘤患者。这些因素在解读和比较上述疗效数据时需予以考虑。)
PCV化疗目前仍是具有成熟生存数据支持的标准系统治疗方案,而IDH抑制剂作为一种机制明确的靶向治疗替代方案,早期疗效确切且安全性显著更优。由于研究设计差异及IDH抑制剂长期OS数据有限,目前尚无法对这两类治疗方案开展直接对比。未来需开展前瞻性头对头试验以明确最佳治疗顺序,但在此之前,本研究为现阶段临床实践提供了推荐方案。
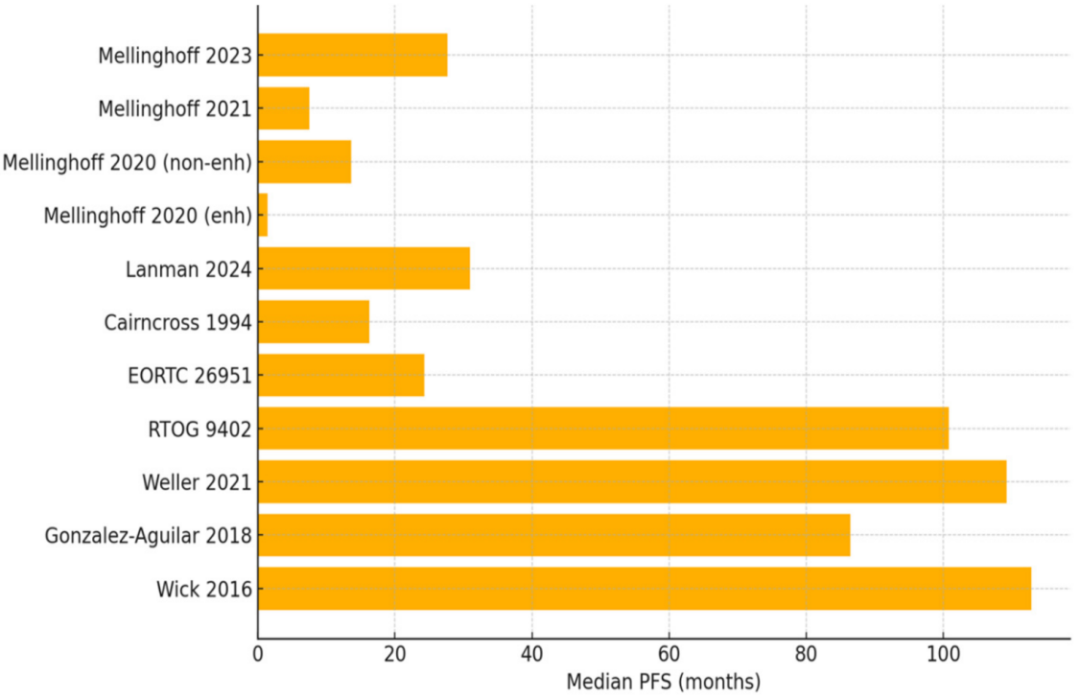 图8:对比IDH抑制剂与PCV方案在IDH突变型少突胶质细胞瘤患者中的中位PFS
图8:对比IDH抑制剂与PCV方案在IDH突变型少突胶质细胞瘤患者中的中位PFS
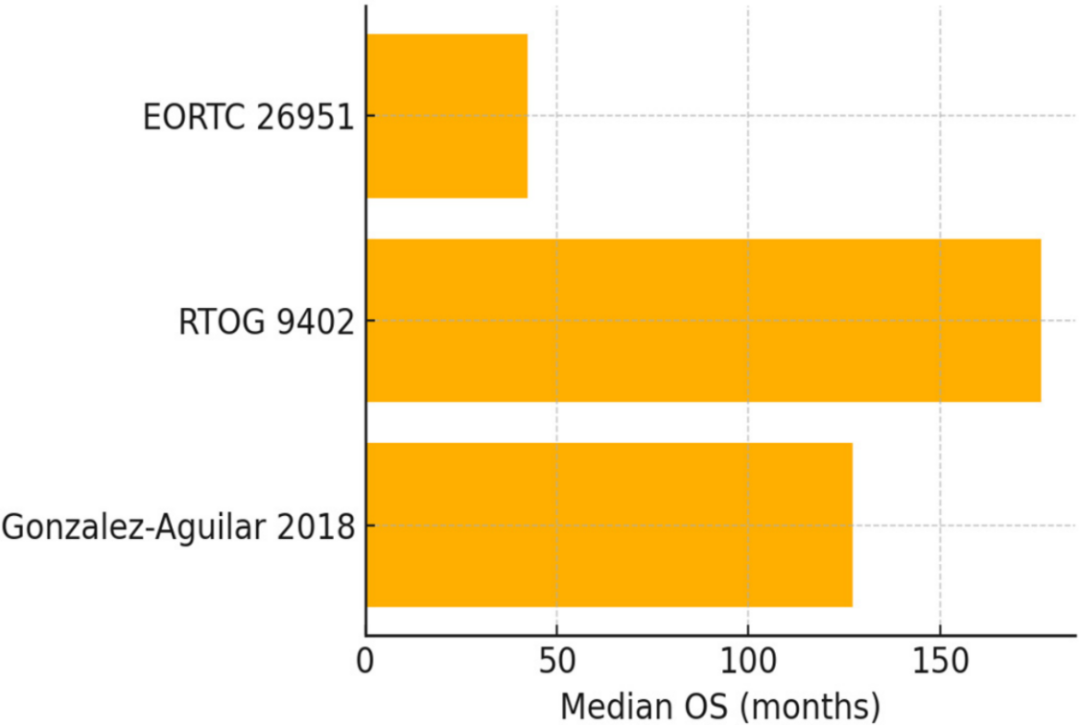 图9:基于PCV的治疗方案治疗IDH突变型少突胶质细胞瘤的研究中的中位OS
图9:基于PCV的治疗方案治疗IDH突变型少突胶质细胞瘤的研究中的中位OS
重庆大学附属肿瘤医院神经外科科主任
主要从事神经肿瘤的手术治疗及机制学研究
中国抗癌协会肿瘤神经病学专委会副主任委员
中国抗癌协会神经肿瘤专委会常委
中国临床肿瘤学会(CSCO)神经肿瘤专委会常委
中国抗癌协会脑胶质瘤专委会委员
中国医师协会脑胶质瘤专委会手术学组委员
中国医学装备协会神经外科分会委员
中国解剖学会神经解剖专委会委员
重庆市医师协会神经外科分会副会长
重庆市医师协会脑胶质瘤专委会副主任委员
重庆抗癌协会脑胶质瘤专委会主任委员
重庆抗癌协会神经肿瘤专委会副主任委员
重庆市医药生物技术协会神经外科专委会主任委员
1.Cloughesy TF, van den Bent MJ, Touat M, et al. Vorasidenib in IDH1-mutant or IDH2-mutant low-grade glioma (INDIGO): secondary and exploratory endpoints from a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2025;26(12):1665-1675.
2.Karschnia P, Young JS, Wijnenga MMJ, et al. A prognostic classification system for extent of resection in IDH-mutant grade 2 glioma: an international, multicentre, retrospective cohort study with external validation by the RANO resect group. Lancet Oncol. 2025;26(12):1638-1650.
3.Park JW, Kwak J, Kim KW, et al. IDH-mutant gliomas arise from glial progenitor cells harboring the initial driver mutation. Science. 2026;391(6781):eadt0559.
4.Colman H, Lombardi G, Wong ET, et al. STELLAR: Phase III, Randomized, Open-Label Study of Eflornithine Plus Lomustine Versus Lomustine Alone in Patients With Recurrent Grade 3 Astrocytoma. J Clin Oncol. Published online December 1, 2025.
5.Rossi J, Picca A, Santonocito OS, et al. Advances in the management of patients with IDH-mutant glioma. Oncologist. 2025;30(12):oyaf391.
6.Duran G, Pichardo-Rojas D, Ali AH, et al. Comparing Isocitrate Dehydrogenase Inhibitors with Procarbazine, Lomustine, and Vincristine Chemotherapy for Oligodendrogliomas. Cancers (Basel). 2025;17(23):3880. Published 2025 Dec 4.
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-VORAS-CN-202601-00009











 苏公网安备32059002004080号
苏公网安备32059002004080号


