胃癌是全球严峻的公共卫生挑战。在中国,胃癌负担尤为沉重,且由于早期筛查普及度受限,约 65% 的患者确诊时已处于晚期,预后极差。尽管曲妥珠单抗联合化疗已确立为 HER2 阳性晚期胃癌的一线标准治疗,但患者在治疗失败后的二线选择长期匮乏。虽然近期德曲妥珠单抗(T-DXd)打破了僵局,但临床仍迫切需要更多高效且安全性更优的精准靶向方案。
近日,由中国人民解放军总医院徐建明教授团队牵头开展的一项多中心、随机、双盲、III期临床试验(KC-WISE)取得重大突破,成果发表于国际顶尖肿瘤学期刊Annals of Oncology(IF: 65.4,2026年最新接收)。该研究确证了新型HER2双特异性抗体安尼妥单抗(Anbenitamab,KN026)联合化疗在经曲妥珠单抗治疗失败的HER2阳性晚期胃癌患者中的显著生存获益,成功将中位总生存期(OS)延长至近20个月,与安慰剂联合化疗相比的OS HR仅0.29,为此类难治性胃癌的后线治疗确立了新的里程碑。

解放军总医院第一医学中心消化肿瘤科 主任 博士生导师
中国抗癌协会大数据与真实世界专业委员会主任委员
中国研究型医院 肿瘤学专业委员会 副主任委员
中国临床肿瘤学会胃肠胰腺神经内分泌肿瘤专业委员会 首任主任委员
研究背景
HER2阳性晚期胃癌的治疗策略近年来持续演进。ToGA研究奠定了化疗联合曲妥珠单抗靶向治疗的一线标准地位,近期的KEYNOTE-811研究则开启了“靶免化”三联的新时代。然而,一线方案失败后的二线治疗一直是临床“洼地”。虽然DESTINY-Gastric04研究证实了抗体偶联药物(ADC)德曲妥珠单抗(DS-8201)相较于化疗的优效性,但临床仍迫切需要更多高效且安全性优异(尤其是肺毒性风险更低)的国产方案。
安尼妥单抗是一种创新的HER2靶向双特异性抗体,可同时结合HER2胞外域的两个不同表位(结构域IV和结构域II),这种独特的机制能实现更全面的信号阻断,诱导更强的受体聚集及内吞降解。此前,KC-WISE 01(II期)研究已初步显示出其良好的抗肿瘤活性。基于此,本次公布的III期研究(KC-WISE, NCT05427383)则旨在通过更大样本量随机对照设计,正式确证安尼妥单抗联合化疗对比单纯化疗在后线人群中的生存获益。
研究方法
本研究为一项多中心、随机、双盲、安慰剂对照的III期临床试验,在中国51家临床中心同步开展。入组标准包括:年龄为18岁及以上;组织学证实的局部晚期、复发或转移性GC/GEJ腺癌;HER2阳性(IHC 3+,或 IHC 2+/FISH+);此外,患者必须经历过含曲妥珠单抗方案的治疗失败,这包括在辅助/新辅助治疗期间或结束后6个月内出现的疾病进展。基础生理指标如ECOG PS评分需为0或1,左室射血分数(LVEF)需不低于50%(或正常值低限)。
符合条件的患者按1∶1的比例随机分配接受:
安尼妥单抗组:安尼妥单抗30mg/kg,静脉输注,Q3W;
对照组:安慰剂,静脉输注,Q3W。
两组均联合研究者选定的化疗方案(紫杉醇175 mg/m² d1、多西他赛 75 mg/m² d1或伊立替康125 mg/m² d1 + d8,Q3W)。治疗持续直至疾病进展、毒性不可耐受、患者撤回知情同意、开始新的抗肿瘤治疗、失访、死亡或研究终止(以先发生者为准)。
主要终点为独立评审委员会(IRC)根据RECIST 1.1标准评估的无进展生存期(PFS)和总生存期(OS);次要研究终点包括其他疗效指标,如IRC和研究者评估的总缓解率(ORR)、缓解持续时间(DoR)和疾病控制率(DCR),研究者评估的PFS、安全性和免疫原性。
研究结果
患者特征与治疗暴露
自2023年1月13日至2025年4月3日,共入组188例患者(占预设总人群的76.4%),安尼妥单抗组95例,对照组93例,其临床特征呈现出典型的晚期、难治性特点。截至 2025 年 4 月 3 日,中位随访时间在安尼妥单抗和安慰剂组分别为 9.7和9.8 个月。
基线特征显示,患者以HER2 IHC 3+为主(约 82%),ECOG PS 1分者占比超过80%。约16%的患者既往已接受过≥2线治疗,提示本研究纳入了较高比例的难治人群。此外,对照组中存在3个及以上器官转移的患者比例(37%)略高于安尼妥单抗组(24%)。
治疗暴露方面,安尼妥单抗组的中位治疗持续时间为6.5个周期,显著长于对照组(安慰剂)的3.0个周期。在联合化疗方案中,安尼妥单抗组联合紫杉醇、多西他赛及伊立替康的中位周期数分别为7.0、8.0和5.0,而对照组仅为4.0、4.0和2.0。安尼妥单抗组共有约44%的患者发生了剂量下调,45%出现给药中断,11%治疗停用,其比例高于对照组(分别为 31% 、32%和2%),这一差异主要源于安尼妥单抗组获得了显著更长的药物暴露时间与观察窗口期,从而增加了积累毒性导致的剂量调整概率。截至数据截止日,安尼妥单抗组共有49例患者已停止治疗,主要原因为疾病进展(35 例,占该组停药人数的 71.4%)。
疗效
OS与PFS实现全线突破。中期分析结果显示,安尼妥单抗联合化疗展现出极其强劲的生存获益。
PFS:对照组IRC评估的中位PFS仅为2.7个月,而安尼妥单抗组显著延长至7.1个月。疾病进展或死亡风险降低75%(HR 0.25; 95% CI 0.17~0.39; P<0.0001)(图1A)。研究者评估的PFS与 IRC保持高度一致(HR 0.23; 95% CI 0.15~0.35; P<0.0001)(图1B)。
OS:安尼妥单抗组中位OS长达19.6个月(95% CI 15.0个月~不可评估),显著优于安慰剂组的11.5个月(95% CI 6.5~14.4个月)。死亡风险显著降低71%(HR 0.29; 95% CI 0.17~0.50; P<0.0001)(图1C)。
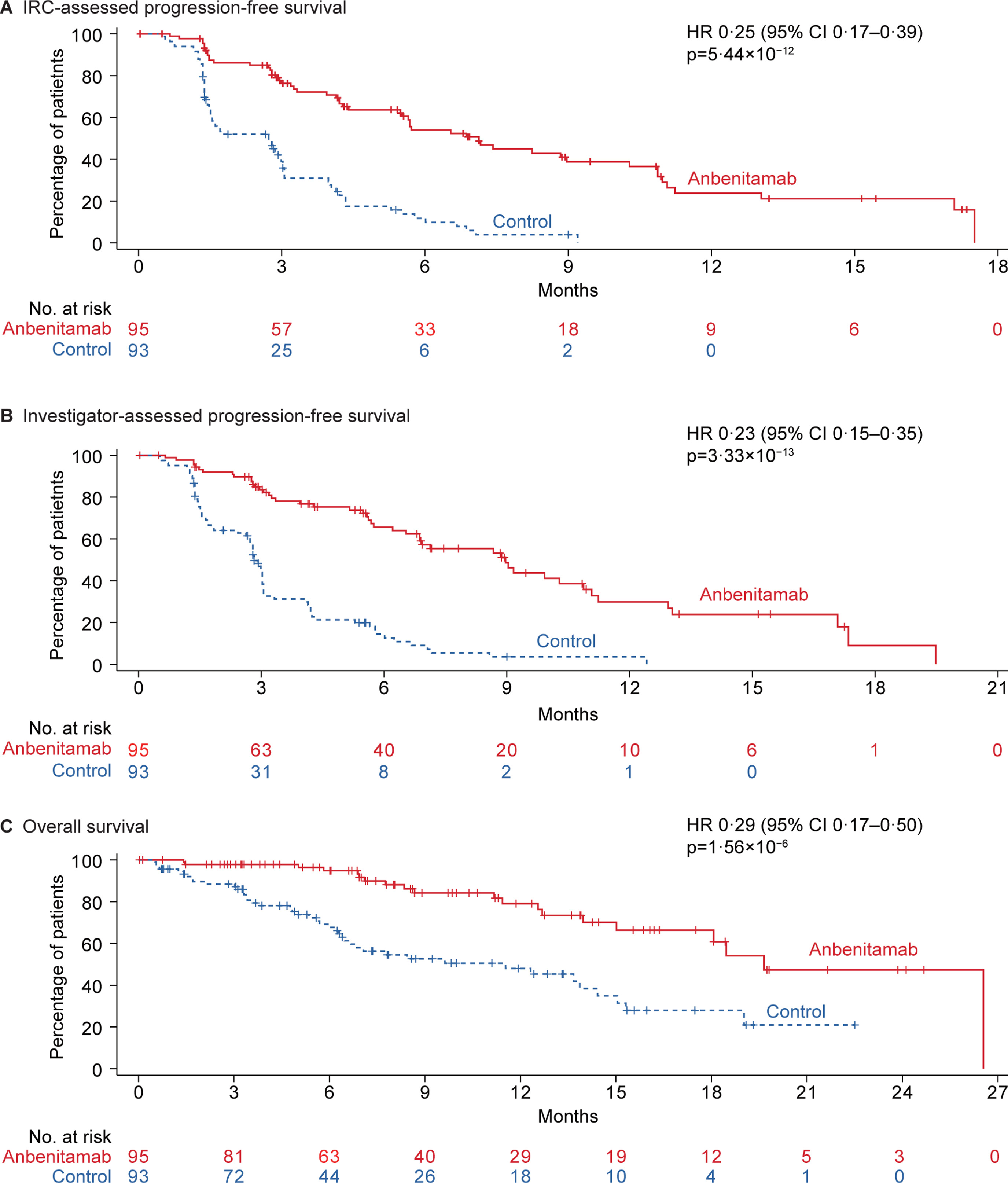
图1. (A)IRC评估的PFS、(B)研究者评估的PFS和(C)OS结果
ORR:安尼妥单抗组IRC评估的ORR高达56%,远高于对照组的11%。此外,DCR也实现了倍增(80% vs 42%)。
安全性
间质性肺病(ILD)风险极低,耐受性良好。两组≥3级治疗相关不良事件(TRAE)发生率分别为60%和45%。最常见的血液学毒性包括中性粒细胞减少(30%)、白细胞减少(21%)和贫血(18%),多归因于化疗药物作用,安全性特征与化疗及既往单药研究一致。特别关注的心脏毒性方面,两组均观察到为3%患者出现LVEF下降,且安尼妥单抗组未观察到ILD病例,提示该联合方案具有极高的安全性窗口。
研究结论
KC-WISE研究的预设中期分析确证:安尼妥单抗联合化疗在既往曲妥珠单抗治疗失败的HER2阳性晚期胃癌患者中,能够提供统计学显著且具有临床意义的OS、PFS及ORR获益。该研究不仅验证了HER2双抗联合化疗的可靠性,更以OS HR 0.29这一极其罕见的获益幅度,为后线胃癌治疗树立了新的标杆。
讨论
KC-WISE 研究的成功不仅在于生存数据的突破,更在于其通过机制创新解决了临床耐药痛点。首先,安尼妥单抗独特的双表位架构(同时锚定 HER2 的 ECD2 与 ECD4)能诱导更强效的受体聚簇与内吞降解,并利用强效的 ADCC 效应有效对冲曲妥珠单抗经治后常见的 HER2 表达下调现象。其次,尽管对照组受高比例多器官转移及后线治疗等高危基线影响表现稍弱,但安尼妥单抗在各亚组中稳健的HR值确证了其疗效的普适性。相比 ADC 类药物在全球研究(DESTINY-Gastric04)中约13.9%的ILD风险,安尼妥单抗凭借“零ILD”的卓越表现,为心肺储备有限的患者提供了更优的安全窗口。综上,安尼妥单抗联合化疗不仅确立了曲妥珠单抗失败后的二线治疗的潜力,更通过 PFS、OS 与 ORR 的全方位改善,为后续挑战包括含雷莫西尤单抗方案在内的更新标准疗法奠定了坚实的循证医学基石。
Liu R, Zhao J, Zhang R, et al. Anbenitamab in previously treated HER2-positive gastric cancer (KC-WISE): pre-specified interim analysis of a randomized, phase III clinical trial. Annals of Oncology (2026). DOI: 10.1016/j.annonc.2026.01.006.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


