基于循证医学证据的诊疗模式重塑了现代医学的诊疗路径,肺癌作为研究更新较为迅速的疾病,集中体现了精准医学的诊疗进展。【肿瘤资讯】定期总结顶级期刊发表的最新研究进展,与读者分享,以帮助同行提高临床诊疗水平,了解前沿进展。
斯鲁利单抗联合化疗±HLX-04在局部晚期或转移性非鳞非小细胞肺癌(NSCLC)患者中的疗效及安全性:一项随机、双盲、多中心、多队列临床研究(ASTRUM-002)
来源:The Lancet Respiratory Medicine
研究背景
斯鲁利单抗是一款针对PD-1的免疫检查点抑制剂,HLX-04是一款贝伐珠单抗的生物类似物,本研究旨在探索斯鲁利单抗±HLX-04以及含铂双药化疗,在非鳞NSCLC患者中的疗效及安全性。
研究方法
这是一项随机、双盲、多中心、III期、三队列临床研究,纳入年龄18~75周岁的初治局部晚期或转移性非鳞NSCLC患者,患者不携带EGFR/ALK/ROS1等驱动基因变异。符合入组标准的患者,按1:1:1的比例随机分配接受斯鲁利单抗4.5 mg/kg联合HLX-04 15mg/kg联合培美曲塞/卡铂,或斯鲁利单抗联合化疗或单纯化疗。主要研究终点为独立评审委员会评估的无进展生存期(PFS),次要研究终点包括总生存期(OS)及安全性。
研究结果
最终四药组、三药组和两药组分别入组212例,214例和210例患者。数据分析时,三组中位随访时间分别为23.4个月、23.1个月和23.0个月,中位PFS分别为12.6个月、11.0个月和5.6个月。三药组和双药组相比,HR=0.55,P<0.0001;四药组与三药组相比,差异无统计学意义,HR=0.86,P=0.25。三组治疗相关严重不良反应发生率分别为39%、37%和24%,3级及以上治疗相关不良反应发生率分别为71%、66%和57%。因治疗相关不良反应而导致患者死亡的比例分别为5%、2%和3%。
研究结论
斯鲁利单抗联合化疗相较单纯化疗在局部晚期或转移性非鳞NSCLC患者的一线治疗中具有更好的PFS,HLX-04的加入并未带来进一步获益。
研究解读
该研究为斯鲁利单抗在非鳞NSCLC患者中的应用提供了高级别循证医学证据,与其他获批的PD-1抑制剂共同为临床治疗提供了新的治疗选择。本研究的另外一个亮点是设计了四药组合方案。临床中,在化疗联合PD-1抑制剂的基础上是否应当进一步联合抗血管生成药物存有争议。该研究中,在斯鲁利单抗的基础上进一步联合HLX-04并未给患者带来进一步获益。结果提示,对晚期非鳞NSCLC患者而言,联合PD-1抑制剂已经足够,进一步联合HLX-04非但未能给患者带来获益,反而增加了不良反应。
Olomorasib联合帕博利珠单抗治疗KRAS G12C突变NSCLC患者的疗效及安全性
来源:Journal of Thoracic Oncology
研究背景
免疫为基础的治疗方案是携带KRAS G12C突变NSCLC患者的一线标准治疗,但疗效有待进一步提高。既往研究中,KRAS G12C抑制剂与免疫治疗的联合主要受限于安全性。本研究报道了Loxo-RAS-2001研究中,Olomorasib联合帕博利珠单抗治疗KRAS G12C突变NSCLC患者的疗效及安全性。
研究方法
这是一项I/II期临床研究,患者经病理学诊断确认且携带KRAS G12C突变,无论既往是否接受过治疗及PD-L1表达水平均纳入本研究。符合入组标准的患者,接受50mg、100mg或150mg口服,每日两次的Olomorasib,联合标准剂量帕博利珠单抗治疗。主要研究终点为安全性及客观缓解率(ORR)。
研究结果
共99例患者入组,中位年龄68周岁,PD-L1表达0~49%和≥50%的患者占比分别为52%和36%。51%的患者接受一线治疗,93例接受50mg或100mg,每日两次Olomorasib联合帕博利珠单抗治疗。任何级别治疗相关不良反应发生率为81.7%,最常见的不良反应为腹泻34.4%,谷丙转氨酶升高24.7%,谷草转氨酶升高22.6%,3级及以上治疗相关不良反应发生率为33.3%,因不良反应而导致Olomorasib剂量降低及治疗终止的患者分别为20.4%和6.5%。91例疗效可评估的人群,中位随访时间12.5个月,ORR为57.1%,一线治疗的ORR为73.9%,PD-L1≥50%患者的ORR为90%。
 研究摘要
研究摘要
研究结论
无论患者PD-L1表达水平如何,Olomorasib联合帕博利珠单抗在携带KRAS G12C突变的NSCLC患者中,显示出可管理的安全性及良好的抗肿瘤活性,且这一联合方案在PD-L1高表达患者中效果更优。
研究解读
目前,多款KRAS G12C抑制剂已经获批临床后线应用,但整体ORR约50%,中位PFS约5-8个月。对于携带KRAS G12C突变的晚期肺癌患者而言,当前的一线标准治疗为免疫检查点抑制剂联合含铂双药化疗,中位PFS约10个月,ORR约60%。因此,KRAS G12C抑制剂的一线布局需要与其他治疗策略进行合理联合。其中,与免疫检查点抑制剂联合是考虑方向之一。既往的联合方案合均存在明显的安全性问题,尤其是肝脏毒性问题会导致进一步的研究受到限制。Olomorasib是一款新型KRAS G12C抑制剂,联合帕博利珠单抗显示出良好的抗肿瘤活性,尤其是针对PD-L1高表达患者。然而,PD-L1高表达患者接受免疫单药的疗效较好,联合方案是否能带来额外获益,仍需随机对照临床研究的进一步验证。
埃万妥单抗联合兰泽替尼在EGFR非经典突变肺癌患者中的疗效及安全性:CHRYSALIS-2研究
来源:Journal of Clinical Oncology
研究背景
埃万妥联合兰泽替尼已获批一线治疗EGFR经典突变NSCLC患者,但这一联合方案在非经典突变中的疗效目前尚不明确。本研究报道了CHRYSALIS-2中,该联合方案在非经典突变患者中的疗效及安全性。
研究方法
研究纳入局部晚期或转移性NSCLC患者,患者携带非经典突变,主要包括G719X、S768I、L861Q,既往治疗线数≤2线。若患者接受过一代或二代EGFR-TKI治疗,允许入组;合并存在20插入突变,19del或21L858R突变的患者不允许入组。符合入组标准的患者接受埃万妥单抗(1050mg,静脉,前4周每周一次,随后每两周一次)联合兰泽替尼(口服,240mg,每日一次)。主要研究终点为研究者评估的ORR。
研究结果
105例患者最终接受研究药物治疗,初治和经治人群分别为49例和56例患者。初治和经治患者中,基线分别有27%和36%的患者有脑转移。经治患者中,61%的患者接受阿法替尼治疗,16%的患者接受其他一代或二代药物治疗,13%的患者接受含铂双药化疗,11%的患者接受阿法替尼联合含铂双药化疗。在初治和经治人群中,18G719X占比分别为55%和57%,21L861X突变占比分别为24%和27%,20S768I占比分别为27%和20%,是最常见的三种突变。初治和经治人群的中位随访时间分别为17.3个月和15.4个月,ORR分别为57%和48%,中位缓解持续时间(DoR)分别为20.7个月和11.0个月,中位PFS分别为19.5个月和7.8个月,中位OS分别为未达到和22.8个月,1年OS率分别为77%和34%。
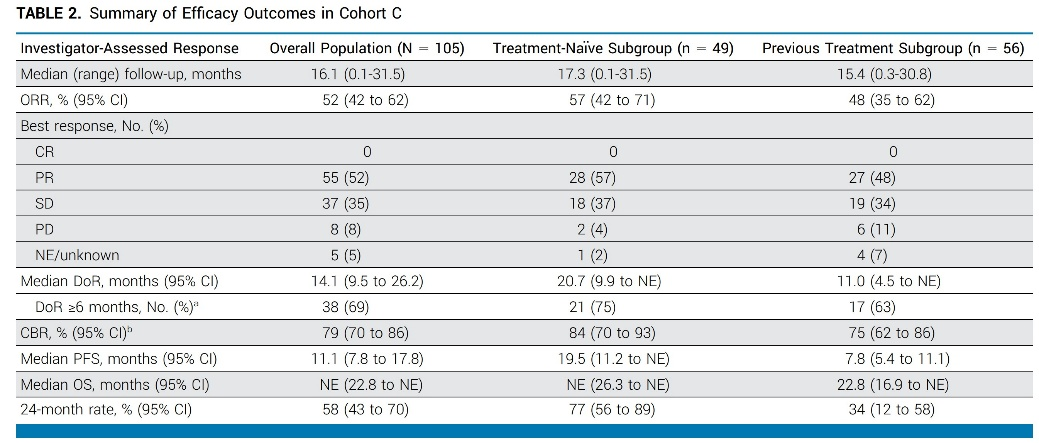
全组任何级别、全因不良反应发生率为100%,3级以上全因不良反应发生率为70%,严重不良反应发生率为50%,因不良反应而导致治疗中断、剂量降低以及永久性终止治疗的比例分别为70%、50%和28%。较常见的3级及以上不良反应包括皮疹13%、甲沟炎5%、口腔炎2%、低白蛋白血症8%、外周水肿3%、输液反应4%、乏力7%、肺栓8%、肺炎10%。
研究结论
在携带EGFR非经典突变的患者中,埃万妥联合兰泽替尼显示出有临床意义的抗肿瘤活性,没有新的安全性信号出现。
研究解读
EGFR非经典突变主要指发生在18-21号外显子中,除敏感突变(19del、L858R)、20号外显子插入突变(20ins)及T790M突变以外的其他突变。针对这部分患者,二代药物具有更好的疗效,但其对野生型EGFR的阻断作用常导致明显的不良反应;三代EGFR-TKI虽然疗效略差,但具有更好的安全性,因此也是临床常见的用药选择。在MARIPOSA研究中,与奥希替尼单药相比,埃万妥联合兰泽替尼在19del和21L858R突变患者中显示出更优的PFS和OS,但是在非经典突变中的疗效不明。本研究中,这一联合方案无论在初治还是经治人群都显示出良好的抗肿瘤活性。值得注意的是,尽管该联合方案在初治患者中的中位PFS接近20个月,但在单臂临床研究中,ORR往往能更直接、客观地反映药物的抗肿瘤活性,因此对PFS数据的解读需保持审慎。此外,针对经治患者,该联合方案显示出近50%的ORR,提示可以作为耐药后的治疗选择。
PD-L1抑制剂联合化疗新辅助治疗I~III期小细胞肺癌的疗效及安全性
文献来源:Cell Discovery
研究背景
免疫检查点抑制剂联合化疗新辅助治疗NSCLC患者已成为当前标准治疗,本研究旨在探索免疫联合化疗新辅助治疗小细胞肺癌的疗效及安全性。
研究方法
研究纳入I~III期小细胞肺癌患者,术前给予4周期 TQB-2450联合化疗,随后进行手术或放疗,术后给予1年的免疫维持治疗。主要研究终点为ORR。
研究结果
40例患者接受治疗并纳入分析。新辅助治疗后,21例患者接受后续手术治疗,14例患者后续接受放疗,5例患者在诱导治疗阶段撤销知情同意。主要研究终点ORR为92.5%,经过中位25.8个月的随访,全组患者的中位EFS为16.2个月,中位OS未达到。21例患者接受手术,Ib期、IIb期、IIIa期、IIIb期、IIIc期占比分别为4.8%、0%、57.1%、28.6%和9.5%。主要病理学缓解和完全病理学缓解率分别为61.9%和42.9%。2年EFS率和2年OS率分别为61.9%和85.7%,9例淋巴结为N1的患者接受手术,2年EFS率和OS率分别为66.7%和88.9%。
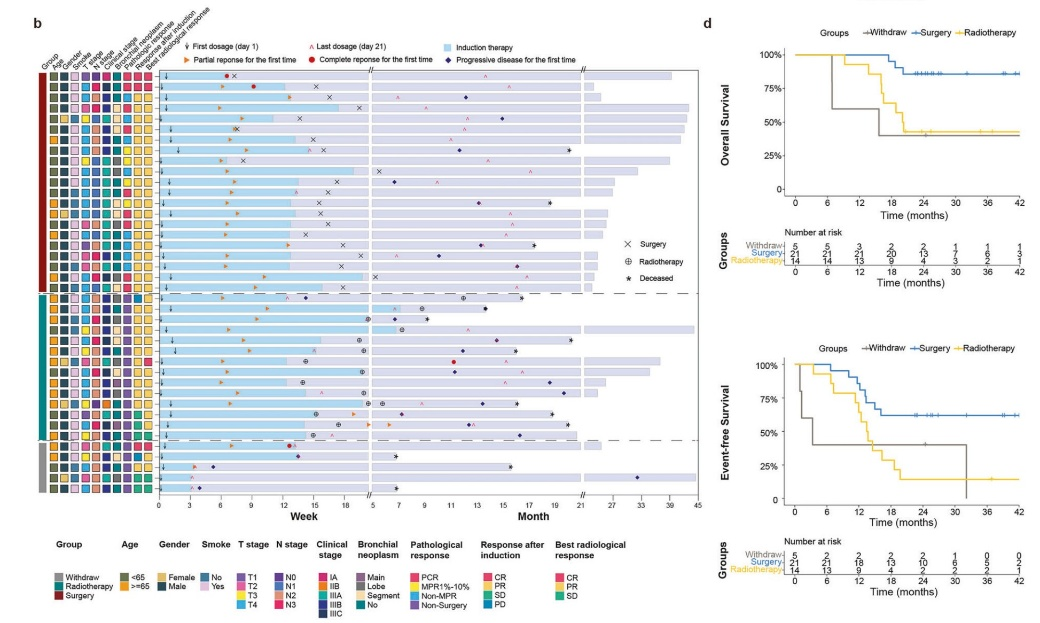
研究结论
针对I-III期小细胞肺癌患者,采用新辅助治疗序贯手术切除的治疗模式具有临床可行性。
研究解读
对于不可手术的局限期小细胞肺癌患者,同步放化疗是当前的主要治疗选择。鉴于小细胞肺癌高度侵袭性的生物学行为,传统观点常将其视为一种系统性疾病,临床实践多侧重于内科治疗,导致围手术期研究相对匮乏。本研究通过一项单臂、小样本探索性试验发现,针对部分可手术患者,借鉴NSCLC围手术期理念积极给予围手术期治疗,有望改善患者预后。
DOI:10.1016/S2213-2600(25)00263-2
DOI:10.1016/j.jtho.2025.11.018
DOI :10.1200/JCO-24-02835
DOI:10.1038/s41421-025-00838-5
排版编辑:肿瘤资讯-HYF











 苏公网安备32059002004080号
苏公网安备32059002004080号


