慢性髓系白血病(CML)是一种起源于骨髓造血干细胞的恶性增殖性疾病,酪氨酸激酶抑制剂(TKI)的问世彻底改变了其治疗格局,使患者生存期显著延长。如今,在TKI治疗时代,CML管理的核心目标已从单纯控制疾病转变为实现持续深度分子学缓解(DMR),进而争取无治疗缓解(TFR)——即通过治疗大幅降低白血病负荷后停药,且无需重启治疗的持续缓解状态 。
然而,针对以TFR为目标的最佳一线TKI选择,临床仍存在争议。第二代TKI对BCR::ABL1融合基因的抑制作用更强、选择性更高,能更快更深地降低疾病负荷,理论上更适合作为追求TFR的一线方案。但这类药物可能存在的中长期脱靶效应(如心血管风险),使其在合并基础疾病的老年患者中应用受限。
另一种策略是先采用伊马替尼一线治疗,仅对未达最佳应答的患者早期切换至第二代TKI,既为部分患者保留了安全性优势,又试图通过换药弥补疗效不足。此前缺乏前瞻性研究直接比较这两种策略的优劣,SUSTRENIM研究应运而生,旨在明确哪种方案能更有效地诱导深度分子应答,为后续TFR创造条件。
近日,发表于Leukemia杂志的SUSTRENIM研究首个共同主要终点结果公布:在新诊断慢性期CML(CP-CML)患者中,以TFR为目标时,尼洛替尼一线治疗相比伊马替尼一线治疗联合早期换药策略(未达最佳应答时切换至尼洛替尼),能更有效地诱导DMR,为患者后续追求TFR奠定更坚实的基础。

SUSTRENIM研究是是一项多中心、前瞻性、随机对照Ⅱ期临床试验,于2016年11月启动,纳入意大利53家中心和荷兰8家中心的新诊断CP-CML患者,旨在比较尼洛替尼一线治疗与伊马替尼一线治疗联合早期换药策略(未达最佳应答时切换至尼洛替尼)在新诊断CP-CML患者中的疗效。
患者按1:1比例随机分配至尼洛替尼组(NIL组)或伊马替尼组(IM 组),分层因素包括Sokal风险评分(高危 vs 中低危)和国家。研究设定两个序贯共同主要终点:一是24个月时的MR4.5应答率(本文报道结果),二是进入TFR阶段后12个月仍维持无分子复发的持续TFR率。
患者基线特征
最终448例患者符合条件并完成随机分组,其中尼洛替尼组228例,伊马替尼组220例,患者中位随访时间45.9个月(范围1.7~73个月),所有患者均完成至少24个月随访。
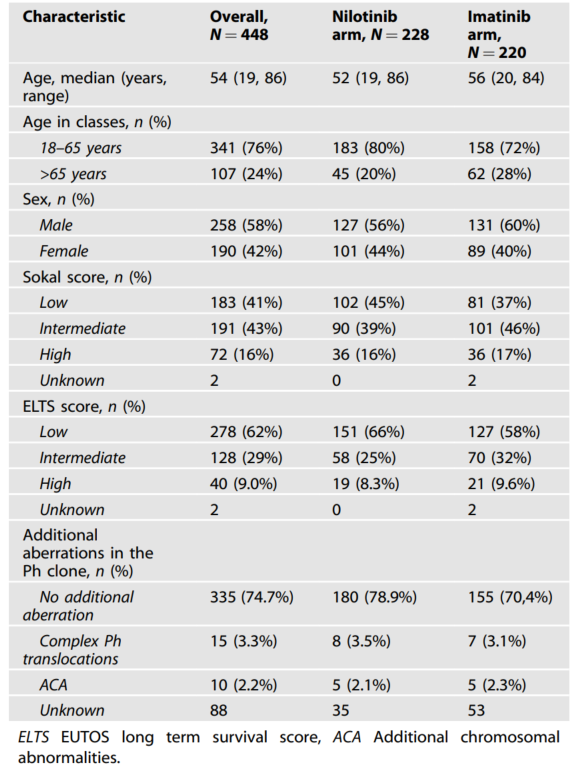
两组患者基线特征均衡可比:整体中位年龄54岁(范围19~86岁),尼洛替尼组和伊马替尼组≥65岁患者占比分别为20%和28%;男性占比分别为56%和 60%;Sokal高危患者占比均为16%左右;ELTS高危患者占比分别为8.3%和9.6%;绝大多数患者(74.7%)表现为典型t(9;22)易位,额外染色体异常发生率仅2.2%(表1)。
表1. 患者基线特征
伊马替尼组换药情况
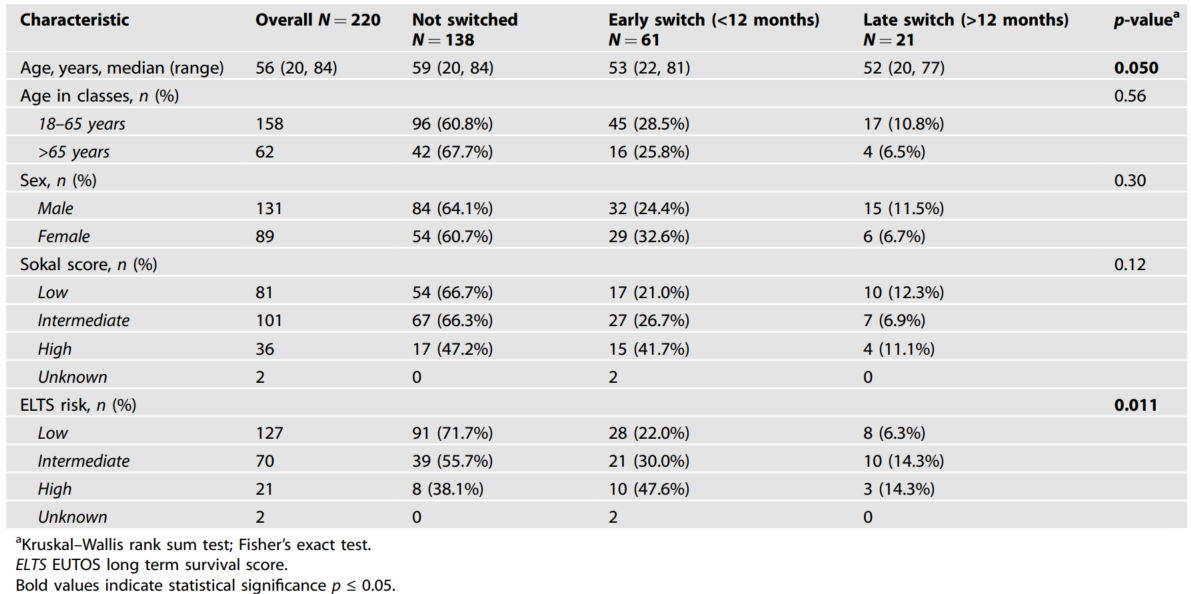
伊马替尼组中,82例患者(37.2%)因未达最佳应答(n=65)或治疗不耐受(n=17)转换至尼洛替尼治疗。其中74%(61 例)的换药发生在治疗前12个月,26%(21例)发生在后续6个月内。
基线风险评分与换药率密切相关:伊马替尼组中,Sokal高危患者换药率为52.8%(P=0.05),ELTS高危患者换药率高达61.9%(P=0.01),显著高于低危患者;而年龄、性别、BCR::ABL1转录本类型对换药概率无显著影响(表2)。
表2. IMA组(n=220)中因治疗非最佳应答而转为NIL治疗的患者的特征
深度分子学缓解(MR4.5)结果
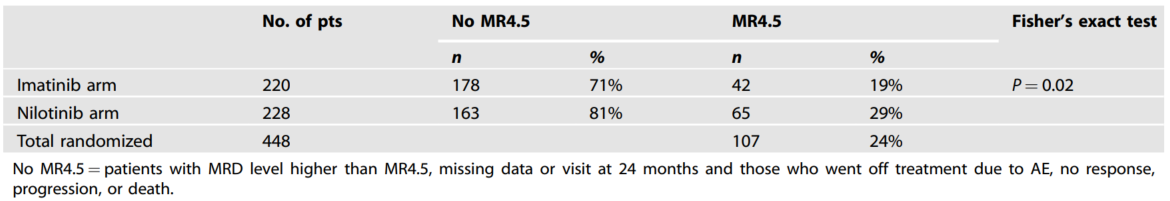
24个月时,448例患者中共有107例(24%)达到MR4.5缓解,尼洛替尼组缓解率显著高于伊马替尼组(29% vs 19%,P=0.02)(表3)。
表3. 基于意向治疗分析,比较两个随机化组之间24个月随访时的MR4.5缓解率
进一步分析伊马替尼组内不同亚组的应答情况:116例维持伊马替尼治疗且达早期最佳缓解的患者中,24%达到MR4.5;58例早期换药(<12个月)患者中,仅17%达到MR4.5;20例晚期换药(>12个月)患者中,20%达到MR4.5,亚组间无显著差异(P=0.59)(表4),提示即使早期换药,也难以弥补与尼洛替尼一线治疗的疗效差距。
表4.根据早期或晚期转为NIL治疗,随机分配至IM组的患者在24个月随访时的MR 4.5率

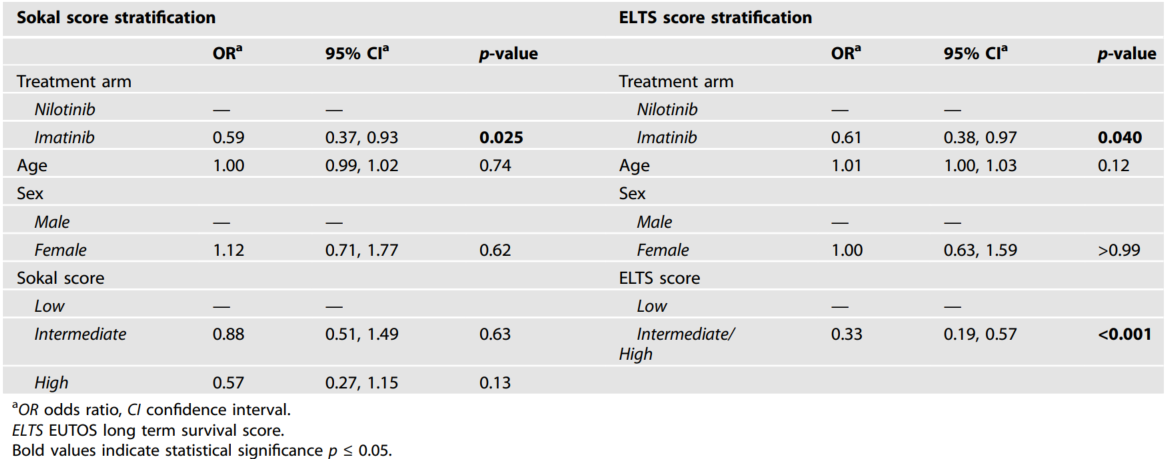
多因素分析显示,治疗组和ELTS风险评分是预测24个月MR4.5缓解的独立因素:与尼洛替尼组相比,伊马替尼组的MR4.5缓解比值比为0.61(95%CI:0.38-0.97,P=0.04);ELTS中高危患者的缓解比值比仅为低危患者的0.33(95%CI:0.19-0.57,P<0.001)(表5)。
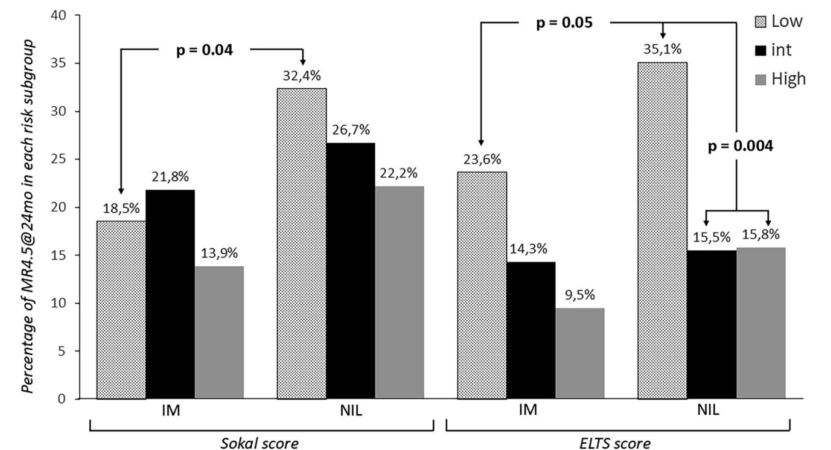
表5. 根据Sokal或ELTS风险评分分层的患者在多变量分析中24个月随访时达到MR 4.5的比值比
 值得注意的是,老年患者(≥65岁)中,尼洛替尼组MR4.5缓解率(38%)显著高于伊马替尼组(18%,P=0.05),提示尼洛替尼在老年患者中同样具有疗效优势,且未观察到年龄对深度缓解率的不利影响。
值得注意的是,老年患者(≥65岁)中,尼洛替尼组MR4.5缓解率(38%)显著高于伊马替尼组(18%,P=0.05),提示尼洛替尼在老年患者中同样具有疗效优势,且未观察到年龄对深度缓解率的不利影响。
安全性结果
整体不良事件(AE)发生率:尼洛替尼组为64.9%,伊马替尼组为58.6%。不同系统不良事件分布存在差异:血液淋巴系统、肌肉骨骼系统、胃肠道及眼部不良事件在伊马替尼组更常见;皮肤及神经系统不良事件在尼洛替尼组(包括伊马替尼换药后)更常见。
3~4级严重不良事件发生率两组相近(伊马替尼组29 例 vs 尼洛替尼组30例)。心血管相关不良事件在尼洛替尼暴露人群中更常见:伊马替尼组仅报告1例1级动脉狭窄和1例3级房室传导阻滞;尼洛替尼组及换药人群共报告7例动脉狭窄(含2例3级、1例4级卒中)、1例高血压、1例视网膜血管炎,以及7例心脏不良事件(含2例3级、1例4级心肌梗死)。两组各有1例因心肌梗死死亡,均未明确与药物直接相关。
老年患者与年轻患者的不良事件类型和发生率无显著差异,证实尼洛替尼在老年人群中具有可接受的安全性。
总结
SUSTRENIM 研究首个共同主要终点结果明确证实,以无治疗缓解为目标时,尼洛替尼一线治疗新诊断CP-CML患者的深度分子缓解率显著高于伊马替尼一线治疗联合早期换药策略。即使伊马替尼组中有37.2%的患者因未达最佳缓解或不耐受早期转换至尼洛替尼,仍未能缩小与尼洛替尼一线治疗在MR4.5缓解率上的差距,这一结果为临床治疗策略选择提供了关键参考。
从临床实践角度,该研究具有重要指导意义:首先,对于ELTS低危患者,无论年龄、性别如何,尼洛替尼一线治疗能带来较高的深度缓解率(35.1%),是追求TFR的优选方案;其次,伊马替尼一线治疗联合早期换药策略可作为ELTS中高危患者的备选,这类患者即使使用尼洛替尼一线治疗,深度应答获益也相对有限;此外,研究证实尼洛替尼在老年患者中疗效和安全性均可控,打破了“老年患者不宜使用第二代 TKI”的固有认知。
总体而言,SUSTRENIM研究为CML的个体化治疗提供了重要依据。尼洛替尼一线治疗凭借更优的深度分子缓解诱导能力,有望成为以无治疗缓解为目标的CP-CML患者(尤其是ELTS低危患者)的标准治疗选择;而伊马替尼联合早期换药策略可作为中高危患者的务实选择。
未来,随着第二个共同主要终点结果的公布,将进一步明确深度分子应答优势能否转化为更高的无治疗缓解率,为CML治疗目标的最终实现提供更完整的证据链。
Castagnetti F, Breccia M, Abruzzese E, et al. Nilotinib versus imatinib with early switch from imatinib to nilotinib to obtain treatment-free remission in newly diagnosed chronic myeloid leukemia patients: the analysis of the first co-primary endpoint: CHRONIC MYELOID LEUKEMIA[J]. Leukemia, 2025: 1-8.
排版编辑:mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


