日本国立癌症研究中心东医院消化道肿瘤科Kohei Shitara教授以“Beyond PD-1/PD-L1: Novel immunotherapy approaches”为题,系统阐述了消化道肿瘤领域免疫治疗的最新进展与未来方向。在PD-1/PD-L1抑制剂已成为多种消化道肿瘤标准治疗的当下,如何克服原发性和获得性耐药仍是临床亟待解决的核心问题。Shitara教授从增强效应细胞功能、重塑肿瘤微环境、扩展抗肿瘤免疫、重定向细胞毒性及过继性细胞治疗五大维度,全面梳理了新兴免疫治疗策略的机制原理与临床转化进展,为消化道肿瘤免疫治疗的精准化和个体化发展提供了重要参考。
免疫检查点抑制剂(ICI)在消化道肿瘤中的应用现状与耐药挑战
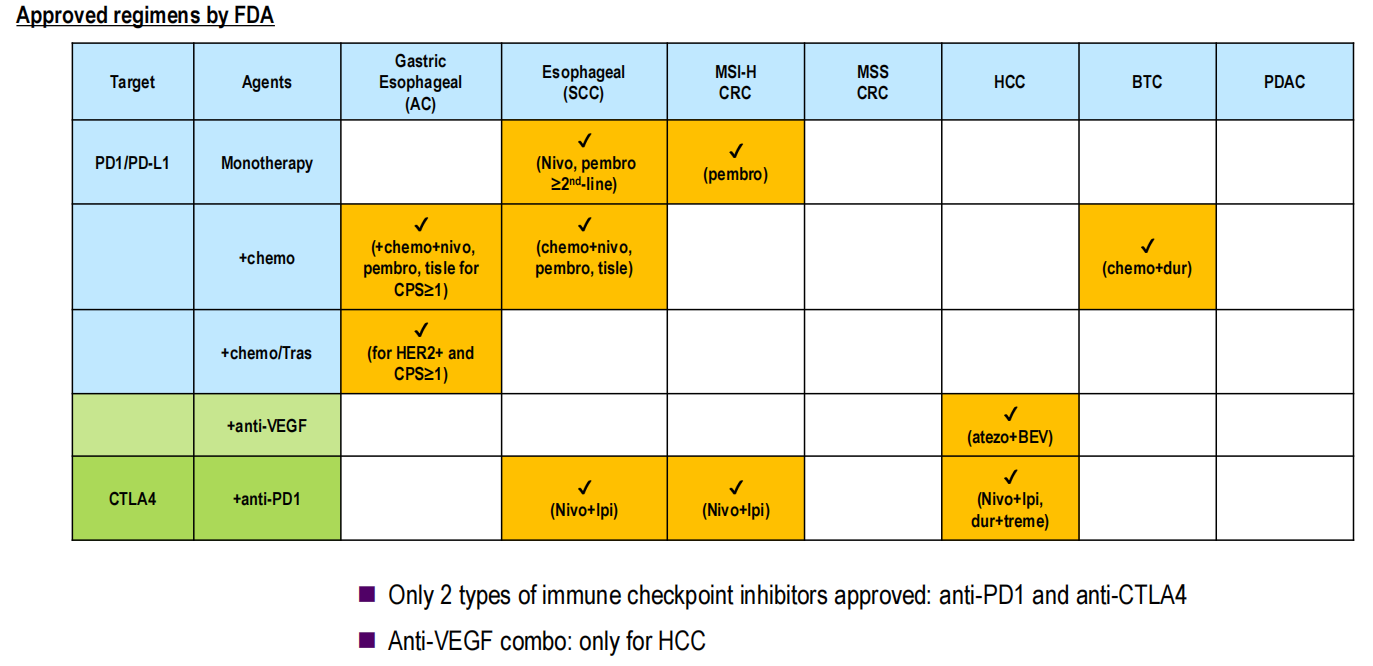
目前,美国FDA批准用于晚期消化道肿瘤的免疫检查点抑制剂(ICI)仅有两类,即抗PD-1/PD-L1抗体和抗CTLA-4抗体。免疫联合抗VEGF治疗目前仅在晚期肝细胞癌(HCC)中获得批准,而在微卫星稳定(MSS)结直肠癌和胰腺癌中,ICI的疗效仍十分有限。
针对ICI治疗耐药机制的研究揭示了多重影响因素。在胃癌/胃食管结合部癌中,PD-L1 CPS阴性、高血管生成或单核髓源性抑制细胞(mMDSC)基因特征、高间质或染色体不稳定(CIN)分型、高拷贝数改变、高可变启动子使用负荷、高PD-1+调节性T细胞(Treg)浸润(尤其伴RHOA突变或MYC扩增)、MSI-H肿瘤中的低肿瘤突变负荷(TMB)或PTEN突变伴高M2型巨噬细胞水平、以及高β-catenin/WNT信号通路激活等,均与免疫治疗获益降低相关。从肿瘤微环境角度可归纳为“免疫沙漠”(对应CPS<1)和“免疫排斥”(对应高血管生成、上皮间质转化及间质细胞富集)两种主要耐药表型。
结直肠癌(CRC)领域的免疫治疗面临较大挑战:(1)MSI-H仅占结直肠癌的4%~5%,POLE突变伴超高TMB的患者比例更低(约1%)。(2)相较于胃癌,MSS结直肠癌普遍呈现低CD8+肿瘤浸润淋巴细胞(TIL)和低IFN-γ基因特征。(3)CMS4分型(高TGF-β和高血管生成)表现为免疫排斥表型。(4)肝转移灶则富集Treg、巨噬细胞和CD11b+单核细胞,形成免疫抑制微环境,导致免疫治疗获益受限。
表1 消化道肿瘤领域克服ICI耐药的新策略
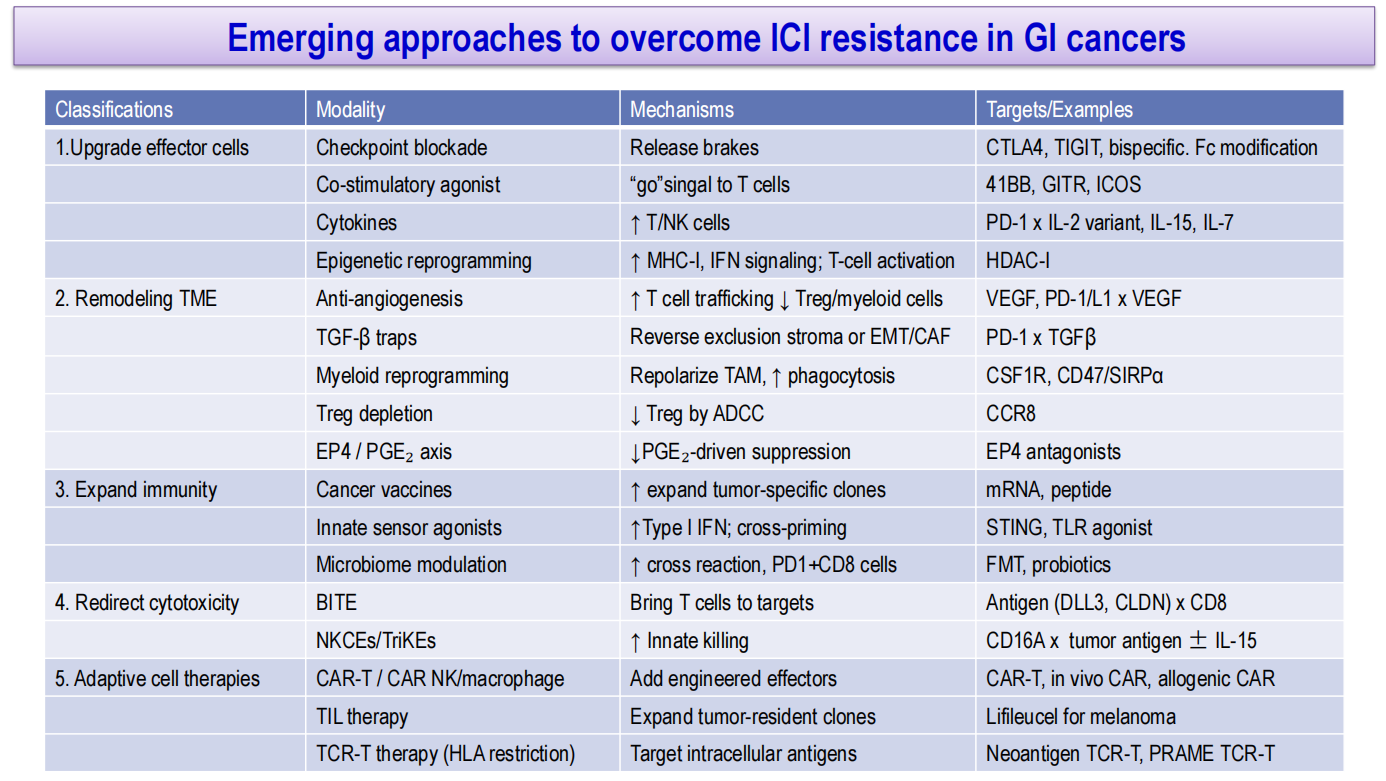
增强效应细胞功能:新型检查点阻断、细胞因子
TIGIT是继PD-1和CTLA-4之后备受关注的免疫检查点靶点,在自然杀伤(NK)细胞和效应性Treg中表达最高,其与CD226形成的共抑制-共刺激信号轴是调控抗肿瘤免疫的关键环节。临床前和早期临床研究显示,PD-1与TIGIT双重阻断增强抗肿瘤免疫反应。然而,多项III期临床试验的结果却令人失望:无论是在非小细胞肺癌、小细胞肺癌、黑色素瘤、肝细胞癌还是食管鳞癌中,多款抗TIGIT抗体联合PD-1/PD-L1抑制剂均未能达到预期终点。
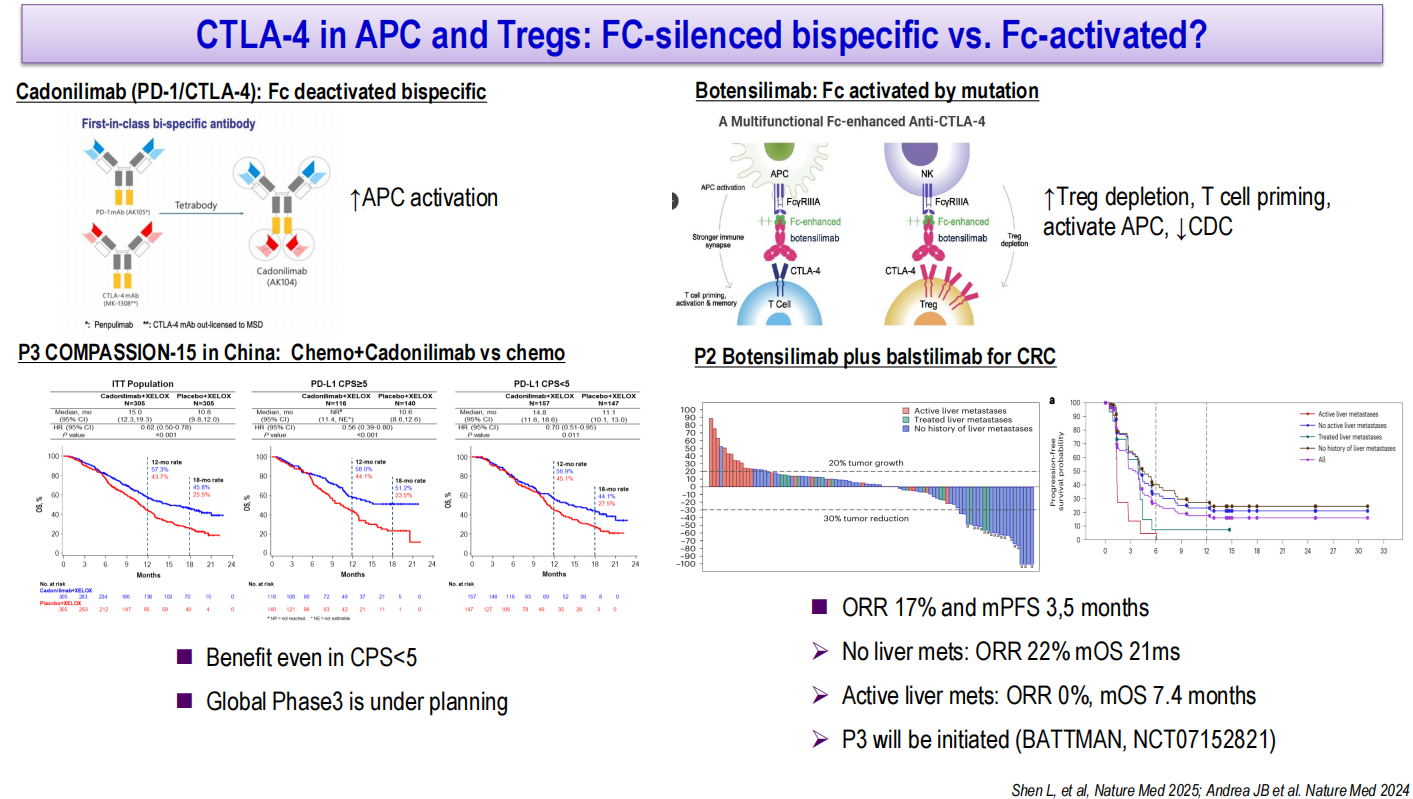
值得关注的是,抗TIGIT抗体的Fc段功能差异可能影响疗效和安全性。Fc段活性保留的抗体可通过Fc受体介导TIGIT阳性Treg耗竭和髓系细胞重塑,但也可能带来Treg相关毒性和CD8+效应细胞非靶向耗竭的风险;而Fc段沉默的抗体则不具备Treg耗竭作用,可能通过激活前体耗竭型CD8+T细胞发挥抗肿瘤效应,且毒性风险更低。针对PD-1/CTLA-4靶点,不同设计理念的药物也在临床中展现出差异化特征。卡度尼利单抗是一种Fc段沉默的PD-1/CTLA-4双特异性抗体,可增强抗原呈递细胞(APC)激活。中国开展的III期COMPASSION-15研究评估化疗联合卡度尼利单抗对比化疗一线治疗胃癌,结果显示总生存期(OS)显著改善(HR 0.62),即使在CPS<5亚组中也观察到获益(HR 0.70),全球III期研究在布局中。Botensilimab则是一种Fc段增强型抗CTLA-4抗体,可增强Treg耗竭、T细胞启动和APC激活。II期研究评估botensilimab联合balstilimab治疗MSS结直肠癌,ORR为17%,mPFS为3.5个月,但疗效在有无肝转移患者中存在明显差异:无肝转移患者ORR为22%、中位OS达21个月,而肝转移患者ORR为0%、中位OS 7.4个月。III期BATTMAN研究已启动。
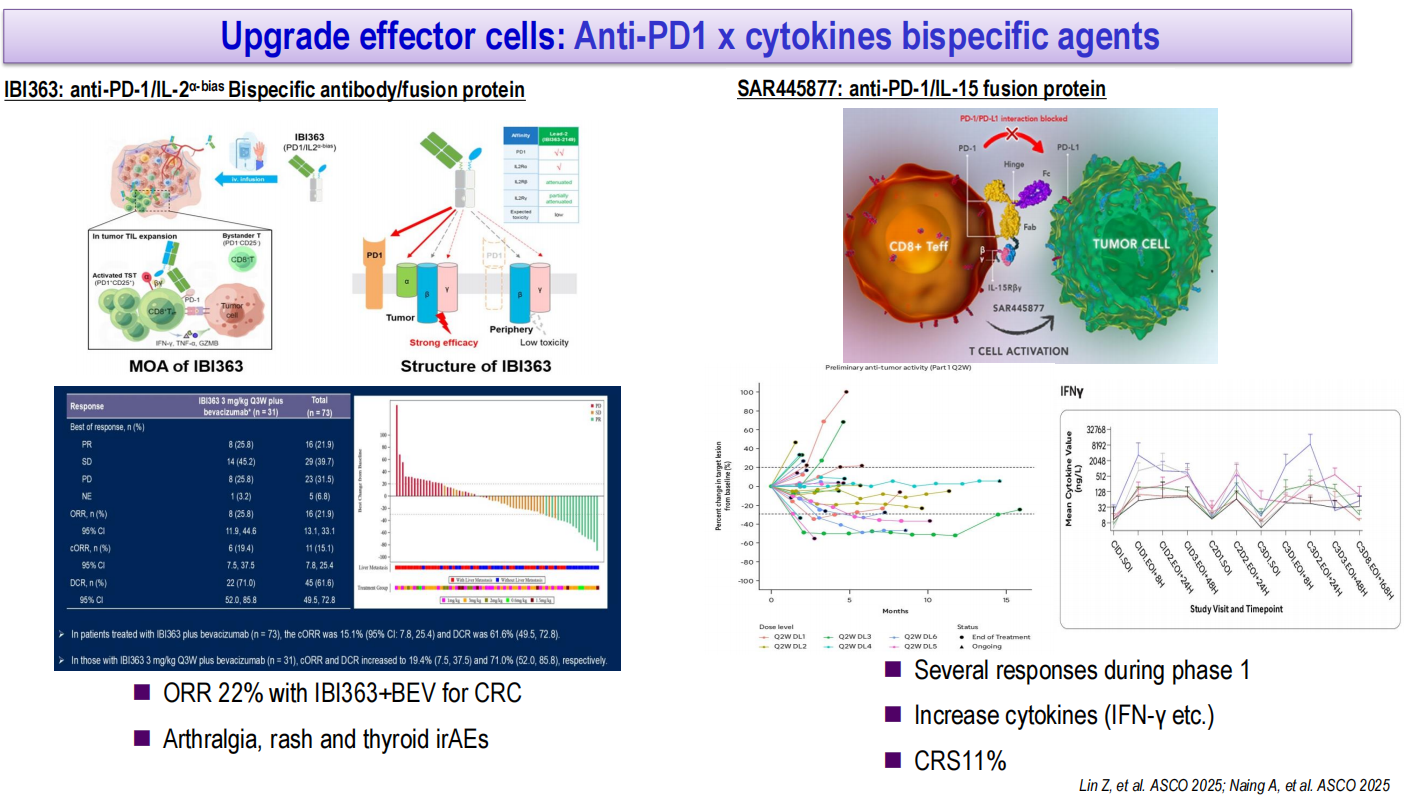
在细胞因子融合蛋白领域,IBI363是一种抗PD-1/IL-2α-bias双特异性抗体融合蛋白,可优先激活肿瘤微环境中的T细胞。该药联合贝伐珠单抗治疗MSS结直肠癌的ORR约达22%,主要不良事件包括关节痛、皮疹和甲状腺功能异常。SAR445877是一种抗PD-1/IL-15融合蛋白,I期研究显示可诱导IFN-γ等细胞因子升高,并观察到肿瘤缓解,细胞因子释放综合征(CRS)发生率为11%。
Invikafusp则是一种选择性TCR和IL-2R双重激动剂,可选择性激活和扩增Vβ6/Vβ10“记忆样效应”T细胞(约占肿瘤浸润淋巴细胞的11%)。早期临床研究显示,该药单药在TMB-H的MSS结直肠癌患者(既往接受过抗PD-1治疗)中诱导了快速、深度、持久缓解,CRS发生率为87%(3级为9%)。
重塑肿瘤微环境:抗血管生成、TGF-β抑制与Treg耗竭
针对肿瘤微环境的免疫抑制特征,多种治疗策略正在探索中。临床前和临床研究表明,瑞戈非尼和仑伐替尼可减少肿瘤微环境中的Treg和巨噬细胞浸润。日本开展的瑞戈非尼联合纳武利尤单抗(RegoNivo)I期研究在胃癌和结直肠癌中观察到肿瘤缓解。然而,III期研究结果并不理想:INTEGRATE-2b研究评估RegoNivo方案对比化疗用于三线及以上胃癌,OS未显著改善(HR 0.88);LEAP-15研究评估化疗联合帕博利珠单抗和仑伐替尼对比化疗一线治疗胃癌,OS差异无统计学意义(HR 0.84);LEAP-14研究在食管鳞癌中同样未能证实三药联合较化疗联合帕博利珠单抗的获益(OS HR 0.92)。
在MSS结直肠癌领域,多项PD-1联合策略的研究均以失败告终,包括PD-1联合MEK抑制剂(IMBLAZE370)、PD-1联合LAG-3抑制剂(RELATIVITY-123、MK-4280A-007)以及PD-1联合仑伐替尼(LEAP-017)。值得注意的是,STELLAR-303研究评估zanzalintinib(一种同时抑制VEGFR、MET和TAM激酶的多靶点TKI)联合阿替利珠单抗对比瑞戈非尼,结果为阳性(OS HR 0.80),无论有无肝转移均观察到获益。

抗VEGF与抗PD-1/PD-L1双特异性抗体是当前热点研究方向。Ivonescimab是一种靶向VEGF-A和PD-1的双特异性抗体,HARMONi研究在EGFR突变型非小细胞肺癌中显示该药联合化疗较安慰剂联合化疗显著延长PFS(HR 0.52)。然而,抗PD-1单药(CM722研究)在相似人群中未能改善预后,而抗PD-1联合抗VEGF虽改善PFS但OS获益有限。这提示双特异性抗体可能具有超越单抗组合的优势,但确切机制和最佳获益人群仍需进一步探索。
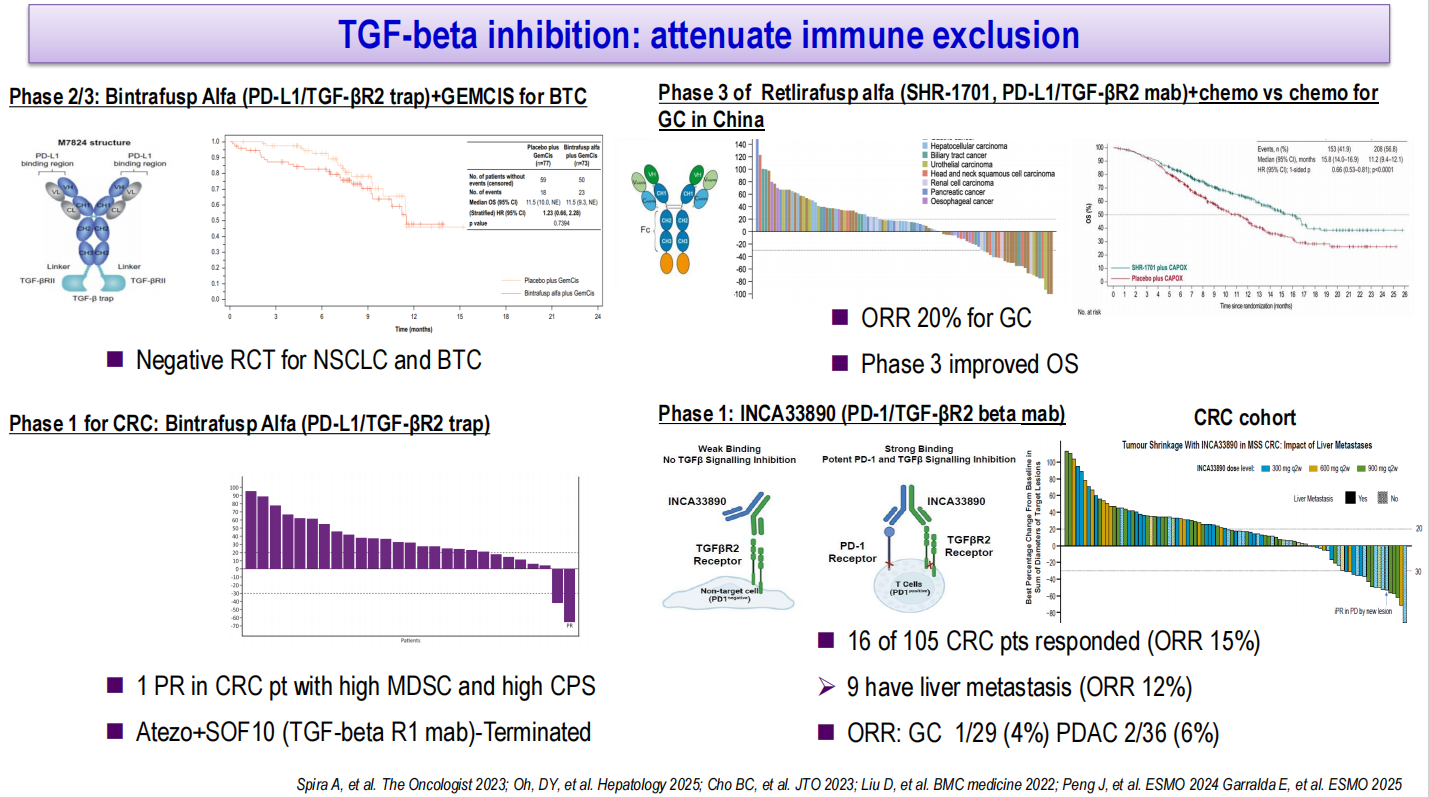
TGF-β信号通路与免疫排斥和间质细胞富集密切相关。Bintrafusp alfa是一种PD-L1/TGF-βRII双功能融合蛋白,在I期研究中对部分高mMDSC和高CPS的结直肠癌患者有效,但在非小细胞肺癌和胆道肿瘤的随机对照研究中均为阴性。SHR-1701是另一种PD-L1/TGF-βRII双功能融合蛋白,中国开展的III期研究评估该药联合化疗对比化疗一线治疗胃癌,结果显示OS显著改善(mOS 15.8个月 vs 11.2个月,HR 0.66,P<0.0001)。INCA33890是一种PD-1/TGF-βRII双特异性抗体,其设计特点是仅在与PD-1阳性T细胞结合后才能有效抑制TGF-β信号。研究显示,该药在MSS结直肠癌患者中的ORR达15%(105例中16例缓解),其中9例伴有肝转移(ORR 12%);在胃癌中ORR为4%,在胰腺导管腺癌中为6%。
前列腺素E2(PGE2)-EP4轴是肿瘤微环境免疫抑制的重要介质。ONO-4578是一种EP4受体拮抗剂,可抑制PGE2介导的免疫抑制,增强细胞毒性T细胞和NK细胞功能。I期研究显示,ONO-4578联合纳武利尤单抗治疗免疫治疗经治晚期胃癌患者的ORR为16%,并伴有T效应细胞基因特征和CD68+巨噬细胞浸润的增加。II期研究评估化疗联合纳武利尤单抗加用ONO-4578对比化疗联合纳武利尤单抗,PFS主要终点达成,后续研究正在规划中。
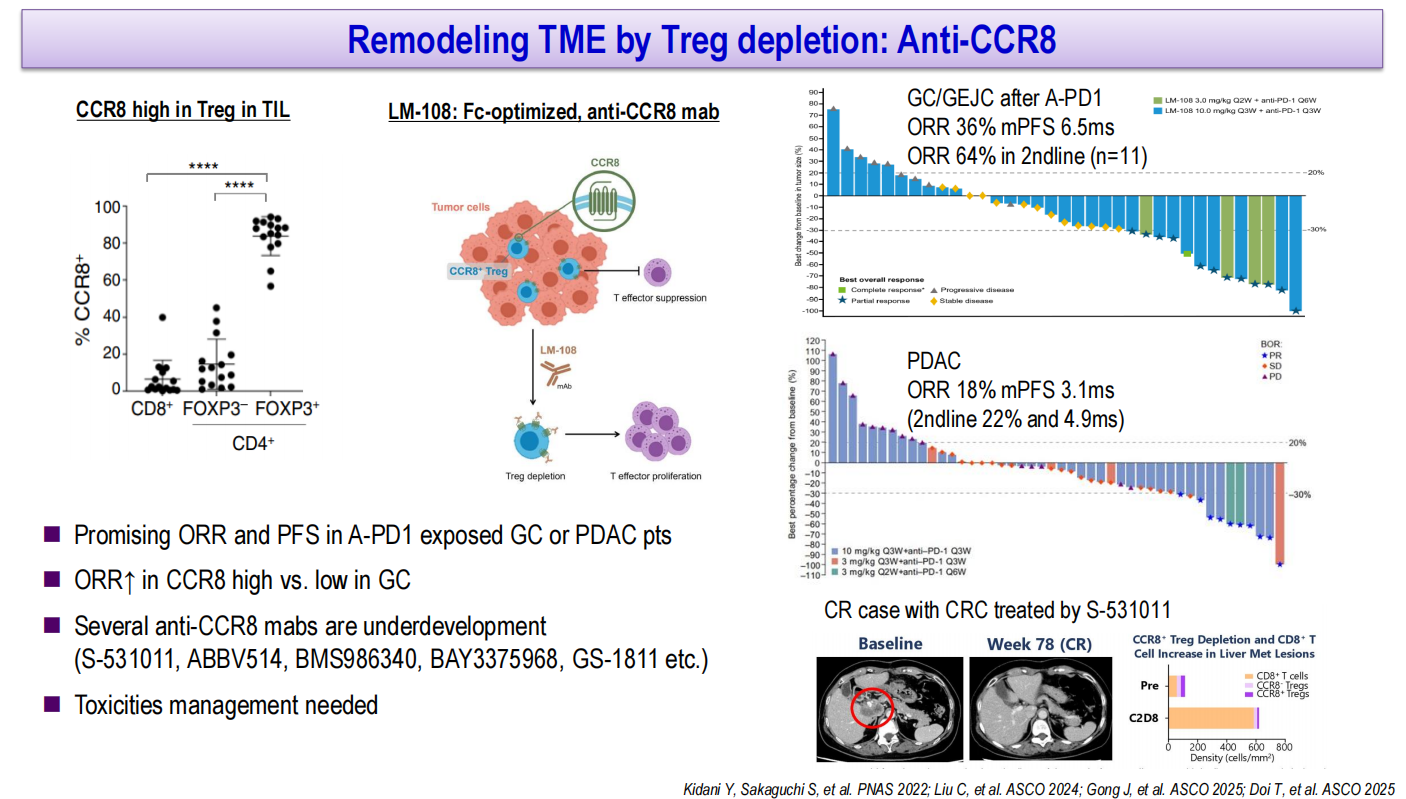
Treg耗竭是克服免疫抑制的另一个重要策略。CCR8在肿瘤浸润Treg中高表达,可作为选择性耗竭肿瘤相关Treg的靶点。LM-108是一种Fc段优化的抗CCR8单克隆抗体。I期研究显示,该药联合抗PD-1抗体治疗抗PD-1抑制剂经治胃癌患者的ORR达36%,mPFS为6.5个月,二线治疗(n=11例)的ORR高达64%;在胰腺癌中ORR为18%,mPFS为3.1个月(二线治疗ORR 22%,mPFS 4.9个月)。在胃癌中,CCR8高表达与更高ORR相关。S-531011是另一种抗CCR8单克隆抗体,在结直肠癌患者中观察到完全缓解病例,伴随CCR8+ Treg耗竭和CD8+ T细胞浸润增加。目前多种抗CCR8单克隆抗体(包括ABBV514、BMS986340、BAY3375968、GS-1811等)正在研发中。
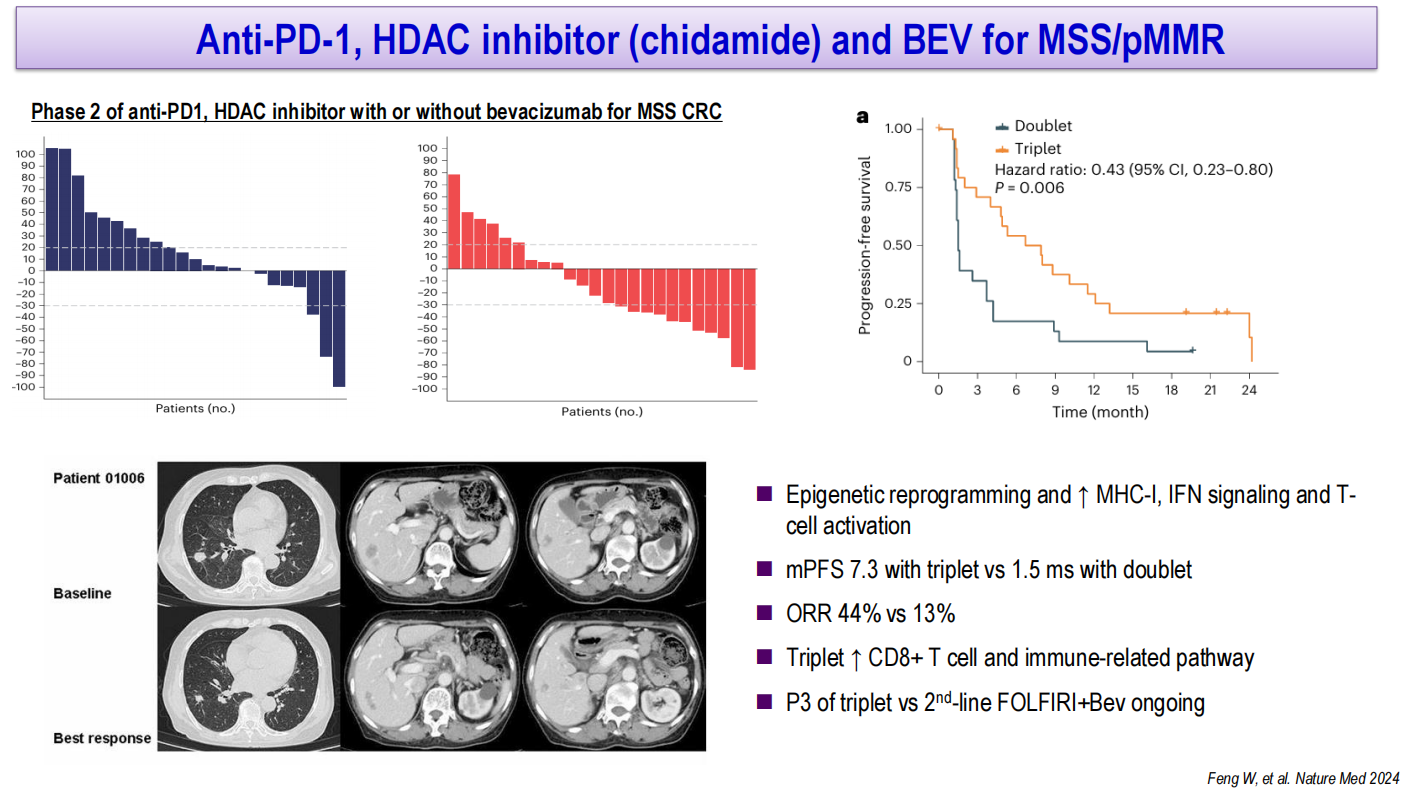
此外,HDAC抑制剂通过表观遗传重编程可上调MHC-I表达、IFN信号通路和T细胞激活。II期研究评估抗PD-1联合HDAC抑制剂西达本胺和贝伐珠单抗三药联合对比双药联合治疗MSS结直肠癌,结果显示三药联合组mPFS显著优于双药联合组(7.3个月 vs 1.5个月),ORR分别为44%和13%,伴随CD8+T细胞和免疫相关通路的激活。该方案对比二线FOLFIRI联合贝伐珠单抗的III期研究正在进行中。
超越PD-1/PD-L1(下):消化道肿瘤免疫治疗的新型策略与前沿进展
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


