
第67届美国血液学会(ASH)年会已圆满落幕。在海量数据的洪流中,我们清晰地看到了血液肿瘤治疗理念的迭代:临床关注点正从单纯追求缓解率(ORR),向追求长期总生存(OS)获益、真实世界的可及性以及特殊人群的精准治疗转移。
本届大会上,关于抗体偶联药物(ADC)、CD20/CD3双特异性抗体及新型免疫调节剂的一系列重磅研究,恰恰回应了这些深层次的临床需求。无论是维泊妥珠单抗(Polatuzumab vedotin)在真实世界中的大样本验证,还是格菲妥单抗(Glofitamab)与莫妥珠单抗(Mosunetuzumab)在长期随访中展现的生存韧性,亦或是Cevostamab在多发性骨髓瘤中的靶点突围,都标志着精准免疫治疗正在迈入“高效、持久、低毒”的新阶段。
本文将从四大临床维度出发,为您深度复盘本届ASH的核心启示。
Part1. 时间的验证(Long-term)——双抗长期随访数据确立“功能性治愈”新希望
免疫治疗最大的魅力在于其可能带来的“拖尾效应”。对于复发/难治性(R/R)淋巴瘤患者而言,短期缓解固然重要,但能否转化为长期的生存获益(OS)才是衡量疗效的“金标准”。本届ASH公布的两项长期随访数据,为双特异性抗体在治疗全景中的地位提供了坚实的注脚。
R/R DLBCL的生存期再度延长:STARGLO研究3年随访
在复发/难治性弥漫性大B细胞淋巴瘤(R/R DLBCL)领域,Abstract #5519带来了III期 STARGLO研究的3年随访数据。该研究对比了格菲妥单抗联合吉西他滨和奥沙利铂(Glofit-GemOx)与利妥昔单抗联合GemOx(R-GemOx)在二线及以上不适合移植患者中的疗效。
随着随访时间的延长(中位35.1个月),生存曲线的分离趋势愈发明显。数据显示,Glofit-GemOx组的中位OS达到25.5个月,显著优于R-GemOx组的12.5个月(HR=0.60, 95% CI: 0.43-0.83)。更令人振奋的是,在双抗联合组,36个月的OS率高达47.1%,而对照组仅为27.4%。对于既往接受过1线治疗的患者,获益更为显著(HR=0.58)。这一结果有力地确证了格菲妥单抗联合方案作为R/R DLBCL标准治疗方案的长期价值,打破了该类患者“生存期短、难治愈”的固有印象。
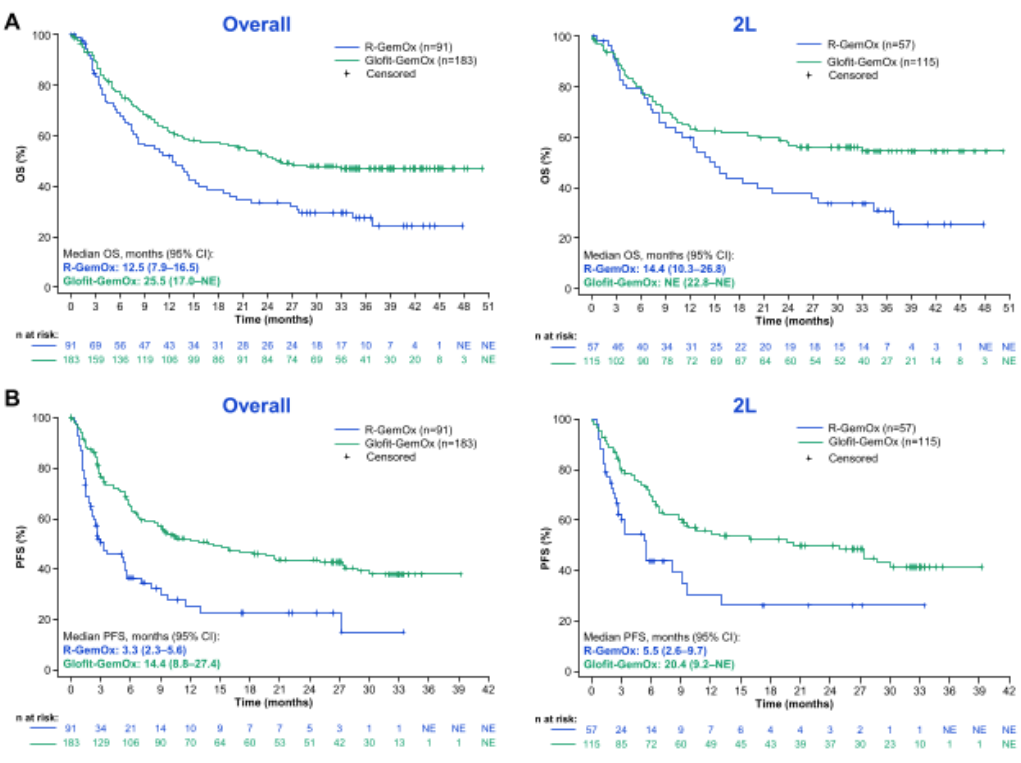 图1. STARGLO研究3年随访总生存(OS)与无进展生存(PFS)数据
图1. STARGLO研究3年随访总生存(OS)与无进展生存(PFS)数据
R/R FL的“治愈”曙光:莫妥珠单抗5年随访
对于惰性淋巴瘤如滤泡性淋巴瘤(FL),临床治疗目标是在延长生存的同时兼顾生活质量。Abstract #5352公布了莫妥珠单抗单药治疗R/R FL关键II期研究的5年随访结果,这也是目前双抗领域随访时间最长的研究之一。
数据显示,在经过中位24个月的治疗结束后,患者的5年总生存(OS)率高达78%。更为关键的是,在完成固定疗程治疗并获得完全缓解(CR)的患者中,5年无进展生存(PFS)率达到57%。这意味着超过半数的深度缓解者在停止治疗后的数年内仍未复发。这种“固定疗程(Fixed-Duration)”带来的长生存模式,提示双抗单药可能帮助部分多线复发的惰性淋巴瘤患者实现“功能性治愈”,让患者真正回归正常生活。
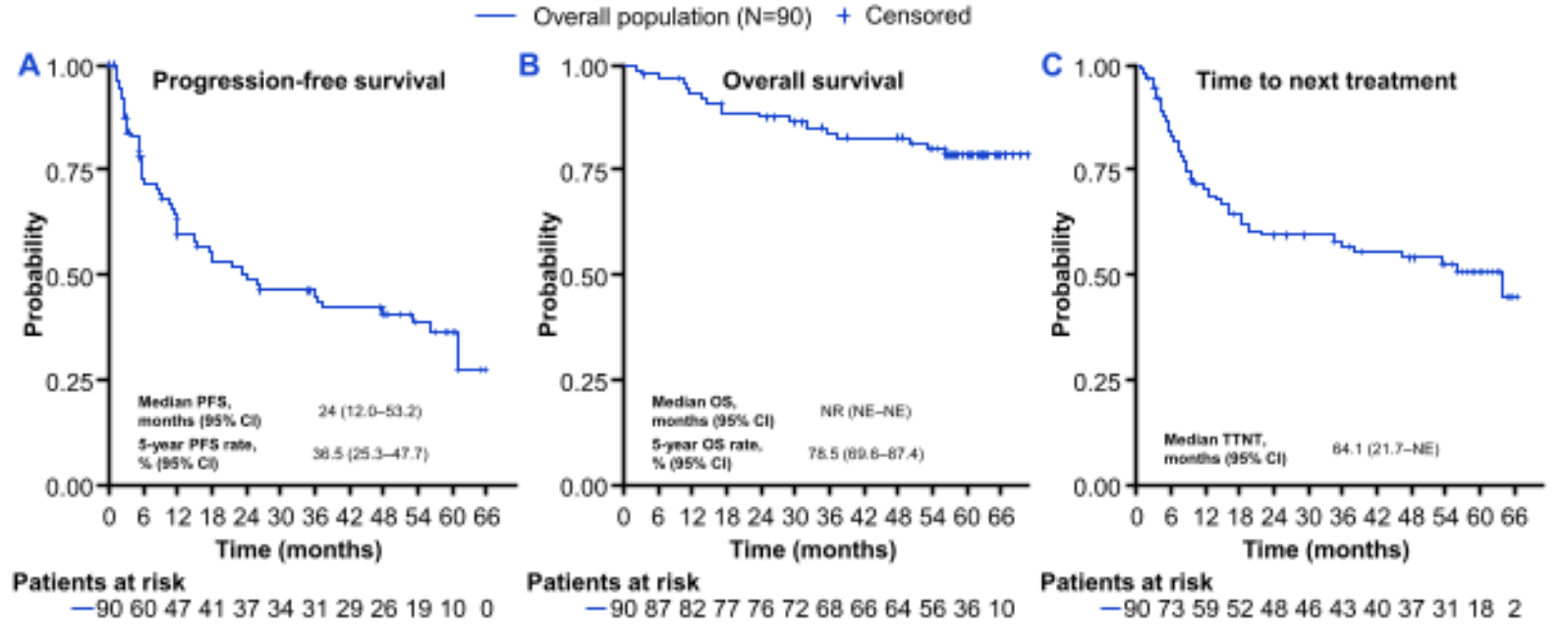
(A) 总体人群的无进展生存期(PFS);(B) 总体人群的总生存期(OS);(C) 总体人群的至下一次治疗时间(TTNT)。数据表明固定疗程治疗后,患者获得了长期的生存获益。 数据来源:ASH 2025 Abstract #5352
Part2. 现实的答案(Real-world)——真实世界大样本研究验证ADC一线基石地位
临床研究中,随机对照试验(RCT)严格的入组标准往往排除了高龄、合并症多等复杂患者。而真实世界研究(RWE)则是对新药真实疗效的补充。本届ASH上,关于维泊妥珠单抗的大规模RWE成为了焦点。
大规模中国临床实践:POLAREAL研究
Abstract #6293 (POLAREAL)是本届大会备受瞩目的中国声音,也是迄今为止中国最大规模的维泊妥珠单抗真实世界研究。该研究由赵维莅教授牵头,纳入了794例中国DLBCL患者,涵盖了高龄(中位年龄76.1岁)、ECOG评分较差等在注册临床试验中常被排除的群体。
中期分析显示,在“不适合/虚弱(Unfit/Frail)”的初治队列(Cohort 1)中,维泊妥珠单抗联合方案(如Pola-R-miniCHP)的最佳客观缓解率(BORR)高达90.7%;在适合强化疗的初治队列(Cohort 2)中,BORR更是达到了93.5%。安全性方面,虽然85.4%的患者报告了不良事件,但整体可控,周围神经病变的发生率极低(≥2级仅0.7%)。这一数据证实了含Pola方案在中国真实临床环境中的疗效与安全性与全球POLARIX研究高度一致,为中国医生在广泛人群中的处方决策提供了最强有力的信心支持。
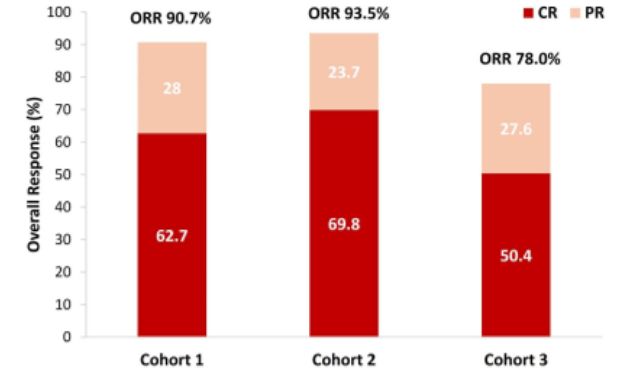
Cohort 1(不适合/虚弱初治患者)和 Cohort 2(适合初治患者)均显示出极高的缓解率,证实了维泊妥珠单抗联合方案在中国真实世界人群中的优异疗效。 数据来源:ASH 2025 Abstract #6293
大数据的卫生经济学研究:TriNetX数据库分析
来自美国的Abstract #2759则利用TriNetX数据库分析了10万余例DLBCL患者的数据。通过倾向性评分匹配(PSM),研究发现一线接受Pola-R-CHP治疗的患者,其总生存期(OS)显著优于R-CHOP组(HR=0.653, p<0.0006)。更重要的是,Pola组患者进展至下一线治疗的风险降低了44%(HR=0.560)。这从卫生经济学和全病程管理的角度,再次验证了维泊妥珠单抗作为一线基石药物,能够通过“治好第一线”来最大限度地改善患者的终局预后。
Part3. 减法的艺术(Chemo-free)——“去化疗/轻化疗”策略破解老年虚弱人群困局
随着人口老龄化加剧,如何让不能耐受高强度化疗的老年/虚弱患者获得有效治疗,是临床面临的巨大挑战。本届ASH上,基于双抗和ADC的“去化疗(Chemo-free)”或“轻化疗(Chemo-light)”探索成为了“减法艺术”的典范。
双抗的“轻”时代
Abstract #62 (MorningSun研究)展示了莫妥珠单抗皮下制剂(SC)单药一线治疗老年/不适合化疗DLBCL患者的潜力。在这一中位年龄高达82.5岁的高龄群体中,ORR达到了73.5%,且安全性良好,为无法接受R-CHOP的患者提供了极具吸引力的“无化疗”选择。此外,Abstract #61 探索了格菲妥单抗+维泊妥珠单抗+利妥昔单抗(R-Pola-Glo)的“全免疫”组合,在老年/虚弱LBCL患者中实现了85%的1年PFS率,且34%的患者未发生任何3级以上不良事件,显示了极高的治疗指数。
中国学者公布最新“去化疗”方案
中国研究者在这一领域同样走在前列,贡献了多项“基石药物+新型口服靶向药”的创新方案:
⭐️ Abstract #5477 (PRO方案):由江苏省人民医院李建勇教授团队等开展,使用维泊妥珠单抗联合奥布替尼和利妥昔单抗一线治疗老年/虚弱DLBCL,CR率达到66.7%,ORR高达94.5%。
⭐️ Abstract #3696 (Pola-ZR2):瑞金医院团队探索了维泊妥珠单抗联合泽布替尼和来那度胺的方案,同样显示出优异的疗效。
⭐️ Abstract #3597:展示了奥妥珠单抗联合奥布替尼在边缘区淋巴瘤(MZL)中的高效协同。
这些研究共同表明,对于不耐受化疗的人群,基于维泊妥珠单抗或奥妥珠单抗的“去化疗”组合,正逐步从理想变为现实,让患者能够“免于化疗之苦”而获“精准治疗之效”。
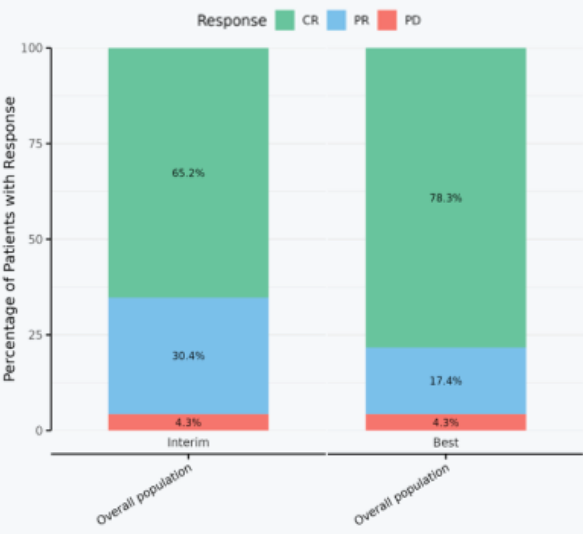
柱状图展示了在期中分析(Interim)和治疗结束(End of Therapy)时,患者获得完全缓解(CR,绿色)和部分缓解(PR,蓝色)的高比例,显示了“去化疗”方案的深度缓解潜力。 数据来源:ASH 2025 Abstract #5477
Part4. 攻坚的利刃(New Targets)——新靶点与新机制协同突破耐药瓶颈
面对多线复发、对现有CD19 CAR-T或CD20单抗耐药的这一临床治疗困境,亟需新的破局者。本届ASH展示了新靶点与新机制组合的攻坚能力。
MM治疗的新赛道:Cevostamab
在多发性骨髓瘤(MM)领域,BCMA靶点的竞争已趋白热化。Abstract #252聚焦于靶向FcRH5/CD3的双特异性抗体Cevostamab。研究显示,Cevostamab联合泊马度胺和地塞米松(Pd)在复发/难治性MM患者中展现了深度缓解潜力。生物标志物分析进一步揭示,该方案能有效清除肿瘤细胞并维持T细胞的适应性(Fitness),为克服BCMA耐药提供了全新的机制选择。
强强联合的协同效应:双抗+ADC
Abstract #3735公布了莫妥珠单抗与维泊妥珠单抗(Mosun-Pola)联合治疗R/R LBCL的3年随访数据。这一组合巧妙地利用了双抗药物与ADC药物两种不同机制的协同效应。结果显示,在多线治疗失败(包括CAR-T后复发)的患者中,36个月的OS率仍维持在48%。这种两类创性药物的组合模式,为后线挽救治疗开辟了更为广阔的路径。
Part5. 总结——未来展望,精准与人文并重
纵观2025 ASH,血液肿瘤的治疗边界正在被不断拓宽。如果说长生存数据的更新夯实了“精准治疗”的深度,那么真实世界研究和去化疗方案的探索则拓展了“人文关怀”的广度。
从维泊妥珠单抗在广泛人群中确立的一线基石地位,到双特异性抗体在长生存与便捷给药上的双重突破,再到中国学者在“去化疗”领域的积极贡献,这些循证证据共同构成了一幅波澜壮阔的诊疗新图谱。未来的血液肿瘤治疗,将不再仅仅是药物的叠加,而是基于患者个体特征、生存需求与生活质量的全方位优化。随着这些创新成果的临床转化,会有更多患者迎来“长生存”与“优生活”并存的明天。
[1] Jeremy Abramson et al. Sustained clinical benefit of glofitamab plus gemcitabine and oxaliplatin (GemOx) versus rituximab plus GemOx (R-GemOx) in patients with relapsed/refractory (R/R) diffuse large B-cell lymphoma (DLBCL): 3-year follow-up of STARGLO. ASH 2025; Abstract #5519.
[2] Elizabeth Budde et al. Fixed treatment duration mosunetuzumab continues to demonstrate clinically meaningful outcomes in patients with relapsed/refractory (R/R) follicular lymphoma (FL) after ≥2 prior therapies: 5-year follow-up of a pivotal Phase II study. ASH 2025; Abstract #5352.
[3] Pengpeng Xu et al. Effectiveness and safety of polatuzumab vedotin in real-world clinical practice in Chinese patients with diffuse large B-cell lymphoma (POLAREAL): An interim analysis from a prospective, multicenter, observational registry study. ASH 2025; Abstract #6293.
[4] Danielle Thor et al. Real-world comparative outcomes of pola-R-CHP versus R-CHOP in patients with diffuse large B-cell lymphoma. ASH 2025; Abstract #2759.
[5] Jeff Sharman et al. Fixed treatment duration subcutaneous mosunetuzumab monotherapy in elderly/unfit patients with previously untreated diffuse large B-cell lymphoma: Interim results from the Phase II MorningSun study. ASH 2025; Abstract #62.
[6] Björn Chapuy et al. Phase II frontline chemolight R-Pola-Glo trial induces high and durable response rates in elderly and medically unfit/frail patients with aggressive B-cell lymphoma. ASH 2025; Abstract #61.
[7] Wenyu Shi et al. Polatuzumab vedotin combined with orelabrutinib and rituximab (PRO Regimen) as frontline therapy in elderly and frail patients with diffuse large B-cell lymphoma (DLBCL): Results from a Phase II study. ASH 2025; Abstract #5477.
[8] Fan Zhang et al. A prospective, multicenter, randomized, controlled clinical trial comparing polatuzumab vedotin, zanubrutinib, lenalidomide, and rituximab (Pola-ZR2) versus zanubrutinib, lenalidomide, and rituximab (ZR2) in the treatment of previously untreated, elderly patients with diffuse large B-cell lymphoma. ASH 2025; Abstract #3696.
[9] Hu Mao Gui et al. Efficacy and safety of first-line orelabrutinib combined with obinutuzumab (With or Without Bendamustine) in high-risk marginal zone lymphoma: Results from the orchid study. ASH 2025; Abstract #3597.
[10] Simon Harrison et al. Tumor clearance, T-cell fitness, and minimal residual disease (MRD) outcomes in patients with relapsed/refractory multiple myeloma (RRMM) treated with cevostamab plus pomalidomide and dexamethasone: Biomarker analyses from CAMMA 1 Arm B. ASH 2025; Abstract #252.
[11] Manali Kamdar et al. Fixed-duration intravenous mosunetuzumab plus polatuzumab vedotin combination therapy continues to demonstrate durable responses in patients with large B-cell lymphoma: 3-year follow-up from a Phase Ib/II study. ASH 2025; Abstract #3735.
往期精彩回顾:
ASH 氏野|学术发表量领跑!中国强音定调真实世界,维泊妥珠单抗构筑DLBCL全线治疗新高地
排版编辑:肿瘤资讯-JYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


