在全球恶性肿瘤疾病谱中,肺癌的高发病率与高病死率始终是重大公共卫生挑战。我国非小细胞肺癌(NSCLC)患者占比高,EGFR敏感突变人群从EGFR-TKI治疗中获益显著,但耐药难题仍是临床治疗的“达摩克利斯之剑”。寻找兼顾疗效与安全性的耐药后治疗方案,已成为全球肿瘤领域的核心探索方向。
在此背景下,夏旸教授团队于2025年11月在国际顶级期刊Nature Reviews Clinical Oncology(IF=82.2)发表重磅综述[1],系统梳理并前瞻性阐释了EGFR-TKI耐药机制的全景与诊疗进展,为该领域的科研与临床实践提供了重要的理论框架与方向指引。
值得关注的是,该综述中提出的若干策略,已在近期得到实质性呼应与推进。例如,荣登ESMO大会主席论坛并同步发表于《新英格兰医学杂志》(NEJM)的OptiTROP-Lung04研究,作为全球首个EGFR-TKI耐药NSCLC领域单药取得双阳性III期研究[2],正是这一转化轨迹的有力印证。2025年9月30日,芦康沙妥珠单抗获国家药品监督管理局批准,成为全球首个获批该适应症的TROP2 ADC药物,为患者带来全新生存希望。2025年12月,芦康沙妥珠单抗成功纳入2025年国家医保目录,大大提高了药物可及性,减轻患者的经济负担。
为此,【肿瘤资讯】“POWER INVESTIGATOR”系列专家访谈特邀夏旸教授,结合综述核心观点与OptiTROP-Lung04研究突破,深度解析EGFR突变NSCLC的耐药机制研究新进展、芦康沙妥珠单抗的临床价值,以及全程治疗的优化策略。
浙江大学医学院附属第二医院呼吸与危重症医学科 科室副主任
国家优青、全国优秀中青年呼吸医师
学术任职:
中国医师协会呼吸医师分会青委委员
中华医学会呼吸病分会介入呼吸病学组秘书
国际肺癌学会(IASLC)临床科学委员会委员
中国临床肿瘤学会(CSCO)非小细胞肺癌专委会委员
中国临床肿瘤学会(CSCO)青年专家委员会委员
浙江省医学会呼吸病分会委员

问题一:您近期发表的综述文章,系统总结了EGFR突变NSCLC的TKI耐药机制与治疗进展,重磅发表于Nature Reviews Clinical Oncology,请您为肺癌医生提炼下综述的核心结论与最具临床价值的关键观点。
夏旸教授:EGFR是肺癌精准治疗中最具代表性的驱动基因,经过20余年发展,已从一代TKI演进至三代TKI,治疗场景也从后线拓展至一线,更衍生出单药、联合等多种治疗模式,让更多患者以更低毒性获得更好疗效与更长生存。但耐药始终是不可避免的核心挑战,基于近年领域内的大量探索与突破,我们团队在综述中对耐药机制与应对策略进行了系统梳理。
耐药机制层面,仍延续经典的“在靶、脱靶、组织学转化”三大分类,但临床中第三代TKI耐药后,不少耐药机制尚未明确,这一群体的治疗需求尤为迫切。而应对耐药的策略,我们将其划分为“克服耐药”与“预防耐药”两大核心方向,这也是当前临床实践与研究的重点。
“克服耐药”即TKI治疗失败后的后续方案选择,具体可分为两类模式:一是生物标志物指导的精准治疗策略,针对已知耐药机制如MET扩增、RTK融合等,采用对应的双靶联合等方案,这是精准治疗的核心路径;二是生物标志物非选择性的all-comer策略,适用于无明确靶点或机制不明的患者,近年来该领域突破显著,例如免疫治疗领域的ORIENT-31、HARMONi研究,以及TROP2 ADC药物芦康沙妥珠单抗的系列研究。尤其是芦康沙妥珠单抗研究稳扎稳打,从三线头对头战胜多西他赛,到二线对比含铂双药化疗方案取得双终点阳性,为EGFR突变耐药患者提供了明确获益的新选择。
“预防耐药”则是在一线治疗阶段通过优化方案,延长TKI治疗时长、延缓耐药发生,主要包括两种底层逻辑:一是以FLAURA2研究为代表的“清除耐药克隆”策略,通过TKI联合化疗清除药物诱导的潜在耐药克隆(DTP),这类克隆在多种实体瘤的耐药诱导中均发挥关键作用;二是以MARIPOSA研究为代表的“预阻断耐药旁路”策略,针对MET扩增等常见旁路耐药机制,通过TKI联合双抗等方案提前阻断,从而延缓耐药出现。
需要强调的是,从临床研究到临床实践的转化过程中,疗效是基础,安全性、治疗便利性与药物经济学同样是重要考量因素。我们期待无论是克服耐药还是预防耐药的新策略,都能具备更优的综合获益,让更多患者从EGFR靶向治疗中持续获益。
问题二:您的综述特别指出,第三代TKI耐药后高达75%的耐药机制属于“未知”或高度复杂的旁路信号激活,这类患者此前缺乏有效治疗手段。而芦康沙妥珠单抗凭借双重稳定与双重释放独特机制,选择了“ALL-comer”策略,在OptiTROP-Lung04研究中实现了PFS与OS双重突破。请您从研究数据层面解读该研究的亮点内容。
夏旸教授:第三代TKI耐药后,机制不明或高度复杂的患者占比很高,这类患者此前缺乏有效的治疗手段,临床上面临“束手无策”的困境。而芦康沙妥珠单抗凭借生物标志物非选择性的all-comer策略,在该领域取得了突破性进展,其相关研究数据的亮点尤为突出。
芦康沙妥珠单抗的系列研究形成了完整的证据链:OptiTROP-Lung03研究发表于BMJ,回答了TKI耐药且含铂双药耐药后该药物的治疗价值[3];而OptiTROP-Lung04研究更进一步,以含铂双药化疗为对照,在TKI耐药二线人群中开展研究,其成果能发表于《新英格兰医学杂志》,核心数据支撑十分扎实。
首先,PFS与OS实现双重突破,达到了临床最关注的“金标准”终点。研究数据显示,芦康沙妥珠单抗单药组中位PFS达8.3个月,较含铂双药化疗的4.3个月实现翻倍,疾病进展或死亡风险显著降低51%(HR=0.49,95%CI: 0.39-0.62;P<0.0001);更关键的是,该研究实现了OS这一核心终点的显著获益——化疗组中位OS为17.4个月,而芦康沙妥珠单抗组中位OS尚未成熟,患者死亡风险显著降低40%(HR=0.60,95%CI:0.44-0.82;P=0.001)。这是首个通过非选择人群达到如此优异生存获益的III期随机对照研究,打破了既往治疗“仅能短期控制病情、无法改善长期生存”的困境,为机制不明的耐药患者提供了明确的生存改善方案。
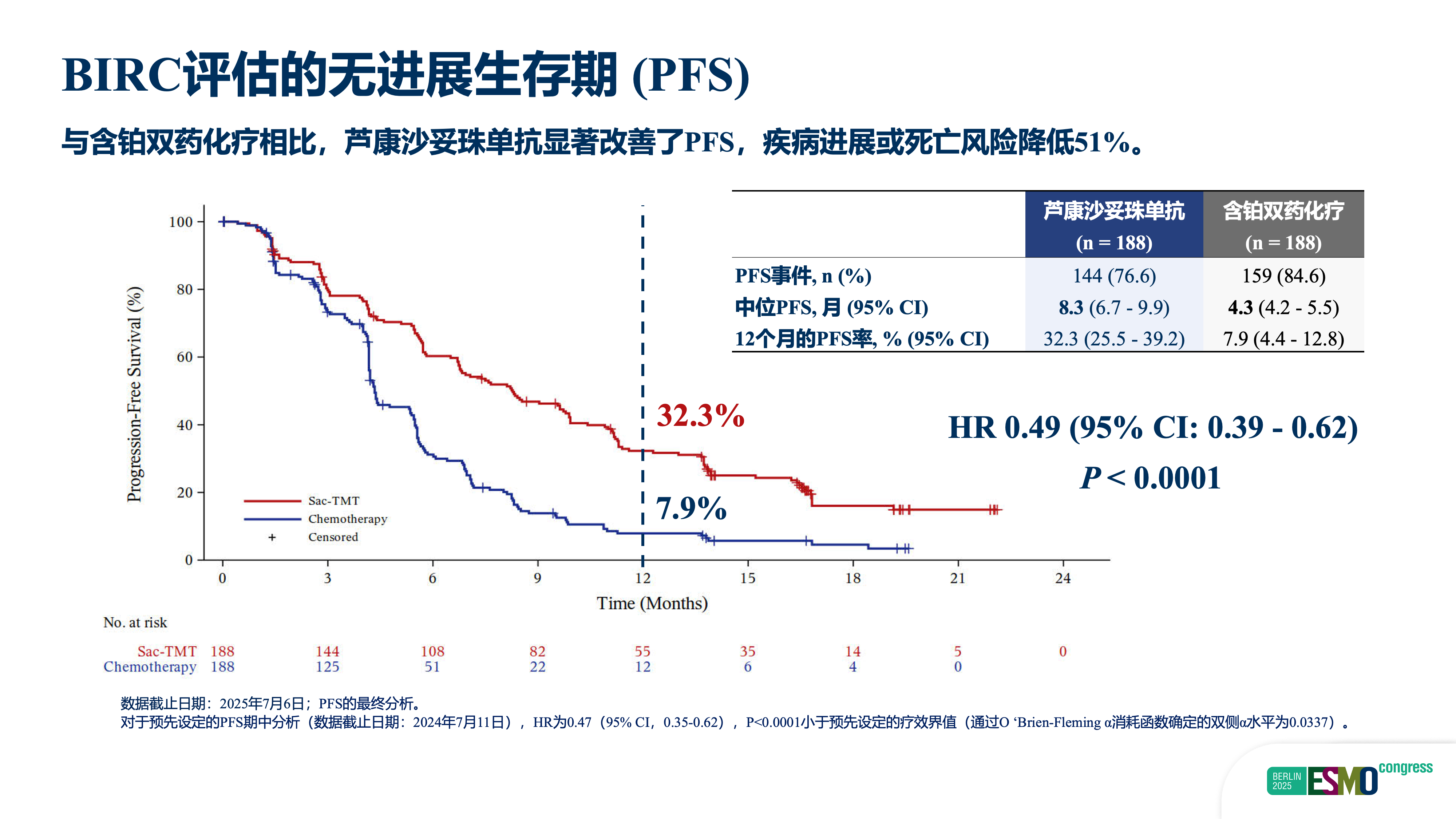
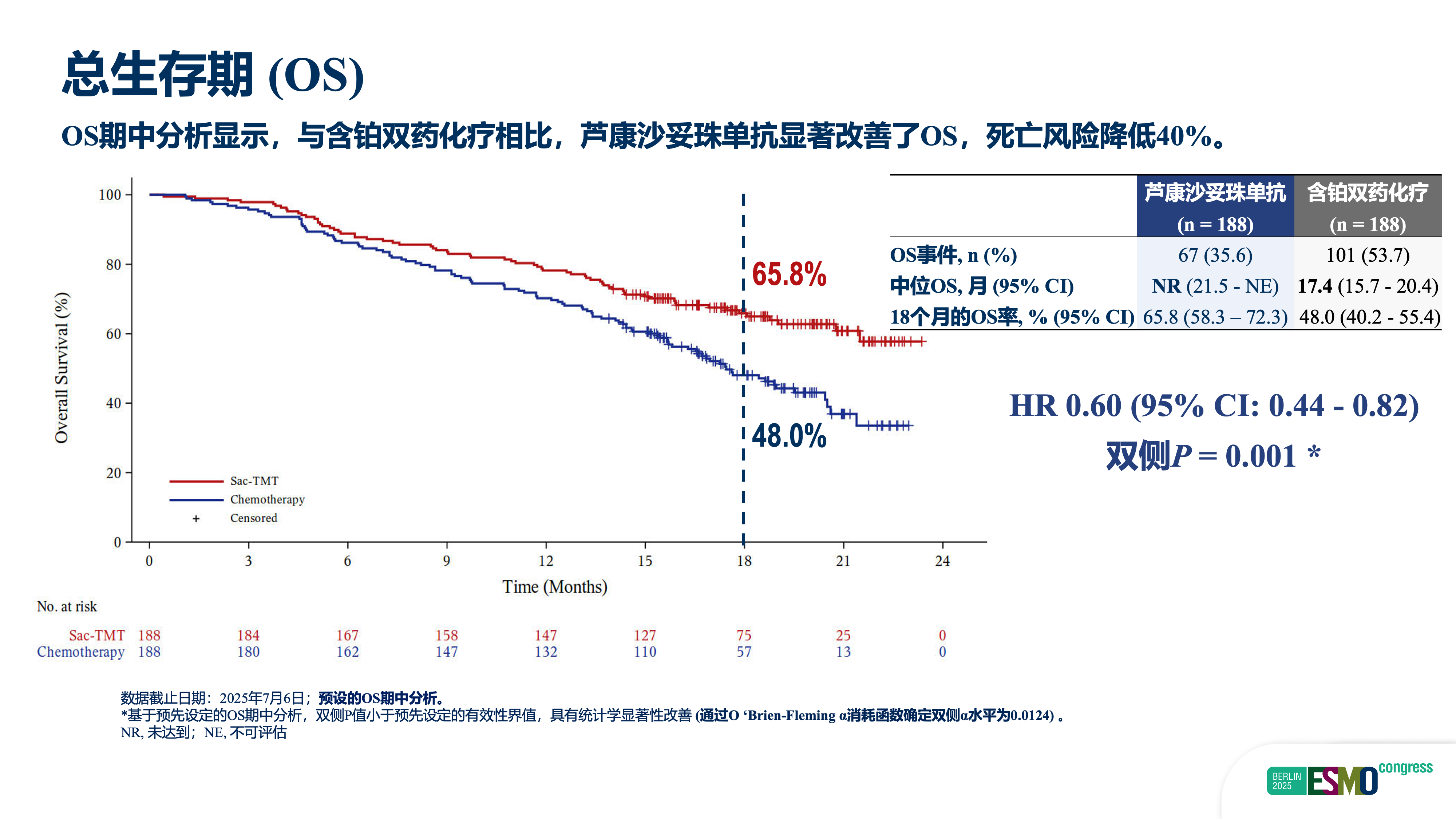
其次,该研究的阳性结果并非耐药机制探索的终点。目前基因组检测仅能解释部分耐药原因,临床中三代药物耐药后,活检仍然是必要的流程,但基因组只是我们对耐药理解的一部分。未来还需依托转录组、代谢组等新的检测技术,进一步将“未知”转化为“已知”,开发芦康沙妥珠单抗联合治疗策略,持续推进耐药领域的研究进展。
问题三:当下精准治疗仍在持续演进,TKI联合化疗,TKI联合双抗均取得了令人瞩目的结果,芦康沙妥珠单抗实现了EGFR-TKI耐药二线,三线的PFS与OS阳性结果。结合您对全程管理的研究积累,认为EGFR突变NSCLC的一线、二线及后续治疗应如何“排兵布阵”,才能在精准分型基础上最大化患者长期获益?
夏旸教授:如何延长EGFR-TKI的疗效与疾病缓解持续时间(DOR),是学术界长期探索的核心话题。过去A+T、一代TKI联合化疗等策略虽改善PFS,但均未实现OS突破,而今年FLAURA2、MARIPOSA两项研究相继公布OS阳性结果,为一线治疗带来新方向。
一线治疗需综合四大因素精准分层:疗效上,联合策略在PFS与OS上均优于单药;但安全性方面,三级以上不良反应增加,且联合方案多需静脉用药,牺牲了TKI单药口服的便利性,同时药物经济学成本更高。因此,脑转移等高危患者可优先选择联合策略,而年龄较大、耐受性差或重视便利性的患者,三代TKI单药仍是标准。目前联合策略仍有局限性,OptiTROP-Lung07研究通过芦康沙妥珠单抗联合奥希替尼一线治疗EGFR突变NSCLC,旨在从“克服耐药”走向“延缓耐药”。
在二线治疗(2L) 中,EGFR-TKI耐药后的方案选择需兼顾“普适性”与“特殊性”。从普适性来看,OptiTROP-Lung04研究证实,芦康沙妥珠单抗单药对“ALL Comer”人群实现了PFS与OS双获益,且单药治疗的毒性谱更清晰,便于临床鉴别与管理。相较于联合治疗中“难以区分化疗相关、免疫相关或抗血管相关毒性”的困境,单药方案能让临床医生更精准地判断不良反应来源,为患者提供更安全的治疗保障,因此成为EGFR-TKI耐药后重要的标准选择之一。
全程管理中,精准分层的探索不会停止。从一线的单药与联合策略选择,到二线的机制导向治疗,每一步都需要结合患者的个体情况综合判断,最终实现长期生存与生活质量的双重目标。
结语
夏旸教授团队发表于国际顶刊Nature Reviews Clinical Oncology的重磅综述,以其系统的理论框架,为EGFR-TKI耐药机制的解析与临床应对策略提供了权威指引,展现出重要的学术引领价值。而OptiTROP-Lung04研究的成功则让芦康沙妥珠单抗这款“大国重器”在all-comer人群中实现生存突破,二者共同推动EGFR突变NSCLC诊疗迈向新高度。
从耐药机制的“已知”到“未知”探索,到治疗策略的“预防”与“克服”并重,再到全程管理的“精准分层”,中国创新药物与临床研究正持续改写肺癌治疗格局。未来,随着分子检测技术的进步、联合治疗方案的探索以及更多原研创新药的涌现,EGFR突变NSCLC患者的治疗路径将更加清晰,长期生存与生活质量的双重目标将逐步实现,为全球肺癌治疗贡献更多“中国智慧”与“中国方案”。
1.Zhao J, Xu W, Zhou F, et al. Navigating the landscape of EGFR TKI resistance in EGFR-mutant NSCLC - mechanisms and evolving treatment approaches. Nat Rev Clin Oncol. 2025 Nov 11. doi: 10.1038/s41571-025-01085-z. Epub ahead of print. PMID: 41219394.
2.Fang W, Wu L, Meng X, et al. Sacituzumab Tirumotecan in EGFR-TKI-Resistant, EGFR-Mutated Advanced NSCLC. N Engl J Med. 2025 Oct 19. doi: 10.1056/NEJMoa2512071. Epub ahead of print. PMID: 41124220.
3. Fang W, Li X, Wang Q, et al. Sacituzumab tirumotecan versus docetaxel for previously treated EGFR-mutated advanced non-small cell lung cancer: multicentre, open label, randomised controlled trial. BMJ. 2025 Jun 5;389:e085680. doi: 10.1136/bmj-2025-085680.
排版编辑:Crystal











 苏公网安备32059002004080号
苏公网安备32059002004080号


