神经营养酪氨酸受体激酶(NTRK)基因融合是多种实体瘤(包括原发性中枢神经系统[CNS]肿瘤)的关键致癌驱动因素。拉罗替尼作为全球首个高选择性、具有中枢神经系统穿透能力的TRK抑制剂,已成为治疗携带NTRK融合实体瘤患者(无论成人或儿童)的重要精准治疗药物。
在2025年欧洲肿瘤内科学会(ESMO)年会上,一项关于拉罗替尼对获得长期缓解的TRK融合癌症患者的疗效和安全性分析数据公布,长期缓解(≥2年)的TRK融合癌患者5年DoR率达到66%、5年PFS率达到68%、6年OS率达到84%,并对创新的“等待-观察”治疗策略进行了探索。为深入解读该研究的临床意义,肿瘤资讯特邀首都医科大学三博脑科医院张俊平教授和四川大学华西第二医院郭霞教授,围绕该研究进行专业点评。
首都医科大学三博脑科医院副院长
神经肿瘤化疗中心主任
肿瘤学博士
神经肿瘤化疗博士后
哈佛大学Dana-Farber肿瘤中心神经肿瘤化疗访问学者
获2022第八届北京优秀医师奖
北京抗癌协会神经肿瘤专委会青年委员会 主任委员
中国抗癌协会神经肿瘤专业委员会 副主任委员
中国医师协会胶质瘤专业委员会 委员
中华医学会儿科学分会血液学组委员
国家卫生健康委员会儿童血液病
恶性肿瘤专家委员会淋巴瘤专业委员会秘书长
中国抗癌协会小儿肿瘤专业委会委员
中国抗癌协会儿童整合康复专委会委员
中国妇幼保健协会精准医学专委会
儿童血液疾病与保健学组委员
中国研究性医院学会儿童肿瘤专业委员会委员
四川省学术和技术带头人后备人选
四川省卫计委学术技术带头人后备人选
四川省抗癌协会理事会理事
四川省抗癌协会肿瘤相关血栓疾病专业委员会常务委员
四川省医学会儿科分委会血液学组委员
四川省医师协会血液科医师分会委员
成都市高新医学会罕见病专委会常务委员
《中国小儿血液与肿瘤杂志》编委
《中华儿科杂志》审稿专家
研究速递
研究名称
拉罗替尼对获得长期缓解的TRK融合癌症患者的疗效和安全性。
研究背景
拉罗替尼是同类首创、高选择性、中枢神经系统 (CNS) 活性TRK抑制剂,基于在患有各种肿瘤类型的患者中观察到的稳健且持久的客观缓解率,该药物获准用于治疗患有TRK融合癌症的儿童和成人患者(无论肿瘤类型如何)。本次分析旨在评估拉罗替尼对长期治疗有反应的患者的疗效和安全性。
研究方法
本研究是一项汇总分析,数据来源于三项拉罗替尼的临床试验:NCT02637687 [SCOUT]、NCT02576431 [NAVIGATE] 和 NCT02122913的非 CNS TRK 融合实体瘤患者。研究纳入了经独立审查委员会根据RECIST v1.1(实体瘤疗效评价标准1.1版)标准评估达到完全缓解 (CR)、病理性 CR (pCR) 或部分缓解 (PR) 至少 2 年患者。成人患者接受每天两次100 mg拉罗替尼治疗,大多数儿童患者则接受每天两次100 mg/m²的剂量。本次分析的数据截止日期为2024年7月20日。
研究结果
⊙ 患者基线特征
截至数据截止,在304例基线时可测量的非中枢神经系统TRK融合肿瘤患者中,31%(共95例,含53例成人和42例儿童)实现了长期缓解(≥2年),其中22%的患者缓解持续时间超过5年。
肿瘤类型有10种,其中最常见的是软组织肉瘤(25例,26%)和婴儿纤维肉瘤(23例,24%)(表1)。78例(82%)患者通过二代测序(NGS)鉴定出NTRK基因融合,11例(12%)患者通过荧光原位杂交鉴定出NTRK基因融合,5例(5%)患者通过聚合酶链式反应鉴定出NTRK基因融合,1例(1%)患者通过染色体微阵列鉴定出NTRK基因融合。共有 17 种独特的基因融合,其中 ETV6::NTRK3 最为常见(n=46;48%)。
在转移性/不可切除的病例中,46 名(48%)患者未接受过全身治疗,24 名(25%)患者接受过 2 种或 2 种以上的既往治疗。
表1. 患者基线特征
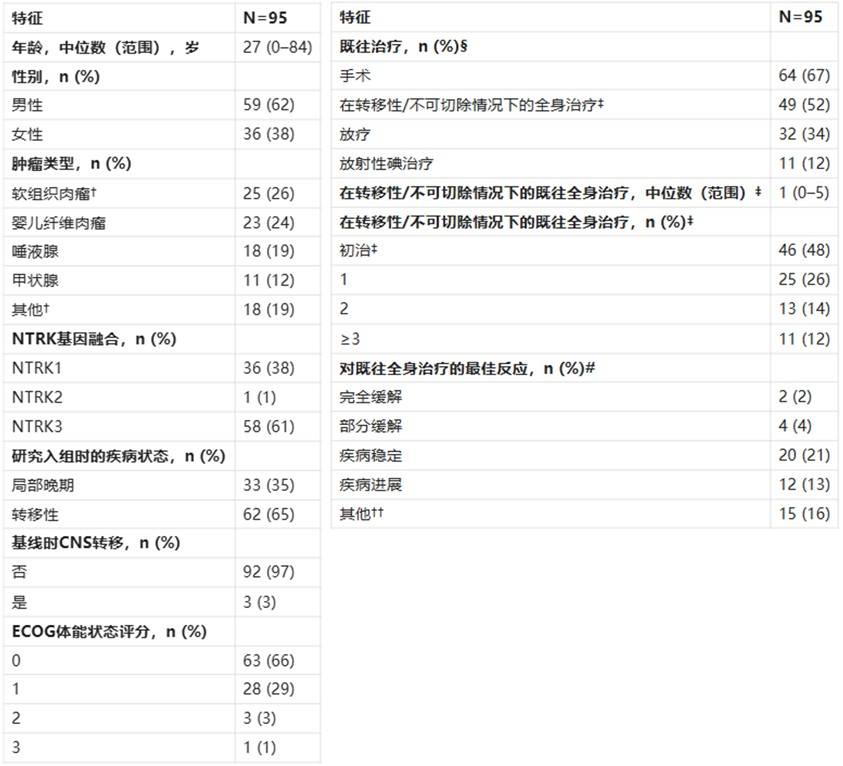
⊙ 疗效数据
共有46 名(48%)患者达到 CR,14 名(15%)患者达到 pCR,35 名(37%)患者达到 PR。
在 21 名反应持续≥5年的患者中,13 名(62%)达到 CR,4 名(19%)达到 pCR,4 名(19%)达到 PR。
中位持续治疗时间为 52 个月。中位至缓解时间为 1.8 个月(范围 0.9-22.9)。截至数据截止时,51 名(54%)患者继续使用拉罗替尼,44 名(46%)患者停药;其中 11 名(25%)患者因病情进展而停药。
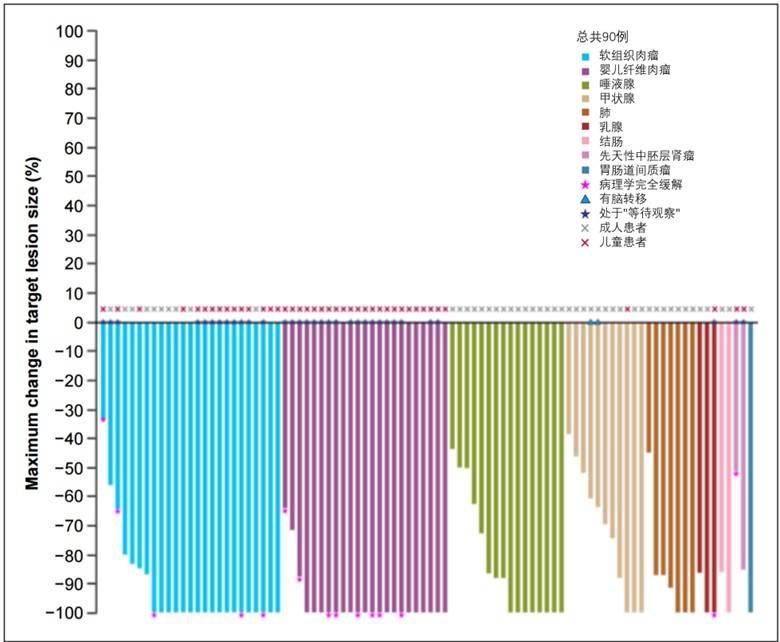
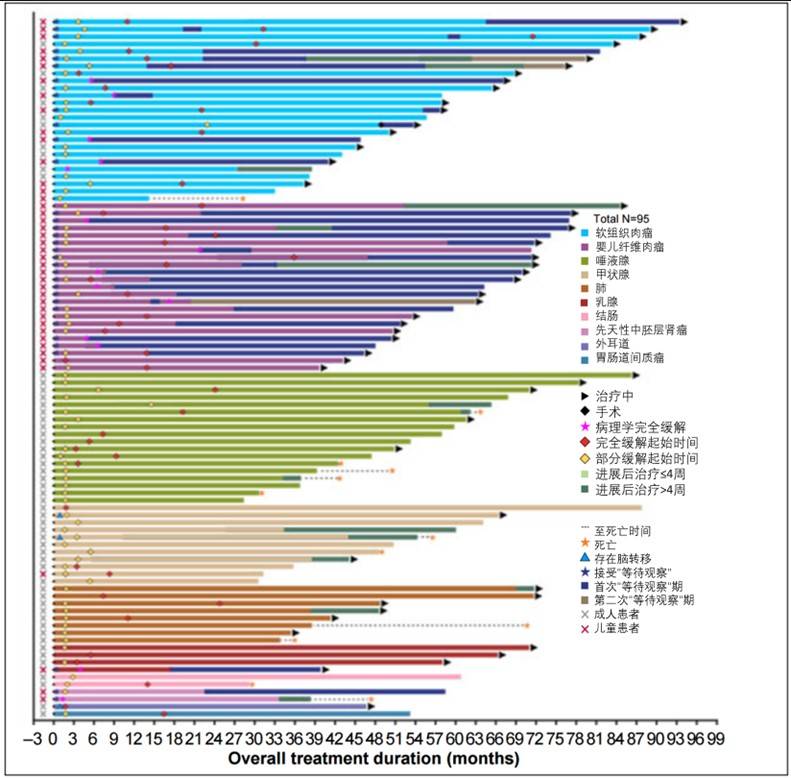
中位缓解持续时间(DoR)、中位无进展生存期(PFS)、中位总生存期(OS)见图3。
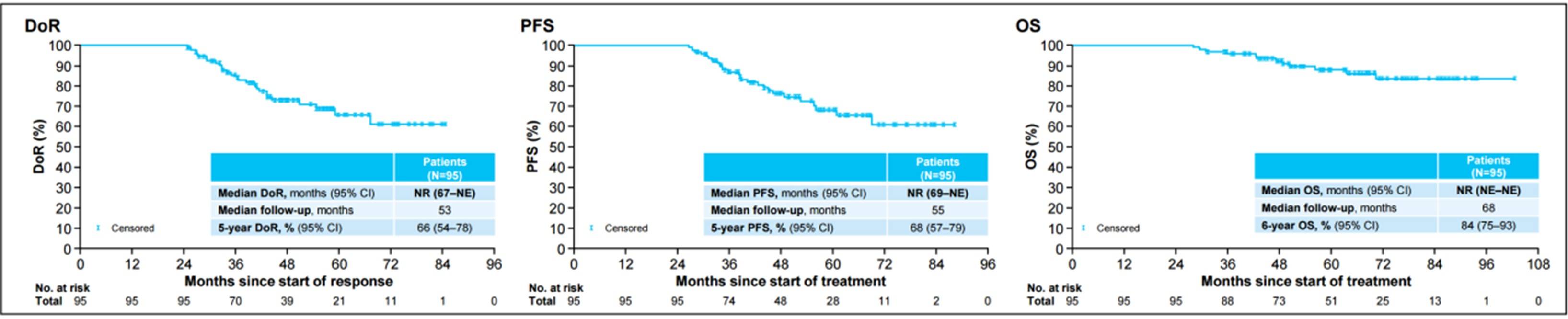
⊙ “等待-观察”状态分析
在SCOUT研究的42例患者中,33例(79%)在未出现进展的情况下暂停拉罗替尼治疗,进入‘等待-观察’期。截至数据截止时,16 名(48%)患者正处于第一个“等待—观察”期。第一个“等待—观察”期的中位持续时间为 33 个月(范围 1-72)。在退出第一个“等待—观察”期的 17 名(52%)患者中,9 名病情进展并恢复治疗(3 名 CR、2 名 PR [1 名有待确认]、2 名SD、1 名无法评估和 1 名未定义)。另外 8 名(24%)患者结束了研究并在数据截止时仍然存活。
⊙ 安全性数据
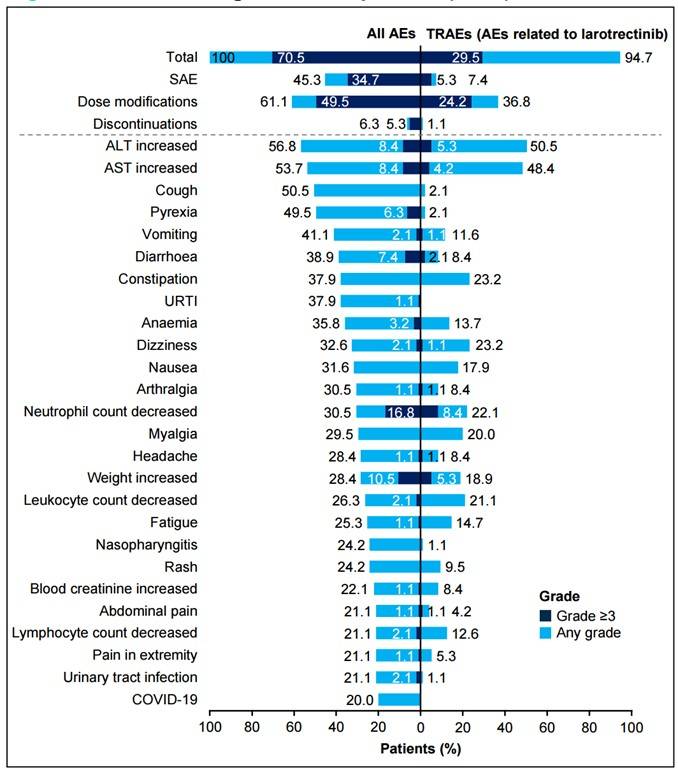
拉罗替尼的安全性可控。治疗相关不良事件(TRAEs)主要为1–2级。28 例(29%)患者出现 3/4 级 TRAE。最常见的是中性粒细胞计数减少(8 例)、丙氨酸氨基转移酶升高和体重增加(各 5 例)、天冬氨酸氨基转移酶升高(4 例)以及血碱性磷酸酶升高和腹泻(各 2 例)。一名(1%)患者因 TRAE(情感贫乏)而停止治疗。没有患者因TRAE而死亡。
研究结论
拉罗替尼对非中枢神经系统 TRK 融合癌症患者表现出持久的长期反应、延长的生存期和可控的安全性。在304名患者中,95 名(31%)对拉罗替尼的疗效持续至少2年。“等待—观察”结果提示,对于部分儿童患者,停用拉罗替尼可能是可行的。然而,仍需更多有关最佳治疗时长的信息。
研究结果支持更广泛地采用NGS检测,包括NTRK基因融合来识别可能受益于TRK抑制剂治疗的患者。

专家点评
张俊平教授: 这次ESMO大会上公布的拉罗替尼长期数据,确实让我们很受鼓舞,也带来了很多启发。其中最亮眼的就是它展现出的长期生存效益。我们看到,那些获得长期缓解(超过2年)的患者,6年总生存率能达到84%,5年无进展生存率也有68%。这说明什么呢?说明对于有特定驱动基因的肿瘤,我们通过基于分子分型的精准治疗,完全有可能把一些过去认为很棘手、预后差的侵袭性肿瘤,变成一种可以长期管理的慢性病。
这个研究让我们更加相信拉罗替尼的安全性。患者长期用药的安全性,是医患都非常关注的问题。数据显示,大部分治疗相关的不良反应都比较轻微,是1-2级的;3/4级的相对少见,而且可控,更重要的是没有出现和药物相关的死亡事件。拉罗替尼长期耐受性良好,为患者能够持续用药、最终获益打下了坚实基础,也让我们临床医生用起来更有底气。
我想强调的是该研究再次印证了 “检测先行,治疗随后”的精准治疗核心理念。NTRK基因融合是个关键的致癌驱动,只有先精准地把它找出来,后续的治疗才能有的放矢。研究里超过80%的患者都是通过NGS检测发现的融合基因。这就提醒我们,对于所有晚期的成人和儿童实体瘤患者,都应该把全面的分子检测(尤其是DNA+RNA-NGS双重检测)作为标准流程来推行。只有这样,我们才能确保不落下任何一个可能从拉罗替尼这类精准药物中获益的患者。
郭霞教授:作为儿科肿瘤医生,这次更新的数据,特别是对儿童患者的深入分析,给我们的临床实践提供了非常重要的参考。
儿童肿瘤治疗,我们的目标不仅仅是提高生存率,还要高度重视患儿未来的生活质量和生长发育。这项研究纳入了42名儿童患者,结果显示拉罗替尼在他们身上取得了持久且深度的缓解。它能够有效缩小肿瘤,这为我们实施功能保全手术创造了条件,甚至让部分患儿避免了手术,这对保障他们远期的生活质量至关重要。
这项研究还有一个非常创新的点,就是探索了“等待-观察”策略。在SCOUT研究的患儿里,有高达79%的患儿在获得深度缓解后,尝试了停药进入观察期,而且这个观察期的中位时间长达33个月。这个策略直面了我们儿科治疗中的一个核心关切:怎么尽可能地减少患儿长期暴露在药物下的时间,降低对生长发育的潜在影响。而且数据还告诉我们,即使有部分患儿后来复发了,重新用上拉罗替尼依然有效,这就给尝试“等待-观察”策略提供了重要的安全底线。这个探索为我们未来制定更个体化、更人性化的方案打开了新思路——在严密监控下,给那些达到深度缓解的患儿一个“治疗假期”,让他们有机会更好地回归正常生活。
另外,大家都知道,儿童的器官功能还没完全发育成熟,对药物更敏感。这项长达数年的随访数据,再次证实拉罗替尼在儿童中的安全性是可控的,没有出现新的、意想不到的长期毒性信号,这让我们在临床上可以更放心地为患儿推荐和使用这一药物。
总而言之,这项研究不仅再次确立了拉罗替尼是NTRK融合阳性儿童患者一个不可或缺的治疗选择,它通过对“等待-观察”策略的前瞻性探索,更是引领我们去追求儿童肿瘤治疗的更高目标——在治愈疾病的同时,守护好患儿的成长和未来。要实现这个目标,我们必须把NTRK融合检测全面纳入儿童实体瘤的常规诊断,确保每一个可能获益的患儿都不会被遗漏。
排版编辑:Crystal











 苏公网安备32059002004080号
苏公网安备32059002004080号


