每年11月10日为神经内分泌肿瘤日(NET Cancer Day),设立该纪念日旨在提高大众对神经内分泌肿瘤的认知,为神经内分泌肿瘤这一罕见肿瘤的患者群体发声,以改善该疾病的诊断、治疗、护理及研究。2025年的神经内分泌肿瘤日,由上海市防癌抗癌事业发展基金会主办,陈洁教授领衔的复旦大学附属肿瘤医院神经内分泌肿瘤多学科团队,联合国内多位神经内分泌肿瘤专家,举办了公益云问诊,为神经内分泌肿瘤患者提供线上公益问诊,解答患者及家属在神经内分泌肿瘤诊治过程中可能存在的困惑,以期患者得到更好的治疗和照护。本期详细阐述云问诊的第2例病例—副神经节瘤(PGL)的诊治经过及多学科讨论,并记录了陈洁教授对患者及家属提出的问题进行的细致解答。
病例介绍
患者基本情况:男性,35岁。
主诉:发现右侧颈部肿物2年。
诊疗经过:2023年10月发现右侧颈部肿物,未治疗,后至西安交大二院。
MRI增强示:右侧咽旁间隙肿物,较大截面3.9*2.0cm,考虑颈静脉球体瘤可能。B超示右侧咽旁间隙低回声肿块,考虑咽旁间隙新生占位伴右侧颈部淋巴结转移。右侧颈部淋巴结穿刺病理:圆形细胞肿瘤,结合免疫组化考虑副神经节瘤。免疫组化:CgA(+)、Syn(+)、CD56(+)、S-100灶(+)、CD34血管(+)、P53少数(+)、P16(-)、Ki-67(+)5%、CK(-)、CK18(-)、CK19(-)、EMA(-)、P63(-)、CK5/6(-)、Calponin(-)、CD117(-)、CEA(-)、SMA(-)。
家族史:父亲于2023年确诊前列腺癌晚期伴骨转移,曾行基因检测提示: SDHB基因胚系变异。

2024年5月31日复查MRI示右侧咽旁间隙、右侧颈血管走行区至右侧颈静脉球区异常强化肿块,考虑肿瘤性病变,颈静脉球瘤?较前稍增大。
患者未治疗,于2024年10月至上海九院就诊。CT示:右颈鞘区-颈静脉孔区占位,病灶部分包绕右颈内外动脉。MRI示:右侧颈静脉孔区、颈动脉分叉处、颈鞘前外侧多发占位,副神经节瘤可能。
手术治疗:2024年10月16日全麻下行“右侧颈静脉孔病损切除术(岩枕跨乙状窦径)+颈部肿瘤切除手术”。术后病理:(颈静脉球瘤肿物)符合副神经节瘤。免疫组化:CK(-), Syn(+), CHGA(+), CD56(+), CD34(血管+), S100(支持细胞+), SOX-10(支持细胞+), SSTR-2(少量+), SDHB(+), INSM1(+), EMA(-), Ki67(3%+)。
术后未进一步药物治疗,2024年11月6日术后复查MRI示:“右颈静脉孔肿瘤术后”改变,未见明确肿瘤复发。

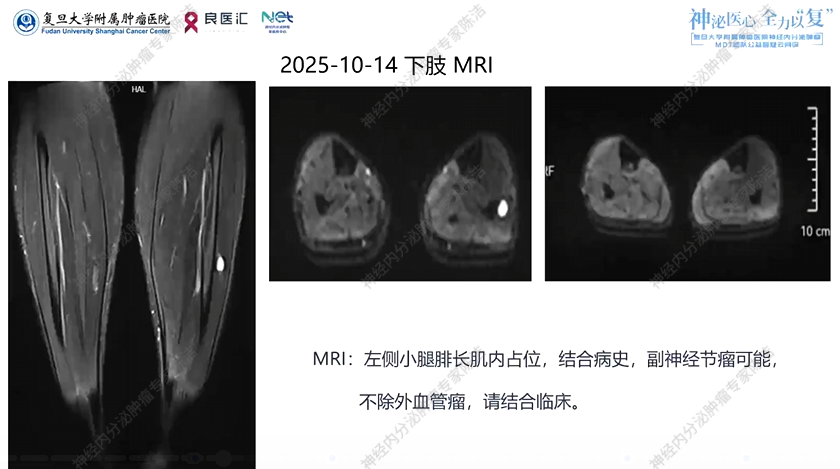
2025年9月,患者无意中发现左下肢肿物,至运城市中心医院,2025年10月14日行MRI示:左侧小腿腓长肌内占位,结合病史,副神经节瘤可能,不除外血管瘤。
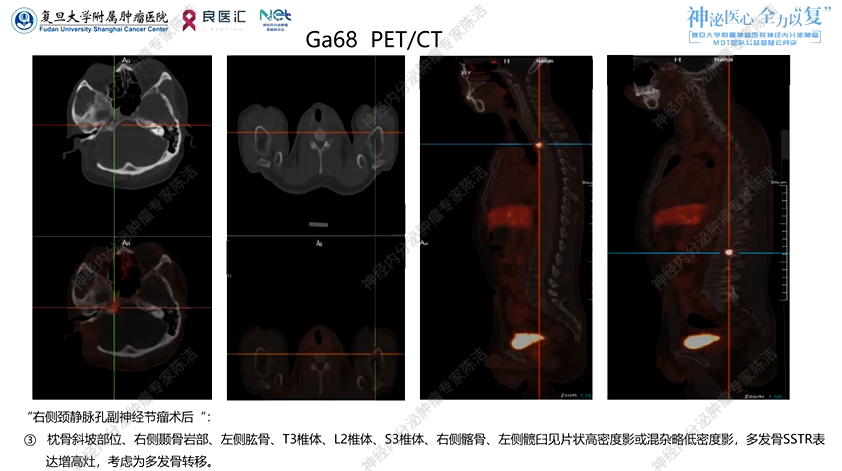
后至上海九院复查,2025年10月21日复查MRI增强示:右侧颈静脉孔及颈鞘区异常强化结节(右侧颈静脉孔及颈鞘区可见斑片状、结节状异常信号,最大截面约13*9mm)。2025年10月28日南京第一医院行Ga68-DOTANOC PET-CT,检查结果示:①鼻咽右侧咽旁间隙结节影、SSTR表达增高,考虑为肿瘤灶。②右颈部胸锁乳突肌内侧略大淋巴结,SSTR表达增高,考虑为淋巴结转移;③枕骨斜坡部位、右侧颞骨岩部、左侧肱骨、T3椎体、L2椎体、S3椎体、右侧髂骨、左侧髋臼见片状高密度影或混杂略低密度影,多发骨SSTR表达增高灶,考虑为多发骨转移。
目前已行基因检测,结果尚未回报。
目前无明显骨痛等症状,外院建议安罗替尼治疗,患者暂未开始治疗。

MDT讨论
病理科李媛教授:这个病例的病理诊断是明确的。副神经节瘤属于非上皮性的神经内分泌肿瘤。我们通过免疫组化进行鉴别:首先,上皮标记物CK是阴性的,排除了上皮源性肿瘤;其次,神经内分泌标记物Syn、CgA、CD56均呈阳性。此外,副神经节瘤还有一个特征,即存在支持细胞,这在免疫组化上表现为S100阳性,而本例患者S100呈散在阳性。结合病理形态、免疫组化表型及发生部位,诊断符合副神经节瘤。

核医学科徐俊彦教授:根据患者提供的磁共振影像,在左侧腓肠肌外侧可以看到一个异常信号结节,从DWI(弥散加权成像)上看,其血供是比较丰富的。这一表现符合副神经节瘤发生肌肉转移的影像特征。
患者接受了生长抑素受体(SSTR)PET-CT显像。在手术区域(右侧颈静脉孔区)及右颈后部,我们仍能看到SSTR高表达的病灶,考虑为肿瘤残留或复发。同时,在颈部淋巴结(左侧颈动脉鞘区)也观察到了高表达的转移灶。
在骨骼系统,虽然CT平扫未见明确的骨质破坏,但SSTR-PET显示在枕骨斜坡、T3椎体、L2椎体、S3椎体、骶骨及左侧髂骨均存在多发、散在的SSTR高表达病灶,考虑为多发骨转移。这提示SSTR-PET在诊断NET骨转移方面远比CT敏感,可能提前3-6个月发现病灶。
患者还补充进行了一次MFBG(间氟苄胍)显像,这是一种类似MIBG的显像,通常用于评估是否适合MIBG治疗。影像显示小腿的病灶并未摄取MFBG。
对于副神经节瘤这类肿瘤,多模态显像非常重要。需要特别注意的是,PGL在发生转移时常表现出高度的异质性,尤其是在肝转移灶上,SSTR的表达可能低于原发灶或其他转移灶。因此,在制定PRRT(肽受体放射性核素治疗)方案前,必须全面评估所有病灶的SSTR表达情况。


陈洁教授总结(并回答患者提问)

这是一例诊断明确的病例,结合其明确的SDHB突变家族史,考虑为“SDHB基因突变相关的遗传性/家族性副神经节瘤”。目前患者已出现淋巴结及多发骨转移,分期为IV期。
针对患者提出的问题进行解答:
1、恶性副神经节瘤骨转移如何分期?积极治疗存活期多久?
陈洁教授:患者目前已出现骨和肌肉转移,属于IV期(晚期)。但副神经节瘤,尤其是头颈部的,通常生长非常缓慢。骨转移是PGL常见的转移途径,特别是SDHB突变相关的PGL。虽然已发生骨转移,但目前肿瘤负荷相对较低,仅为散在的几个小病灶。因此,积极治疗的预期生存期不会太短,超过5年乃至更久是很有可能的。
2、骨转移部位感觉到多痛的时候,需要去做骨水泥?
陈洁教授:是否需要行骨水泥(PVP)治疗,不是根据疼痛程度,而是根据影像学(CT)显示的骨质破坏程度。骨水泥适用于溶骨性破坏、有潜在病理性骨折风险的患者。目前你的骨转移灶在CT上均不明显,尚未达到需要骨水泥干预的程度。
3、安罗替尼和替莫唑胺数据效果都好,可以两个结合使用吗?耐药后,后续的治疗方案?
陈洁教授:PGL的全身治疗方案选择,很多时候是参考其他神经内分泌肿瘤的数据。包括生长抑素类似物(SSA):如奥曲肽或兰瑞肽。适用于SSTR阳性、肿瘤负荷低的患者;TKI类靶向药:如舒尼替尼、安罗替尼等;化疗:如替莫唑胺;核素治疗:包括基于SSTR表达的PRRT(如Lu-177)和基于MIBG的核素治疗。我们中心的回顾性研究显示,TKI和替莫唑胺的无进展生存期(PFS)约1-1.5年。SSA的PFS看似更长,但这存在选择偏倚,因为我们主要给肿瘤负荷不高的患者使用SSA。针对你目前的病情,肿瘤负荷较低,可以选择相对温和的治疗,即SSA(奥曲肽或兰瑞肽)。但是在治疗前,需先做一个肝脏的增强MRI或CT,以排除SSTR阴性的肝转移。如果没有肝转移,建议从低剂量的SSA(如兰瑞肽90mg)开始。而安罗替尼、舒尼替尼或化疗是后续进展后的药物选择,可保留在后面使用。
4、颈部手术后导致声音嘶哑一年了,后续计划脂肪填充手术修复声音,会影响肿瘤吗?
陈洁教授:不影响。因术后声音嘶哑想做脂肪填充等修复手术,是可以的,这与肿瘤治疗不冲突。
5、需要给孩子做基因检测吗?现在6岁,每年体检哪些项目?
陈洁教授:必须检测!目前考虑是家族性PGL,由SDHB致病突变引起,这是一种常染色体显性遗传,你的子女有50%的概率遗传了这个突变基因。孩子现在6岁,应尽快抽血进行胚系基因检测。如果孩子未携带致病突变,那么他就是健康的,这方面无需过多关注。但如果他携带致病突变,鉴于PGL的发病年龄可能很早,他需要从现在开始,每年进行严格的体检筛查(例如全身体检及增强CT等)。
6、患者追问小腿病灶是否副神经节瘤转移。
陈洁教授:PGL转移到肌肉(如腓肠肌)是比较罕见的。你提供的MRI影像(DWI)不完整,且SSTR-PET未能覆盖到小腿。建议你下次复查SSTR-PET时,务必提醒医生要扫描到足踝部,如果这个小腿病灶也摄取SSTR,那么转移诊断成立;如果不摄取,则需进一步评估其异质性或考虑其他诊断。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看神经内分泌肿瘤MDT云诊室-国际神经内分泌肿瘤日在线科普义诊暨CACA神经内分泌肿瘤专委会系列科普活动回放:
https://doctor.liangyihui.net/#/doc/158041

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。











 苏公网安备32059002004080号
苏公网安备32059002004080号


