每年11月10日为神经内分泌肿瘤日(NET Cancer Day),设立该纪念日旨在提高大众对神经内分泌肿瘤的认知,为神经内分泌肿瘤这一罕见肿瘤的患者群体发声,以改善该疾病的诊断、治疗、护理及研究。2025年的神经内分泌肿瘤日,由上海市防癌抗癌事业发展基金会主办,陈洁教授领衔的复旦大学附属肿瘤医院神经内分泌肿瘤多学科团队,联合国内多位神经内分泌肿瘤专家,举办了公益云问诊,为神经内分泌肿瘤患者提供线上公益问诊,解答患者及家属在神经内分泌肿瘤诊治过程中可能存在的困惑,以期患者得到更好的治疗和照护。本期详细阐述云问诊的第1例病例—肺不典型类癌的诊治经过及多学科讨论,并记录了陈洁教授对患者及家属提出的问题进行的细致解答。
病例介绍
患者基本情况:女性,52岁。
诊疗经过
2023年11月,患者因背痛就诊,于外院行胸部CT检查提示右下肺软组织影,大小约27mm*16mm。肿瘤标志物检测提示:NSE 27.91 ng/ml,胃泌素释放肽前体 735.81 pg/ml。行EBUS-FNA活检,病理提示未见肿瘤细胞。患者选择中医治疗,并定期复查。
2024年1月,患者发现左乳肿块,暂无治疗。
2024年5月,患者左乳肿物疼痛明显,查体:左乳肿块,2*2cm,质韧偏硬,边界欠清,活动度欠佳。乳腺彩超提示左乳实质性结节,BI-RADS 4b类。胸部CT平扫提示:1.左乳内下象限结节21*16mm,符合乳腺癌改变;2.右肺下叶团片灶30*16mm,感染?3.右肺上叶病变,结核可能;4.双肺多发微小结节;5.肝左内叶稍低密度灶30*22mm,血管瘤?6.T3体异常密度灶。乳腺MR提示左乳外下象限结节(2个),BI-RADS4类。患者行左乳肿块粗针穿刺活检术。
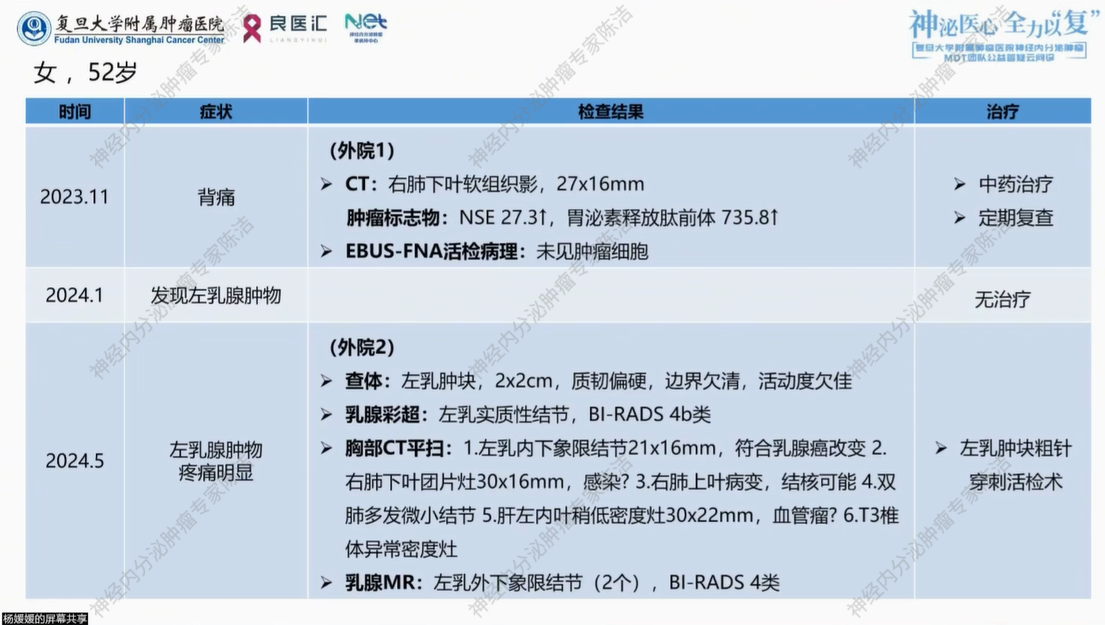
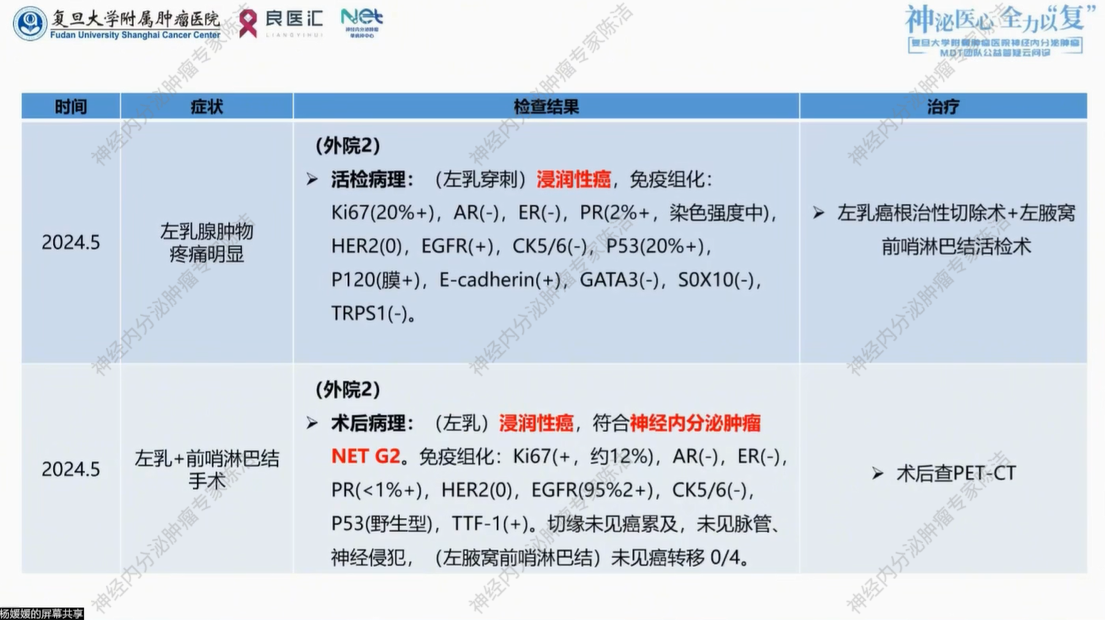
穿刺活检病理提示为浸润性癌,免疫组化:Ki67(20%+),AR(-),ER(-),PR(2%+,染色强度中),HER2(0),EGFR(+),CK5/6(-),P53(20%+),P120(膜+),E-cadherin(+),GATA3(-),SOX10(-),TRPS1(-)。
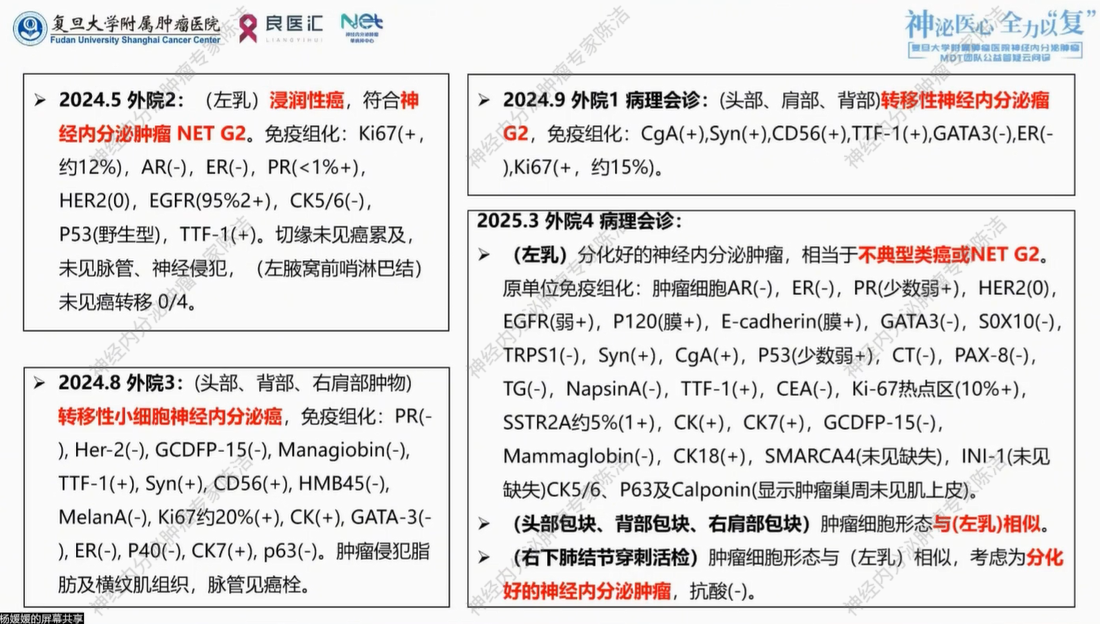
患者于外院行左乳癌根治性切除术+左腋窝前哨淋巴结活检术。术后病理提示:(左乳)浸润性癌,符合神经内分泌肿瘤NET G2。免疫组化:Ki67(+,约12%),AR(-),ER(-),PR(<1%+),HER2(0),EGFR(95%2+),CK5/6(-),P53(野生型),TTF-1(+)。切缘未见癌累及,未见脉管神经侵犯,(左腋窝前哨淋巴结)未见癌转移0/4。
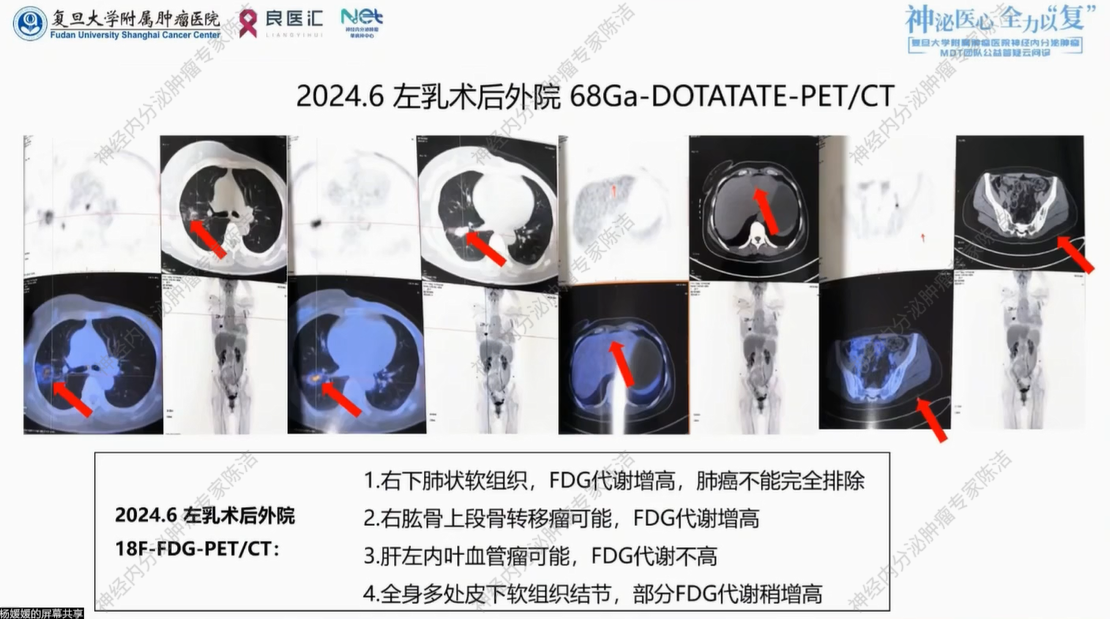
2024年6月,患者术后于外院复查PET-CT,18F-FDG及68Ga-DOTATATE-PET/CT双扫提示:1.左乳术后复查,术区皮肤稍增厚,FDG代谢稍增高,SSTR表达不高;左腋窝区团片灶,FDG代谢稍增高,SSTR表达不高;双腋窝区多发小淋巴结,FDG代谢不高,SSTR表达不高;右下肺团块状软组织密度灶,FDG代谢增高,SSTR表达稍增高考虑炎性肉芽肿,肺癌不排除;2.右肱骨上段稍高密度灶,SSTR表达增高,多为骨转移瘤;3.肝左内叶稍低密度灶FDG代谢不高,SSTR表达不高,考虑血管瘤;4.全身多处皮下软组织结节,部分FDG代谢稍增高,部分SSTR表达稍增高。
胸部CT平扫提示:对比2024.1.16,右肺上叶、右肺下叶26x14mm、左肝稍低密度灶,较前相仿。
后患者分别于2024.6.26、2024.7.17、2024.8.8于外院按左乳浸润性癌行EC-T方案(环磷酰胺+表柔比星)化疗3程。

2024年8月,患者出现皮肤多处结节病灶疼痛难忍,分别行头部、背部、右肩肿物切除术。术后病理提示:(头部、背部、右肩部肿物)转移性小细胞神经内分泌癌,免疫组化:PR(-),Her2(-),GCDFP-15(-),Managiobin(-),TTF-1(+),Syn(+),CD56(+),HMB45(-),MelanA(-),Ki67约20%(+),CK(+),GATA-3(-),ER(-),P40(-),CK7(+),p63(-)。肿瘤侵犯脂肪及横纹肌组织,脉管见癌栓。
术后外院给予索凡替尼300mg qd治疗。
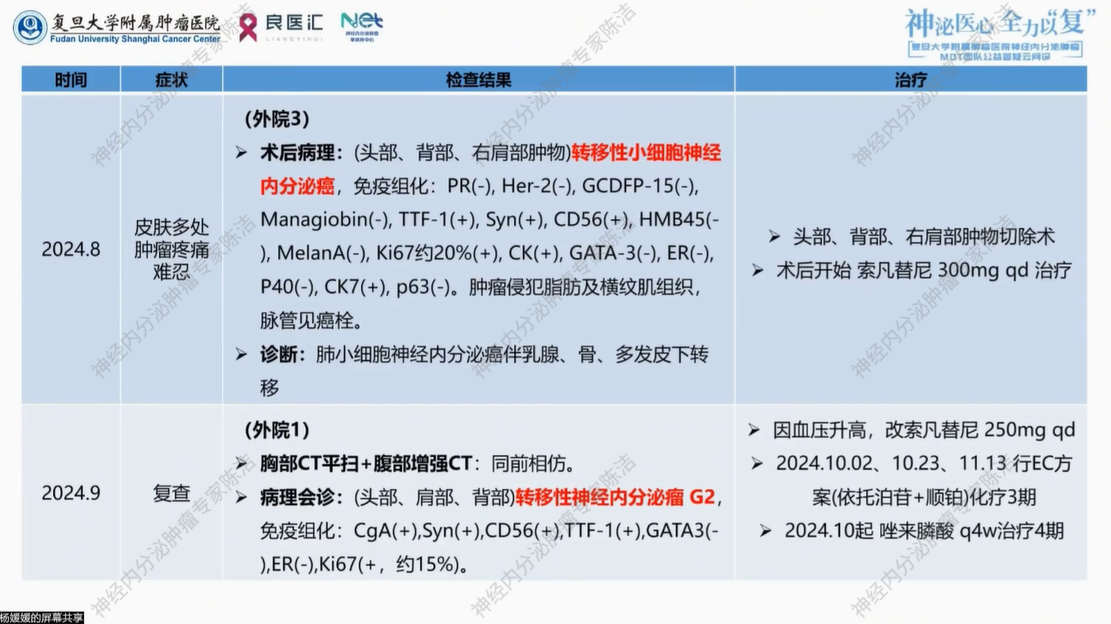
2024年9月复查,胸部CT平扫+腹部增强CT提示同前相仿。外院行病理会诊:(头部、肩部、背部)转移性神经内分泌瘤 G2。免疫组化:CgA(+),Syn(+),CD56(+),TTF-1(+),GATA3(-),ER(-),Ki67(+,约15%)。治疗期间患者因血压升高,改索凡替尼250mg qd。2024.10.02、10.23、11.13外院行EC方案(依托泊苷+顺铂)化疗3程,并于2024年10月给予唑来膦酸q4w治疗4期。
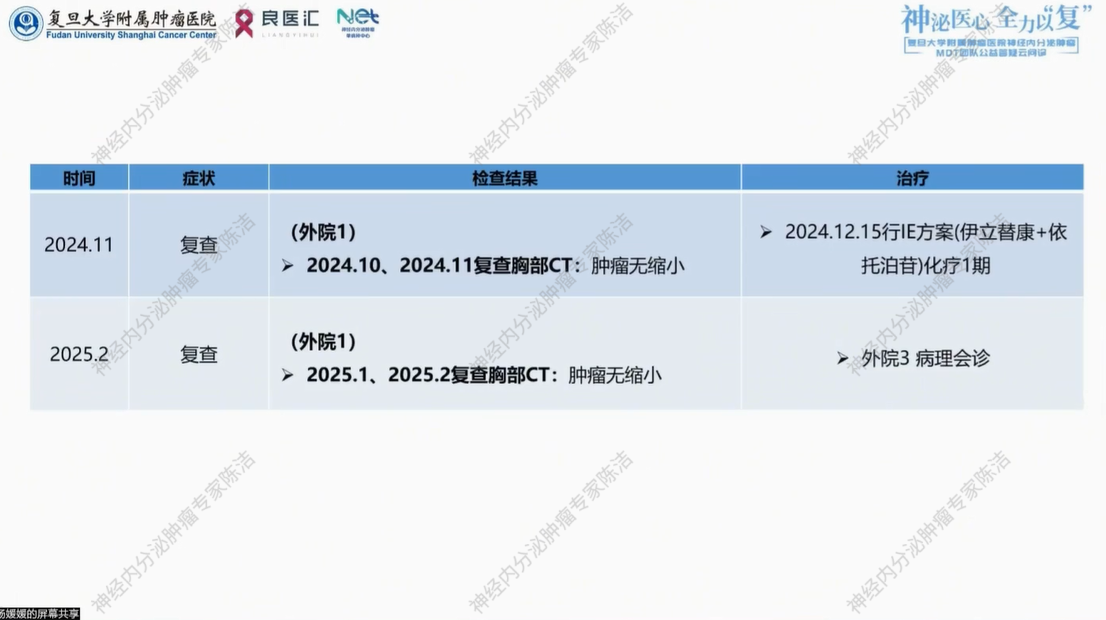
患者分别于2024年10月、11月、2025年1月及2月复查胸部CT,提示肿瘤无缩小。外院于2024.12.15予IE方案(伊立替康+依托泊苷)化疗1程。
2025年2月患者于另一家外院行多部位病灶的病理会诊:
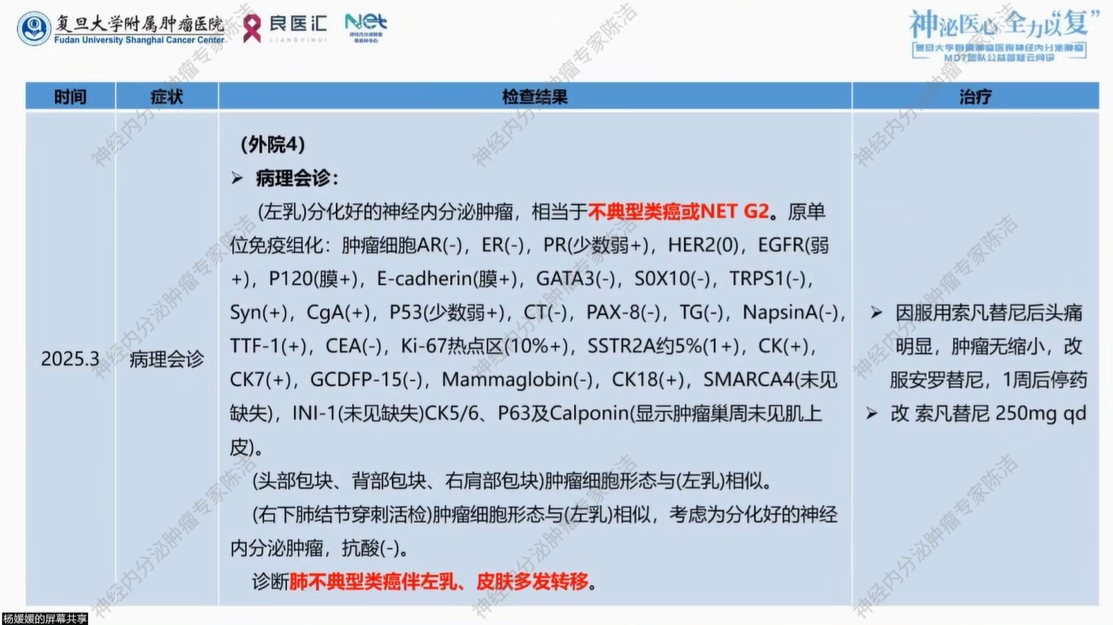
(左乳)分化好的神经内分泌肿瘤,相当于不典型类癌或NET G2。原单位免疫组化:肿瘤细胞AR(-),ER(-),PR(少数弱+),HER2(0),EGFR(弱+),P120(膜+),E-cadherin(膜+),GATA3(-),S0X10(-),TRPS1(-),Syn(+),CgA(+),P53(少数弱+),CT(-),PAX-8(-),TG(-),NapsinA(-),TTF-1(+),CEA(-),Ki-67热点区(10%+),SSTR2A约5%(1+),CK(+),CK7(+),GCDFP-15(-),Mammaglobin(-),CK18(+),SMARCA4(未见缺失),INI-1(未见缺失)CK5/6、P63及Calponin(显示肿瘤巢周未见肌上皮)。
(头部包块、背部包块、右肩部包块)肿瘤细胞形态与(左乳)相似。
(右下肺结节穿刺活检)肿瘤细胞形态与(左乳)相似,考虑为分化好的神经内分泌肿瘤,抗酸(-)。
患者因服用索凡替尼后头痛明显,肿瘤无缩小,于外院改用安罗替尼,1周后停药,后改回索凡替尼250mg qd。
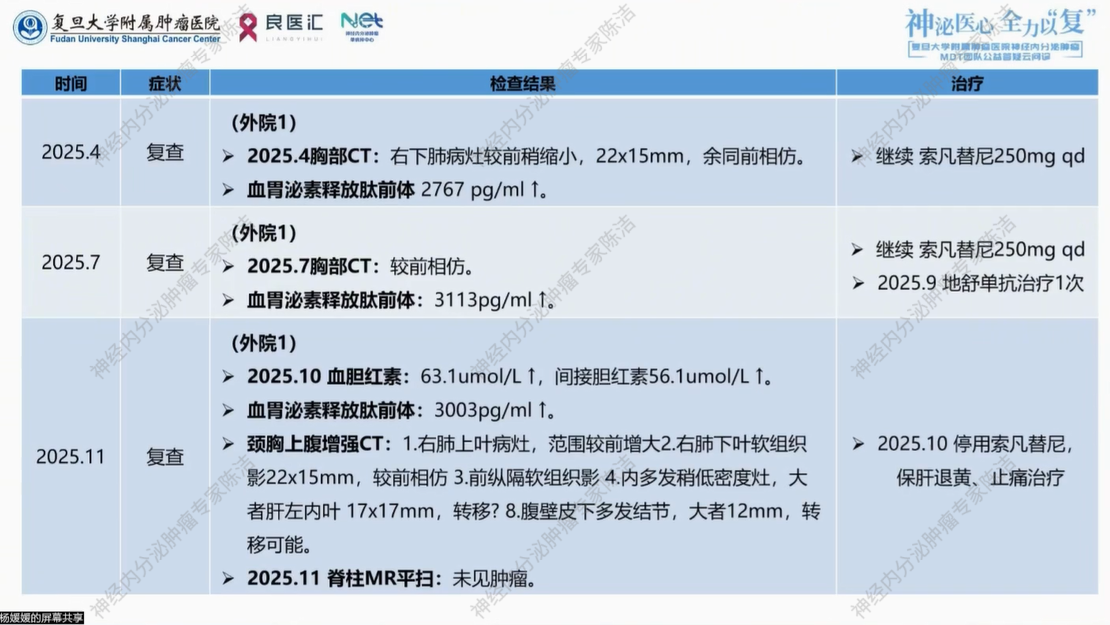
2025年4月,患者复查,胸部CT提示:右下肺病灶较前稍缩小,22*15mm,余同前相仿。血胃泌素释放肽前体767 pg/ml↑。患者继续应用索凡替尼250mg qd。
2025年7月,患者复查,胸部CT提示较前相仿。血胃泌素释放肽前体3113pg/ml。患者继续应用索凡替尼250mg qd,并于2025年9月予以地舒单抗治疗1次。
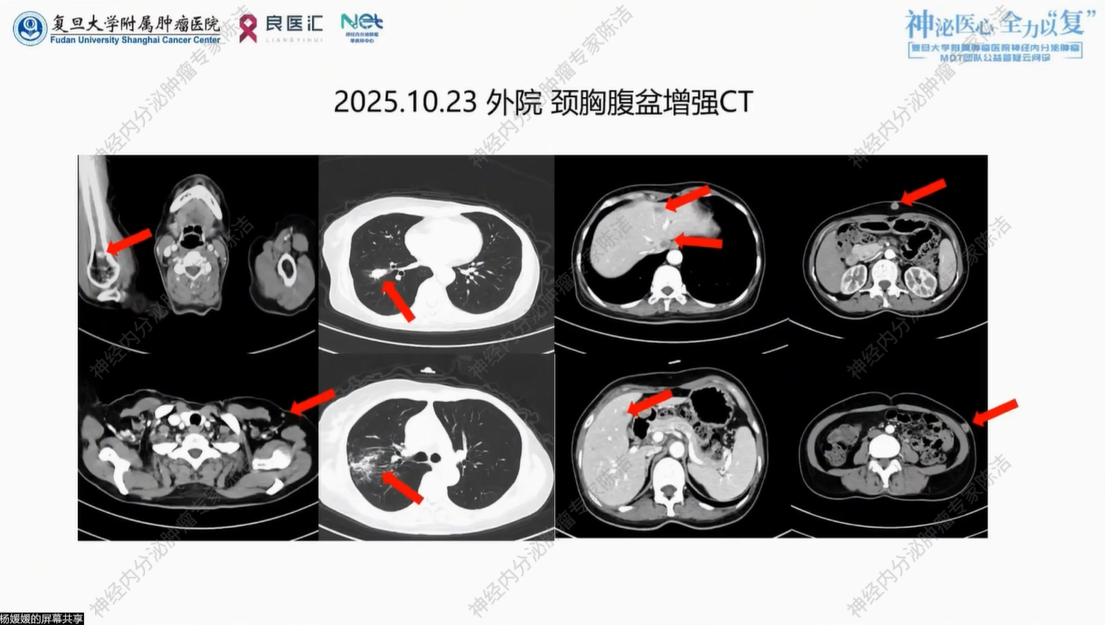
2025年11月外院复查,血胆红素:63.1umol/L,间接胆红素56.1umol/L。血胃泌素释放肽前体:3003pg/ml。颈胸上腹增强CT提示:1.右肺上叶病灶,范围较前增大;2.右肺下叶软组织影22*15mm,较前相仿;3.前纵隔软组织影;4.内多发稍低密度灶,大者肝左内叶17*17mm,转移?8.腹壁皮下多发结节,大者12mm,转移可能。脊柱MR平扫提示未见肿瘤。患者于2025年10月停用索凡替尼,保肝退黄、止痛治疗。
MDT 讨论
病理科李媛教授:本病例的病理诊断具有挑战性。首先,针对2024年5月左乳肿块最初被诊断为“NET G2”,虽然它是低级别神经内分泌肿瘤,但其免疫组化显示TTF-1阳性。TTF-1阳性在低级别NET中提示肿瘤可能来源于肺或胸腺,而真正的乳腺原发神经内分泌肿瘤较为罕见,因此当时应首先考虑肺神经内分泌肿瘤转移。其次,对于2024年8月多发转移灶被诊断为“转移性小细胞神经内分泌癌”存疑,因为小细胞神经内分泌癌作为低分化癌,其Ki-67通常极高,而本例仅为20%左右,直到后续会诊修正为“转移性神经内分泌肿瘤G2”。综合所有病变部位(乳腺、皮下等)的分化程度和表型来看,它们高度一致,均符合分化较好的神经内分泌肿瘤(相当于NET G2或不典型类癌)。结合影像学显示的“原发灶小、转移灶广泛”的特点,考虑这并非多原发肿瘤,而是一例原发于肺的不典型类癌,随后发生了全身多处的转移。
核医学科徐俊彦教授:在FDG-PET/CT图像中,右下肺可见高糖代谢原发肿瘤,伴有周围阻塞性炎症。对于此前怀疑的右侧肱骨病灶,在PET/CT图像上未明确显示。值得注意的是,肝左叶在脂肪肝背景下显示出一个更低密度的病灶,虽糖代谢不高,但考虑到部分神经内分泌肿瘤本身代谢活性较低,不能仅凭FDG低代谢排除转移,需结合解剖影像综合判断。
通过CT影像对比,虽然右下肺原发灶形态上略有缩小扁平化,但疾病整体呈现明显的进展,出现了多新发转移灶。CT明确显示右侧肱骨上端有成骨性改变;同时在腋窝及腹壁皮下发现多发实性结节,这解释了患者的疼痛症状,皮肤是肺/喉来源神经内分泌肿瘤常见的转移部位。CT显示肝左叶、尾状叶及右前叶多发病灶边缘强化,影像特征支持转移瘤。建议后续进行普美显增强MRI,以更精准地评估肝内肿瘤负荷及性质。
陈洁教授总结并回答患者提问
该病例是一例肺不典型类癌多发转移的病例,患者从2023年发病到2025年才明确病理,走了一条弯路:首先是对疾病初期迹象不够重视,随后在病理诊断上被误判为恶性程度高的小细胞肺癌,并因此错误地接受了针对小细胞肺癌的化疗方案,但效果不佳。超过半数肺不典型类癌患者在外院初诊时都可能被误诊为小细胞肺癌,导致治疗方向从一开始就出现偏差。此外,该病例表现的胃泌素释放肽前体升高、乳腺转移和疼痛性皮下结节,都是肺不典型类癌特征性的生物学行为和转移特点。
在药物治疗原则上,由于该患者肿瘤SSTR表达阴性,无法使用生长抑素类似物或PRRT,治疗锁定在靶向药和化疗。在靶向药索凡替尼的使用上,直接应用300mg的标准剂量对多数患者而言毒性过大,这位患者也一样难以耐受300mg的索凡替尼。对于索凡替尼的使用,建议从200mg起始,根据耐受性缓慢增量,以实现疗效与安全性的平衡。其次,对于生长缓慢的不典型类癌,药物治疗的主要目标是实现疾病稳定,而非追求肿瘤缩小。患者前期在未达到疾病进展标准时,就因肿瘤未缩小而频繁切换治疗方案(从靶向到化疗再回靶向),导致了治疗方案的混乱。最后,患者因不良反应和肝损伤停用索凡替尼,也凸显了加强药物不良反应管理的重要性。

针对患者及家属在治疗过程中咨询的问题,陈洁教授给出了以下解答:
问题一:黄疸消退后,是否可使用“卡培他滨+替莫唑胺”(CAPTEM方案)进行化疗?副作用如何管理?
陈洁教授:CAPTEM方案是一个可选的治疗方案。在神经内分泌肿瘤的治疗中,CAPTEM方案是针对几乎每位分化较好的神经内分泌肿瘤患者,在病程的中后期都可能会用到该方案。根据我们的临床经验,其不良反应相对可控。主要副作用集中在消化道反应(如恶心、呕吐)和骨髓毒性(如白细胞和血小板减少),但出现严重骨髓抑制的概率较低。CAPTEM的副作用管理反而相对容易。
考虑到患者目前的肿瘤负荷主要表现为肝内及皮下的散在结节,整体负荷并未达到极高程度。因此,除了CAPTEM方案外,依维莫司(mTOR抑制剂)也是一个可行的治疗方案。可以根据患者恢复后的具体体能状态,将替莫唑胺类化疗保留至肿瘤负荷进一步增大或级别转化时使用,目前先尝试依维莫司,也是合理的策略。
问题二:是否必须要使用吗啡止痛?有无更合适的止痛药可以提高生活质量?
陈洁教授:针对患者目前皮下结节引起的疼痛,患者目前使用非甾体抗炎药(NSAIDs)效果不佳,根据WHO三阶梯止痛原则,建议先升级至第二阶梯弱阿片类药物,如曲马多,这类药物对于目前描述的疼痛强度,可能提供显著且稳定的镇痛效果。对于皮下转移结节,如果药物镇痛效果仍不理想,且疼痛主要集中在个别孤立的结节上,可以考虑外科手术切除作为一种局部姑息手段。切除疼痛最剧烈的结节可以迅速缓解症状,提高生活质量。但需注意,这仅适用于结节数量少、定位明确的情况,并非对所有皮下结节的常规处理手段。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看神经内分泌肿瘤MDT云诊室-国际神经内分泌肿瘤日在线科普义诊暨CACA神经内分泌肿瘤专委会系列科普活动回放:
https://doctor.liangyihui.net/#/doc/158041

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。











 苏公网安备32059002004080号
苏公网安备32059002004080号


