人表皮生长因子受体2(HER2,又称ERBB2)是一种跨膜酪氨酸激酶受体,隶属于ERBB家族,HER2基因也是重要的原癌基因之一[1]。HER2的激活可通过PI3K/AKT和MAPK等下游信号通路,驱动肿瘤的发生与发展[1]。在非小细胞肺癌(NSCLC)中,HER2变异主要表现为HER2基因突变、HER2基因扩增和HER2蛋白过表达三种形式[2, 3, 4]。在过去,HER2变异的NSCLC患者缺乏有效的靶向治疗手段,预后较差。然而,近年来,随着以德曲妥珠单抗(T-DXd)为代表的新型抗体偶联药物(ADC)以及新一代HER2-TKI的问世,HER2变异NSCLC的治疗格局已被彻底改写。基于此,【肿瘤资讯】特邀中山大学附属第一医院唐可京教授盘点HER2变异NSCLC的检测诊断现状,并对其未来发展进行展望。
中山大学附属第一医院
呼吸与危重症医学科副主任、药学部主任/党总支部书记、感染性疾病科主任
中山一院肺癌MDT首席专家,Ⅲ期肺癌多学科联合规范化诊疗中心、肺癌诊疗一体化中心、肿瘤免疫治疗不良反应MDT团队负责人
美国范德堡 (Vanderbilt) 大学医学中心访问学者
美国德州大学西南医学中心 (UTSW) Harold C. Simmons综合癌症中心访问科学家
中国医师协会呼吸医师分会肺癌工作委员会 委员
中国肺癌防治联盟免疫治疗委员会 常务委员
中国抗癌协会个案管理专业委员会 常务委员
中国初级卫生保健基金会胸部肿瘤精准治疗专委会 常务委员
广东省医学会呼吸病学分会 副主任委员
广东省医学会临床药学分会 副主任委员
广东省医学会肺部肿瘤学分会 常务委员
广东省临床试验协会(GACT / CTONG) 理事
广东省医师协会临床试验专业委员会 副主任委员
广东省女医师协会肺癌专业委员会 副主任委员
广东省医疗行业协会肺部肿瘤管理分会 副主任委员
广东省药学会医院药学专业委员会 副主任委员,等
HER2变异的检测
精准的检测是实现HER2靶向治疗的前提。NSCLC中HER2突变的发生率约为2-4%[5],HER2突变的类型多样,以酪氨酸激酶结构域第20外显子的插入突变最为常见,但也存在非激酶区(non-TKD)的其他外显子(如8、17)突变[6]。由于传统PCR方法可能遗漏非常见突变,目前临床强烈推荐使用二代测序(NGS)技术进行检测,以大panel全面覆盖所有已知的突变亚型[7]。
HER2蛋白过表达(IHC 2+/3+)在NSCLC中发生率可达2-35%[5]。免疫组化(IHC)是检测HER2蛋白过表达的标准方法。2025版CSCO指南和NCCN指南均已建议检测[8, 9]。最新发布的《HER-2变异晚期非小细胞肺癌诊疗专家共识(2025版)》[10] 建议,HER2 过表达肺癌患者可参考胃癌 HER2 过表达患者的判读标准[11]:IHC3+的患者定义为阳性,即≥10%癌细胞呈现强烈、完整膜染色,可为基底外侧或外侧膜染色。临床实践和多项关键临床试验(如DESTINY-Lung01、DESTINY-PanTumor02、DESTINY-CRC024)也普遍采用这一判读标准[12, 13]。
HER2扩增在NSCLC中发生率为10-20%[5],HER2扩增可通过荧光原位杂交(FISH)或NGS进行检测。HER2扩增与HER2蛋白过表达存在一定相关性,但并不完全一致[14]。
HER2变异NSCLC的治疗
HER2突变
HER2变异NSCLC的诊疗已进入分子分型驱动的精准治疗时代。目前,对于HER2突变NSCLC患者,一线治疗仍以铂类联合培美曲塞等化疗±免疫治疗(PD-1/L1抑制剂)为主,后线治疗是HER2靶向药物的主战场。最新版NCCN指南将德曲妥珠单抗和宗艾替尼列为HER2突变NSCLC患者的“首选(Preferred)”后线治疗方案[8],2025 CSCO指南将德曲妥珠单抗作为HER2突变NSCLC患者后线治疗的唯一I级推荐[9](图1)。

抗体偶联药物 (ADC)
ADC通过抗体将高效化疗药物精准递送至HER2阳性细胞,是目前HER2突变NSCLC后线治疗的核心药物。德曲妥珠单抗是一种HER2靶向ADC,由抗HER2抗体、可裂解的连接子和拓扑异构酶I抑制剂(DXd)组成。其作用机制是抗体结合肿瘤细胞表面HER2后,通过内吞进入细胞,释放毒性小分子,从而破坏DNA或微管蛋白并杀伤肿瘤细胞。德曲妥珠单抗具有高达8:1的药物-抗体比(DAR),且其载荷DXd具有高膜通透性,可扩散至周围HER2低表达甚至阴性的肿瘤细胞,实现高效的“旁观者效应”[15, 16]。
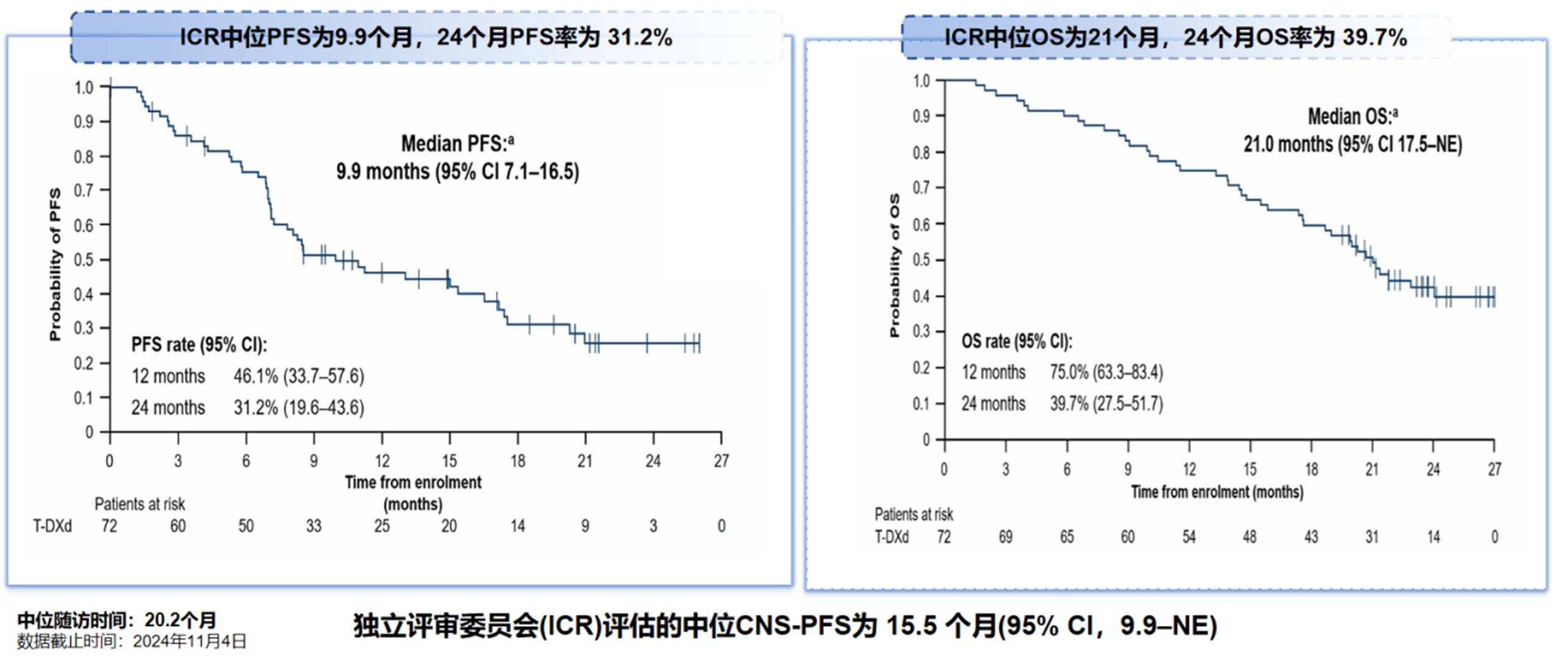
全球DESTINY-Lung02研究奠定了德曲妥珠单抗(5.4 mg/kg)的地位,其客观缓解率(ORR)达到50.0%,中位无进展生存期(mPFS)为10.0个月,中位总生存期(mOS)为19.0个月;在安全性方面,≥3级 治疗相关不良反应(TRAE)发生率为39.6%[17]。针对中国人群的DESTINY-Lung05研究最终分析结果显示,德曲妥珠单抗治疗经治的HER2突变NSCLC患者,ICR评估的ORR高达 56.9% ,mPFS为 9.9个月 ,mOS长达 21.0个月(图2)[18],这一结果显示中国患者获益与全球人群一致。德曲妥珠单抗的疗效较传统化疗时代实现跨越式提升,且是目前唯一取得长期 OS 结果的 HER2 靶向治疗药物。在安全性方面,德曲妥珠单抗的安全性被认为是可管理的,≥3级 TRAE发生率为55.6%,因AE导致患者停药比例仅 5.6%。需要重点关注的特殊不良事件是间质性肺病(ILD)/肺炎(pneumonitis) ,在中国人群中的发生率为12.5%,但绝大多数为1-2级,仅1例为3级[18]。基于德曲妥珠单抗在中国人群中的优异表现,2025 CSCO指南将德曲妥珠单抗在HER2突变NSCLC后线治疗中的推荐级别从II级提升至I级,成为目前CSCO指南中唯一作为I级推荐的治疗方案,开启了HER2突变NSCLC治疗的新格局。此外,因德曲妥珠单抗在HER2突变NSCLC后线治疗中的优异表现,德曲妥珠单抗一线治疗HER2突变NSCLC的Ⅲ期DESTINY-Lung04研究结果也非常值得期待,其结果有望推动德曲妥珠单抗治疗阵地前移,从而更新 HER2 突变晚期 NSCLC 的全程管理策略。
瑞康曲妥珠单抗(SHR-A1811)是一种新型ADC,在HORIZON-Lung研究中显示了极具潜力的疗效,其在HER2突变NSCLC患者中的ORR达73.4%,mPFS为11.5个月,≥3级TRAE发生率为67%[19]。此外,多款在研的新型ADC(如GQ1005、BB-1701、TQB2102等)也在HER2突变NSCLC的治疗中显露出一定的潜力,期待这些ADC的疗效和安全性在后续研究中得到进一步证实。
HER2-TKI
小分子HER2-TKI为HER2突变NSCLC的治疗提供了更多选择。宗艾替尼是一种高选择性HER2-TKI,其作用机制是竞争性抑制ATP与HER2激酶结构域(TKD)位点结合,阻断PI3K/AKT和MAPK通路中的酪氨酸残基磷酸化。在Beamion LUNG-1研究中,宗艾替尼治疗HER2-TKD突变(如Exon 20)经治患者的ORR达71%,mPFS为12.4个月[20,21]。基于此,2025年8月,FDA和NMPA均批准其正式上市,用于治疗HER2激活突变且既往接受过全身治疗的不可切除或转移性NSCLC的成年患者(FDA仅批准HER2-TKD激活突变适应证)。除了宗艾替尼,BAY 2927088也在SOHO-01研究中披露了未经HER2靶向治疗人群的数据,其中TKD激活突变NSCLC患者ORR为70%,非TKD突变患者ORR为14%,针对HER2-TKD激活突变中最常见的Y772_A775dupYVMA (YVMA)突变,其mPFS为12.2个月[22]。
德曲妥珠单抗与新型HER2-TKI相比,两者在作用机制和临床适应证上存在差异,这使得两者有望实现优势互补,进一步拓展HER2突变NSCLC的治疗版图。德曲妥珠单抗独特且多重的作用机制赋予其对所有激活突变的一致疗效,且其载荷DXd具有高膜通透性,可实现高效的“旁观者效应”。此外,德曲妥珠单抗的抗体部分(曲妥珠单抗)靶向的是HER2蛋白的胞外结构域,而TKI则靶向胞内的激酶区[23],这意味着德曲妥珠单抗的疗效不受激酶区是否突变的影响,对于所有激活突变(包括非TKD突变)都可能有效。
HER2过表达
除了在HER2突变NSCLC领域表现优异,德曲妥珠单抗在HER2过表达的适应证也有力地填补了相应的治疗空白。德曲妥珠单抗凭借其高效的递送和旁观者效应,对HER2过表达NSCLC同样有效。DESTINY-Lung01研究(Cohort 1a)显示,德曲妥珠单抗 (5.4 mg/kg) 治疗HER2过表达NSCLC,在IHC 3+的患者中,ORR达到了53%,mPFS为7.5个月[12]。DESTINY-Lung03研究再次证实了德曲妥珠单抗在HER2过表达(IHC 3+)NSCLC患者中的疗效(ORR 56.3%)[24]。基于DESTINY-PanTumor02、DESTINY-Lung01、DESTINY-CRC02等研究的积极数据, 2024年4月5日,FDA加速批准德曲妥珠单抗用于治疗既往经治的、不可切除或转移性HER2蛋白过表达(IHC 3+)的实体瘤(包括NSCLC),NCCN非小细胞肺癌指南也随即将德曲妥珠单抗纳入HER2蛋白过表达(IHC 3+)治疗的“其他推荐”。
总结与展望
HER2变异NSCLC的治疗在德曲妥珠单抗的引领下已进入新的时代。德曲妥珠单抗凭借其独特的作用机制(靶向胞外域、旁观者效应),不仅对HER2突变(包括非TKD突变)NSCLC展现了强劲疗效,成为2L+标准治疗,更开创性地成为首个获批用于HER2过表达(IHC 3+)NSCLC的靶向药物。与此同时,以宗艾替尼为代表的新一代TKI在HER2-TKD突变患者中显示出高缓解率。未来,随着更多研究结果的公布,HER2靶向治疗有望向NSCLC一线治疗推进。此外,进一步优化HER2变异NSCLC诊疗的关键在于检测的标准化(特别是IHC判读标准的统一)、脑转移的管理、耐药机制的探索,以及治疗策略的优化(如ADC与TKI的序贯或联合、ADC与免疫的联合等)。相信随着医学研究的不断深入和技术的持续进步,HER2变异NSCLC的诊疗将迎来更多突破性的进展。
[1] Arteaga CL, et al. Nat Rev Clin Oncol. 2011 Nov 29;9(1):16-32.
[2] Mar N, et al. Lung Cancer 2015;87:220-25.
[3] Pollock NI, et al. Cin Cancer Res 2015;21:526-33.
[4] Iqbal N, et al. Mol Biol Int 2014; 2014:852748.
[5] J.A. Marks, et al. 2025 WCLC P2.06.44.
[6] Nat Rev Clin Oncol. 2023 Apr;20(4):229-249.
[7] Thorac Cancer. 2023 Jan;14(1):91-104.
[8] Non-Small Cell Lung Cancer. National Comprehensive Cancer Network. 2026 Version1.
[9] 2025 CSCO NSCLC 诊疗指南.
[10]HER-2变异晚期非小细胞肺癌诊疗专家共识制定专家组,中国抗癌协会整合肺癌委员会 ,中国抗癌协会非小细胞肺癌专业委员会. HER-2变异晚期非小细胞肺癌诊疗专家共识(2025版). 中华肿瘤杂志 2025 年9 月第 47 卷第 9 期.
[11]Bartley A N, Washington MK, Colasacco C, et al. HER2 testing and clinical decision making in gastroesophageal adenocarcinoma: guideline from the College of American Pathologists, American Society for Clinical Pathology, and the American Society of Clinical Oncology[J]. J Clin Oncol,
2017, 35(4):446-464.
[12] Smit EF,et al. Lancet Oncol. 2024 Apr;25(4):439-454.
[13] Meric-Bernstam F, et al. J Clin Oncol. 2024;42(1)47-58.
[14] Yeramaneni S, et al. 2025 WCLC P1.17.22
[15]Tsao LC, Wang JS, Ma X, et al. Effective Extracellular Payload Release and Immunomodulatory Interactions Govern the Therapeutic Effect of Trastuzumab Deruxtecan (T-DXd). Nature Communications. 2025;16(1):3167.
[16] Ali A, Graff SL. Exploring DESTINY: The Past, Present, and Future of Trastuzumab Deruxtecan. Current Oncology Reports. 2024;26(1):1-9.
[17] Pasi A. Janne et al. J Clin Oncol 42, 8543-8543(2024).
[18] Ying Cheng et al. 2025 WCLC #P2.10.12
[19] Li Z, et al. Lancet Oncol. 2025 Apr;26(4):437-446
[20] Cooper AJ,et al. J Clin Oncol. 2022 Mar 1;40(7):693-697.
[21] Girard, ELCC 2025
[22] Nicolas Girard, 2025 ESMO 2001P.
[23] Jeesun Yoon, et al. Nat Rev Clin Oncol. 2024 Jul 22.
[24] Planchard D, et al. 2024 WCLC. OA16.05.
排版编辑:Crystal
本篇内容源自北京康盟慈善基金会支持的“非小细胞肺癌罕见靶点诊疗进展解读项目”。











 苏公网安备32059002004080号
苏公网安备32059002004080号


