作为经典的局部治疗手段,放疗在局晚期或晚期肺癌患者的治疗中均具有重要的临床价值。放疗可对局部病灶达到良好的控制作用,甚至与系统治疗形成协同。然而,肿瘤细胞的放射抵抗和正常组织的剂量限制,仍是制约放疗疗效的关键瓶颈。放疗增敏剂的应用则为突破这一困境提供了新的方向,带来了达到1+1+1>3的可能,有望为患者带来更好的治疗结局。本文将分享3例接受不同系统治疗与放疗的肺腺癌患者,这些患者的治疗中均应用了放疗增敏剂甘氨双唑钠,体现了放疗增敏剂在不同系统治疗模式中的潜在增敏作用,为不同的患者群体提供了新的治疗思路。


病例一
病例分享专家
湖南省肿瘤医院 胸部放疗二科 住院医师
临床医学博士
中国抗癌协会委员
中国医药教育协会肿瘤放射治疗专业委员会委员
主持长沙市自然科学基金1项
以第一/共一发表SCI 6篇
病例点评专家
中南大学医学博士
湖南省肿瘤医院 胸部放疗二病区
中国医药教育协会肿瘤放射治疗专业委员会委员
湖南省医促会呼吸病专业委员会委员
湖南省医促会肿瘤放疗和放射免疫专委会委员
湖南省抗癌协会食管癌专业委员会
湖南省女医师协会头颈肿瘤专业委员会委员
湖南省健康服务业协会肿瘤多学科诊疗专业委员会委员
湖南省健康服务业协会基层医疗分会理事
广东省医院品牌建设专委会委员
从事肿瘤临床工作及教学工作多年
主持湖南省科技厅课题一项
参与湖南省科技厅、湖南省卫健委多项课题
以第一作者及参与作者发表高质量SCI及中文期刊多篇
病例介绍
基本信息:患者女,67岁。
就诊经过:
现病史:2024-06-14因咯血一天到该院就诊,完善检查示左肺门占位,当地急诊行支气管动脉栓塞术,并予以头孢等消炎对症处理,后完善支气管镜:左主、左上叶新生物,头部MRI、全身骨扫描未见明显异常。后活检报告:恶性肿瘤。
2024-07-03,患者第一次入我院。
2024-07-04 ,行肺高分辨CT,平扫+增强,上腹部三期CT扫描,下腹部CT平扫+增强:1. 左肺门占位,考虑中央型肺癌,并左上肺阻塞性肺炎,并肺门、纵隔淋巴结转移;右心隔角区小淋巴结,建议追观复查。2. 肝S4段稍低密度结节灶,转移瘤?肝S3段小片低密度灶,不典型血管瘤?建议结合MRI检查。3. 双肾囊肿。4. 所示甲状腺右叶弱强化小结节,建议超声进一步检查。
2024-07-04 心脏彩超:1. 心内结构及活动未见明显异常;2. 左室顺应性减退,收缩功能正常范围。
2024-07-10 肝多期动态增强MR成像:1. 肝S4段动脉期强化灶,局灶灌注不良?2. 肝S3段局灶肝内胆管扩张。3. 双肾囊肿。入院完善血常规、电解质、肝肾功能、凝血功能、甲状腺功能、空腹血糖、心肌酶、大便常规均未见明显异常。
诊断结果:原发性支气管肺癌,腺癌,左上叶,cT2N3(前纵隔、对侧肺门淋巴结转移)M0 IIIC期 驱动基因阴性。
MDT会诊意见:建议全身治疗有效基础上,酌情局部放疗,并请心内科会诊建议定期检测凝血功能等。患者有化疗指征。
2024-07-12至07-14、08-06至08-07、08-30至09-01、09-20至09-23,行AP方案化疗4周期,剂量为培美曲塞0.7g+顺铂120mg d2,化疗期间,倍他米松抗过敏,盐酸帕洛诺司琼止呕,西咪替丁防止化学性胃炎,维生素注射液补充电解质水化。患者化疗结束,复查血常规基本正常。
2024-10-12,患者为求进一步治疗再入我科,入院完善相关检查。
2024-10-16 上腹部三期CT扫描 :1. 肺癌治疗后:左上肺门旁软组织密度影较前稍缩小,双肺门及纵隔淋巴结较前相仿。2. 右上肺小结节,炎性结节可能;右中肺钙化灶。3. 前纵隔软组织密度影同前,胸腺瘤或胸腺增生可能,建议复查。4. 肝左外叶部分肝内胆管扩张同前。5. 双肾囊肿同前。
2024-10-16 脑MR平扫+增强+功能成像(DWI):头部MR扫描未见明显异常。
2024-10-23 胸部PET-CT 肺癌化疗后:左肺上叶前段片状高密度影,PET于相应部位未见异常放射性浓聚影,考虑肺癌治疗后改变,局部肿瘤细胞处于代谢抑制状态。纵隔(2R、4L、5、7区)、左肺门淋巴结,PET于相应部位见淡淡放射性浓聚影,结合本院既往CT,考虑淋巴结转移治疗后改变。纵隔(3A、4R区)、右肺门淋巴结,PET于相应部位见淡淡放射性浓聚影,考虑淋巴结增生可能性大。右肺上叶尖段硬结灶;右肺上叶后段胸膜下慢性炎性病变;右侧水平裂钙化灶。前纵隔2枚稍低密度结节影,PET示放射性缺损,考虑纵隔囊肿。胸部其它部位未见明显异常。
2024-10-18 MDT会诊:1. 肺门肿块明显缩小,纵膈淋巴结未见明显缩小,前纵隔占位考虑良性病变可能性大;2. 建议完善PET-CT明确对侧肺门淋巴结性质,酌情肺癌根治性放疗;3. 建议放疗后可酌情行免疫维持治疗。
临床诊断:原发性支气管肺癌 腺癌 左上叶 cT2N3(前纵隔、对侧肺门淋巴结转移)M0 IIIC期 驱动基因阴性
治疗经过:
系统治疗:
2024-07-12至07-14、08-06至08-07、08-30至09-01、09-20至09-23,行AP方案化疗4周期,剂量为培美曲塞0.7g+顺铂120mg d2。
放疗:
2024-11-07至2024-12-18,行放射治疗,放疗部位:左肺门原发灶+纵隔转移淋巴结引流区,放疗剂量:PTV 60Gy/30f,放疗期间联合使用甘氨双唑钠放疗增敏,期间患者未诉特殊不适,定期复查血象均未见明显异常。
疗效评估:
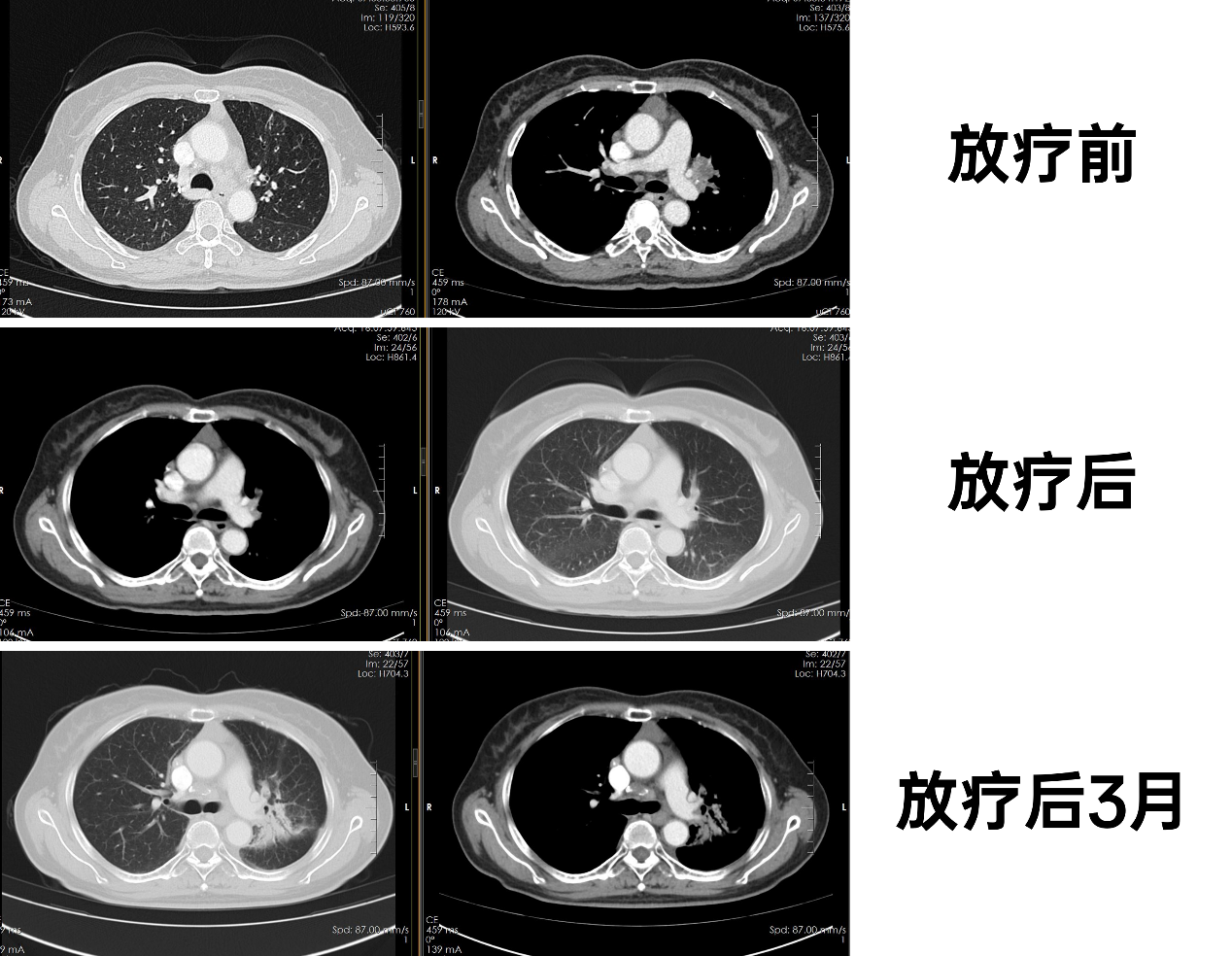
化疗前:2024-07-04,胸腹部CT:1. 左肺门占位,考虑中央型肺癌,并左上肺阻塞性肺炎,并肺门、纵隔淋巴结转移;右心隔角区小淋巴结,建议追观复查。2. 肝S4段稍低密度结节灶,转移瘤?肝S3段小片低密度灶,不典型血管?建议结合MRI检查。3. 双肾囊肿。4. 所示甲状腺右叶弱强化小结节,建议超声进一步检查。
放疗前:2024-10-16,胸腹部CT:1. 肺癌治疗后:左上肺门旁软组织密度影较前稍缩小,双肺门及纵隔淋巴结较前相仿。2. 右上肺小结节,炎性结节可能;右中肺钙化灶。3. 前纵隔软组织密度影同前,胸腺瘤或胸腺增生可能,建议复查。4. 肝左外叶部分肝内胆管扩张同前。5. 双肾囊肿同前。
放疗后1月:2025-02-12,胸腹部CT:1. 肺癌治疗后,现左肺炎性病变(考虑放射性肺炎)掩盖左上肺门旁软组织灶;双肺门及纵隔淋巴结较前相仿。2. 右上肺小结节同前,慢性炎性结节可能性大;右中肺钙化灶同前。3. 前纵隔软组织密度灶同前,胸腺瘤或胸腺增生可能,建议复查。4. 甲状腺右侧叶结节大致同前。5. 肝左外叶部分肝内胆管扩张同前。6. 左肾囊肿同前。
放疗后3月:2025-05-16,胸腹部CT:1. 肺癌治疗后,左肺炎性病变(考虑放射性肺炎)较前稍好转,掩盖左上肺门旁软组织灶;双肺门及纵隔淋巴结较前相仿。2. 右上肺小结节同前,慢性炎性结节可能性大;右中肺钙化灶同前,右中肺少许纤维灶。3.前纵隔软组织密度灶同前,胸腺瘤或胸腺增生可能,建议复查。4. 甲状腺右侧叶结节大致同前。5. 肝左外叶部分肝内胆管扩张同前。6. 双肾囊肿同前。


病例二
病例分享专家
临沂市肿瘤医院 内五科 副主任
临沂市抗癌协会肿瘤靶向治疗专委会秘书
临沂市抗癌协会放疗专业委员会委员
临沂市抗癌协会化疗专业委员会委员
临沂市抗癌公益联盟科普专家库成员
临沂市医师协会肿瘤医师分会委员
山东省抗癌协会放射肿瘤学分会委员
山东省医药教育协会肺癌专委会委员
山东省医学会肿瘤放射治疗专委会委员
山东省临床肿瘤学会转化医学专家委员会委员
山东省疼痛研究会癌痛与姑息治疗专委会委员
山东省康复医学会肿瘤康复分会专家委员会委员
白求恩精神研究会肿瘤医学专家委员会常务委员
病例点评专家
临沂市肿瘤医院放疗二科主任
山东省抗癌协会放射肿瘤学分会委员
山东省免疫学会肿瘤免疫专业委员会委员
山东省老年学与老年医学会肺癌免疫治疗专业委员会常务委员
山东省医学会肿瘤放射治疗学分会食管癌学组委员
山东省医药教育协会肿瘤放疗专业委员会委员
临沂市医师协会肿瘤放疗医师分会委员
临沂市抗癌协会放疗专业委员会委员
临沂市抗癌协会肺癌专业委员会委员
病例介绍
基本信息:患者女,65岁。
就诊经过:
现病史:
2021-01,患者因“刺激性咳嗽1月”于外院就诊,CT示左肺占位。
2022-02-17患者入住我院,诊断为左肺腺癌并双肺转移,无手术指征,EGFR基因检测提示基因突变。患者开始口服奥希替尼,服药后咳嗽减轻。
患者于外院行颅脑MRI检查,提示脑转移,2022-03-31第二次入院。
2022-04-04,排除禁忌后开始行调强放疗,勾画靶区:GTV:可见右侧小脑转移灶,PGTV:GTV外扩4mm。应用IMRT技术,PGTV:DT 40Gy/10F,4Gy/F,5F/W,并予降颅压对症治疗,过程顺利。
2022-04-15 患者好转出院,继续口服奥希替尼靶向治疗,期间复查病情稳定。后患者再度出现头晕、头痛,伴恶心、呕吐,2022-12行颅脑MR复查,考虑脑转移进展。
辅助检查:
2021-02-15 胸部CT:左肺上叶尖后段支气管截断,左肺上叶局部不张,双肺见多发大小不等结节影。
2021-02-19 气管镜:气管隆突居中,右肺未见明显异常,左肺上叶后段开口处呈外压性狭窄,可见少量出血,刷检2次。细胞学:找到恶性瘤细胞,考虑癌,建议进一步确诊。
2022-03-17 胸部CT: 原诊“左肺 ca靶向治疗后”复查,与2021-11-18对比:1. 左肺上叶可见软组织肿块影,最大截面约37m×28m,形态不规则,相应支气管截断,远端可见阻塞性肺不张,较前略缩小。2. 余双肺内可见多发结节影,边缘毛糙,较前变化不著。3. 纵隔可见多发小淋巴结,较前变化不著。4. 双侧胸腔及心包未见积液,同前相仿。5. 甲状腺可见结节及钙化影,较前变化不著,建议超声检查。
2022-03-28颅脑MRI:右侧小脑半球示不规则实性占位,边界欠清,约35mm×31mm×23mm,增强扫描实性部分及囊壁呈不均匀较明显强化,邻近脑实质受压,第四脑室受压变形,双侧颞叶少许斑点状T2-Flair高信号。脑室系统形态、大小如常,中线结构居中。
2022-12-01 颅脑MR:原诊“肺癌脑转移放疗后”复查,与2022-08-18日片相比:1. 右侧小脑半球仍示结节灶,呈长T1长T2信号,增强呈边缘强化,最大横截面约17mm×16mm,整体范围变化不著,实性成分较前增多;周围水肿带较前增大。2. 右侧额叶见线样强化影,同前。3. 双侧半卵圆中心区散在缺血灶,同前。4. 双侧脑室略扩张。部分脑沟、脑裂增宽加深。中线居中。5. 颅骨局部信号欠均,随诊。
临床诊断:
左肺癌脑转移,IV期,EGFR突变
治疗经过:
靶向治疗:
2022-02起,口服奥希替尼靶向治疗。
放疗:
2022-04-04,排除禁忌后开始行调强放疗,勾画靶区:GTV:可见右侧小脑转移灶,PGTV:GTV外扩4mm。应用IMRT技术,PGTV:DT 40Gy/10F,4Gy/F,5F/W,并予降颅压对症治疗,过程顺利。
2023-01至2023-02,予以局部放疗,GTV:右肺上叶原发灶;CTV:GTV外扩5mm;PTV:CTV外扩约4mm。放疗剂量:PTVDT50Gy/2Gy/25F,5次/w,期间予以内科降颅压治疗,联合贝伐珠单抗抗血管生成靶向治疗,联合使用甘氨双唑钠放疗增敏。
疗效评估:
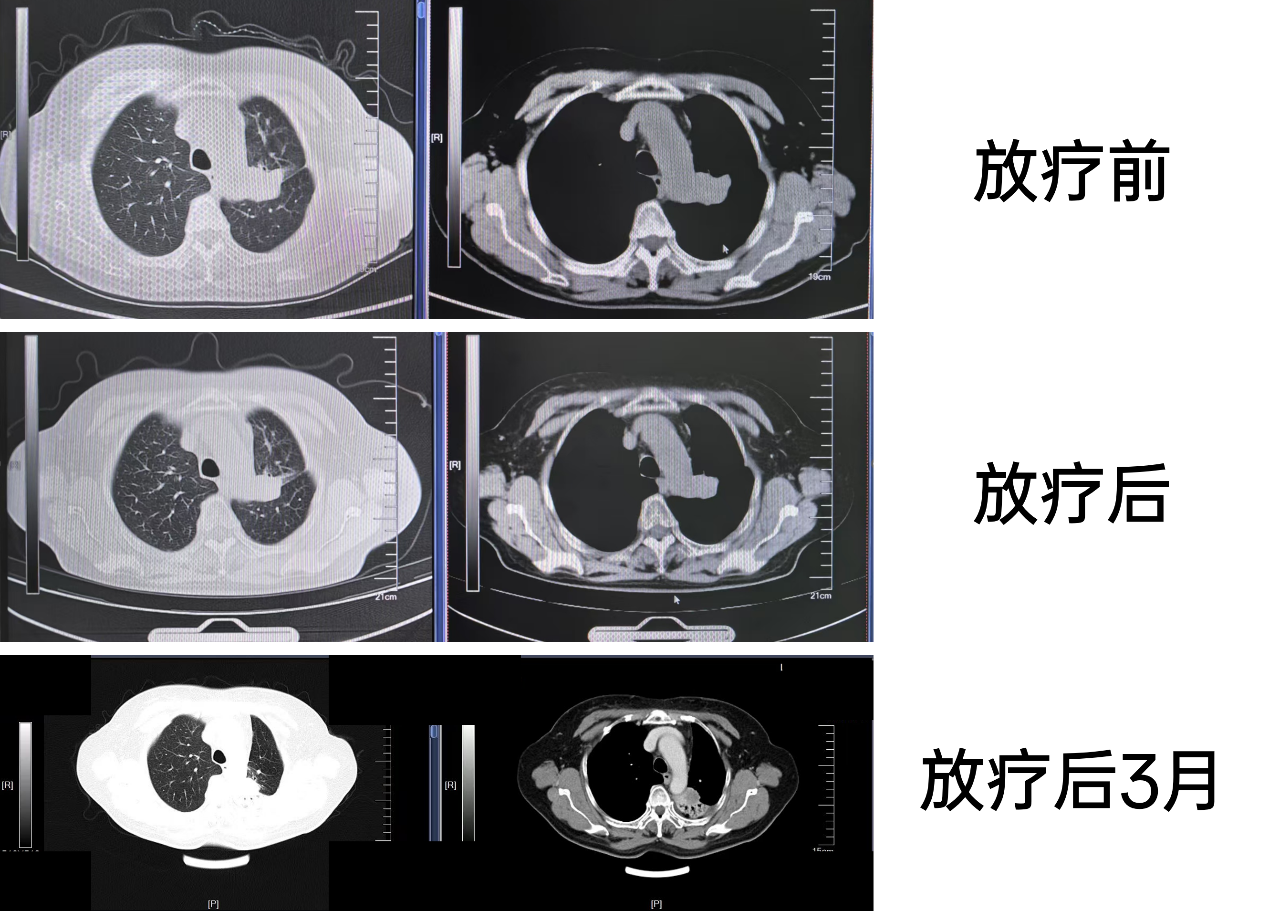
放疗前:2022-11-29, 原诊“肺癌脑转移放疗后半年”复查,与2022-08-16对比:左肺上叶可见软组织肿块影,最大截面约39mm×25mm,形态不规则,相应支气管截断,远端可见阻塞性肺不张,较前略增大。2. 余双肺内可见多发结节影,边缘毛糙,较前变化不著。3. 纵隔可见多发小淋巴结,较前变化不著。4. 双侧胸腔及心包未见积液。5. 甲状腺可见结节及钙化影,较前大致相仿,结合超声。6. 右侧第3肋骨局部密度不均匀,较前变化不著。7. 肝右缘斑点状致密影,较前相仿。8. 胆囊、胰腺、脾脏、双肾及肾上腺未见明显异常密度灶。9. 腹腔、腹膜后未见明显肿大淋巴结影。未见腹腔积液。
放疗后:2023-02-28,原诊“肺癌脑转移治疗后”复查,与2023-01-29比较:左肺上叶可见软组织肿块影,最大截面约29mm×20mm,形态不规则,相应支气管截断,远端可见阻塞性肺不张,较前稍缩小。2. 余双肺内可见多发结节影,边缘毛糙,较前变化不著。3. 纵隔可见多发小淋巴结,较前变化不著。4. 双侧胸腔及心包未见积液。5. 甲状腺可见结节及钙化影,较前大致相仿,结合超声。6. 右侧第3肋骨局部密度不均匀,较前变化不著。7. 肝右缘斑点状钙化灶,较前相仿。
放疗后3个月:2023-05-29,复查上腹部+胸部CT:原诊“左肺癌脑转移治疗后复查,与2023-04-04比较:1. 左肺上叶可见软组织肿块影,最大截面约32mm×23mm,形态不规则,轻度强化,相应支气管截断,周围可见肺不张,整体范围较前增大。2. 左肺片絮影,范围缩小,大部分已不明确。余双肺内可见多发结节影,边缘毛糙,较前变化不著。3. 纵隔可见多发小淋巴结,较前变化不著。4. 双侧胸腔及心包未见积液。5. 甲状腺可见结节及钙化影,较前大致相仿,结合超声。6. 双侧多条肋骨局部密度增高,考虑为陈旧性骨折,结合临床。7. 肝右缘斑点状致密影,较前相仿。8、胆囊、胰腺、脾脏、双肾及肾上腺未见明显异常密度灶,较前相仿。9. 腹腔、腹膜后未见明显肿大淋巴结影。10. 未见腹腔积液。


病例三
病例分享专家
江阴市人民医院 医学硕士
江苏省医学会放射肿瘤治疗学专业委员会青年委员
主持市级课题1项
病例点评专家
博士,硕士生导师
江阴市人民医院 放疗科主任
无锡市医学会放射肿瘤治疗学分会 候任主任委员
江苏省免疫学会放射与免疫专业委员会 副主任委员
中国临床肿瘤学会(CSCO)转化医学委员会委员
江苏省医学会第九届放射肿瘤治疗学专业委员会 委员
江苏省放射治疗专业质量控制中心 成员
江苏省免疫学会肿瘤免疫专委会 常委
江苏省抗癌协会放射肿瘤治疗学专业委员会 委员
江苏省医师学会/研究型医院学会放射肿瘤学分会 委员
江苏省研究型医院学会生物治疗学专业委员会委员
江苏省肿瘤防治联盟放射治疗专家委员会 委员
华人肿瘤放疗协作组江苏放疗营养分会 副主任委员
《中华放射医学与防护杂志》通讯编委
江苏省卫生拔尖人才
江苏省第五期“333”人才工程培养对象
无锡市医学创新团队学科带头人
无锡市首届“太湖人才计划”医疗卫生拔尖人才
江阴市“暨阳英才计划”重点高层次人才
江阴市“十大科技之星”
病例介绍
基本信息:患者男,70岁。既往高血压病史,口服药物控制。
就诊经过:
现病史:
2022-11,患者体检查胸部CT示:左肺下叶占位,建议增强;肺气肿;右肺下叶结节,建议随诊;两肺下叶少许炎症;局部冠脉钙化。右侧第4、5后肋陈旧性骨折。附见肝小囊肿。
后患者进一步就诊于我院呼吸科,完善相关检查后穿刺病理活检示(2022-11-15):浸润性生长的腺上皮细胞,异型性明显。
免疫组化:CK7(少量+),TTF-1(+),CK5/6(-),P40(-)。诊断为:肺腺癌明确。
患者自行至外院行PET-CT:左下肺肿块伴FDG代谢异常增高,考虑恶性病变;左下肺支气管旁FDG代谢增高灶,倾向淋巴结转移。左侧胸壁皮下结节伴FDG摄取增高。后患者转入我院胸外科评估后考虑患者血气偏低,无法耐受手术,与患者及家属沟通后建议至内科进一步综合治疗;现患者今为行进一步治疗来院。
影像学检查:
2022-11,患者体检查胸部CT示:左肺下叶占位,建议增强;肺气肿;右肺下叶结节,建议随诊;两肺下叶少许炎症;局部冠脉钙化。右侧第4、5后肋陈旧性骨折。附见肝小囊肿。
外院PET-CT:左下肺肿块伴FDG代谢异常增高,考虑恶性病变;左下肺支气管旁FDG代谢增高灶,倾向淋巴结转移。左侧胸壁皮下结节伴FDG摄取增高。
病理活检:
2022-11-15,病理活检:浸润性肺腺癌。
免疫组化:CK7(少量+),TTF-1(+),CK5/6(-),P40(-)。
临床诊断:左肺腺癌 cT2N2M0 III期
治疗经过:
同步放化疗:
2022-12-06予CT下定位。
2022-12-07予根治性放疗,靶区勾画范围:GTV:左肺肿块+肺门淋巴结;PTV:CTV外扩0.5cm;
靶区及OAR剂量:95%PTV:60Gy/30f;放疗期间联合使用甘氨双唑钠放疗增敏。
OAR受量:脊髓:Dmax:35.7Gy;左肺:V20:26.05%;V30:18.55%;双肺:V20:13.1%;V30:9.32%;Dmean:8.82Gy;心脏:V30:11.35%;Dmean:17.4Gy。
排除禁忌,2022-12-09、12-31予重组人血管内皮抑制素注射液210mg微泵维持d1-7;
2022-12-13、2023-01-03予化疗,具体为:培美曲塞二钠注射剂0.75g静滴+卡铂注射液450mg静滴,辅以抑酸护胃、止吐、中药抗肿瘤等对症治疗,过程顺利。
2022-12-30完善CT下定位,评估肿块退缩情况并酌情予以缩野放疗,后患者顺利完成放疗。
后复查示肺炎,考虑放射性肺炎,予以地塞米松静滴并逐减量抗炎治疗,同时予以对症治疗。
免疫治疗:
2023年2月17日,予以度伐利尤单抗500mg免疫治疗,过程顺利。
疗效评估:
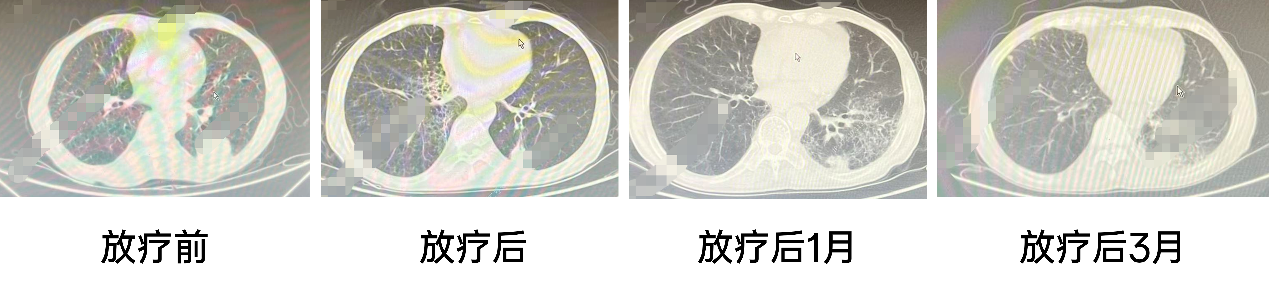
放疗前:2022-11-13 胸部增强CT:左肺下叶占位,考虑肿瘤性病变;肺气肿;右肺下叶结节;两肺下叶少许慢性炎症;局部冠脉钙化;右侧第4、5后肋陈旧性骨折。
放疗后:2023-01-27 胸部CT:左肺下叶CA较前变小;右肺下叶小结节较前相仿;肺气肿;右肺中叶、两肺下叶散在炎症,较前片新增;冠脉粥样硬化。
放疗后1月:2023-03-10 胸部CT:左肺下叶Ca较前大致相仿;双肺散在小结节、较前片大致相仿;肺气肿;两肺散在间质性改变(左肺尤著);冠脉钙化;右侧第4、5后肋陈旧性骨折。
放疗后3月:2023-05-02 胸部CT:左肺下叶Ca较前病灶略缩小,左肺下叶肺门淋巴结增大,伴支气管管腔变窄;右肺下叶小结节、较前片大致相仿;肺气肿;右肺中叶、双肺下叶间质性改变;冠脉钙化。右锁骨、右侧第4、5后肋陈旧性骨折改变。
放疗后8月:2023-09-25 胸部CT:左肺下叶Ca治疗后,较前相仿,周围炎症稍有吸收,右肺下叶小结节,较前稍减小;肺气肿;右肺中叶、双肺下叶少许间质性炎症;冠脉钙化。右锁骨、右侧第4、5后肋陈旧性骨折改变。

总结:甘氨双唑钠助力局晚期/晚期肺腺癌患者,在放化疗±靶向治疗或免疫治疗中,联合获益高、经济又安全
本次病例分享带来3例局晚期不可切除/晚期肺腺癌病例,3类患者接受了不同的系统治疗模式,但均在放疗中联合应用甘氨双唑钠且使得疾病得到不同程度的控制,提示了甘氨双唑钠在不同的系统治疗联合方案中,给患者带来了更多获益。
放疗的主要应用价值在于局部控制,无论是脑转移灶还是肺部原发病灶,均可通过放疗控制局部肿瘤进展。3例患者分别接受了原发病灶及脑转移灶的照射。值得关注的是,尽管当下放疗手段已经趋于精准,但照射剂量与并发症的平衡仍是难题。放疗增敏剂的应用,则有望在保障安全的前提下,达到更好的效果。甘氨双唑钠作为目前唯一获批的放疗增敏剂,适用于对头颈部肿瘤、食管癌、肺癌等实体肿瘤进行放射治疗的患者,其在多部指南中推荐为一种高效低毒的放疗增敏剂,并已进入新版国家医保。未来,在局晚期/晚期肺腺癌患者的不同系统治疗联合方案中,均可尝试联用甘氨双唑钠,联合获益高、经济又安全。
1. 陈光辉,闫慧,孙长义,等. 非小细胞肺癌患者癌组织和血浆中microRNA-21的表达及意义[J].临床检验杂志,2014,32:652-655.
2. 重庆医科大学学报,2009,34( 8) :1108-1111
3. 甘氨双唑钠研究论文集[C],2001:4-26.
4. 肿瘤防治研究,2009,36( 7) :606-608.
5. Min X, et al. J Cancer. 2019 Jan 1;10(2):305-312
6. 魏民,等. 国际肿瘤学杂志,2018,45(12):727-730.
7. Li L, et al. Bioengineered. 2021 Dec;12(1)1066-1077
8. CSCO非小细胞肺癌诊疗指南(2025版)
9. Jabbour SK, et al. Pembrolizumab Plus Concurrent Chemoradiation Therapy in Patients With Unresectable, Locally Advanced, Stage III Non-Small Cell Lung Cancer: The Phase 2 KEYNOTE-799 Nonrandomized Trial. JAMA Oncol. 2021 Jun 4;7(9):1–9.
10. Ross HJ, et al. Atezolizumab Before and After Chemoradiation for Unresectable Stage III Non-Small Cell Lung Cancer: A Phase II Nonrandomized Controlled Trial. JAMA Oncol. 2024 Sep 1;10(9):1212-1219.
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


