急性淋巴细胞白血病(ALL)是一种发病年龄呈双峰分布的异质性疾病,好发于1-4岁的儿童和60岁以上的成人。成人ALL病例中约有20%的患者为BCR-ABL阳性。在儿童BCR-ABL阳性ALL患者中已有骨质破坏相关病例报道,但该症状在成人ALL中较为罕见。近日,成都市第五人民医院史丽君教授及其团队在Frontiers杂志报道一例以骨质破坏为首发临床表现的BCR-ABL阳性ALL患者1。该患者经酪氨酸激酶抑制剂(TKI)联合化疗后获得完全缓解(CR),BCR-ABL转阴;但影像学提示骨质破坏广泛进展,骨髓活检提示白细胞浸润。【肿瘤资讯】特此整理,以飨读者。

病例介绍:骨痛“危机”,一例成人BCR-ABL阳性ALL的非典型开局
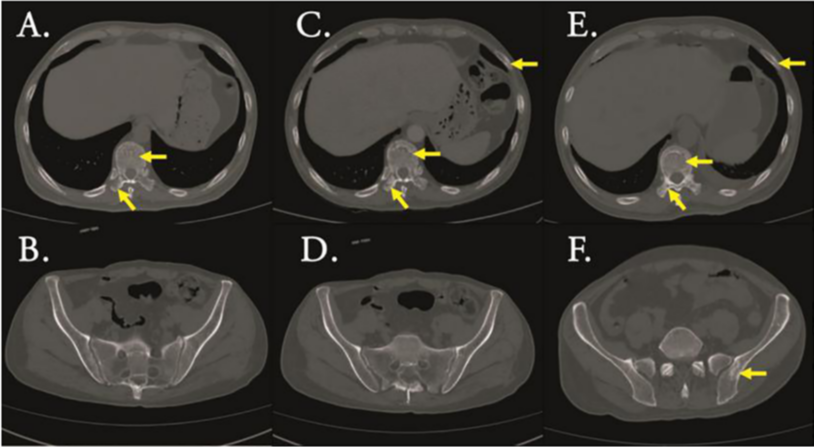
患者男性,47岁,因“腰背部疼痛3月余,加重伴皮下出血1日”入院。2022年6月23日患者无诱因出现腰背部疼痛,伴间歇性肋部疼痛,未予规范治疗。2022年7月患者疼痛加重,日常活动受限。当地医院胸部CT示胸椎及右侧横突局灶性骨质破坏(图1)。患者的血常规结果示白细胞(WBC)计数9.8×10⁹/L,血红蛋白(Hb)水平142g/L,血小板(Plt)计数106×10⁹/L。予对症止痛治疗后,患者的疼痛症状短暂缓解,旋即加重,并于入院前1日出现皮下出血。
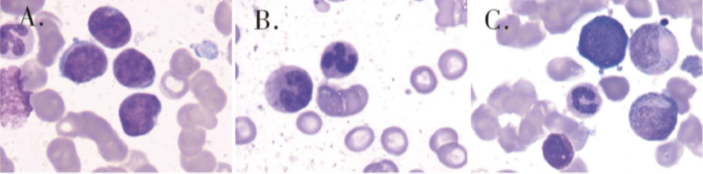
患者再次入院,查血结果示WBC 14.5×10⁹/L,原始未成熟细胞占41%,Hb 139g/L,Plt 7.0×10⁹/L;肾功能正常;血钙3.0mmol/L(正常范围2.17~2.54)。骨髓涂片示原始未成熟淋巴细胞占83%(图2),流式细胞术示原始细胞占37.6%,表达CD10、CD19、CD34、HLA-DR,余CD2、CD3、CD5、CD7、CD8、CD11b、CD13、CD14、CD15、CD16、CD20、CD33、CD56、CD64、CD117均为阴性,符合B-ALL的免疫表型。
另外,患者的染色体核型检查结果为76(3n), XX, -Y, +2, +4, +6, -7, +8, t(9;22) (q34.1;q11.2) , +13, -15, +16, +17, +20, +21, +22/46, XY。融合基因检测示BCR-ABL1(P190)阳性;WT1突变,CDKN2A(chr9p21.3)拷贝数量缺失(NM_058195:外显子1~3 / NM_000077:外显子1~3,长度约26kb),CDKN2B(chr9p21.3)拷贝数量缺失(NM_004936:外显子2,长度约359bp)。基于以上结果,当地医院诊断为BCR-ABL(P190)阳性B-ALL(高危组,伴WT1及CDKN2A突变、三倍体核型)合并高钙血症。患者在当地医院接受鲑鱼降钙素治疗。
治疗经过:病情反复,骨质破坏进展、T315I突变与感染致死的警示
2022年9月20日,患者在当地医院启动VDCLP方案(长春地辛2.8mg/m²[D1,8,15,22],柔红霉素40mg/m²[D1~3],环磷酰胺750mg/m²[D1,15],培门冬酶3750U[D1,15],地塞米松10mg[D1~14,第15天起减量])。该患者于当地医院化疗期间并发重症肺部感染,予以抗感染治疗。
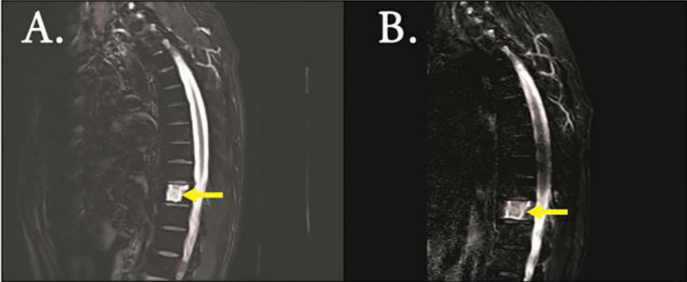
2022年10月18日,患者转入成都市第五人民医院,入院查血象示WBC 8.5×10⁹/L,Hb 73 g/L,Plt 389×10⁹/L;血钙1.9mmol/L。胸部CT提示,患者双肺散在感染灶,胸椎及右侧横突骨质破坏,多根肋骨密度不均(图1)。胸椎MRI示骨质疏松,T10椎体及其附件、T9附件异常信号,结合病史考虑白血病细胞浸润并累及L3上缘、L4上下缘及L5上缘终板(图3)。
2022年10月20日,患者复查骨髓达到CR,原始未成熟淋巴细胞约1.5%(图2)。予头孢哌酮舒巴坦、伏立康唑、两性霉素、卡泊芬净抗感染治疗后,患者仍反复发热咳嗽;支气管肺泡灌洗NGS检出卡氏肺孢子菌。
2022年11月3日,患者接受达沙替尼100mg qd联合VP方案(长春地辛4mg、地塞米松10mg,D1~4,8~11,15~16,21~24)治疗。化疗后复查,患者再次达到CR,BCR-ABL1(P190)转为阴性。
2022年12月9日,患者腰穿常规、生化、流式细胞、免疫分型结果均未见异常,同时予甲氨蝶呤50mg+阿糖胞苷30mg+地塞米松5mg三联鞘内注射,以预防中枢神经系统白血病。但患者仍存在胸骨、肋骨及腰背部持续疼痛,需曲马多镇痛尚能缓解。全身骨显像示,患者出现全身多发代谢活跃灶,考虑为血液系统恶性肿瘤造成的广泛骨浸润(图4)。
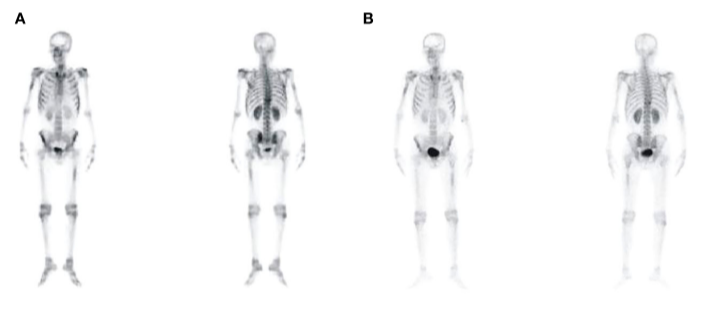
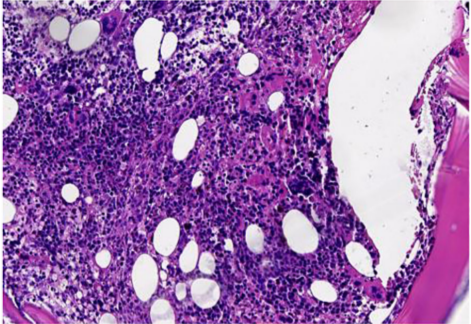
患者T10椎体活检示异型淋巴细胞伴明显纤维化;免疫组化示CD20、CD3、CD79a、TDT、CD99、CD7、MPO、PAX-5、Ki-67均为阳性(约3%~5%),符合B-ALL细胞表型,证实白血病细胞浸润(图5);血清蛋白电泳示M蛋白2.4%(1.39g/L),游离轻链κ 25.28 mg/L、游离轻链λ 36.34 mg/L,血清免疫固定电泳为IgG-k型。尿游离轻链未见异常,尿蛋白电泳未检测到M蛋白。
2023年1月13日,患者接受达沙替尼100mg qd联合VMCP方案(长春地辛2.8mg/m²[D1,8,15,22],米托蒽醌脂质体30mg[D1]、20mg[D8],环磷酰胺750mg/m²[D1,8],泼尼松30mg bid[D1~14,第15天起减量])治疗。
2023年2月3日,患者出院后继续达沙替尼100mg qd口服维持,后续未按时回院接受下一个疗程化疗。
2023年3月6日,患者因腹痛再次入院,肝功能示γ-谷氨酰转肽酶(GGT)5024 U/L(正常范围8~50),碱性磷酸酶(ALP)1298 U/L(正常范围40~150)。CT提示,患者胆囊多发结石伴感染,肋骨、横突和髂骨感染及骨质破坏(图1);予抗感染治疗。患者复查骨髓提示疾病复发,其原始未成熟淋巴细胞占50.5%(图2),BCR-ABL(P190)阳性,基因拷贝数561000。ABL激酶结构域突变分析显示T315I突变,外周血循环肿瘤细胞数为8个,间质型系数为72.97%。
2023年4月6日,患者接受奥雷巴替尼40mg qd联合VP方案(长春地辛2.8mg/m²[D1,8,15,22],泼尼松30mg bid[D1~4,8~11,15~18,22~25])治疗。
2023年5月6日,患者复查骨髓达到CR,原始未成熟淋巴细胞占0%,BCR-ABL(P190)转阴,骨质破坏改善(图3)。但患者GGT、ALP显著升高,并伴腹痛。经地塞米松治疗后GGT、ALP水平下降,腹痛症状缓解,继续1个疗程的奥雷巴替尼联合VP方案治疗。然而,患者后续拒绝异基因造血干细胞移植,自行院外口服奥雷巴替尼,且未定期回院化疗。
2023年8月,患者因继发重症肺部感染不幸离世。
寻根溯源:BCR-ABL阳性ALL出现骨质破坏的治疗挑战——从二代TKI无效到三代TKI的希望与局限
该病例报告中的患者最初出现背部疼痛,逐渐进展为多发性骨质破坏,最终在外周血中出现原始未成熟淋巴细胞后确诊。多发性骨质破坏在各成人恶性肿瘤中的发生率分别为,肺癌27%~35%,乳腺癌25%~30%,多发性骨髓瘤7%~30%,恶性淋巴瘤<10%,而白血病<1%。尽管已有少数类似病例报道,但这些病例均为BCR-ABL阴性ALL2,3。因此BCR-ABL阳性ALL病例较为罕见。
白血病骨质破坏的影像学表现包括骨质减少、干骺端透亮区、虫蚀样改变、骨膜反应、溶骨性骨质破坏、穿孔以及椎体塌陷或硬化。文献报道称,41%~70%的ALL患儿在诊断时即存在骨骼病变4。然而,白血病中多发性骨质破坏和高钙血症的潜在机制仍不明确。这可能与白血病细胞浸润和骨组织直接破坏、以及细胞因子或骨代谢相关激素水平的变化有关,包括甲状旁腺激素、维生素D类固醇、前列腺素E2(PGE2)、肿瘤坏死因子-α(TNF)、白介素(IL)-1、IL-2、IL-6等。B-ALL患者的骨质破坏可能还与核因子κB受体激活剂配体(RANKL)和甲状旁腺激素相关蛋白(PTHrP)有关。
RANKL作为TNF超家族的成员,与巨噬细胞集落刺激因子(M-CSF)和免疫受体酪氨酸激活基序(ITAM)介导的共刺激信号协同作用,激活广泛的信号级联和下游转录调节因子,从而驱动破骨细胞形成。PTHrP通过调节肾小管上皮细胞的钙磷代谢、促进肾源性维生素D的产生以及刺激破骨细胞活性来促进骨吸收。然而,在白血病患者中并未检测到较高的血清PTHr水平,这表明白血病骨质破坏的机制复杂,有待进一步研究证实。遗憾的是,该研究未能监测该患者的25(OH)-维生素D、降钙素和PTHrP水平。此外,骨质破坏是否对ALL预后产生不利影响仍存在争议。
BCR-ABL阳性ALL目前尚无标准化治疗方案。TKI的出现显著提高了BCR-ABL阳性ALL患者的生存率。然而,TKI对于BCR-ABL阳性ALL伴有额外染色体异常的患者疗效不佳已得到研究证实5。该病例患者在接受一个疗程的标准成人ALL诱导方案(VDCLP)后达到CR,并在一个疗程达沙替尼+VP方案后BCR-ABL转阴。然而,骨质破坏却持续进展。骨髓活检证实骨质破坏由白血病细胞浸润引起。
患者重新接受达沙替尼联合脂质体化疗方案治疗,但白血病复发并出现T315I突变。改用第三代TKI奥雷巴替尼后1个月内,患者达到CR,BCR-ABL再次转阴,且骨成像提示多发性骨质破坏改善。这表明在伴有多发性骨质破坏的BCR-ABL阳性ALL患者中,单纯二代TKI联合化疗无法有效解决骨质破坏病灶;三代TKI联合化疗可能对髓外骨质破坏具有一定疗效,且在治疗耐药性Ph阳性ALL中显示出临床疗效,尤其是在携带T315I突变的患者中5。然而,TKI治疗4个月后,该患者再次复发,BCR-ABL转阳并伴有T315I突变。该患者复发是否与额外染色体异常或WT1和CDKN2A突变相关尚不明确。
此外,达沙替尼治疗期间骨髓达到CR且BCR-ABL转阴时,骨质破坏反倒加重。这一现象暂无法解释,有必要行进一步研究以阐明广泛骨质破坏的BCR-ABL阳性ALL患者是否具有独特的生物学特性。临床研究尚不明确针对此类患者的化疗强度,也不清楚二代TKI是否无法控制白血病细胞的增殖。因此,对于以多发性骨质破坏为首发表现的BCR-ABL阳性ALL患者,初始诱导治疗是否直接应用三代TKI尚需进一步评估。同时,TKI联合化疗方案的长期疗效和安全性仍需大规模临床试验验证。
总结
该病例报道了一例以多发性骨质破坏为首发表现的BCR-ABL阳性ALL罕见病例。该患者在接受达沙替尼+VP方案后达到CR,BCR-ABL转阴,但骨质破坏却持续进展。骨髓活检证实骨质破坏由白血病细胞浸润引起。患者在首次复发时出现T315I突变。改用奥雷巴替尼后患者再达CR,BCR-ABL再次转阴,且骨质破坏改善。
此外,在这一罕见病例诊疗过程中出现的问题,包括白血病骨质破坏机制、骨质破坏对ALL患者预后的影响、多发性骨质破坏的BCR-ABL阳性ALL患者的治疗方案选择及其疗效等,均有待进一步研究。
关于“CR-ABL阳性ALL患者在接受一个疗程达沙替尼+VP方案后BCR-ABL转阴,但骨质破坏却持续进展骨质破坏仍进展”的最可能机制,下列哪项叙述最正确?
A. 达沙替尼血药浓度不足,骨髓内药物浓度低于骨质破坏灶,导致局灶耐药。
B. WT1突变驱动白血病细胞向成骨细胞转分化,造成“假性骨质破坏”。
C. 骨质破坏灶内破骨细胞过度活化,而白血病细胞已完全消失,属副肿瘤综合征所致骨病。
D. 白血病细胞通过CXCR4/CXCL12轴迁移并黏附于骨髓基质,形成“庇护所”,使骨病灶持续存在。
上一期《【寻根溯源】光学基因图谱技术揭示常规检测“盲区”下的急性髓系白血病》的答案为B。
1.Lijun S, Zhongrui M, Li W, et al. Case report: BCR-ABL-positive acute lymphoblastic leukemia with bone destruction: a treatment dilemma. Front Oncol. 2024 Feb 21;14:1356311.
2.Virijević M, Vidović A, Colović N, et al. Hypercalcemia with multiple osteolytic lesions and increased circulating tumor necrosis factor in an adult patient with B-cell acute lymphoblastic leukemia. Srp Arh Celok Lek (2016) 144:207–10.
3.Li F, Wang J, Liu A, et al. Prolonged lumbosacral pain as the initial presentation in acute lymphoblastic leukemia in an adult: A case report. Medicine (2019) 98:e15912.
4.Chung SW, Kim S, Choi JR, et al. Osteolytic mandible presenting as an initial manifestation of an adult acute lymphoblastic leukemia. Int J Oral Maxillofac Surg (2011) 40:1438–40.
5.Giudice V, di Rorà GLA, Serio B, et al. Axitinib in ponatinib-resistant B-cell acute lymphoblastic leukemia harboring a T315L mutation. Int J Mol Sci (2020) 21:9724.
排版编辑:Grady











 苏公网安备32059002004080号
苏公网安备32059002004080号


