胃肝样腺癌(HAS)是临床与病理上均少见的一种胃癌亚型,具有高度恶性、侵袭力强和预后不良的特征。对于HER2低表达的晚期胃癌,治疗选择更是有限。本期,重庆大学附属肿瘤医院陈志雄教授和闫孟华教授分享1例HER2低表达(1+)的Ⅳ期胃肝样腺癌伴多发转移的病例。该患者采用以维迪西妥单抗和免疫检查点抑制剂为核心,并先后联合化疗及抗血管生成药物的创新方案进行新辅助治疗,肿瘤显著缩小,疗效评价为部分缓解(PR),最终成功接受根治性手术,术后病理证实达到病理学完全缓解(pCR)。【肿瘤资讯】将病例诊疗过程整理如下,并特邀重庆大学附属肿瘤医院孙浩教授对病例进行点评
病例介绍
专家介绍
外科学博士,副主任医师
重庆市结直肠癌MDT成员
重庆市微创外科胃肠学组委员
重庆市医师协会外科医师分会青年委员
重庆市医学会微创外科腹腔镜/内镜学组委员
同时掌握消化内镜/胃肠外科四级手术
一作SCI 数篇,主持课题2项
专家介绍
重庆大学附属肿瘤医院 胃肠肿瘤中心
毕业于四川大学华西临床医学院
世界内镜医师协会外科联盟理事
重庆市医学会肿瘤MDT专委会胃肠肿瘤学组成员
发表sci 10篇(JCR1区1篇,2区3篇)
参与国家自然科学基金课题2项
主持或主要参与省部级及区级课题4项、专利1项
擅长间质瘤、胃癌及结直肠癌诊断及治疗
熟练掌握常见胃癌、结直肠癌手术方式
基本情况
患者,女,59岁。
主诉:腹痛20天,诊断胃癌1天。
现病史:患者20天前无明显诱因出现腹痛,伴黑便。
既往史:10年前有子宫及乳腺良性肿瘤切除史。
家族史: 无特殊。
辅助检查
肿瘤指标:CEA:1.73 ng/ml;AFP:600.60 ng/ml;CA199:28.69 U/ml。
CT:胃窦壁不规则增厚,较厚处约2.2cm;肝左叶见数个结节、肿块影,大者位于肝左内叶,约3.5*3.5cm(图1)。
MRI:胃窦壁不规则增厚,较厚处约2.4cm;肝门部、腹膜后多个淋巴结显示,大者短径约1.5cm;肝内多发转移,大者约3.9*4.0cm(图2)。
胃镜(2023年12月13日):胃窦大弯侧见3.0cm大小溃疡样肿物,中央凹陷溃烂。穿刺活检病理:(胃窦)低分化腺癌。免疫组化:HER2(1+),CK-pan(+),CK7散在(+),CK20(-),CDX2(+),Ki-67(+)65%,SATB2(+),Villin(+),MLH1(+),MSH2(+),MSH6(+),PMS2(+),PD-L1(CPS<1)。
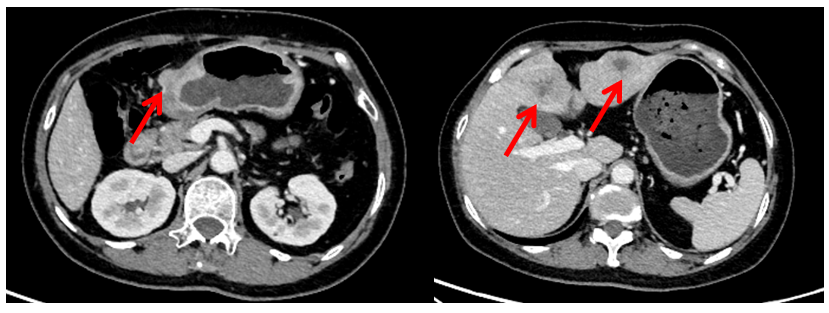
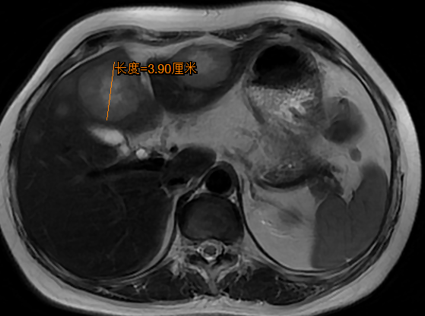
图2. 腹部MRI检查
初步诊断
胃窦恶性肿瘤[cT4N+M1,H1,pMMR,HER2(1+),Ⅳ期]
肝继发恶性肿瘤
淋巴结继发恶性肿瘤(胃周及腹膜后)
诊疗经过
新辅助治疗
患者于2023年12月26日予以替吉奥单药口服治疗1周期。
病理会诊提示(胃窦)低分化腺癌,免疫表型符合肝样腺癌。免疫组化结果:HER2(1+),CK(+),CK8/18(+),CEA(+),AFP(+),Hepatocyte(+),Glypican-3(+),SALL4(+),Syn(+)。
患者于2024年2月6日、2024年2月29日予以维迪西妥单抗+信迪利单抗+奥沙利铂+替吉奥方案治疗。
2024年3月23日复查CT提示胃窦壁稍增厚,较厚处约1.2cm。肝左叶见数个结节影,大者位于肝左内叶,大小约1.6*1.3cm(图3)。
疗效评价:PR。

图3. 腹部CT检查(2024年3月23日)
患者诉不能耐受化疗,于2024年3月24日、2024年4月18日、2024年5月10日予以维迪西妥单抗+信迪利单抗+呋喹替尼治疗。
治疗期间出现免疫相关性不良反应:糖尿病酮症、甲减、心肌酶谱异常。
2024年6月9日复查CT提示胃窦壁稍增厚,较厚处约0.8cm;肝左叶见数个结节影,大者位于肝左外叶下段,大小约1.0*0.6cm(图4)。
疗效评价:PR。
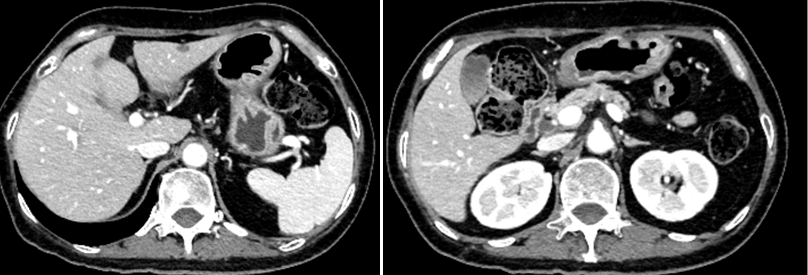
手术治疗
患者于2024年6月11日行腹腔镜胃大部切除伴胃空肠吻合术+空肠吻合术+大网膜切除术+胃周围淋巴结清扫术+左半肝切除术+部分消融治疗。术中见:腹腔无积液及肿瘤结节;肿瘤位于胃窦,面积约1.5*2cm,呈白色疤痕样改变。
术后病理提示(远端胃及肿瘤):“胃癌治疗后”,未见明确肿瘤残留。肿瘤退缩分级TRG:0级。胃周脂肪内淋巴结未见肿瘤转移(0/16)。(12pLN):淋巴结未见肿瘤细胞累及(0/2)。(部分左肝外叶及肿瘤):治疗后改变,未见确切肿瘤细胞残留。
辅助治疗
患者于术后接受替吉奥+卡度尼利单抗方案辅助治疗,至2025年5月。
综合疗效评价:无病生存(NED)。
病例总结
该59岁女性患者,初步诊断为Ⅳ期胃肝样腺癌(HAS)伴多发肝、淋巴结转移,AFP显著升高,HER2表达为1+。经过以维迪西妥单抗联合免疫治疗为核心,并先后联合化疗及抗血管生成药物的多模式转化治疗后,肿瘤负荷显著降低,获得PR,最终成功接受根治性手术切除。术后病理证实原发灶、转移淋巴结及肝转移灶均达到pCR。术后继续辅助治疗,目前处于NED状态。
病例点评
专家介绍
主任医师,硕士生导师
重庆大学附属肿瘤医院胃肠肿瘤中心主任
世界内镜医师协会肝胆胃肠微创外科联盟理事
九三学社重庆市第五届委员会医药卫生专门委员会副主任
中国医师协会结直肠肿瘤专业委员会委员
中国医师协会结直肠肿瘤专业委员会ERAS学组常务委员
中国医师协会结直肠肿瘤专业委员会腹腔镜学组委员
中国抗癌协会第一届腹膜肿瘤专业委员会常务委员
中国抗癌协会第一届肿瘤微环境专业委员会委员
中国医师协会NOSES联盟重庆分会常务理事
重庆市医药生物技术协会胃肠肿瘤联盟理事
重庆市中西医结合学会姑息治疗专委会副主任委员
重庆市健康促进与健康教育学会第一届普外科专委会副主任委员
中国抗癌协会重庆市分会GIST专委会常务委员
全国卫生产业企业管理协会疝和腹壁外科产业及临床研究分会第六学术委员会常务委员
重庆市医学会外科学组常务委员
重庆市医学会肠外肠内营养专委会肿瘤营养学组委员
HAS是一种特殊的胃癌亚型,免疫微环境独特,可能对传统化疗反应不佳,但对免疫治疗可能有效,CPS评分等传统指标的预测价值有限。同时,研究显示HAS人群中HER2扩增率较高,这为抗HER2治疗提供了理论依据。
对于HER2低表达(IHC 1+或2+/FISH-)的患者,传统抗HER2单抗疗效有限。而新型ADC药物维迪西妥单抗,凭借其强大的“旁路杀伤效应”,对低表达的肿瘤细胞效果仍旧较好。RC48-C013研究[1]提示HER2低表达患者人群也可通过靶向联合免疫及化疗获益,其研究结果于2024年1月发表在《柳叶刀》子刊eClinicalMedicine。该研究首次在HER2高表达(IHC3+或IHC2+/FISH+)和HER2低表达(IHC1+或IHC2+/FISH-)胃癌患者中探索了ADC联合免疫治疗的安全性和疗效。
在今年ASCO大会上,一项维迪西妥单抗联合卡瑞利珠单抗和替吉奥对HER2过表达局部晚期胃癌新辅助治疗的疗效和安全性的研究[2]备受医学界关注。研究结果显示,新辅助治疗期间的客观缓解率为80.0%(24/30),其中6例(25%)达到pCR(ypT0N0M0)。R0切除率为100%。中位无病生存期(DFS)和总生存期(OS)尚未达到。该研究进一步证实了维迪西妥单抗在新辅助治疗中的潜力,为临床实践提供了重要参考。值得注意的是,本病例中患者对化疗耐受性较差,因此在后续治疗中调整了方案,采用了维迪西妥单抗联合免疫检查点抑制剂及抗血管生成药物的组合。这一调整不仅有效控制了肿瘤进展,还显著改善了患者的生存质量。
总之,本病例的成功经验表明,针对HER2低表达的晚期胃肝样腺癌,以维迪西妥单抗为核心的联合治疗可能是实现转化治疗并最终达到根治目标的重要途径。未来需要更多大样本、前瞻性研究来进一步优化此类患者的治疗策略,同时探索生物标志物在预测治疗反应中的作用,从而更好地指导临床实践。
[1].Wang Y, Gong J, Wang A, et al. Disitamab vedotin (RC48) plus toripalimab for HER2-expressing advanced gastric or gastroesophageal junction and other solid tumours: a multicentre, open label, dose escalation and expansion phase 1 trial. EClinicalMedicine. 2024;68:102415.
[2].Wang LG, Liu LG, Liu B, et al. Efficacy and safety of disitamab vedotin (RC48) combined with camrelizumab and S-1 for neoadjuvant therapy of locally advanced gastric cancer with HER2 overexpression: Preliminary results of a prospective, single-arm, phase II study. 2025 ASCO, Abstr e16147.
排版编辑:肿瘤资讯-软软











 苏公网安备32059002004080号
苏公网安备32059002004080号


