主持或参加的国家自然科学基金项目/课题多项
发表多篇学术成果
ASCO摘要解读
TRUST: Trial of radical upfront surgical therapy in advanced ovarian cancer (ENGOT ov33/AGO‐OVAR OP7)
摘要
研究背景
在经评估后可行满意减瘤的IIIB-IVB期初治晚期体能状态良好的卵巢癌、输卵管癌和腹膜癌患者中,减瘤术最佳时机仍存在争议。
研究方法
TRUST是一项针对IIIB-IVB期体能状态良好(ECOG 0/1)卵巢癌患者的国际性、随机、多中心III期试验,目的是比较初始减瘤术(PDS)后接受6个周期的静脉化疗与3个周期新辅助静脉化疗(NACT)后进行间歇性减瘤术(IDS)再接受3个周期静脉化疗的疗效差异。研究允许使用贝伐珠单抗和/或PARP抑制剂进行维持治疗。入组患者需符合术前临床和影像学评估确定PDS的潜在适应症,包括可切除性及患者的体能评估。为确保手术质量,参与中心需遵守现场手术质量保证审核,基础设施完备、手术熟练(PDS完全切除率≥50%)以及手术量足够(年PDS≥36次)。主要终点是总生存期(OS),次要终点为无进展生存期(PFS)和手术并发症。
研究结果
共纳入688例患者(中位年龄:63岁;范围:32 - 83岁)接受随机分配:345例被分配到PDS组,343例被分配到NACT/IDS组。91%的患者为高级别浆液性组织学类型。在PDS组中,所有随机分配/所有接受手术的患者中分别有61.7%/62.9%实现了R0切除,而在IDS组中,这一比例为72%/76.6%。PDS组的中位PFS为22.2个月,IDS组为19.7个月(HR 0.80,95%CI:0.66 - 0.96;p=0.02)。PDS组的中位OS为54.3个月,IDS组为48.3个月(HR 0.89,95% CI:0.74 - 1.08;p=0.24)。在PDS后实现R0切除的患者预后最佳,中位PFS和OS分别为27.9个月和67.0个月。在所有分析的亚组中均观察到PDS的长期获益。在III期患者(n=468)中,PDS的获益最为显著:PDS组与IDS组的中位PFS分别为26.3个月和21.4个月;中位OS分别为63.7个月和53.2个月。两组的主要术后并发症发生率均可接受,术后30天死亡率均<1%。
研究结论
在手术质量经认证的专业中心,对于手术耐受性较好的卵巢癌患者,相较于NACT/IDS, PDS可显著延长中位PFS,OS也获得延长趋势。该研究巩固了PDS作为体能良好、经评估可达到满意减瘤的晚期卵巢癌患者标准治疗的地位。
解读境
卵巢癌手术策略之争:TRUST研究如何重塑PDS与NACT-IDS的决策天平?
晚期上皮性卵巢癌患者的主要治疗模式包括初始肿瘤细胞减灭术(PDS)、及新辅助化疗(NACT)联合间歇性肿瘤细胞减灭术(IDS)两种。但这两种治疗模式的选择方面仍存在争议。
PDS与IDS之争
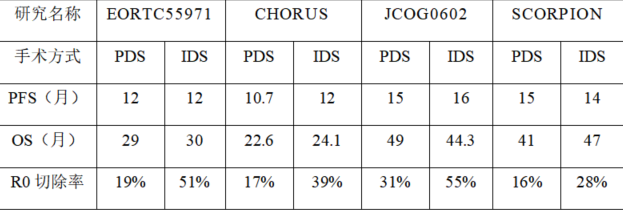
针对上述问题,既往有四项III期前瞻性随机对照试验(RCT)研究:欧洲发起的EORTC 55971试验[1]、英国发起的CHORUS研究[2]、日本临床肿瘤治疗组发起的JCOG0602研究[3]、意大利Fagitti团队发起的SCORPION研究[4]。简要而言,四项研究指出NACT提高了IDS的R0切除率,降低手术并发症,但总生存期(overall survival, OS)和无进展生存期(progression-free survival, PFS)方面并不优于PDS,因而奠定了NACT的在晚期上皮性卵巢癌中的重要地位。但是,
EORTC 55971 和 CHORUS 试验,两项试验入组中心的手术质量参差不齐,导致 PDS 组的R0率不足20%,且术后30天患者死亡率分别为 2.5%和5.6%, 远低于专业妇科肿瘤中心水平,这可能使 PDS 的疗效被低估,无法准确反映该治疗方式的真实效果。此外,研究入组标准进限定分期,其中包括不可切除的广泛转移患者。
JCOG0602 试验以影像学检查作为术前评估,研究未明确提及对手术质量的控制措施,手术质量参差不齐可能对结果产生干扰。SCORPION 试验以腹腔镜术前评估为基础,入组具有高肿瘤负荷(PI评分8-12)ⅢC和Ⅳ期卵巢癌患者,采用单中心优效性设计,减少了多中心手术方面的异质性,使手术操作的标准化和一致性程度更高,但是由于单中心试验的样本量相对较小,可能存在选择偏倚。
TRUST研究亮点与临床指导意义
TRUST(Trialof Radical Upfront Surgical Therapy)试验,是一项国际多中心、开放标签、随机对照 III 期试验。该研究针对上述临床研究设计的不足,优化实验设计,并以总生存期OS作为主要研究终点:
(1) 严格中心资质及手术质量控制:要求参与中心对 FIGO IIIB-IVB 期患者的初始手术 R0 切除率≥50%;年手术量≥36 例,具有高频次手术经验及复杂手术的操作熟练度,如上腹部切除、淋巴结清扫;对手术质量独立审计,要求提交前一年 24 份手术及病理报告,接受 TRUST 质量委员会审查,要求手术范围、并发症率及死亡率符合指南规范。
(2) 强制统一手术范围:所有患者要求全子宫双附件大网膜切除,并根据需根据肿瘤侵犯情况行腹膜切除、肠管 / 脾脏 / 胰腺部分切除、淋巴结清扫等复杂手术。对胸腔积液>500mL或左侧积液者,需行胸腔镜探查,确保胸内病灶可切除性评估完整。
(3) 精准的患者选择:要求入组患者为FIGO IIIB-IVB,且IV期要求可切除转移灶。这个研究和两个铂敏感复发卵巢癌比较手术和化疗的研究类似,(DESKTOPIII研究和SOC1的研究),对于晚期卵巢癌合适的手术患者需要有一定评估标准,包括肿瘤状态和患者手术耐受状态等。晚期卵巢癌患者年龄大,常常伴随低蛋白血症,或合并有肺栓塞,或肿瘤广泛无法满意切除,或切除后可以预期出现严重并发症,都不适合手术。
研究最终得出结论:对于经评估可能完全切除且能耐受手术的晚期卵巢癌患者,初次肿瘤细胞减灭术显著延长患者的PFS,OS表现出获益趋势,特别是在III期卵巢癌患者;且手术死亡率及术后并发症可以接受,两组患者生活质量无差异。此外,TRUST研究将贝伐及parp抑制剂维持治疗引入到研究中,这个更贴合临床实践应用,也更具有时代进步意义。值得注意的一点是,该研究在ITT人群中获得的PFS及OS的获益可能是由于III期卵巢癌患者占比约70%的原因。这也提示我们将该研究成果应用到临床中时,肿瘤分期是一个很重要的因素。
对于III期患者,PDS应视为首选治疗,但术前需充分评估,避免因影像评估不足入组肠管肠系膜广泛转移(如肠系膜挛缩),而无法达到满意减瘤的患者。因此,对于肿瘤负荷较大的III期腹盆腔广泛转移的卵巢癌患者,腹腔镜探查术是一个不错的选择,它一方面从某种程度上增加了PDS的选择率;另一方面,如果术中判断无法达到完全切除,可以改为3个周期新辅助治疗后再手术,因为数据显示,在初始手术中无法切除干净的30%患者中,有一半有机会在接受化疗后实现完全切除,从而依然能从手术中获益。而对于IV期患者,尽管EORTC 55971和CHORUS研究数据指出应优先考虑NACT-ICS,但TRUST研究数据并没有得到一个定论所有IV期卵巢癌患者都不能从PDS中获益,无论从TRUST研究的PFS还是OS上看,对于可切除的IV期患者,PDS均不劣于NACT-ICS。
TRUST研究的思考与延伸
所以,在临床实践中,如何评估晚期卵巢癌的可切除性至关重要。目前欧美在影像学评估时多采用CT或MRI,这也是TRUST研究的评估方式;而在中国的一些中心已采用PET-CT进行术前评估。但实际上,CT或MRI会降低IV期的诊断率,具体而言,一些MRI或CT认为是III期的患者,用PET-CT评估时可能已是IV期。中国的SUNNY研究也是比较晚期卵巢癌采用PDS vs NACT-ICS的多中心随机对照研究,并且术前采用PET-CT进行评估。期待研究结果会提供有益的答案。上文中提到的腹腔镜探查也是一种不错的方式,它的优势在于更准确,从某种程度上会提高PDS选择率,但缺点在于有创,也没有那么经济。此外,生物标记物也是评估PDS或NACT-ICS选择生存获益的方式之一,使用人工智能结合生物亚型及影像组学评估,也许是未来的方向。
R0切除率始终是决定预后的关键因素。我们可以看到,无论是EORTC 55971和CHORUS还是TRUST研究,相比于PDS,NACT均有较高的R0切除率,但是为什么PFS及OS仍然低于PDS 达到R0切除的患者,这可能与化疗消退肿瘤到术者肉眼不可及的状态,但实际上病理层面或分子层面肿瘤仍然存在,也许分子影像诊断技术可以解决这一问题,但如何找到准确性和特异性都很高的分子是问题的关键。另外,通过优化新辅助化疗方案,如调整药物选择、疗程数及给药途径等,提高术者肉眼无瘤的准确率也许是未来另一个研究方向。
对于一个年轻的妇瘤科医生而言,TRUST研究告诉我卵巢癌的手术治疗是最直接的武器,让自己提高手术技术,拥有先进有利的攻击武器至关重要,这促使我要坚定信心,练好技术,努力做好卵巢癌的R0手术。
杨慧娟教授—复旦大学附属肿瘤医院
TRUST研究是第一个支持在评估可实现满意切除晚期卵巢癌患者中,由有经验的妇瘤医生实行的直接手术对比新辅助治疗后的中间细胞减瘤术,患者的无进展生存期有统计学意义和临床意义的提高。这个研究中晚期卵巢癌患者获得了很高比率的R0切除率,高于以往的四项研究,体现了手术减瘤的重要价值。在PARPi维持治疗时代,该研究首次比较了PDS和IDS的生存优劣,依然体现了晚期卵巢癌的手术质量仍然是患者生存的重要决定因素。最后,这个研究结论得益于严格控制中心资质及手术质量,强制统一手术范围,因此作为一名妇瘤外科医生在卵巢癌的手术治疗方面一定要精进技术,要脚踏实地,孜孜不倦做出努力。
【温馨提示】:如果您觉得姜玮医生解读的好,请在下方为她点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
[1] VERGOTE I, TROPÉ C G, AMANT F, et al. Neoadjuvant chemotherapy or primary surgery in stage IIIC or IV ovarian cancer [J]. N Engl J Med, 2010, 363(10): 943-53.
[2] KEHOE S, HOOK J, NANKIVELL M, et al. Primary chemotherapy versus primary surgery for newly diagnosed advanced ovarian cancer (CHORUS): an open-label, randomised, controlled, non-inferiority trial [J]. Lancet, 2015, 386(9990): 249-57.
[3] ONDA T, SATOH T, SAITO T, et al. Comparison of treatment invasiveness between upfront debulking surgery versus interval debulking surgery following neoadjuvant chemotherapy for stage III/IV ovarian, tubal, and peritoneal cancers in a phase III randomised trial: Japan Clinical Oncology Group Study JCOG0602 [J]. Eur J Cancer, 2016, 64(22-31.
[4] FAGOTTI A, FERRANDINA G, VIZZIELLI G, et al. Phase III randomised clinical trial comparing primary surgery versus neoadjuvant chemotherapy in advanced epithelial ovarian cancer with high tumour load (SCORPION trial): Final analysis of peri-operative outcome [J]. Eur J Cancer, 2016, 59(22-33.











 苏公网安备32059002004080号
苏公网安备32059002004080号


