免疫治疗通过唤醒或增强患者自身的免疫系统来识别和攻击癌细胞,为肺癌患者提供了一种能够实现长期的疾病控制的治疗手段。以替雷利珠单抗为代表的PD-1/L1抑制剂被纳入CSCO指南推荐,成为从晚期到早期肺癌的标准治疗。随着对肿瘤生物学和免疫微环境的深入理解,双抗和ADC药物等创新疗法快速发展,临床试验正在全球范围内如火如荼地进行。这些都将驱动肺癌治疗格局的深刻变革,让肺癌的治疗未来可期。
本期【肿瘤资讯】特别邀请哈尔滨医科大学附属肿瘤医院于雁教授进行专访,以飨读者。
本期特邀专家——于 雁 教授
哈尔滨医科大学附属肿瘤医院 内科教研室主任 博士生导师 星联教授
中国临床肿瘤学会(CSCO)理事
黑龙江省抗癌协会常务理事
黑龙江省医学发展基金理事
黑龙江省医学会理事会理事
中国抗癌协会化疗专业委员会常委中国临床
中国临床肿瘤学会肿瘤支持与康复治疗委员会常委
中国医促进会肿瘤肿瘤舒缓治疗学分会常委
中国医药教育协会肺部肿瘤专业委员会 常委
中国抗癌协会癌症康复与姑息治疗委员会常委
中国抗癌协会肺癌专业委员会委员
中国抗癌协会肿瘤异质性与个体化治疗专委会常委
黑龙江省医师协会肺癌专业委员会主任委员
黑龙江省医学会癌症姑息息治疗委员会主任委员
黑龙江省抗癌协会癌症康复与姑息治疗专业委员会主任委员
黑龙江省抗癌协会肿瘤药物临床研究专委会 候任主任委员
中华转移性肿瘤杂志编委
中国肿瘤临床与康复杂志 编委
免疫治疗长生存引领肺癌治疗变革,向肿瘤“治愈”更进一步
Q1. 随着精准医学时代的到来,肺癌治疗格局已发生翻天覆地的变化。从对无进展生存期的显著改善,到对总生存期持续而有力的验证,免疫治疗的地位日益凸显。对此,请您从临床角度谈谈免疫治疗对诊疗实践的深远影响?
于雁教授:肺癌作为我国最常见的恶性肿瘤之一,严重威胁着人们的生命健康。传统的治疗手段如手术、放疗和化疗虽有一定疗效,但对于晚期肺癌患者,治疗后的中位总生存期约10-12个月,5年生存率仅有10%左右,疗效和长期生存仍有很大的提升空间。近年来,免疫治疗作为一种新兴的治疗手段,在肺癌治疗中取得了显著的疗效,为肺癌患者带来了长生存的希望。从2015年纳武利尤单抗获批上市,免疫治疗至今经历了十年的发展历程。这期间,不同免疫药物陆续公布了多个III期肺癌研究证据,从无进展生存数据到总生存数据,均一致验证了免疫治疗优异的远期疗效,让晚期患者实现“慢病化”,未来还有“治愈”的可能。
回顾KEYNOTE 042研究,免疫单药对比化疗治疗PD-L1阳性非小细胞肺癌(NSCLC)患者的5年OS率分别为21.9%和9.8%;KEYNOTE 189和KEYNOTE 407两项研究结果显示,免疫联合化疗一线治疗NSCLC 的5年OS率均达到约20%,相比化疗的5年OS率翻倍。
中国原研创新免疫治疗药物同样交出了令人满意的答卷,,RATIONALE-307和RATIONALE-304研究近期公布的更新随访数据,再次补充和巩固了免疫治疗的长生存证据。
RATIONALE-304研究长随访结果显示,替雷利珠单抗联合化疗一线治疗晚期非鳞非小细胞肺癌的4年总生存率达到32.8%,相比化疗组提升10%;同样,RATIONALE-307研究长随访结果显示,替雷利珠单抗联合化疗一线治疗晚期肺鳞癌显著延长患者生存,4年总生存率达32.2%,相比化疗组提升13%。无论鳞癌、非鳞癌,已全面实现三分之一患者活过4年。从研究曲线不难观察到,接受免疫治疗患者在42个月后的生存进入平台期,有望后续维持持久、稳定的肿瘤缓解(图1-2)。此外,RATIONALE-304/307研究中完成≥35周期的替雷利珠单抗长治疗(Long-term exposure, LTE)人群4年OS率分别高达89.3%和97.5%,相比ITT人群4年OS率提升超55%。从这些数据可以看出,免疫治疗具有突出的长拖尾效应,相比传统化疗时代,极大的改善了患者预后。
基于这些最新的临床研究证据,替雷利珠单抗5项肺癌适应症均获得CSCO指南I级推荐,也是唯一在《2025 CSCO非小细胞肺癌诊疗指南》和《2025 CSCO小细胞肺癌诊疗指南》中均获得I级推荐的免疫治疗药物。
目前,免疫治疗在我国已经得到广泛的应用,无论是高级别医院还是基层医院,肿瘤医生的治疗观念也随之改变。化疗时代,基于化疗药物的特性,往往很难做到持续的治疗,治疗中断可能导致肿瘤再次复发,甚至产生耐药。免疫时代来临,我们希望通过持续规范的治疗,让肿瘤得到持久的缓解。因此,在临床实践中,需要特别关注患者的评估和随访工作,实现从研究到Real world的长生存复制。
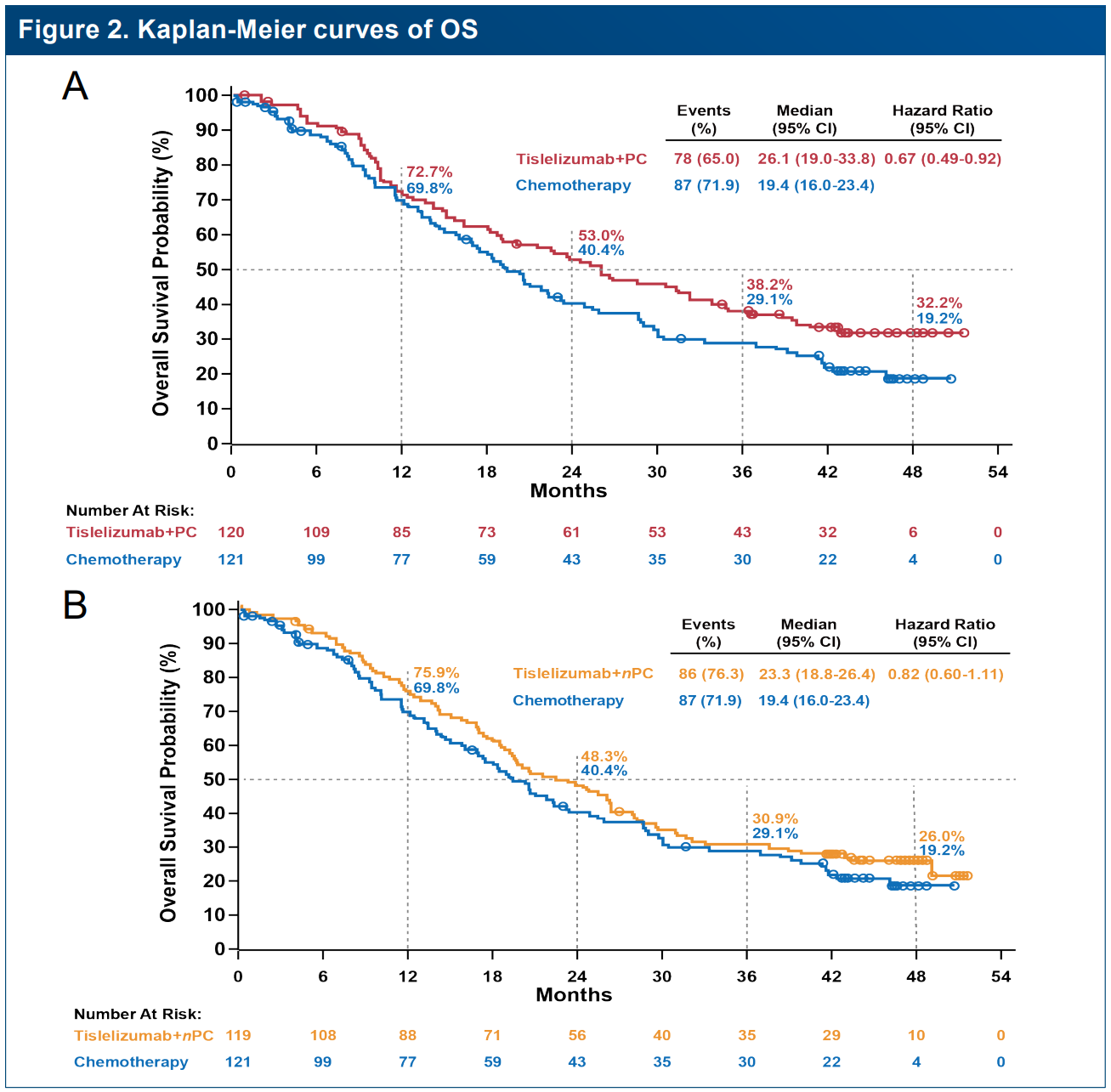 图1 RATIONALE 307研究长期随访数据
图1 RATIONALE 307研究长期随访数据
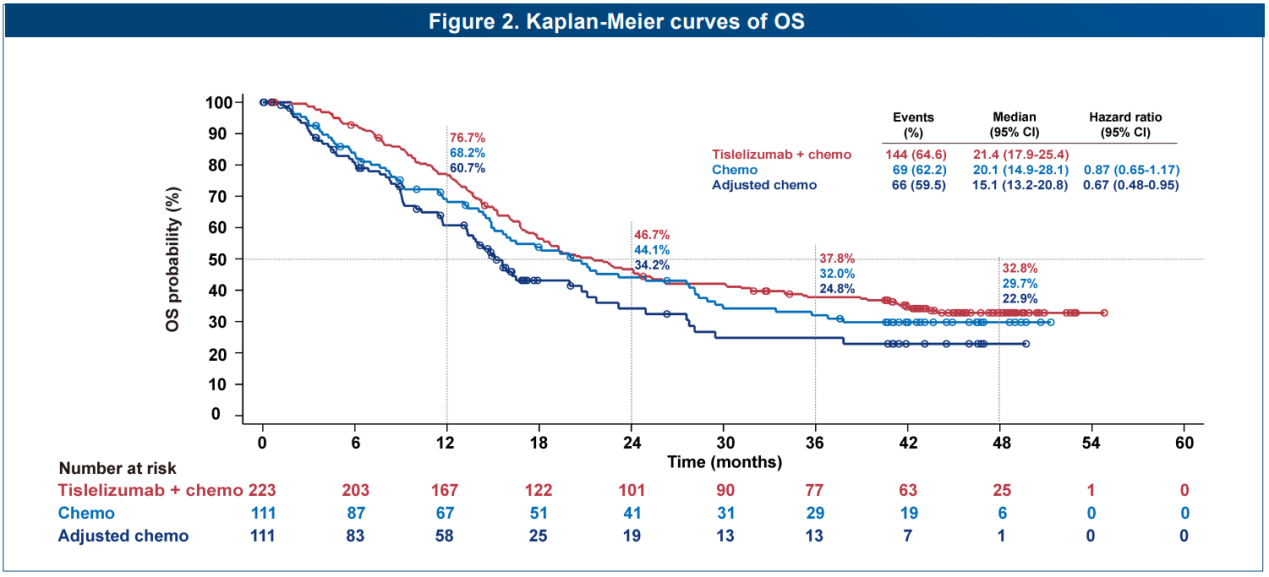 图2 RATIONALE 304研究长期随访数据
图2 RATIONALE 304研究长期随访数据
新型疗法加速,抗癌武器有望更加精准、强效
Q2. PD-1/L1抑制剂的成功研发全面变革肺癌的治疗,在此基础上,免疫治疗的迭代之路充满挑战。您如何看待新型免疫治疗的发展方向,如双特异性抗体?
于雁教授:以PD-1/L1抑制剂为代表的一批免疫治疗药物的获批,改变了从晚期到早期NSCLC和小细胞肺癌(SCLC)的治疗决策,从长期随访数据来看,确实有部分患者的生存可以达到4年或5年以上。如何让更多患者早期无进展生存期(PFS)的显著优势向总生存期(OS)转化是大家的核心关注点。新型免疫药物的研发,为肺癌治疗提供了新的思路。
目前,有超过200种双特异性抗体(bsAbs)正在临床开发中,其中约50%已进入II期和III期临床试验,还有部分双特异性抗体已获批上市。大多数用于肿瘤免疫疗法的双特异性抗体要么通过 T 细胞驱动的天然或内源性免疫发挥作用,例如增强已有的抗肿瘤反应和/或克服检查点抑制,要么通过双特异性抗体驱动的免疫细胞参与、激活和招募等方式提供合成免疫。
例如,埃万妥单抗(Amivantamab)是一种针对表皮生长因子受体 (EGFR) 和间充质上皮转化因子的双特异性抗体,对具有 EGFR 外显子 20 插入的非小细胞肺癌 (NSCLC) 患者以及在前线和复发环境中激活 EGFR 突变(外显子 19 和 21)的患者均显示出疗效,但需要特别关注独特的不良反应。伊沃西单抗(Ivonescimab)是一种 PD-1/血管内皮生长因子双特异性抗体,旨在增强免疫反应,同时抑制血管生成,目前正在进行的 III 期试验显示出在肺癌治疗中的前景,但总生存数据还有待验证。
此外,T细胞衔接器(TCEs)是一类能够将T细胞招募到肿瘤细胞附近,并通过这些免疫细胞来杀伤肿瘤细胞的双特异性抗体。塔拉妥单抗(Tarlatamab),一种靶向DLL-3和CD-3的双特异性T细胞衔接器(BiTE),可以实现对小细胞肺癌的精准打击。2024年5月16日,基于塔拉妥单抗DeLLphi-301研究,美国FDA加速批准塔拉妥单抗用于含铂化疗后进展的广泛期小细胞肺癌。2025年美国临床肿瘤学会(ASCO)公布的DeLLphi-304研究结果显示,与标准化疗方案(SOC)相比,塔拉妥单抗在总生存期(OS)方面获得了具有统计学和临床意义的显著改善,在既往接受过一线含铂化疗失败的SCLC患者中展现出显著的生存优势。同时,针对既往接受过至少二线治疗(包括含铂化疗)失败的广泛期小细胞肺癌中国患者的DeLLphi-307研究报阳,塔拉妥单抗有望为中国小细胞肺癌患者的二线、三线及后线治疗提供新的用药选择。目前,塔拉妥单抗已被《小细胞肺癌免疫治疗专家共识(2025版)》纳入治疗推荐。
未来,期待针对不同靶点,不同作用机制的早期开发中的免疫药物能够早日进入临床试验,以确证的疗效和安全性造福更多的肺癌患者。
Q3. 在肿瘤治疗领域,除免疫治疗外,ADC 药物无疑是近年来的明星。作为一种创新的抗肿瘤疗法,如何看待ADC药物在肺癌治疗的应用前景?
于雁教授:抗体偶联药物(ADC)是由单克隆抗体、细胞毒药物及连接子构成,通过靶向递送机制实现精准杀伤肿瘤细胞,兼具高选择性和高效力。ADC药物的本质是具有靶向作用的化疗药物。近年来,ADC在肺癌治疗领域取得显著进展,2022年FDA批准德曲妥珠单抗治疗HER2突变非小细胞肺癌,标志肺癌ADC治疗元年的开启。目前,靶向HER2、TROP2等靶点的ADC在NSCLC中的应用价值已得到临床试验证据的支持。
从第一代ADC到第三代ADC,跨越近20余年,才迎来较为成熟的ADC技术。尽管如此,已经上市的ADC仍然存在着一些尚未解决的问题。一方面是连接子的优化,目前的连接子还不能做到完全稳定,毒素仍然会在正常组织中部分释放,导致ADC药物的不良反应较多,无论是第二代ADC药物T-DM1,还是第三代ADC药物DS-8201都存在着诸多的全身不良反应。另一方面,还面临着生物标志物、治疗窗窄、耐药,以及药物疗效不稳定等问题。
以HER2靶点为例,Trastuzumab deruxtecan(T-DXd)是首个在HER2突变NSCLC中显示显著活性的ADC药物。DESTINY-Lung01研究是一项多队列II期试验,其队列2纳入91例既往接受过治疗的HER2突变晚期NSCLC患者,接受T-DXd(6.4mg/kg,q3w)治疗。结果显示,客观缓解率(ORR)达55%,中位无进展生存期(PFS)为8.2个月,中位总生存期(OS)为17.8个月。基于此,2022年8月FDA加速批准T-DXd用于HER2突变NSCLC。然而,Patritumab deruxtecan(HER3-DXd)在NSCLC中的研究结果不尽如人意。2025年ASCO会议上公布的HERTHENA-LUNG02研究结果显示,HER3-DXd在PFS方面相较对照组仅延长0.4个月,HR=0.77,OS方面未达到统计学显著性,且安全性方面,HER3-DXd组中有14例患者(5%)出现了被判定与药物相关的间质性肺病(ILD),包括2例间质性肺病致死事件。同样,在SCLC中,靶向DLL3的ADC药物,ROVA-T的III期研究失败也一度为该靶点的研发带来了一定的难度。
令人欣喜的是,在刚刚结束的2025 ASCO大会上仍有12项肺癌领域ADC研究入选大会口头报告,涵盖多种靶点和肺癌类型,包括针对c-MET、Nectin-4、EGFR、HER3、DLL-3等靶点的ADC药物在非小细胞肺癌和小细胞肺癌中的应用探索。期待这些数据和研发技术的升级可以进一步拓展ADC药物在肺癌治疗中的应用。
总结
随着多项免疫治疗III期研究的长期生存数据公布,肺癌治疗领域迎来了重大突破。以替雷利珠单抗为代表的国产创新PD-1抑制剂被纳入CSCO指南推荐,全面重塑了中国肺癌的治疗格局,同时确立了免疫治疗在临床实践中的基石地位。新型免疫治疗和ADC药物的成功研发,标志着肿瘤治疗进入了多元化的新时代,未来不同药物组合疗法的探索前景广阔。
排版编辑:肿瘤资讯-高惠











 苏公网安备32059002004080号
苏公网安备32059002004080号


