由福建省抗癌协会癌痛专业委员会和福建省抗癌协会中西医整合肿瘤专委会青年委员会主办的【十邑论坛】开播啦!论坛于每周四推出,带您用中文听原汁原味的欧洲肿瘤内科学(ESMO)研究。本期邀请来自英国皇家自由医院和伦敦大学学院癌症研究所的Tim Meyer教授聚焦肝细胞癌的辅助治疗的最新进展。【肿瘤资讯】特邀三明市第二医院杨兰芳教授进行相关研究解读。
三明市第二医院 肿瘤科 主治医师
肝细胞癌(HCC)是全球范围内常见的恶性肿瘤之一,其高发病率和高死亡率严重威胁着人类健康。尽管手术切除是目前治疗HCC的主要手段,但术后复发仍是影响患者预后的主要因素。辅助治疗旨在降低复发风险,提高治愈率,已成为HCC治疗研究的热点领域。近年来,随着免疫检查点抑制剂等新型抗肿瘤药物的出现,HCC辅助治疗领域取得了新的进展,为改善患者预后带来了新的希望。
辅助治疗的基本原则
辅助治疗作为一种辅助性治疗手段,通常在手术后用于防止HCC的复发。其基本目标是通过降低疾病复发的风险来提高治愈率,并延长患者的无复发生存期(RFS)和总生存期(OS)。在理想情况下,所有患者都能从辅助治疗中获益,但临床实践表明,即使接受了辅助治疗,许多患者仍会面临复发的风险。这意味着仅有一部分患者,尤其是那些具有高复发风险的患者,可能真正从长期辅助治疗中获得更多益处。
然而,辅助治疗的获益与风险并存。医生在制定治疗方案时,必须仔细权衡患者可接受的毒性水平,因为晚期和早期疾病患者对治疗相关毒性的耐受性存在差异。目前,HCC辅助治疗主要有三种模式:术后辅助治疗、术前新辅助治疗和围手术期治疗。每种模式都有其自身的优势和局限性,需要根据患者的具体情况进行选择。
辅助治疗的研究进展
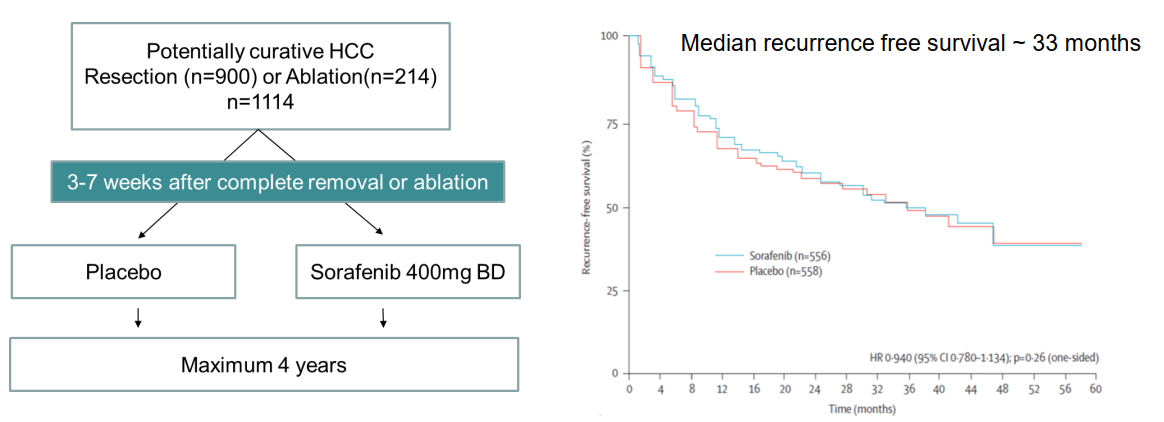
近年来,HCC的辅助治疗研究取得了一些重要进展。最具代表性的研究之一是HCC切除或消融后辅助性索拉非尼治疗研究(STORM)结果。索拉菲尼作为一种多靶点酪氨酸激酶抑制剂(TKI),其在HCC的治疗中取得了初步的成功。STORM研究是是首个评估索拉非尼辅助治疗HCC的大型Ⅲ期临床试验,其结果表明,尽管该研究未能达到预期的临床终点,但该项研究中位RFS为33个月,为HCC的辅助治疗提供了有价值的基线数据(图1)。这些数据可以帮助我们更好地了解了高风险患者的特征,并为后续的辅助治疗研究奠定了基础。在该试验中,研究者将高风险患者定义为肿瘤多发、微血管侵犯、分化差等患者,并发现该类患者在接受索拉菲尼辅助治疗后,虽然无复发生存期有所改善,但并未显著提高总体生存期。
除此之外,免疫治疗在HCC的辅助治疗中也引起了广泛关注。韩国的一项研究结果表明,免疫治疗能够显著提高RFS,且这一效益能够转化为OS的提高。研究发现,通过刺激患者的免疫系统,免疫检查点抑制剂能够有效地杀伤肿瘤细胞,从而减缓肿瘤的复发和转移。尽管这项研究样本量较小,且大多数患者接受了射频消融治疗,但其结果为免疫治疗在HCC辅助治疗中的应用提供了初步的证据。
此外,PD-1/PD-L1抑制剂等免疫疗法在其他癌症领域的成功应用,也使得其在HCC治疗中的前景更加广阔。一项来自中国的Ⅱ期临床试验研究了PD-1抑制剂——信迪利单抗在HCC辅助治疗中的应用。这项开放标签的随机试验纳入了来自6家中国医院的198患者,并根据微血管侵犯程度来评估患者的复发风险。患者被随机分配到信迪利单抗组(3周方案,共8个周期)或观察组,其中78%的患者完成了8个周期的治疗。该研究的主要终点是RFS。
基线特征方面,观察组肝硬化患者比例更高(56% vs 44%),且具有更多高风险特征,包括更高的微血管侵犯发生率(图2)。尽管两组患者的肿瘤大小和STORM研究相似(平均约5 cm,且大多数患者为单个肿瘤),但信迪利单抗组的RFS显著改善,达到27.7个月(HR=0.534)(图3)。然而,与STORM研究中索拉非尼组33个月的RFS相比,该研究对照组的RFS仅为15.5个月,这表明对照组的RFS数据并不成熟。亚组分析未发现任何特定亚组患者(例如乙肝患者或不同微血管侵犯程度的患者)从信迪利单抗辅助治疗中获得额外获益(图4)。

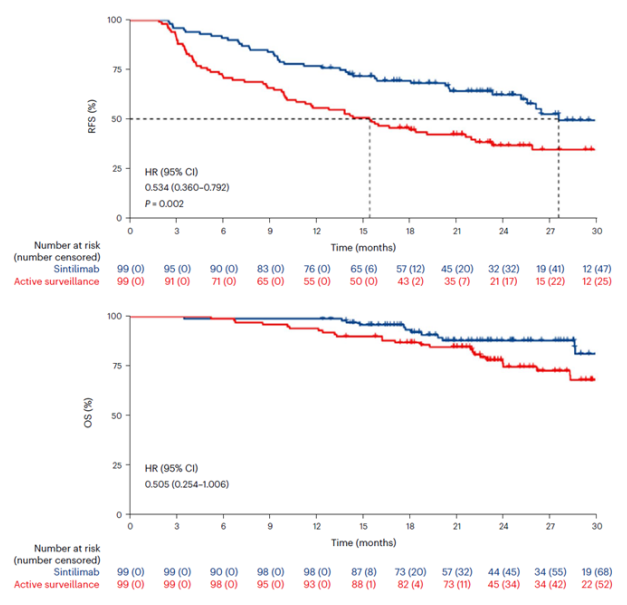
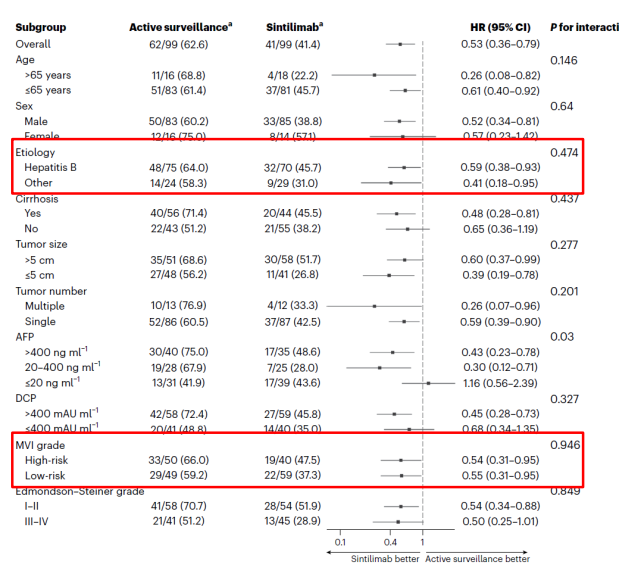
这项研究存在一些局限性,包括开放标签设计、仅在中国进行、以及对照组RFS数据不成熟等。尽管如此,该研究的结果具有重要意义,为PD-1抑制剂在HCC辅助治疗中的应用提供了初步证据。目前,两项全球性的Ⅲ期临床试验(Keynote 937和Checkmate 9DX)正在进一步评估PD-1抑制剂在HCC辅助治疗中的疗效和安全性。
另一项重要的研究是IMbrave 050研究,该研究评估了PD-L1抑制剂阿替利珠单抗在HCC辅助治疗中的应用。这项研究将高危HCC患者随机分配接受12个月的阿替利珠单抗联合贝伐珠单抗(Atezo/Bev)治疗或安慰剂,主要终点是RFS,并允许交叉治疗。与STORM研究相似,IMbrave050研究也针对高危患者人群,例如肿瘤较大、存在微血管侵犯、多发肿瘤或分化不良等。基线特征方面,IMbrave 050研究中的患者大多来自亚洲(71%),体能评分良好,且大多数患者感染乙型肝炎病毒(图5)。
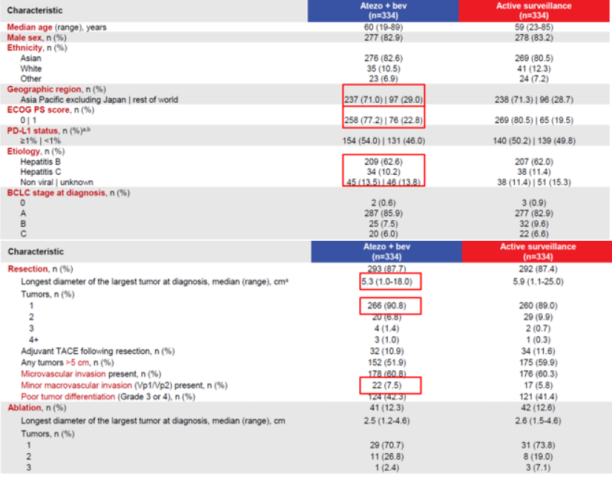
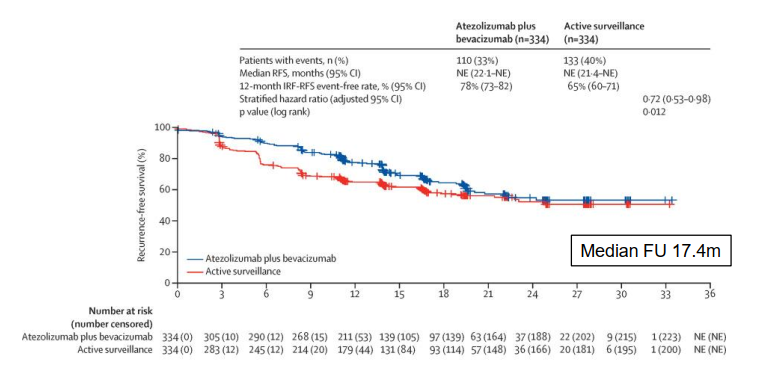
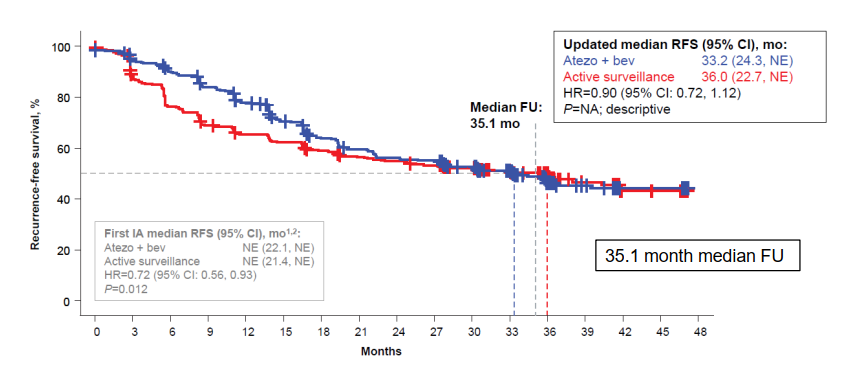
该研究的结果于2023年底发表在Lancet期刊。虽然首次中期分析显示Atezo/Bev组的RFS显著改善(HR=0.72),但在长期随访中,这种优势并未得到维持(图6)。最新数据显示,两组的RFS曲线在18个月左右开始趋于一致,最终的HR为0.90,差异无统计学意义(图7)。这表明,阿替利珠单抗辅助治疗可能仅带来短期获益,而无法提供长期生存优势。
亚组分析也未能发现任何特定亚组患者可以从阿替利珠单抗辅助治疗中获得明确的额外获益。此外,该研究还观察到,约1/3的患者出现了3级或4级的治疗相关毒性反应,治疗相关死亡率接近1%。
IMbrave 050研究结果暴露出HCC辅助治疗的困境:免疫治疗的疗效为何逐渐减弱?12个月的治疗持续时间是否足够?如何平衡疗效和毒性?这些问题亟待解答,以期为患者提供更优的辅助治疗方案。
为了更好地理解HCC辅助治疗的复杂性,我们可以借鉴其他肿瘤类型的研究经验。例如,帕博利珠单抗辅助治疗肾癌的研究显示,无疾病生存期(DFS)的改善确实转化为了OS的获益(HR=0.62),且交叉治疗和后续治疗并未影响这一结果。黑色素瘤中伊匹木单抗辅助治疗也观察到了类似的结果,DFS的获益转化为持续的OS获益。
HCC辅助治疗的未来方向
尽管IMbrave 050研究未能证实阿替利珠单抗辅助治疗可以带来长期OS获益,但来自细胞因子诱导的杀伤细胞研究的长期随访数据显示,即使在存在第二原发肿瘤风险的乙肝患者中,仍可以观察到生存曲线的显著分离。这表明,对于特定HCC患者群体,辅助治疗仍有可能带来OS获益。
我们需要对HCC患者进行长期随访,以最终确定辅助治疗对OS的影响。在与患者讨论治疗方案时,我们需要充分告知其潜在的毒性风险以及治疗获益的不确定性。此外,我们还需要不断优化临床试验设计,例如延长随访时间、采用更复杂的统计分析方法等,并积极探索预测性生物标志物,以便更准确地评估辅助治疗的疗效并更好地选择患者。
新辅助治疗和围手术期治疗也为HCC辅助治疗提供了新的方向。这些治疗模式的优势在于可以更早地进行治疗干预,并有可能帮助我们筛选出对治疗敏感的患者。目前,一些小型研究正在探索免疫检查点抑制剂在新辅助治疗和围手术期治疗中的应用,初步结果显示出一定的潜力。例如,英国正在进行的PRIMER 1研究评估了围手术期帕博利珠单抗联合仑伐替尼治疗HCC的疗效,主要终点是主要病理缓解率。
目前,我们已经看到了一些初步迹象,表明免疫检查点抑制剂无论是在新辅助治疗还是辅助治疗中,都可能对可手术的HCC患者带来益处。然而,我们还需要更多的研究来证实这些结果,并解决当前HCC辅助治疗面临的挑战,例如疗效的持续性、治疗的持续时间、患者选择以及毒性管理等。相信随着研究的不断深入,我们终将找到更有效的HCC辅助治疗策略,为改善患者预后做出更大的贡献。
大家可以自行下载对应幻灯,再配合本音频听,效果更好。
排版编辑:xiaodong











 苏公网安备32059002004080号
苏公网安备32059002004080号


