FGFR2b是胃癌新兴靶点,靶向FGFR2b过表达的贝玛妥珠单抗首次将晚期HER2阴性胃癌总生存突破2年,开启精准 “诊”“疗”新征程。近日,其Ⅲ期确证性研究FORTITUDE-101公布FGFR2b过表达数据,这也是全球最大样本量数据,全文“Prevalence of FGFR2b Protein Overexpression in Advanced Gastric Cancers During Prescreening for the Phase III FORTITUDE-101 Trial”见刊于JCO Precision Oncology。本期特别邀请FORTITUDE-101研究者、文章共同作者之一,来自哈尔滨医科大学附属肿瘤医院消化内科的张艳桥教授,以及来自北京协和医院病理科的周炜洵教授,共话胃癌精准“诊”“疗”发展以及FGFR2b带来的新突破。
专家介绍
哈尔滨医科大学附属肿瘤医院
黑龙江省消化道肿瘤诊疗中心主任
黑龙江省结直肠癌临床医学研究中心主任
黑龙江省肿瘤免疫学重点实验室主任
国务院特殊津贴专家
国家卫健委有突出贡献中青年专家
中国医师奖获得者
首届龙江名医,龙江工匠
中国临床肿瘤学会(CSCO)胃癌专家委员会候任主任委员
中国临床肿瘤学会(CSCO)结直肠癌专家委员会副主任委员
中国临床肿瘤学会(CSCO)临床研究专家委员会副主任委员
中国抗癌协会 肿瘤大数据与真实世界研究委员会首任主任委员
中国抗癌协会 肿瘤药物临床研究专业委员会副主任委员
专业方向为消化道肿瘤的精准诊疗和转化研究。先后主持国家自然科学基金 6 项(含区域重点 1 项),国家科技重大专项子课题 1 项。获省政府科技进步一等奖 1 项,二等奖 2 项,中国抗癌协会科技二等奖 1 项。发表SCI论文 100 余篇,代表性研究发表于 Cancer Cell,Cancer Res,Clin Cancer Res,Adv Mater 等杂志。授权国家发明专利 2 项。
专家介绍
北京协和医院病理科主任医师
中华医学会病理学分会消化系统学组组长
中华医学会消化分会炎症性肠病协作组
中国抗癌协会肿瘤病理委员会胃癌中青年协作组等学术团体的委员
《中华病理学杂志》编委
以消化道病理作为专业方向,对消化道肿瘤及炎症性疾病的诊断有丰富的经验。
FORTITUDE-101研究设计
首个全球多中心、前瞻性、大样本Ⅲ期确证性研究,在晚期HER2阴性且FGFR2b过表达胃癌患者中探索贝玛妥珠单抗联合化疗一线治疗的疗效和安全性。
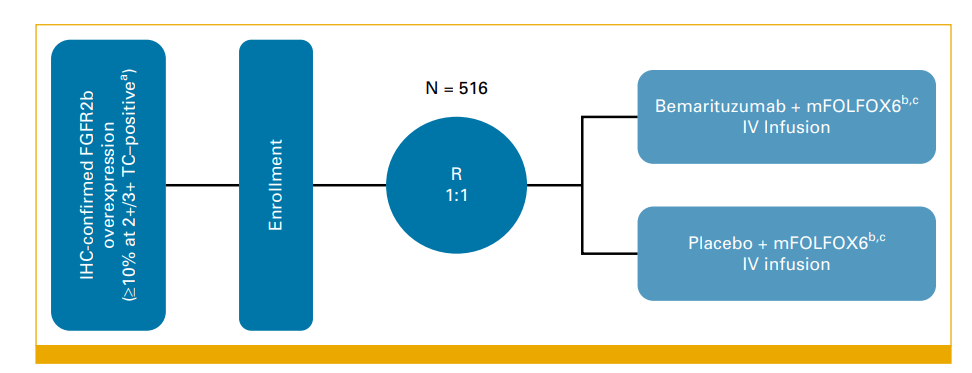
(最开始入组FGFR2b过表达(任何2+/3+)患者,后续方案修订为仅入组FGFR2b过表达(≥10% 2+/3+)患者)
FORTITUDE-101研究初步结果
在预筛选且具有可评估FGFR2b过表达结果的3782例患者中:
37.8%的患者存在FGFR2b过表达(任何2+/3+)[即经免疫组化(IHC)检测到任意肿瘤细胞FGFR2b膜染色2+/3+];
16.2%的患者存在FGFR2b过表达(≥10% 2+/3+)(即经IHC检测到≥10%肿瘤细胞FGFR2b膜染色2+/3+);
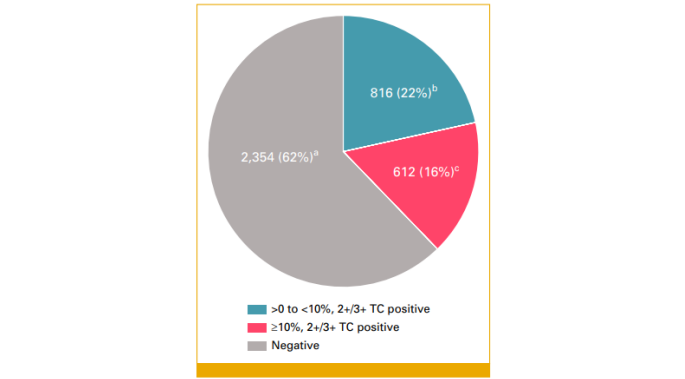
FORTITUDE-101研究预筛选患者FGFR2b过表达情况
(a 95% CI, 60.7-63.8; b 95% CI, 20.3-22.9; c 95% CI, 15.0-17.4; TC:肿瘤细胞)在不同年龄(<65/≥65)、性别(男性/女性)、肿瘤组织样本收集部位(原发灶/转移灶)、收集方法(活检/手术)、原发肿瘤类型(胃癌/胃食管结合部癌)和地区区域亚组中,FGFR2b过表达患者比例相似(无论是任何2+/3+,还是≥10% 2+/3+),与整体人群一致。
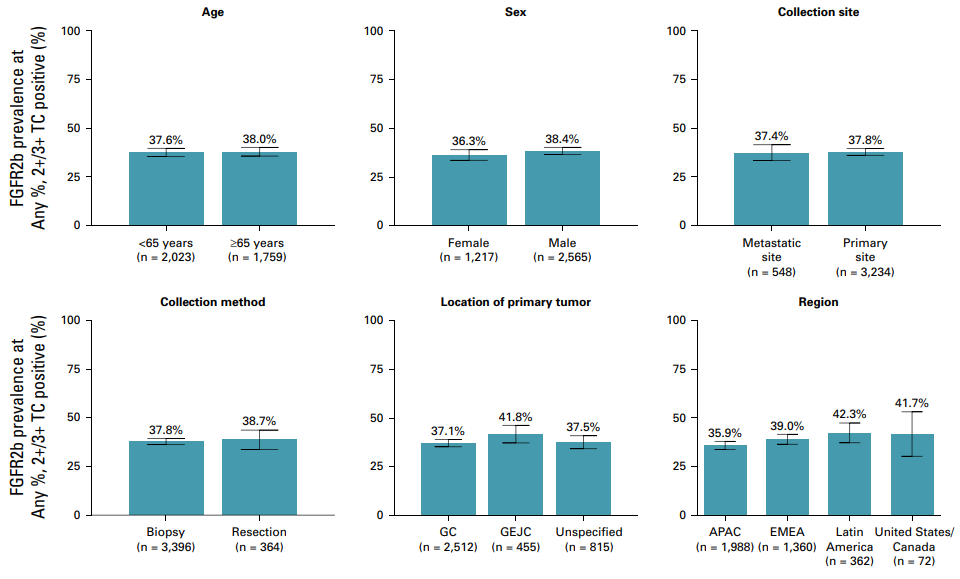
不同亚组中FGFR2b过表达(任何2+/3+)患者比例 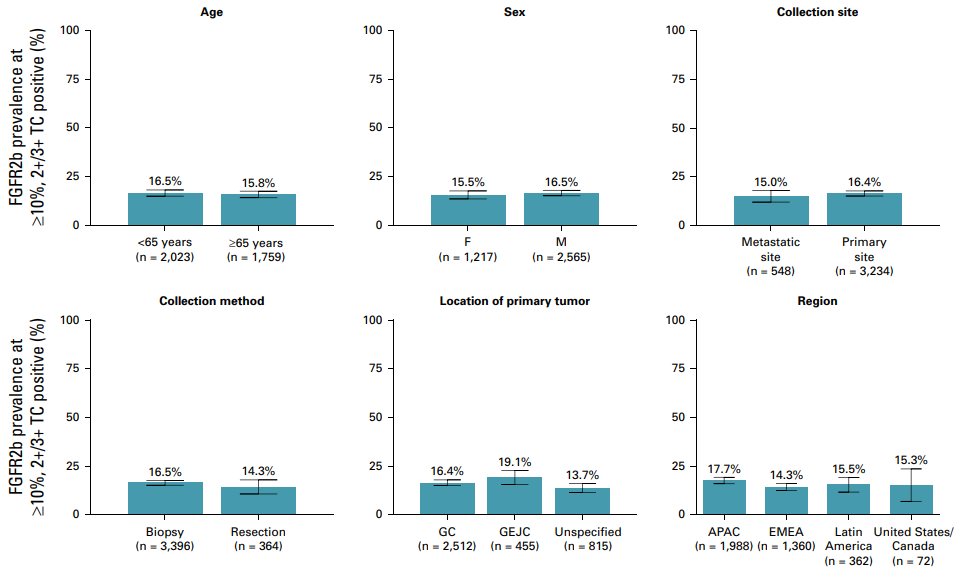
不同亚组中FGFR2b过表达(≥10% 2+/3+)患者比例
晚期胃癌精准治疗演变及突破?
近些年来,相比于肠癌等消化道肿瘤,胃癌治疗进步较快。胃癌精准治疗领域已经有了抗HER2、PD-1和CLDN18.2,特别是这两年比较关注的新靶点FGFR2b。
过去没有精准诊疗的时代,晚期胃癌以化疗为主,患者平均生存期很难超过1年。抗HER2药物曲妥珠单抗的出现,使得晚期胃癌患者中位总生存期远超1年,达到14~16个月。然后,多个免疫检查点抑制剂将晚期胃癌生存延长至1年以上,长达16~17个月,这是胃癌领域新的突破。近两年,大家更多关注的是CLND18.2靶点,包括单抗、ADC和CAR-T等多种药物已在研发中,目前临床研究结果显示抗CLDN18.2单抗同样延长了晚期胃癌生存,达18个月左右。从化疗时代患者生存难以突破1年,到后来抗HER2/免疫/抗CLDN18.2 患者生存达到14~18个月,晚期胃癌精准诊疗不断突破,但仍需持续探索。
这两年我们也关注到FGFR2b这一靶点,特别是贝玛妥珠单抗FIGHT研究给我们带来很多新的想法,该药在Ⅱ期研究中疗效非常好,但我们对于FGFR2b靶点发病率和预后等情况了解较少。
FGFR2b在胃癌发生和发展中的作用?为什么FGFR2b能够成为胃癌新兴靶点?
FGF/FGFR信号通路与细胞生长、增殖和血管侵犯等密切相关,FGFR基因或蛋白表达异常时可能就会促进肿瘤发生和发展。我们比较了解的是FGFR1~4基因异常,但基因异常与蛋白过表达有所区别。FGFR2基因异常可能会导致FGFR2b蛋白过表达,但即使基因正常的情况下,在后续转录、翻译和蛋白质合成中发生异常时也会导致FGFR2b蛋白过表达。
作为临床医生,如果我们要探讨FGFR2b蛋白过表达在临床领域的相关性,我们需要简易、可行、易获得且可以广泛推广的检测手段来检测,免疫组化(IHC)是最成熟的方法,主要检测蛋白过表达。我们目前比较期待能够在胃癌领域检测FGFR2b过表达,因为其与肿瘤发生/发展相关,而且能够有助于我们比较全面地发现FGFR异常在胃癌领域的应用。我特别想通过这个问题来呼吁各个中心医院的病理科,特别是三级医院的病理科能够先行,将FGFR2b IHC检测开展起来,因为FGFR2b可能与胃癌预后和淋巴结转移相关。进行FGFR2b过表达检测有助于未来快速进入FGFR2b治疗进程,当前,FGFR2b靶向药物研发如火如荼,比如贝玛妥珠单抗已经获得突破性疗法,很快就能够走进临床,Ⅱ期数据显示患者生存期达到2年,Ⅲ期研究正在进行中;FGFR2b ADC等其他药物也在研发路上。靶向治疗,病理检测先行,只有有病理检测,我们才有下一步FGFR2b靶向治疗的可能性。
晚期胃癌患者中FGFR2b过表达情况如何?
既往基础和临床研究中均看到了胃癌中存在FGFR2b过表达。FIGHT是首个全球多中心、前瞻性探索晚期胃癌FGFR2b过表达情况及贝玛妥珠单抗一线治疗疗效和安全性的Ⅱ期研究。结果显示,约30%患者中存在FGFR2b过表达(任何2+/3+),并且能够从贝玛妥珠单抗靶向治疗中获益。
在此基础上,贝玛妥珠单抗开展了更大样本量的Ⅲ期确证性研究FORTITUDE-101,该研究为国际多中心,在包括中国在内的37个国家287家研究中心进行。我们中心也加入了该研究,并入组了一些患者。
近日,FORTITUDE-101研究首先发表FGFR2b过表达结果:37.8%患者存在FGFR2b过表达(任何2+/3+),16.2%患者存在FGFR2b过表达(≥10% 2+/3+)。此外,在不同年龄(<65/≥65)、性别(男性/女性)、肿瘤组织样本收集部位(原发灶/转移灶)、收集方法(手术切除/胃镜活检)、原发肿瘤类型(胃癌/胃食管结合部癌),以及地理区域亚组患者中,FGFR2b过表达(包括任何2+/3+,≥10% 2+/3+)患者比例相似,均与整体人群一致。这一数据是非常值得信任的,因为其来自于近3800例患者大样本数据。我们预测将来这一Ⅲ期临床研究结果应该是普适用于各个地区和各种人群,是非常有意义的。
晚期胃癌FGFR2b靶向治疗进展?
第一个获得突破性进展的就是贝玛妥珠单抗,是首个靶向FGFR2b的治疗药物;此外FGFR2b ADC等药物也在研发中。我们更多了解的是贝玛妥珠单抗,已经有了很好的Ⅱ期研究结果,Ⅲ期也已入组结束,我们也非常期待研究结果。
贝玛妥珠单抗具有双重作用机制:1、与肿瘤细胞表面FGFR2b结合,竞争性阻断FGF7/10/22配体与FGFR2b结合,从而阻断FGFR2b信号通路;2、Fc段去除了核心岩藻糖,诱导增强的ADCC效应,通过NK细胞的募集实现潜在的肿瘤细胞杀伤。
Ⅱ期FIGHT研究显示,与化疗相比,贝玛妥珠单抗联合化疗改善了晚期HER2阴性胃癌一线总生存(OS),中位OS分别为19.2个月 vs 13.5个月;特别是FGFR2b过表达(≥10% 2+/3+)患者,中位OS分别为24.7个月 vs 11.1个月,首次将晚期胃癌总生存突破2年,我们非常看好这一数据。在东亚人群中甚至疗效更好,FGFR2b过表达(≥10% 2+/3+)患者总生存长达30个月,当然这一数据也需要在Ⅲ期临床研究中进一步证明,我们也特别期待能够尽早看到FORTITUDE-101研究结果,相信能够改变胃癌未来治疗格局。
病理专家访谈—周炜洵 教授
胃癌分子分型的发展及临床应用现状?
胃癌分子分型目前广为人知的有TCGA和ACRG分型。分子分型能够揭示胃癌分子异质性,为精准治疗提供新视角,例如MSI型和EBV型可能对免疫治疗有较好响应。但是由于检测技术和成本要求高、缺乏直接对应的靶向治疗策略等诸多因素,TCGA和ACRG分型在临床中应用有限。
HER2靶点的发现及曲妥珠单抗的成功标志着胃癌进入精准诊疗时代。免疫治疗也使得PD-1/PD-L1和MSI-H/dMMR逐渐成为胃癌常规检测的生物标志物。靶向治疗,精准检测先行,目前国内外指南均推荐对于胃癌患者进行HER2、PD-L1和MSI-H/dMMR等生物标志物检测,以指导治疗决策。近年来,CLDN18.2和FGFR2b等新靶点及新型药物涌现,不断拓宽胃癌精准诊疗范畴,相信更多患者将从中获益。
FGFR2b过表达与FGFR2基因扩增有何区别,如何检测FGFR2b?
FGFR2b蛋白是由FGFR2基因转录时发生选择性剪切,随后翻译产生的蛋白质之一。理论上,除FGFR2基因扩增外,从DNA到蛋白质合成过程中其他生物学功能(如转录调控,翻译调控、以及蛋白质合成和降解)异常时也可能导致FGFR2b蛋白过表达。
FGFR2基因扩增在胃癌中发生率约为5%~10%,但FGFR2b过表达发生率更高。FORTITUDE-101研究显示,晚期HER2-胃癌患者中37.8%存在FGFR2b过表达(任何2+/3+),16%患者存在FGFR2b过表达(≥10% 2+/3+)。
此外,FGFR2b过表达与FGFR2基因扩增检测方法不同。FGFR2b基因扩增是通过NGS/PCR方法检测,而FGFR2b过表达则通过IHC检测。采用NGS或PCR方法检测FGFR2基因扩增会导致大量FGFR2b过表达患者漏检,所以IHC才是FGFR2b检测的“金标准”。
因此,从发生原因、发生率及检测方法三个方面来看,FGFR2基因扩增均不等同于FGFR2b过表达,不能将二者混为一谈。
晚期胃癌FGFR2b过表达检测面临哪些机遇和挑战?
FGFR2b过表达可能与胃癌分化差、淋巴结转移和患者不良预后相关。另外FIGHT研究也让我们看到FGFR2b过表达胃癌患者能够从FGFR2b靶向治疗中获益。因此,在胃癌患者中进行FGFR2b检测不仅有助于协助医生进行病理诊断和预后评估,还能够识别将来有机会接受FGFR2b靶向治疗患者。
虽然目前有多个FGFR2b抗体可及,但临床应用还比较少。病理医生对于这一新兴靶点的检测和判读标准还有待学习、规范和统一。临床医生对于FGFR2b靶点的临床意义和检测重要性的认知也有待加强。
但是,机遇与挑战并存。对于IHC检测方法我们并不陌生,IHC检测快速、便捷、经济、灵敏度和特异性高,目前已常规用于胃癌生物标志物检测,因此FGFR2b检测可以整合纳入现有胃癌生物标志物检测流程,协助评估患者预后以及指导后续FGFR2b靶向治疗,我们也非常期待未来FGFR2b能够纳入常规检测。FGFR2b检测就像一片尚未开垦的沃土,值得广大病理医生和临床医生携手共进,开展临床和科研探索,助力胃癌精准诊疗发展。
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


