*此报道将发布于良医汇-肿瘤医生APP
肝细胞癌(HCC)是全球最常见的恶性肿瘤之一,其中不可切除肝细胞癌(uHCC)患者的预后较差。药物洗脱珠经动脉化疗栓塞术(DEB-TACE)是治疗uHCC的主要手段之一,但其疗效仍有待提高。因此,亟需探索新的治疗策略以改善uHCC患者的预后。在此背景下,一项在中国12个中心开展的随机、前瞻性、多中心III期临床试验,旨在比较DEB-TACE联合阿帕替尼与单纯DEB-TACE治疗uHCC的疗效和安全性,以期为uHCC患者提供更有效的治疗方案。结果表明,DEB-TACE联合阿帕替尼治疗uHCC,可显著延长患者的PFS和OS,疗效优于单纯DEB-TACE,且安全性良好[1]。【肿瘤资讯】小编整理了其中重点信息,以飨读者。
研究背景
肝细胞癌(HCC)是全球发病率和死亡率均较高的恶性肿瘤,其中不可切除肝细胞癌(uHCC)患者的治疗选择有限,预后较差。经动脉化疗栓塞术(TACE)是治疗uHCC的重要手段,但传统TACE(cTACE)存在一些局限性,例如药物分布不均、栓塞效果不佳等。为此,近年来发展了药物洗脱珠经动脉化疗栓塞术(DEB-TACE),该技术通过持续释放化疗药物,提高了药物浓度和肿瘤暴露量,增强了抗肿瘤效果。
另一方面,靶向药物的出现为uHCC的治疗带来了新的希望。索拉非尼和阿帕替尼等靶向药物通过抑制肿瘤血管生成等机制,能够有效控制肿瘤进展。其中,阿帕替尼对VEGFR-2的抑制效果更强,与TACE联合应用具有协同作用。
尽管DEB-TACE和阿帕替尼均已在临床应用,但关于两者联合应用的研究仍然有限。既往研究主要集中于cTACE联合靶向治疗,而DEB-TACE联合阿帕替尼的疗效和安全性尚需进一步评估。因此,该研究开展了一项III期临床试验,旨在比较DEB-TACE联合阿帕替尼与单纯DEB-TACE治疗uHCC的疗效和安全性,为uHCC患者提供更优的治疗方案。
研究方法
该项III期临床试验采用随机、开放标签设计,于2021年1月至2022年6月在中国12家医院进行。研究纳入了符合入选标准的uHCC患者,并以1:1的比例随机分配到DEB-TACE单独治疗组和DEB-TACE联合阿帕替尼组(图1)。
所有患者均接受标准化的DEB-TACE治疗,由经验丰富的介入放射科医生操作。DEB-TACE+阿帕替尼组患者在DEB-TACE术后3-5天开始口服阿帕替尼,初始剂量为500 mg,每日一次。
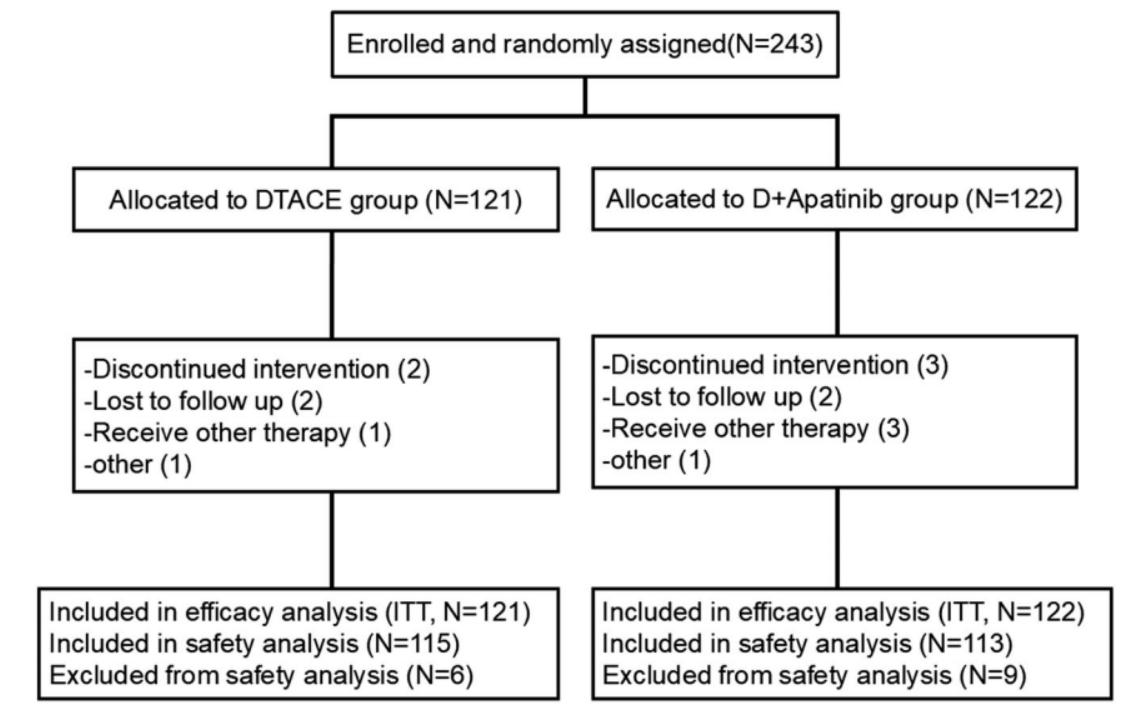
该研究的主要终点是无进展生存期(PFS),次要终点包括总生存期(OS)、mRECIST标准的客观缓解率(ORR)和疾病控制率(DCR)以及治疗相关不良事件(TRAE)。
研究结果
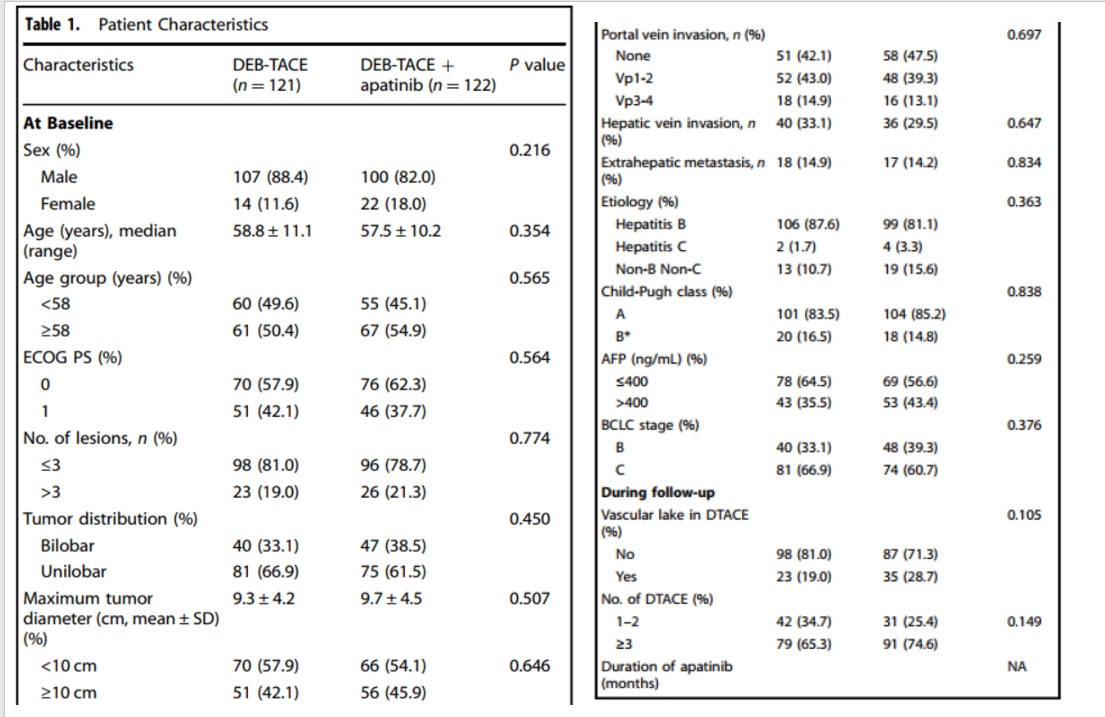
该项研究在中国12家医院招募并随机分配了243名uHCC患者。最终,DEB-TACE组和DEB-TACE+阿帕替尼组分别纳入了121名和122名患者用于疗效分析,115名和113名患者用于安全性分析。两组患者在基线时的特征具有可比性(表1)。
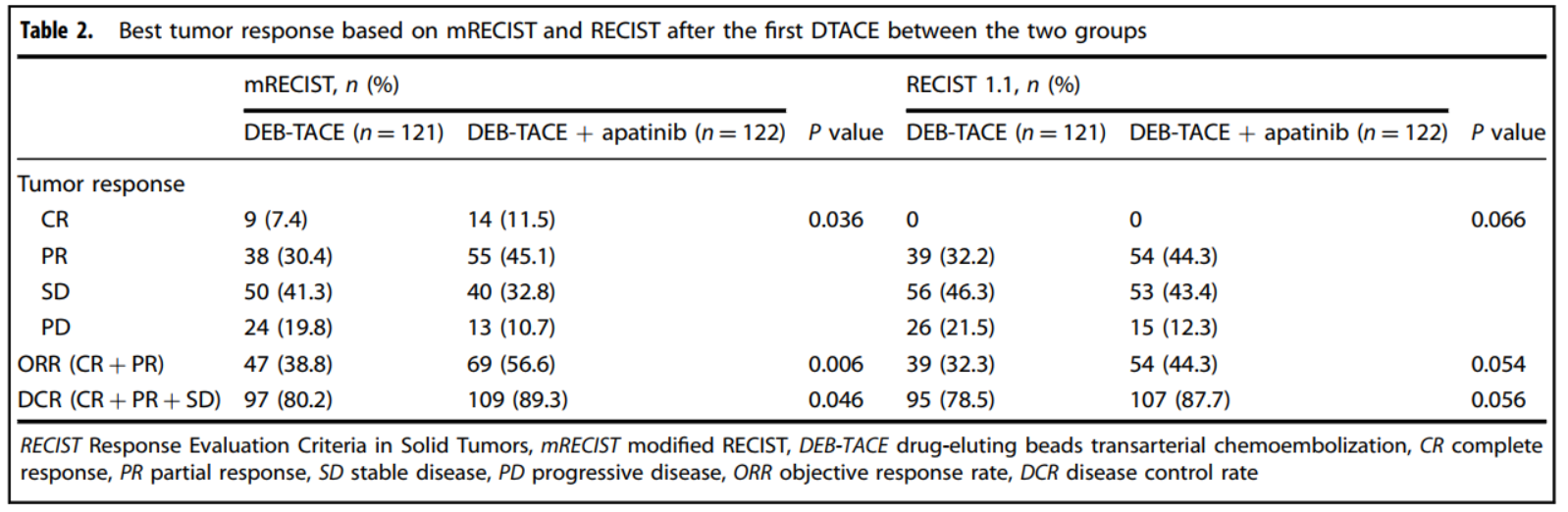
首次TACE治疗后,DEB-TACE联合阿帕替尼组的肿瘤缓解情况显著优于单纯DEB-TACE组。根据mRECIST标准,联合治疗组的ORR为56.6%,而DEB-TACE组为38.8%(P<0.001);联合治疗组的DCR为89.3%,而DEB-TACE组为80.2%(P <0.001)。然而,根据RECIST 1.1标准,两组的肿瘤缓解情况相似(表2)。
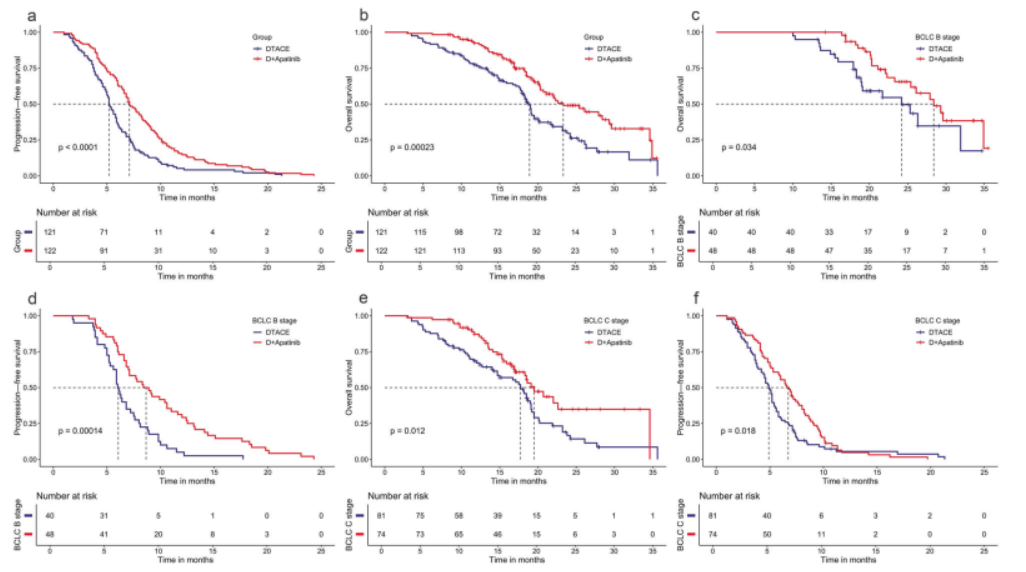
该研究随访至2023年7月1日,DEB-TACE组中位随访时间为24.3个月,DEB-TACE+阿帕替尼组为23.9个月。结果显示,DEB-TACE + 阿帕替尼组的中位OS显著长于DEB-TACE组(23.3个月 vs. 18.9个月,P<0.001),中位PFS亦显著延长(7.1个月 vs. 5.2个月,P<0.001)(图2)。亚组分析显示,BCLC B期和C期患者的OS和PFS均在联合治疗组中显著延长。此外,联合治疗组的1年生存率更高(86.1% vs. 71.9%,P< 0.05)。
尽管两组的疾病进展人数和诊断时肺转移发生率相似,但联合治疗组发生新肺转移和肝侧支动脉受累的比例更低。对于伴有肝静脉癌栓的患者,DEB-TACE+阿帕替尼组的ORR也更高。多变量Cox回归分析显示,DEB-TACE+阿帕替尼是OS和PFS的独立保护因素,其他与OS相关的因素包括门静脉侵犯、DEB-TACE中存在血管湖和≥3次TACE疗程,而与PFS相关的因素包括肝静脉侵犯和≥3次TACE疗程。
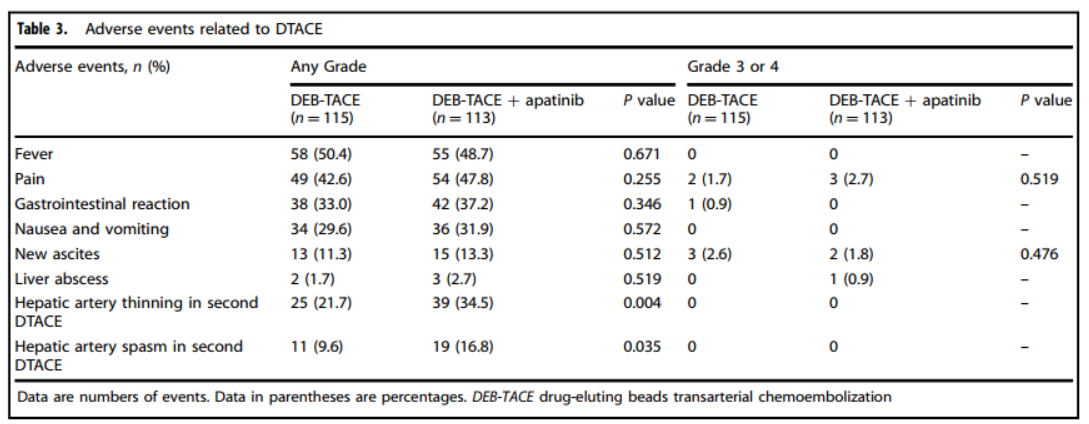
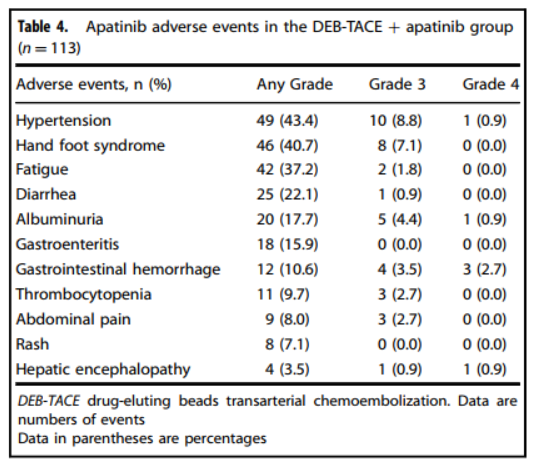
在安全性方面,两组患者的安全性良好,DEB-TACE相关不良事件发生率相似,常见的不良事件包括发热、疼痛、胃肠道反应、恶心、呕吐、新发腹水和肝脓肿等(表3)。然而,在第二次DEB-TACE治疗期间,DEB-TACE+阿帕替尼组的肝动脉变薄和痉挛发生率显著高于DEB-TACE组,这可能是由于阿帕替尼的抗血管生成作用导致血管脆性增加(表4)。值得注意的是,肝动脉痉挛在使用罂粟碱后得到了有效缓解。
此外,两组均有少量患者出现肝脓肿,但经过积极治疗后均得到控制,未发生死亡病例。在DEB-TACE+阿帕替尼组中,最常见的阿帕替尼相关不良事件包括高血压、手足综合征、疲劳和腹泻等,这些不良事件大多为轻中度,未发生导致治疗中断或5级不良事件。两组患者的肝肾功能指标基本相似,DEB-TACE+阿帕替尼组的肝功能指标(AST、白蛋白)和肾功能指标(血清肌酐)在某些时间点优于DEB-TACE组。
所有患者在疾病进展后均重新开始全身治疗,部分患者同时接受了局部治疗。DEB-TACE+阿帕替尼组患者在进展后接受了免疫治疗或换用其他靶向药物(多纳非尼或仑伐替尼)联合免疫治疗。而DEB-TACE组患者在进展后则接受了靶向药物联合免疫治疗,但没有患者接受DEB-TACE+阿帕替尼治疗。此外,部分患者还接受了针对局部复发的治疗,包括再次DEB-TACE治疗、cTACE联合消融治疗、针对肺转移的微波消融或冷冻消融、针对淋巴结转移的碘125粒子植入等。
讨论
该研究结果显示,DEB-TACE联合阿帕替尼治疗uHCC可显著改善患者的OS和PFS,疗效优于单纯DEB-TACE。这可能归因于阿帕替尼抑制了DEB-TACE诱导的血管生成,从而产生协同作用。此外,联合治疗还有助于控制肝外侧支动脉和肺转移,进一步改善预后。
研究还探讨了DEB-TACE治疗过程中血管湖形成的影响,发现其与更好的预后相关。联合治疗组在第二次或后续TACE期间肝动脉变薄和痉挛的发生率较高,但可以通过药物干预有效管理。
与既往研究相比,该研究中阿帕替尼相关不良事件的发生率较低,这可能与阿帕替尼的剂量调整有关。总体而言,DEB-TACE联合阿帕替尼治疗的安全性良好,耐受性良好。
然而,该研究也存在一些局限性,例如样本量较小、后续治疗方案多样、随访时间较短等,这些因素可能对结果的解读产生一定影响。
尽管存在这些局限性,该研究仍为DEB-TACE联合阿帕替尼治疗uHCC提供了重要的临床证据,表明该联合方案是一种有效且安全性良好的治疗选择,有望为uHCC患者带来更好的临床获益。
Duan X, Li H, et. al. Comparison of drug-eluting bead transarterial chemoembolization combined with apatinib versus drug-eluting bead transarterial chemoembolization for the treatment of unresectable hepatocellular carcinoma: a randomized, prospective, multicenter phase III trial. Signal Transduct Target Ther. 2024 Nov 13;9(1):304.
本材料由阿斯利康公司提供,仅供医疗卫生专业人士参考,不用于产品推广目的。涉及具体药物使用,请参考相关药品说明书。
审批编码:CN-150981
有效期至:2025/06/30
排版编辑:肿瘤资讯-Delia











 苏公网安备32059002004080号
苏公网安备32059002004080号


