KRAS突变在结直肠癌(CRC)中占比高达40%,是一个重要的预测预后的生物标志物。靶向KRAS突变的治疗策略从间接抑制到现在的直接靶向,新的 KRAS等位基因特异性抑制剂也在如火如荼地开展临床试验。由于肿瘤内固有的适应性耐药机制,KRAS突变型结直肠癌的治疗不可避免地需要采用联合疗法。
专家介绍
吉林大学中日联谊医院胃肠结直肠外科副主任
瑞典卡罗林斯卡医学院胃肠中心访问学者
德国埃尔兰根大学医学院普通外科访问学者
日本国立癌中心胃外科访问学者
《中华胃肠外科》杂志通讯编委
《中华消化外科》杂志通讯编委
《结直肠肛门外科》杂志编委
人民卫生出版社《腹腔镜医生成长手册》主编
中国医师协会外科医师分会专业信息传播和教育专家工作组专家委员
中国医师协会结直肠肿瘤专业委员会临床技能培训专业委员会秘书长
脏器联合切除与质量控制专业委员会委员
中国医师协会外科医师分会微创外科专家工作组专家委员
中国医师协会外科医师分会经肛腔镜外科专家工作组专家委员
中国医师协会外科医师分会腹膜后及软组织肿瘤专家工作组专家委员
中华结直肠外科学院第一届学术委员会委员
国家卫生健康委能力建设和继续教育外科学专家委员会微创外科专业委员会委员
中国研究型医院学会精准医学与肿瘤MDT专业委员会青年委员会副主任委员、肿瘤临床协作组(东北)委员
中国研究型医院学会肿瘤外科专业委员会委员
中国微循环学会肿瘤学分会胃肠肿瘤学组副组长
中国中西医结合学会普通外科专业委员会直肠癌防治专家委员会常务委员
中国中西医结合学会普通外科专业委员会青年委员
中国经肛腔镜外科学院讲师团讲师
中国老年保健医学研究会老年胃肠外科分会委员
国家远程医疗与互联网医学中心专家委员会常务委员
1. 广谱靶向KRAS通路阶段
KRAS 突变已在多种癌症中被发现,包括胰腺癌、非小细胞肺癌(NSCLC)和结直肠癌(CRC)等。结直肠癌(CRC)是一种异质性大的高发恶性肿瘤,发生机制复杂,其中KRAS突变是最为频发的致癌基因之一,可通过RAS/MAPK通路促进肿瘤生长1。多项研究证实,KRAS突变与CRC患者的不良预后密切相关2-3。KRAS突变患者通常对EGFR抑制剂治疗反应不佳4。
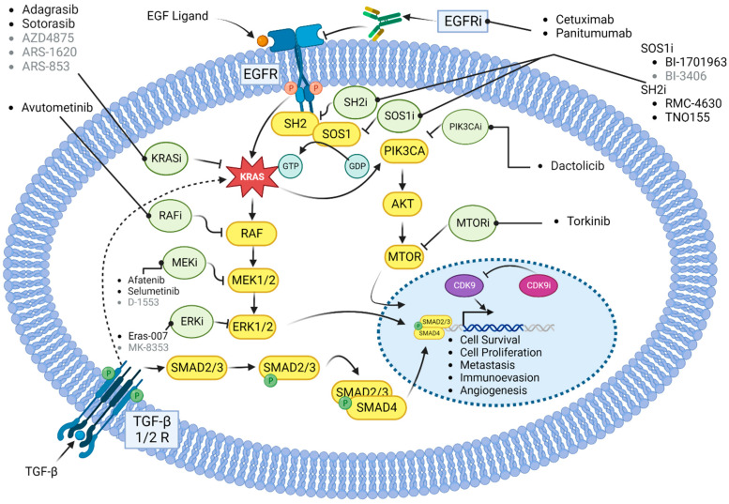
图片来自:Bteich F, Mohammadi M, Li T, et al. Targeting KRAS in Colorectal Cancer: A Bench to Bedside Review. Int J Mol Sci. 2023;24(15):12030.
在过去的二十年里,已制定出多种针对KRAS信号通路的治疗策略,其中包括KRAS蛋白直接抑制、RNA干扰、阻止RAS定位至质膜等。由于设计KRAS直接抑制剂面临困难,早期针对KRAS突变结直肠癌的许多尝试都集中在抑制KRAS上游和下游的靶点上。先前研究主要涵盖了蛋白质定位抑制剂、MEK抑制剂、黏着斑激酶(FAK)抑制剂、细胞周期蛋白依赖性激酶(CDK)抑制剂和异戊烯基结合蛋白(PDEδ)抑制剂,并取得了不同程度的进展1。
2. 选择性靶向KRAS突变阶段
KRAS蛋白的普遍分布,非选择性靶向KRAS方法理论上可能会导致更高的毒性。而KRAS G12C的出现,使用突变等位基因特异性药物可以选择性抑制KRAS,而不会影响其他KRAS突变体和具有野生型KRAS等位基因的正常细胞。首个进入临床试验的直接KRAS G12C抑制剂是安进公司的Sotorasib5;另一种有效的共价KRAS G12C抑制剂是Adagrasib(原名 MRTX849),它具有半衰期长、剂量依赖的药代动力学特性和中枢神经系统 (CNS)渗透率高的优势6;其他有前景的KRAS G12C等位基因特异性抑制剂包括ARS-1620、SML-8-73-1和ASP24531。为提高药物的选择性以及克服第一代抑制剂的局限性,目前研究人员正在探索抑制KRAS的新方法,寻找KRAS第二代抑制剂,并将KRAS抑制剂与其他疗法相结合,以扩大和加深治疗反应,延长患者生存期。
结直肠癌中的突变型KRAS G12C受上游受体酪氨酸激酶信号(RTK)调控。RTK 是一类跨膜蛋白,它们在细胞信号传导中扮演重要角色,通过激活下游信号通路来调控细胞的增殖、分化和生存等功能。EGFR是一种特定的RTK,在结直肠癌中,EGFR的过表达或突变常见,并与肿瘤的侵袭性及预后不良相关。EGFR的异常激活可以促进肿瘤细胞的生长、侵袭和转移,因此EGFR成为结直肠癌靶向治疗的重要靶点。研究显示抗EGFR单抗和KRAS G12C抑制剂的联合治疗对结直肠癌非常有效,如西妥昔单抗和Sotorasib联合使用可抑制结直肠癌细胞中EGFR驱动的MAPK通路的激活,从而维持下游靶标抑制,显著增强KRAS G12C的抑制效果并导致肿瘤消退7。CodeBreaK 101研究表明,KRAS G12C抑制剂Sotorasib与抗EGFR单抗帕尼单抗联合治疗在化疗耐药KRAS G12C突变转移性结直肠癌患者中表现出较好的安全性和疗效,联合治疗的客观缓解率(30% vs. 9.7%)优于单用Sotorasib8。一项研究显示9,Sotorasib或ARS-1620与多种RTK通路抑制剂的组合均显示出对KRAS G12C结直肠癌细胞系异种移植小鼠模型的协同作用,因此针对多种潜在RTK反馈机制(例如MEK抑制剂)的组合治疗策略非常重要。
另一项研究显示,干扰KRAS-SOS1相互作用会通过阻止GDP转化为GTP来阻碍KRAS的激活,在Adagrasib中添加BI-3406(SOS1-panKRAS 抑制剂)可克服对KRAS抑制剂单药治疗诱导的耐药性,目前KRYSTAL-14研究和CodeBreaK 101研究正在进行中1。在KRAS突变癌症中,SHP2抑制与MEK或ERK抑制具有很强的协同作用,TNO155是一种旨在靶向SHP2的抑制剂,正在以广泛的临床联合策略研究以覆盖MAPK通路。例如在KontRASt-01研究中。KontRASt-01是一项Ib/II 期研究,旨在评估新型KRAS G12C抑制剂 JDQ443与TNO155联合治疗包括CRC在内的晚期实体瘤。目前正在招募患者,预计于 2027 年完成1。
LY3537982是一种新型G12C直接抑制剂 (G12Ci),它的药效比第一代KRAS G12C抑制剂强10倍,可以较低剂量给药,对靶点的抑制充分,脱靶效应更少10;Divarasib(或GDC-6036)是一种强效的KRAS G12C突变蛋白不可逆共价抑制剂,与早期研究中的第一代抑制剂相比,该药物表现出相似的缓解率,且毒性较小11。MRTX1133是一种强效的选择性非共价KRAS G12D抑制剂,显示出与GDP结合的KRAS G12D高亲和力相互作用,该药已被证明可在体外抑制KRAS信号传导,在PDX模型中有超过30%的肿瘤退缩12。此外,直接靶向活性GTP结合形式的G12C的抑制剂[也称为KRAS-G12C(ON) 抑制剂]与分子伴侣环丝氨酸蛋白酶A形成三重复合物,从而克服由增强的上游信号传导驱动的耐药性,比如RMC-6291、BI-2865和BI-2493等panKRAS抑制剂被证明可以在大量KRAS突变和KRAS激活的癌细胞系中抑制肿瘤生长和下游MAPK信号传导1。新型的细胞疗法,包括嵌合抗原受体 (CAR) T细胞疗法和基于T细胞受体 (TCR) 的过继性T细胞疗法,以及疫苗疗法,是针对靶向KRAS机制的新希望。
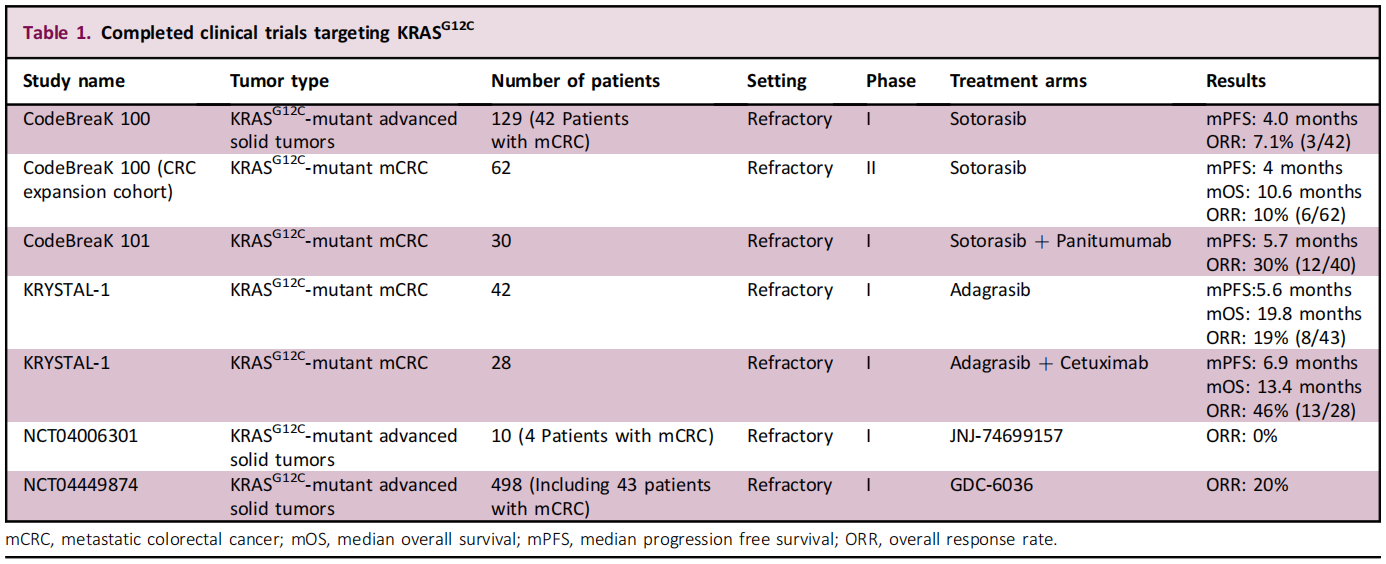
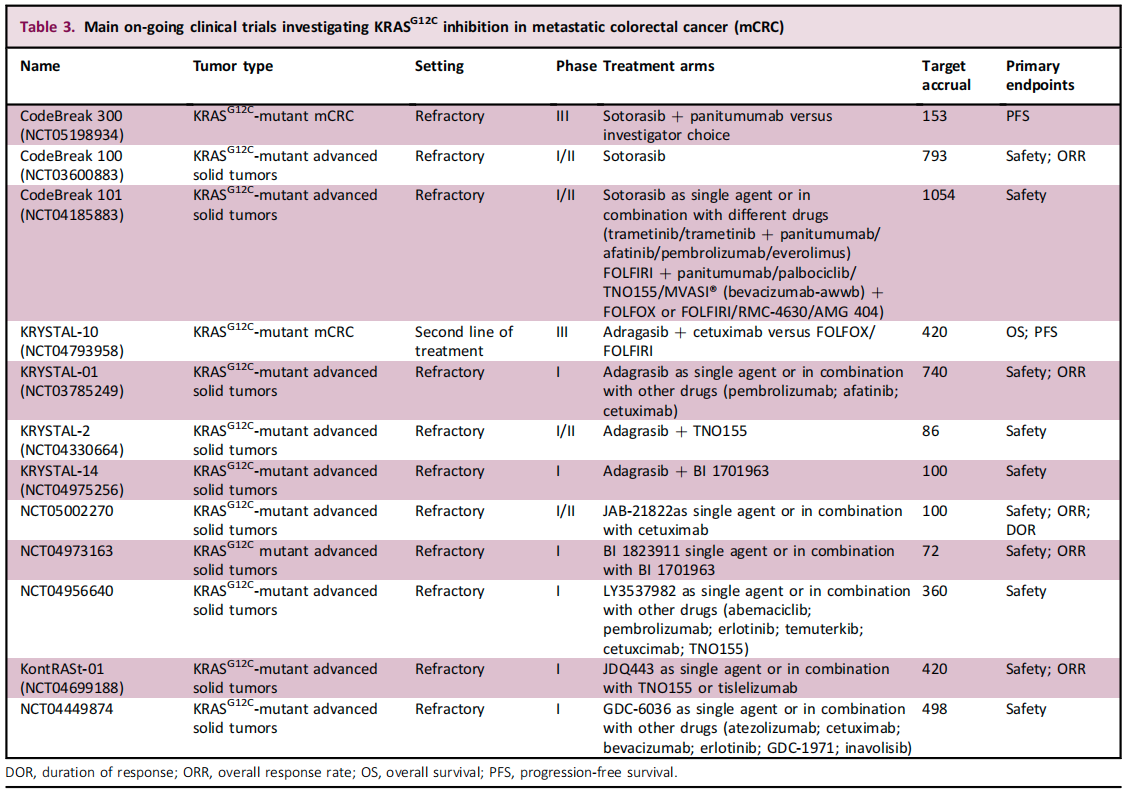
KRAS突变在CRC中的靶向治疗取得了显著进展,新型KRAS抑制剂和联合治疗策略为KRAS突变型CRC患者带来了新的希望。随着KRAS抑制剂研发的蓬勃发展,KRAS基因突变检测的重要性也不可同日而语,发生了巨大变化。针对KARS基因的精准医疗有望进一步提升患者的预后。
3. KRAS突变检测重要性
KRAS 基因突变的检测标本可以是组织,也可以是血液,组织检测仍是金标准。检测方法有很多,包括直接测序法、高通量测序法,高分辨率熔解曲线分析法(high resolution melting,HRM)、焦磷酸测序法、定量PCR法、突变扩增阻滞系统法(amplincationrefractory mutation system,ARMS)、限制性片段长度多态性聚合酶链反应法(restriction fragment length polymorphism,RFLP)、聚合酶链反应-单链构象多态性分析法(PCR-singlestrand confomation polymorphism,PCR-SSCP)以及高效液相色谱分析法等13-14。
传统的诊断方法在检测肿瘤负荷的微小变化方面存在显著局限,而借助高通量技术的发展,循环肿瘤DNA(ctDNA)的基因状态已能较为精准地反映原发肿瘤的表型和遗传学构成,为早期诊断提供了新的可能性。作为一种潜在的实时肿瘤监测标志物,ctDNA检测不仅能够无创地对结直肠癌患者进行早期诊断,还为个体化治疗提供了新的治疗靶点和思路,并能有效监测患者的治疗效果。常见的ctDNA检测技术主要基于两大平台,一种是以聚合酶链式反应(polymerase chain reaction,PCR)为基础扩增,另一种以二代测序(next generation sequencing,NGS)为基础检测14。
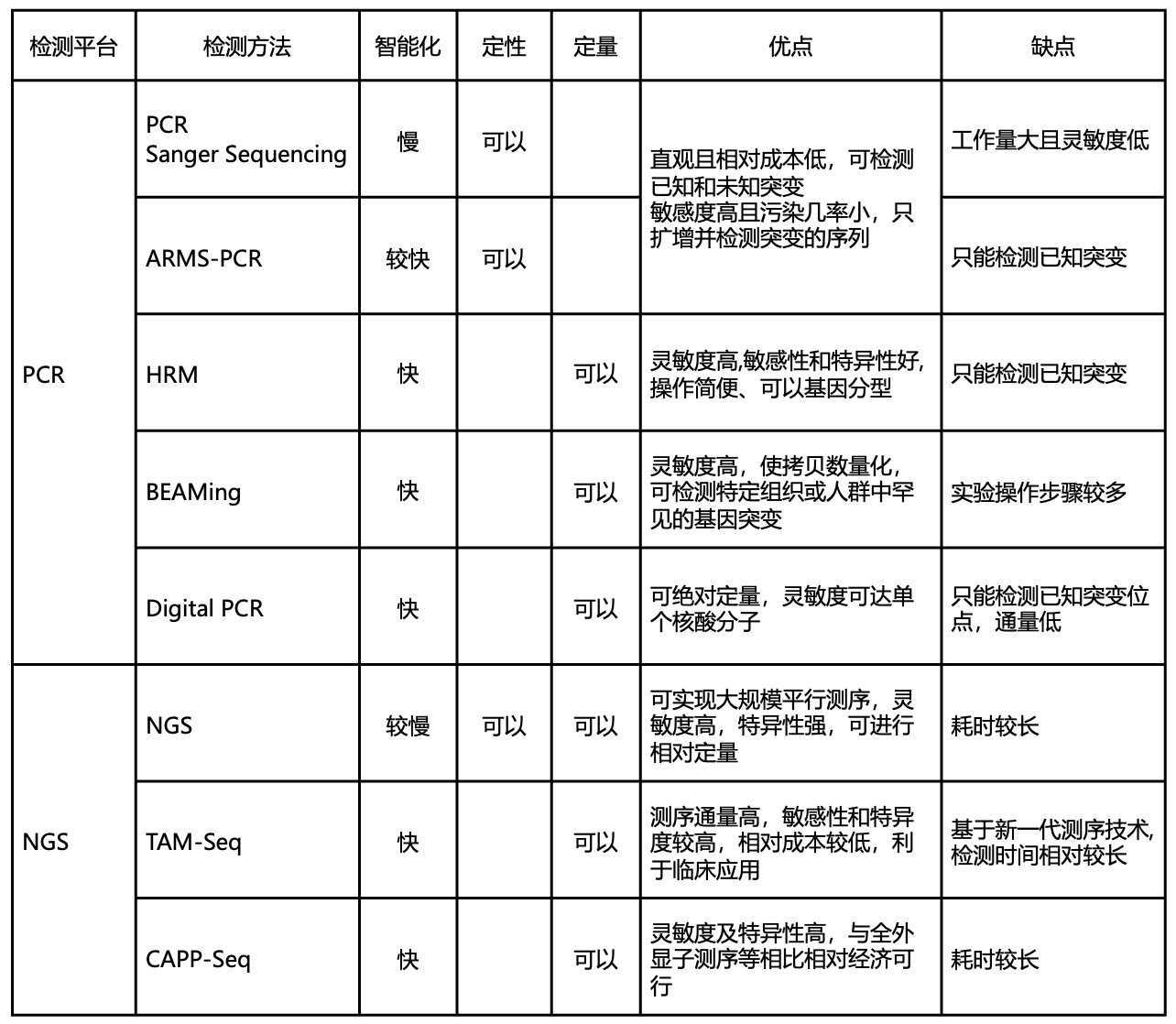
常见ctDNA检测方技术方法优劣13-15
4. KRAS突变检测引领结直肠癌靶向治疗新纪元
在早期结直肠癌(I 期和 II 期)中,治疗主要以手术为主,KRAS 突变的检测并不是常规的,而在晚期或转移性结直肠癌中,KRAS 突变检测尤为重要。KRAS突变状态是决定是否使用EGFR抑制剂(如西妥昔单抗和帕尼单抗)的关键因素。一项大型的荟萃分析显示16,KRAS突变与较差的无病生存[DFS,合并风险比(HR)=1.36,95%置信区间(CI):1.15~1.61,P<0.001]和总生存(OS,HR=1.27,95% CI:1.03~1.55,P=0.03)相关。这一研究强调了对 KRAS 突变进行基因分型的必要性,特别是在辅助治疗中使用新型抗 KRAS 药物或免疫治疗的潜力。
KRAS突变检测的进步推动了结直肠癌靶向治疗进入全新纪元。通过精准识别KRAS突变类型,尤其是KRAS G12C突变,临床医生可以根据患者的基因特征量身定制治疗方案。KRAS抑制剂如Adagrasib和Sotorasib的研发上市,联合EGFR抑制剂、MEK抑制剂、SOS1 抑制剂、SHP2抑制剂等药物,不仅提升了靶向治疗的有效性,还显著改善了患者的无进展生存期和总体生存率。KRAS突变检测对晚期及转移性结直肠癌靶向治疗的重要性显而易见,临床实践中应大力推广KRAS突变检测,从而实现精准分类、个性治疗,为更多结直肠癌患者带去福音。
1.Bteich F, Mohammadi M, Li T, et al. Targeting KRAS in Colorectal Cancer: A Bench to Bedside Review. Int J Mol Sci. 2023;24(15):12030.
2.Zhang M, Hu W, Hu K, et al. Association of KRAS mutation with tumor deposit status and overall survival of colorectal cancer. Cancer Causes Control. 2020;31(7):683-689..
3.Strickler JH, Yoshino T, Stevinson K, et al. Prevalence of KRAS G12C Mutation and Co-mutations and Associated Clinical Outcomes in Patients With Colorectal Cancer: A Systematic Literature Review. Oncologist. 2023;28(11):e981-e994.
4.Rowland A, Dias MM, Wiese MD, et al. Meta-analysis comparing the efficacy of anti-EGFR monoclonal antibody therapy between KRAS G13D and other KRAS mutant metastatic colorectal cancer tumours. Eur J Cancer. 2016;55:122-130.
5.Blair HA. Sotorasib: First Approval. Drugs. 2021;81(13):1573-1579.
6.Dhillon S. Adagrasib: First Approval. Drugs. 2023;83(3):275-285.
7.Amodio V, Yaeger R, Arcella P, et al. EGFR Blockade Reverts Resistance to KRASG12C Inhibition in Colorectal Cancer. Cancer Discov. 2020;10(8):1129-1139.
8.Ciardiello D, Maiorano BA, Martinelli E. Targeting KRASG12C in colorectal cancer: the beginning of a new era. ESMO Open. 2023;8(1):100745.
9.Ryan MB, Fece de la Cruz F, Phat S, et al. Vertical Pathway Inhibition Overcomes Adaptive Feedback Resistance to KRASG12C Inhibition. Clin Cancer Res. 2020;26(7):1633-1643.
10.Peng SB, Si C, Zhang Y, et al. Preclinical characterization of LY3537982, a novel, highly selective and potent KRAS-G12C inhibitor. Cancer Research. 2021 Jul 1;81(13_Supplement):1259.
11.Desai J, Han SW, Lee JS, et al. Abstract CT029: Phase Ib study of GDC-6036 in combination with cetuximab in patients with colorectal cancer (CRC) with KRAS G12C mutation. Cancer Research. 2023 Apr 14;83(8_Supplement):CT029.
12.Hallin J, Bowcut V, Calinisan A, et al. Anti-tumor efficacy of a potent and selective non-covalent KRASG12D inhibitor. Nat Med. 2022;28(10):2171-2182.
13.Malapelle U,Carlomagno C, de Luca C,et al. KRAS testing inchallenges ,metastatic colorectalcontroversiescarcinoma :breakthroughs and beyond[ J]. J Clin Pathol, 2014,67( 1):1 -9.
14.王蕾.循环肿瘤DNA在结直肠癌临床诊疗中的应用及价值[J].中国肿瘤生物治疗杂志, 2017, 024(008):918-922.
15.毛旭华等. 高分辨率熔解曲线技术检测结直肠癌患者KRAS基因突变[J]. 中国肿瘤外科杂志 , 2017年5期
16.Formica V, Sera F, Cremolini C, et al. KRAS and BRAF Mutations in Stage II and III Colon Cancer: A Systematic Review and Meta-Analysis. J Natl Cancer Inst. 2022;114(4):517-527.
排版编辑:斑斑











 苏公网安备32059002004080号
苏公网安备32059002004080号


