结直肠癌(CRC)是全球最常见的恶性癌症之一。根据最新版中国癌症统计报告数据显示,中国CRC的发病率、死亡率在全部恶性肿瘤中分别位居第2和第4位,其中2022年新发病例51.7万,死亡病例24万。大多数患者确诊时已发生转移,导致预后不佳。近年来,免疫疗法的深入研究为dMMR/MSI-H晚期CRC患者带来了显著生存获益和预后改善。目前,多项免疫联合治疗的研究正在进行中,旨在进一步实现疗效升级并改善占比95%的pMMR/MSS型mCRC患者的预后,这些研究为临床实践提供了重要的循证医学支持。
《Hi Strong-消化道病例精粹》系列专栏深入剖析消化道肿瘤免疫治疗优秀临床病例,分享宝贵临床经验,以期共同推动消化道肿瘤免疫治疗学科发展,助力健康中国2030。
本期特邀来自汕头大学医学院第一附属医院医院的李欣欣教授团队分享一例IV期升结肠腺癌伴肝转移病例。患者,男,55岁,纳差、消瘦1年余,确诊为升结肠腺癌伴肝转移(cT4N0M1,IV期)。经过一线化疗联合靶向治疗后,患者肝转移灶出现进展,后改为二线化疗方案,再次出现进展。最终调整为XELOX+贝伐珠单抗+斯鲁利单抗方案治疗5程后,复查全腹部CT提示原发灶及肝转移瘤均较前缩小,治疗疗效评估PR,继续该方案治疗中。
广东省健康管理学会胃肠病学专业会委员
广东省医师协会结直肠外科医师分会第一届委员会器官功能保护专业组委员
广东省医学会加速康复外科学分会青年委员会委员
广东省基层医药学会胃肠疾病专业委员会常务委员
病史简介
基本情况
患者,男,55岁。
主诉
纳差、消瘦1年余。
现病史
患者于1年余前进行牙齿根管治疗后出现纳差,伴厌油腻感,伴消瘦,无腹部不适、四肢乏力、恶心呕吐、无反酸烧心,无腹胀腹泻,无发热头晕等。患者为进一步检查及治疗前来汕头大学医学院第一附属医院消化内科就诊,拟以“消瘦”收住入院。患者目前精神尚可,体力正常,食欲差,睡眠正常,近1年余体重下降约5kg,大便正常,排尿正常。
既往疾病史
患者自诉1年前发现血糖升高,自行服用“降血糖中药”后血糖恢复正常。否认高血压等其他疾病史。
一般情况
BMI:21.9kg/m2,ECOG评分:0分;NRS2000营养评分:4分。
辅助检查
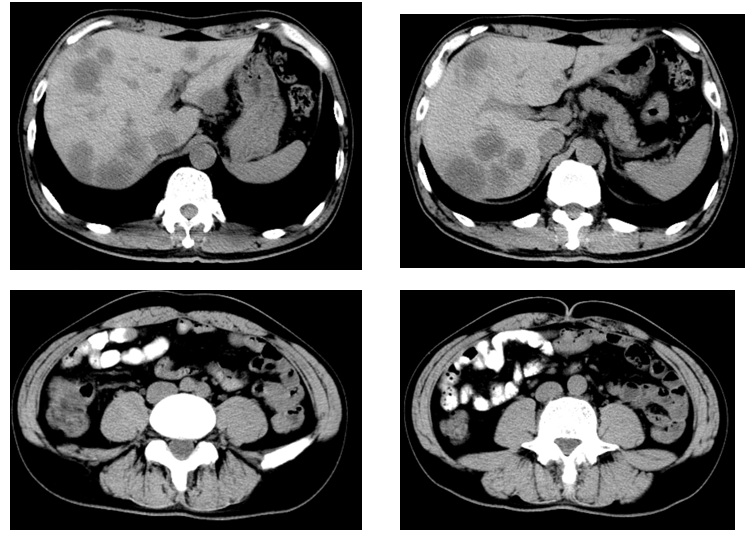
胸腹部CT(2023-08-09):双肺支气管血管束清晰,走行如常,左肺上叶下舌段见条索、索片状密度增高影,邻近胸膜稍肥厚,右肺上叶尖段(4-125)见片结影,大小约9mm×7mm,右肺上叶后段、下叶前基底段及左肺舌段少许斑点状高/稍高密度影,气管及主要支气管通畅。心脏形态及大小未见明显异常。主动脉弓壁见少许弧形高密影。纵隔内未见明显肿大淋巴结影。未见明显胸水征象。扫描野骨质未见明显破坏。肝脏形态、大小、各叶比例未见明确异常。肝内见多发大小不等类圆形稍低密度结节、肿块,较大约35mm×31mm,边缘稍模糊。肝内、外胆管未见明显扩张。胆囊形态、大小未见明确异常,胆囊壁未见明显增厚,腔内未见异常密度影。胰腺形态大小、密度未见异常,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏形态、大小、密度未见明确异常。双肾及双肾上腺形态、大小、密度未见明显异常,双侧肾盂、肾盏及输尿管未见明显扩张积水。膀胱形态、大小未见明显异常,腔内未见明确异常密度影,膀胱壁未见明显增厚。前列腺形态、大小未见异常,内见多发小斑点状高密度影。双侧精囊腺形态、大小、密度未见明确异常。胃腔充盈不佳、壁显示厚,盲肠肠壁增厚似呈软组织肿块凸向腔内,邻近可疑小淋巴结,大小约7mm×8mm,腹部肠管未见扩张积液。腹膜后未见明显增大淋巴结。未见腹水征。L5双侧椎弓峡部不连续(图1)。
影像学意见:1.盲肠肠壁增厚、可疑软组织肿块,胃腔未充盈、壁显示厚,建议增强、内镜检查。2.肝内多发结节、肿块,拟转移瘤或其它,建议增强进一步检查。3.前列腺钙化。4.左肺上叶下舌段少许慢性炎症;右肺上叶后段、下叶前基底段及左肺舌段少许纤维增殖钙化灶。5.右肺上叶尖段片结影,性质待定,建议随诊复查。6.主动脉弓钙化斑。7.L5双侧椎弓峡部裂。
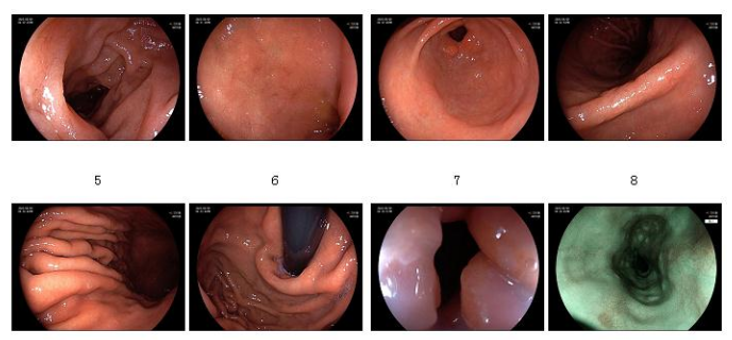
内镜(2023-08-09):食道粘膜光滑,无异常肿胀或病变;贲门E-G连接光滑,胃底、胃体及胃窦粘膜充血水肿,局部可见粘膜糜烂,未见明显肿块;幽门开放良好,表面光滑。十二指肠球部及降段粘膜充血、糜烂。整体检查提示胃部及十二指肠存在糜烂性病变,可能与炎症性改变相关(图2)。内镜诊断:1.幽门隆起:胃窦粘膜脱垂?;2.慢性萎缩性胃炎(C2,待病理);3.HP(+)。
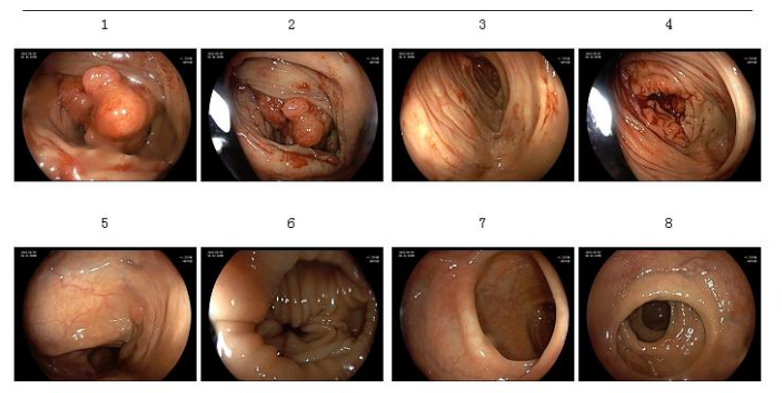
内镜(2023-08-09):肠道清洁度评分为Boston标准9分,回盲部、升结肠、横结肠、降结肠及乙状结肠的粘膜表面光滑,血管纹理清晰,未见异常病变。结肠整体结构正常,肠腔未见狭窄、肿块或异常隆起,黏膜表面无糜烂、溃疡或活动性出血。直肠齿状线距肛门约45 cm处见一扁平隆起样病变,直径约6 mm,表面充血轻微,质地较柔软,未见溃疡或明显异常(图3)。内镜诊断:1.升结肠Ca?(待病理);2.结肠息肉。
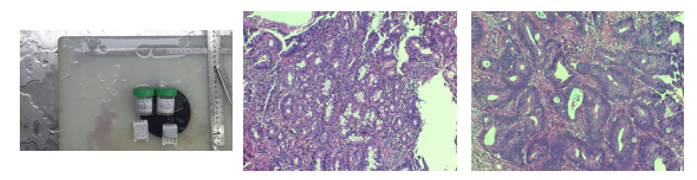
内镜病理(2023-08-09):(胃窦)灰白组织2粒,直径0.2-0.5 cm;(升结肠)灰白组织3粒,直径0.3-0.5 cm。镜下所见:胃窦部粘膜表面上皮部分脱落,粘膜结构变薄,局部层膜体稀疏减少,部分区域可见细胞核拥挤、核大、深染,排列紊乱,呈现杯状细胞,个别腺体可见腺体变形及黏膜层内淋巴细胞浸润,固有层局部较多慢性炎症细胞浸润。升结肠粘膜结构完整,管状腺体增生,部分融合呈绒毛状,膜体细胞层次增多,核深染,排列紊乱,核分裂象易见,固有层内局部较多慢性炎症细胞浸润(图4)。常规石蜡病理诊断:1.(胃窦)慢性萎缩性胃炎伴急性活动、局部黏膜肠上皮化生及幽门螺旋杆菌感染;2.(升结肠)绒毛管状腺瘤局部恶变-腺癌。
基因检测(2023-08-15):共检测到13个体细胞突变,其中具有明确临床意义的突变共8个,包括:KRAS基因p.G12V突变,APC基因p.S932突变,APC基因p.F1491Gfs10突变,FBXW7基因p.R689Q突变,PIK3CA基因p.E545K突变,PIK3CA基因p.E545G突变,PIK3CA基因p.H1047Y突变,以及PIK3CA基因p.H1047R突变。肿瘤突变负荷(TMB)为7.98突变/Mb,微卫星稳定性(MSI)检测结果显示为微卫星稳定型(MSS)(图5)。

临床分期及诊断
临床分期及诊断:
1.升结肠癌并肝脏多发转移(cT3N+M1,IV期,MSS,KRAS突变)
2.直肠息肉
3.慢性萎缩性胃炎
4.右肺结节
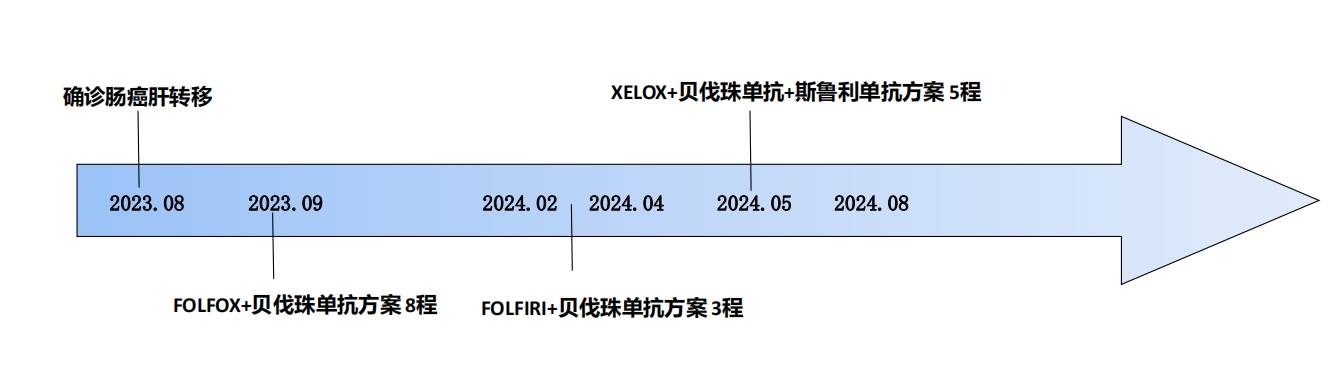
诊疗经过(图6)

第一次复查评估:PR
疗效评价CT(2023-10-29):双肺支气管血管束清晰,走行如常,左肺上叶下舌段见条索、索片状密度增高影,邻近胸膜稍肥厚,大致同前;右肺上叶尖段(3-132)见片结影,大小约9mm×7mm,大致同前;右肺上叶后段、下叶前基底段及左肺舌段少许斑点状高/稍高密度影,大致同前。气管及主要支气管通畅。心脏形态及大小未见明显异常。主动脉弓壁见少许弧形高密影。纵隔内未见明显肿大淋巴结影。未见明显胸水征象。扫描野骨质未见明显破坏。扫描野右侧深静脉置管,管端位于上腔静脉内。
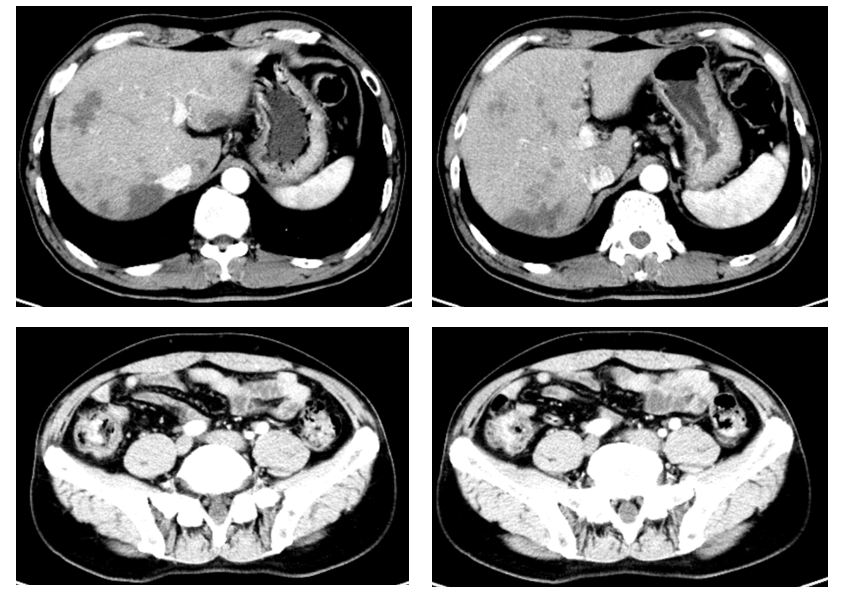
肝脏形态、大小、各叶比例未见明确异常。肝内见多发大小不等类圆形稍低密度结节、肿块,较前缩小、减少,现较大约25mm×19mm,边缘稍模糊,增强扫描边缘似见可疑,部分结节可疑见“牛眼征”。肝内、外胆管未见明显扩张。胆囊形态、大小未见明确异常,胆囊壁未见明显增厚,腔内见密度分层。胰腺形态大小、密度未见异常,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏形态、大小、密度未见明确异常。双肾及双肾上腺形态、大小、密度未见明显异常,双侧肾盂、肾盏及输尿管未见明显扩张积水。膀胱形态、大小未见明显异常,腔内未见明确异常密度影,膀胱壁未见明显增厚。前列腺形态、大小未见异常,内见多发小斑点状高密度影,同前。双侧精囊腺形态、大小、密度未见明确异常。胃腔充盈不佳、局部胃壁显示厚,增强扫描尚均匀;盲肠肠壁增厚呈软组织肿块凸向腔内,较前缩小,增强扫描呈轻中度强化,邻近小淋巴结,大小约7mm×8mm,大致同前,增强扫描稍欠均匀腹部肠管未见扩张积液。腹膜后未见明显增大淋巴结。未见腹水征。L5双侧椎弓峡部不连续。右侧第11后肋片结状稍高密度影(图7)。
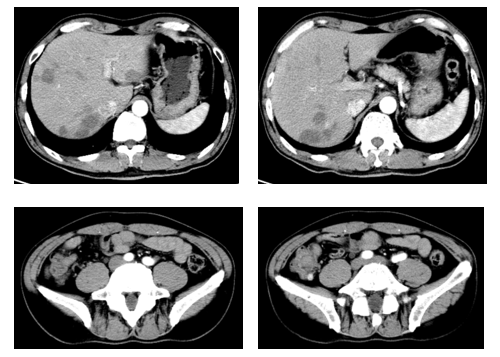
疗效评价MRI(2023-10-30):肝内见多发大小不等异常信号结节,较大者约28mm×17mm,T1WI呈低信号,T2WI呈高信号,DWI呈稍高信号,ADC图呈稍高、高信号,增强扫描以边缘延迟强化为主,呈牛眼征;肝S4见小圆形水样信号影,直径约5mm,增强扫描未见明显强化;肝内、外胆管未见明显扩张。肝门区见1个稍大淋巴结,大小约12mm×11mm, 增强扫描呈均匀中度强化。门静脉主干及左、右支及下腔静脉、肝静脉未见明确异常。胆囊不大,壁不厚,腔内未见明显异常信号影。胰腺形态、大小及信号未见明显异常,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏形态、大小、信号未见明确异常。双肾上腺及双肾形态、大小及信号未见明确异常,双侧肾盂、肾盏未见明显扩张积水。未见腹水征。扫描野左肺上叶下舌段见片结状异常信号影,增强扫描可见强化(图8)。
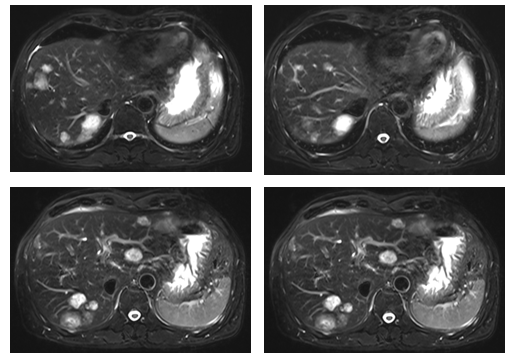
第二次复查评估:原发灶SD;转移灶PD
疗效评价胸腹部CT(2024-01-25):(对比2023-10-29旧片)双肺支气管血管束清晰,左肺上叶下舌段见条索、索片状密度增高影,邻近胸膜稍肥厚,大致同前;右肺上叶尖段(4-69)见片结影,大致同前,大小约9mm×7mm;右肺上叶后段、下叶基底段及左肺上舌段少许斑点状高/稍高密度影,大致同前。主动脉弓壁见少许弧形高密影。纵隔内未见明显肿大淋巴结影。右侧叶间裂稍增厚,余未见明显胸水征象。扫描野右侧输液港,管端位于上腔静脉内。
肝脏形态、大小、各叶比例未见明确异常。肝内见多发大小不等类圆形稍低密度结节、肿块,较前稍增多,部分病灶增大/融合,现较大约32mm×26mm(6-140),边缘稍模糊,增强扫描边缘似见强化,部分结节可疑见“牛眼征”。肝内、外胆管未见明显扩张。胆囊形态、大小未见明确异常,胆囊壁未见明显增厚,腔内未见明显异常密度灶。胰腺形态大小、密度未见异常,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏形态、大小、密度未见明确异常。双肾及双肾上腺形态、大小、密度未见明显异常,双侧肾盂、肾盏及输尿管未见明显扩张积水。膀胱充盈一般、壁稍增厚。前列腺形态、大小未见异常,内见多发小斑点状高密度影,同前。双侧精囊腺形态、大小、密度未见明确异常。
胃腔充盈差、胃壁显示厚,增强扫描尚均匀;盲肠肠壁不均匀增厚呈软组织肿块凸向腔内,较前相仿,增强扫描呈轻中度强化,周围可见少许小淋巴结,大者大小约8mm×7mm,大致同前,增强扫描稍欠均匀。腹部肠管未见扩张积液。腹膜后未见明显增大淋巴结。未见腹水征。
L5双侧椎弓峡部不连续。右侧第11后肋片结状稍高密度影(图9)。
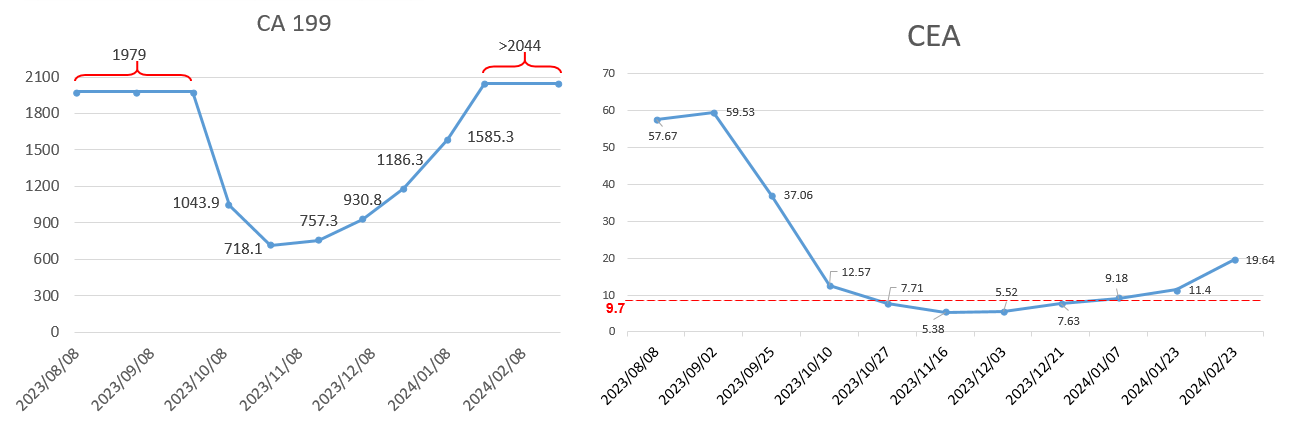
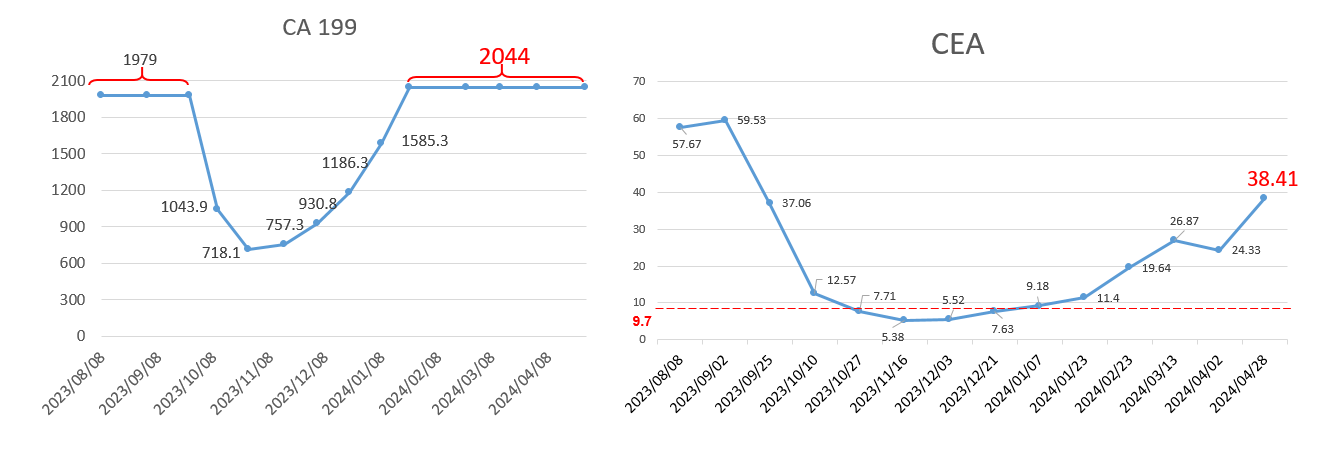
肿瘤标记物(CEA、CA199):化疗联合靶向治疗后逐渐下降,之后肿瘤出现耐药,肝转移瘤出现进展,再次上升(图10)。
后续治疗方案
考虑肿瘤进展,改为二线化疗方案。

第三次复查评估:原发灶SD;转移灶PD。
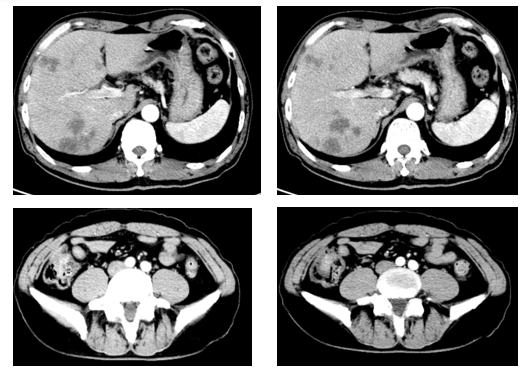
疗效评价胸腹部CT(2024-01-25):(对比2024-01-25旧片)双肺支气管血管束清晰,左肺上叶下舌段见条索、索片状密度增高影,邻近胸膜稍肥厚,大致同前;右肺上叶尖段(4-79)见片结影,大致同前,大小约9mm×7mm;右肺上叶后段、下叶基底段及左肺上舌段少许斑点状高/稍高密度影,大致同前。主动脉弓壁见少许弧形高密影。纵隔内未见明显肿大淋巴结影。右侧叶间裂稍增厚,余未见明显胸水征象。扫描野右侧输液港,管端位于上腔静脉内。
肝脏形态、大小、各叶比例未见明确异常。肝内见多发大小不等类圆形稍低密度结节、肿块,部分较前稍增大,边缘稍模糊,增强扫描边缘似见强化,部分结节可疑见“牛眼征”。肝内、外胆管未见明显扩张。胆囊形态、大小未见明确异常,胆囊壁未见明显增厚,腔内未见明显异常密度灶。胰腺形态大小、密度未见异常,胰周脂肪间隙清晰,胰管未见明显扩张。脾脏形态、大小、密度未见明确异常。双肾及双肾上腺形态、大小、密度未见明显异常,双侧肾盂、肾盏及输尿管未见明显扩张积水。膀胱充盈一般、壁稍增厚。前列腺形态、大小未见异常,内见多发小斑点状高密度影,同前。双侧精囊腺形态、大小、密度未见明确异常。
胃腔充盈差、胃壁显示厚,增强扫描尚均匀;盲肠肠壁不均匀增厚呈软组织肿块凸向腔内,较前相仿,增强扫描呈轻中度强化,周围可见少许小淋巴结,大者大小约8mm×7mm,大致同前,增强扫描稍欠均匀。腹部肠管未见扩张积液。腹膜后未见明显增大淋巴结。未见腹水征。
L5双侧椎弓峡部不连续。右侧第11后肋片结状稍高密度影(图11)。
肿瘤标记物(CEA、CA199):继续上升(图12)。
后续治疗方案
改为XELOX+贝伐珠单抗+斯鲁利单抗。

肿瘤标记物(CEA、CA199):二线方案进展后,改为XELOX+贝伐珠单抗+斯鲁利单抗治疗5程,复查肿瘤标记物逐渐下降(图13)。
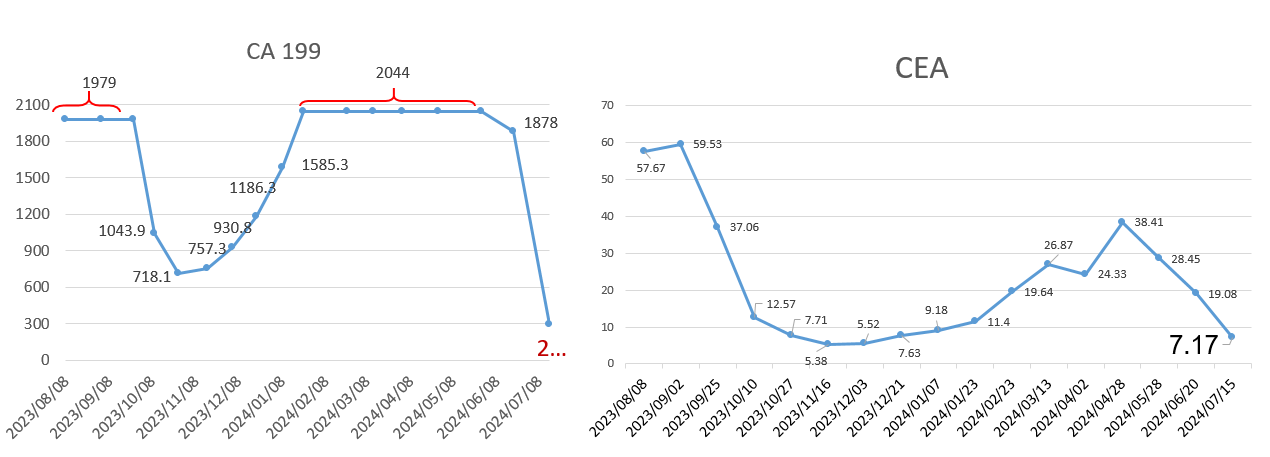
第四次复查评估:原发灶/转移灶PR。
疗效评价胸腹部CT(2024-08-10):(对比2024-04-02日旧片)盲肠肠壁不均匀增厚呈软组织肿块凸向腔内,范围/大小较前略缩小,增强后轻中度强化,程度较前减轻,周围可见少许小淋巴结,大者大小约8mm×7mm,大致同前,增强扫描均匀。腹部肠管未见扩张积液。腹腔后未见明显增大淋巴结。未见腹水征。胃窦、十二指肠球部仍存在充盈欠佳,管壁不规则厚,局部不规则软组织影,增强扫描不均匀,幽门痉挛。
肝脏形态、大小、各叶比例未见明确异常。肝内见多发大小不等类圆形稍低密度结节、肿块,较前不同程度缩小,增强扫描“牛眼”状强化,最大者大小约33mm×22mm(S7段)。肝内、外胆管未见明显扩张。胆囊现呈收缩状态,胆囊壁增厚,粘膜皱褶均匀,腔内未见明显异常密度灶。脾脏形态大小、密度未见异常,脾周脂肪间隙清晰,脾脏未见明显扩张。胰腺形态、大小、密度未见明确异常。双肾及双侧上腺形态、大小、密度及回声均正常,双侧肾盂、输尿管未见明显扩张积水。膀胱充盈一般,壁稍增厚。前列腺形态、大小未见异常,内见多发小斑点状高密度影,前向。
双肺支气管血管束清晰,左肺上叶舌段见条索状小结密度增高影,邻近腔膜稍厚,未见明显胸水征象。右肺中上叶尖段(4-81)见片结影,较前缩小,大小约9mm×7mm。右肺上叶后段、下叶基底段及右肺上后段少许斑点状高/稍高密度影,较前缩小。主动脉弓壁见少许斑点高密影。纵隔内未见明显增大淋巴结影。右侧肋间隙稍增厚,余未见明显胸水征象。扫描野右侧输液港,管端位于上腔静脉内(图14)。
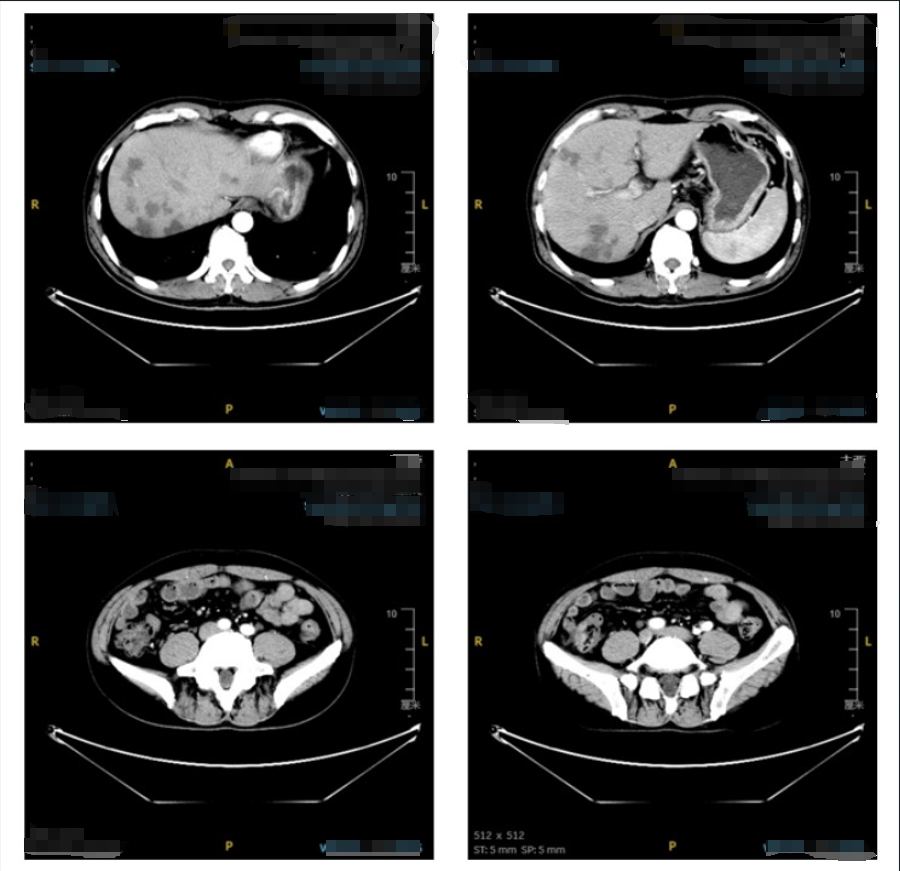
目前情况:患者改为XELOX+贝伐珠单抗+斯鲁利单抗方案5程,肿瘤标记物逐渐下降,复查全腹部CT提示原发灶及肝转移瘤均较前缩小,治疗疗效评估PR,继续该方案治疗。
诊疗流程图见图15。
专家点评
外科学博士,硕士研究生导师,博士后合作导师
广东省临床医学学会结直肠外科学专业委员会副主任委员
广东省医学会加速康复外科学分会常委
广东省医师协会结直肠外科分会常委,胃肠外科分会委员
广东省抗癌协会遗传性肿瘤专委会常委
汕头市抗癌协会肿瘤MDT专业委员会副主任委员
汕头市医学会结直肠肛门外科学专业委员会副主任委员
李欣欣教授:大部分结直肠癌(CRC)患者在确诊时已出现转移,其中微卫星稳定型(MSS型)患者占绝大多数,而微卫星高度不稳定型(MSI-H)患者仅占约5%。MSS型CRC通常表现为“免疫豁免型”或“免疫荒漠型”,患者体内缺乏效应T细胞,对免疫治疗不敏感,免疫检查点抑制剂(ICI)难以发挥显著作用。目前,全球尚无针对pMMR/MSS型转移性结直肠癌(mCRC)的一线免疫疗法获批。
ASTRUM-015研究采用双盲设计,有效减少了主观偏倚的干扰,更客观地评估了治疗方案的疗效和安全性。这项研究探索了斯鲁利单抗(PD-1抑制剂)联合贝伐珠单抗及XELOX方案(奥沙利铂+卡培他滨)的疗效。该联合方案既符合临床实际需求,又达到了令人振奋的临床预期结果[1]。研究成果于2024年6月发表在Cell子刊MED杂志,结果显示出色的疗效。与未联合斯鲁利单抗的对照组相比,联合方案显著延长了无进展生存期(PFS),具体表现为总体患者PFS达17.2个月 vs 10.7个月(HR = 0.60),而对于MSS型mCRC患者,PFS获益更为明显(17.2个月 vs 10.1个月,HR = 0.58)。这一结果为斯鲁利单抗联合方案在临床中的应用提供了强有力的支持,有望为MSS型mCRC患者带来更多治疗获益。当然,仍需更长时间的随访以进一步观察长期结局。
该病例为一位MSS型升结肠腺癌伴肝转移患者在三线治疗中接受斯鲁利单抗联合贝伐珠单抗及化疗(奥沙利铂+卡培他滨)方案后,肿瘤标志物水平逐渐下降,复查显示原发病灶及肝转移瘤明显缩小,疗效评估为部分缓解(PR)。该患者目前仍在持续治疗中,并持续获益。这一病例不仅验证了ASTRUM-015研究的结果,也进一步彰显了斯鲁利单抗联合治疗方案在MSS型mCRC中的有效性,为这一类难治患者群体带来了新的希望。
1. Wang ZX, et. al. First-line serplulimab in metastatic colorectal cancer: Phase 2 results of a randomized, double-blind, phase 2/3 trial. Med. 2024 Sep 13;5(9):1150-1163.e3.
责任编辑:肿瘤资讯-SFS
排版编辑:肿瘤资讯-Delia











 苏公网安备32059002004080号
苏公网安备32059002004080号


