
抗体偶联药物(ADC)是近年来新兴起的明星药物,是继靶向和免疫治疗之后的新型创新药物,开启了实体瘤治疗的新格局。针对HER2靶点的新型ADC引领变革,已在乳腺癌、胃癌、肺癌治疗领域取得了多项适应症。基于DESTINY-Lung02和DESTINY-Lung05研究结果,新型HER2 ADC德曲妥珠单抗于10月9日获得NMPA批准上市,适用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。
【肿瘤资讯-HER2大师课】特邀湖南省第二人民医院杨农教授解析ADC药物创新结构及相关研究进展。
主任医师 博导
海南热带肿瘤研究所、海南省肿瘤医院、海南成美医院 长聘专家
第六届 国之名医·优秀风范
2017-2023七届全国“年度好大夫”
国家科技重大专项首席专家
国家肿瘤质控中心肺癌质控专委会委员
中国医药教育协会肿瘤免疫治疗专委会副主任委员
中国医药教育协会肿瘤临床科研创新发展专委会副主任委员
中国抗癌协会抗肿瘤药物专委会常委、肺癌专委会常委
中国临床肿瘤学会理事及肿瘤免疫治疗、非小细胞肺癌、药物研发专委会委员
中国医师协会肿瘤学分会委员
湖南省抗癌协会肿瘤精准医学专委会主任委员
湖南省老年医学学会临床肿瘤学分会主任委员
肺癌精准诊疗湖南省重点实验室主任
湖南省呼吸肿瘤临床医学研究中心主任
德曲妥珠单抗独特创新结构及抗肿瘤机制
德曲妥珠单抗是采用创新DXd-ADC平台设计的新型ADC,由可裂解的四肽连接子将人源化HER2 IgG1单克隆抗体曲妥珠单抗与强效细胞毒药物拓扑异构酶1抑制剂DXd偶联。德曲妥珠单抗具有HER2靶标抗体,可与肿瘤细胞表面特异性表达HER2抗原结合,精准识别特定肿瘤细胞。德曲妥珠单抗已先后获得FDA和NMPA批准,用于经治HER2突变晚期NSCLC的后线治疗,成为了全球和中国首个针对HER2突变NSCLC的ADC药物。
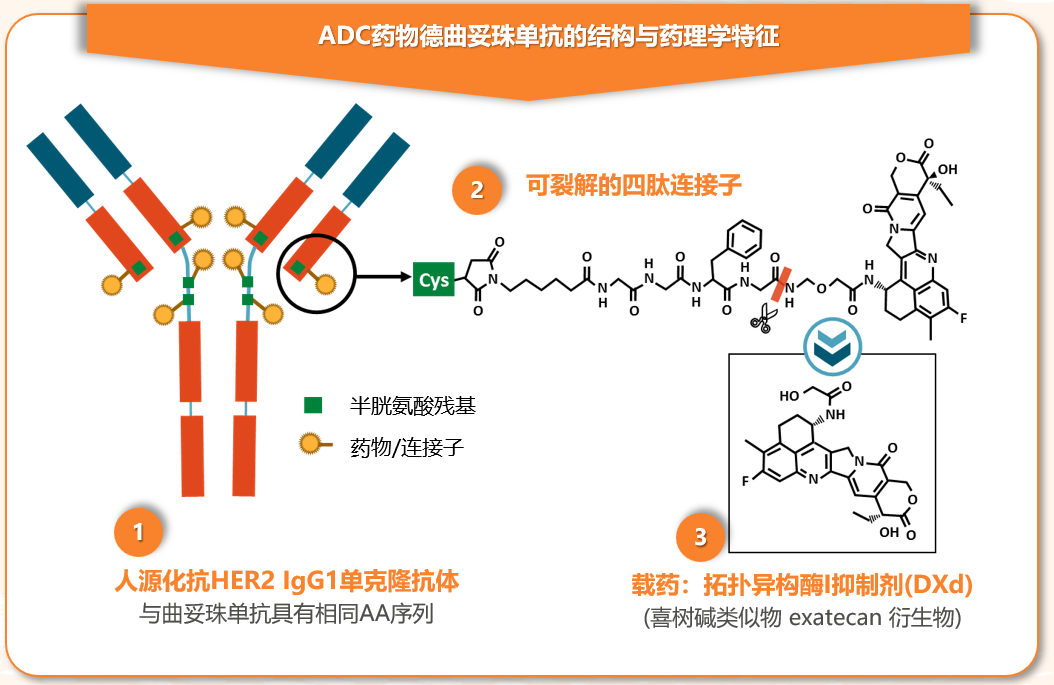 图1 德曲妥珠单抗结构示意图
图1 德曲妥珠单抗结构示意图
HER2靶点:
德曲妥珠单抗治疗HER2突变实体瘤的疗效显著,已在胃癌和乳腺癌相关研究中得到验证。DESTINY-Gastric01研究显示[1],与化疗相比,德曲妥珠单抗用于HER2突变晚期胃癌三线治疗时,中位无进展生存期(PFS)达到5.6个月(HR=0.47),疾病进展及死亡风险下降53%。DESTINY-Breast03研究显示[2],德曲妥珠单抗用于HER2突变乳腺癌二线治疗时,中位PFS能达到28.8个月。研究数据可见,相比传统方案,新一代ADC药物德曲妥珠单抗在降低HER2突变肿瘤的疾病进展风险方面具有优势。
载药DXd:
DXd是新一代拓扑异构酶I抑制剂,与NSCLC中常用化疗药物,如烷化剂、抗肿瘤抗生素、微管蛋白抑制剂、蒽环类药物、抗嘧啶类药物、抗叶酸类等的作用机制不同。因此,DXd用于NSCLC治疗时能一定程度上避免耐药;而且DXd的IC50值为0.31mmol/L,抗肿瘤活性是常用化疗药的100-1000倍[3,4],具有更强效的抑瘤作用。
 图2 常用化疗药物作用机制与IC50值
图2 常用化疗药物作用机制与IC50值
药物抗体比(DAR)为8,半胱氨酸连接产生的ADC更均一:
德曲妥珠单抗的药物抗体比可达到8,即单个抗体携带8个细胞毒药物,利于药物发挥强效抗肿瘤作用。德曲妥珠单抗异质性低,原因在于它采用了半胱氨酸连接的DAR,产生的药物复杂程度低,因而异质性低。既往ADC药物多采用赖氨酸连接的DAR,偶联的载药个数和偶联位置都具有随机性,得到的ADC为异质性混合物,代表药物有恩美曲妥珠单抗(DAR为3.5);而采用半胱氨酸连接的DAR更均一,偶联的载药数量是2的倍数,相对来说异质性会更低,新型ADC药物德曲妥珠单抗是经典代表药物。
连接子:
ADC药物德曲妥珠单抗在与肿瘤细胞结合之前需要在血浆中高度稳定,以避免脱靶引起对正常组织的毒性。此时连接子的特性尤为关键,德曲妥珠单抗采用特异性的四肽连接子,在血液中高度稳定,脱落率极低;在人类血浆中高度稳定,21天仅裂解释放约2%[3,4]。
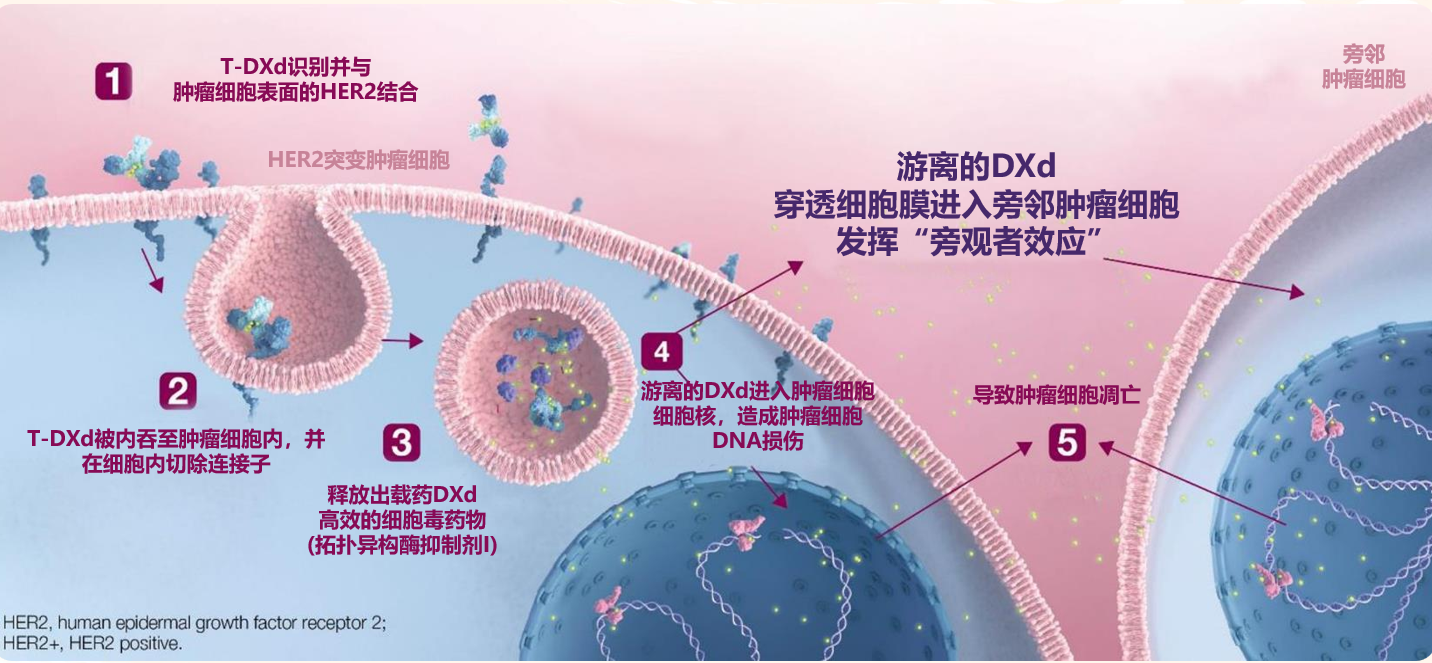 图3 德曲妥珠单抗作用机制图
图3 德曲妥珠单抗作用机制图
总体而言,德曲妥珠单抗一旦进入肿瘤细胞后,能够迅速被蛋白酶裂解并释放出载药,特异性杀伤HER2突变肿瘤细胞。与此同时,游离DXd可穿透细胞膜进入邻近肿瘤细胞,发挥强效旁观者效应。因此,德曲妥珠单抗对旁邻异质性肿瘤细胞亦有较强杀伤作用。从整体药物和游离DXd的动力学特征来看,完整德曲妥珠单抗主要存在于血液中,没有特别的组织滞留;游离DXd全身暴露量较低,DXd在静脉给药后被迅速清除,半衰期仅1.37小时[5]。二者的动力学特征为系统用药安全性提供了基础保障。总而言之,德曲妥珠单抗具有独特的药物结构:高活性载药、高药物抗体比、高效旁观者效应,可保证精准、强效的杀伤肿瘤细胞。
德曲妥珠单抗是全球首个治疗
HER2突变NSCLC的ADC药物
德曲妥珠单抗既往已在DESTINY-Lung系列研究中多次展现出优异疗效。DESTINY-Lung01是一项开放标签、多中心、双队列、II期临床试验,旨在探索5.4和6.4mg/kg德曲妥珠单抗用于HER2过表达NSCLC,以及6.4mg/kg德曲妥珠单抗用于HER2突变NSCLC的疗效和安全性。初步分析结果可见[6],德曲妥珠单抗在HER2突变晚期NSCLC中疗效优异,客观缓解率(ORR)为55%,中位至缓解时间(TTIR)时间短,仅1.5个月。中枢神经系统(CNS)转移不影响ORR结果,基线有和无CNS转移患者的ORR分别为54.5%和55.2%,即使作为大分子药物,德曲妥珠单抗仍在CNS转移患者中显示优异疗效。
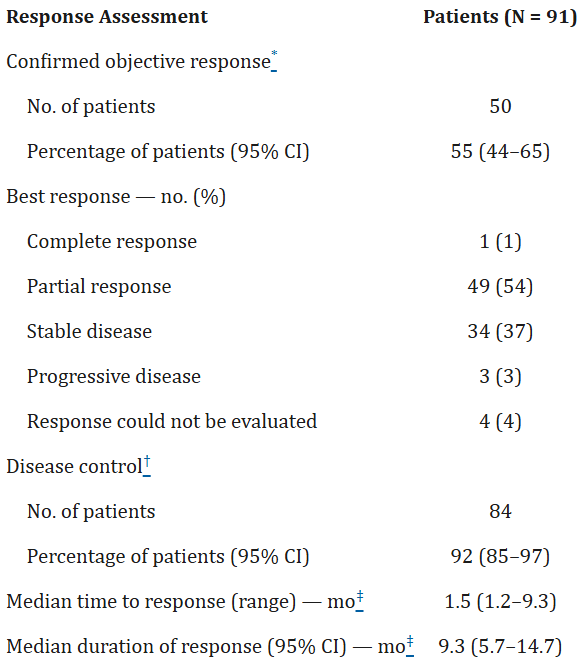
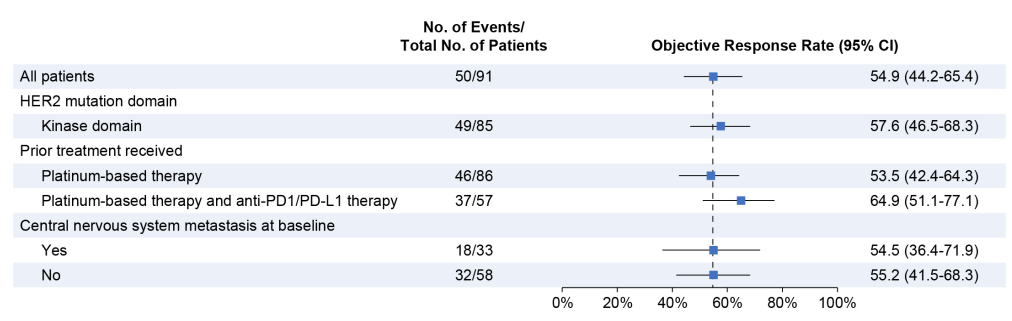 图4 DESTINY-Lung01队列2(HER2突变)初步分析结果
图4 DESTINY-Lung01队列2(HER2突变)初步分析结果
DESTINY-Lung02研究最终分析:
DESTINY-Lung02是一项多中心、随机双盲、剂量优化、非对照研究,旨在评估两种剂量德曲妥珠单抗用于经治HER2突变不可切除或转移性NSCLC患者的疗效。最终分析结果显示,5.4和6.4mg/kg剂量组的疗效和疗效持续时间相当,确认的ORR分别为50%、56%;中位缓解持续时间(DoR)已超过10个月,分别为12.6个月、12.2个月。PFS和总生存期(OS)曲线中可见,两剂量德曲妥珠单抗的生存结果类似,5.4mg/kg德曲妥珠单抗的中位PFS、中位OS分别为10.0个月、19个月。
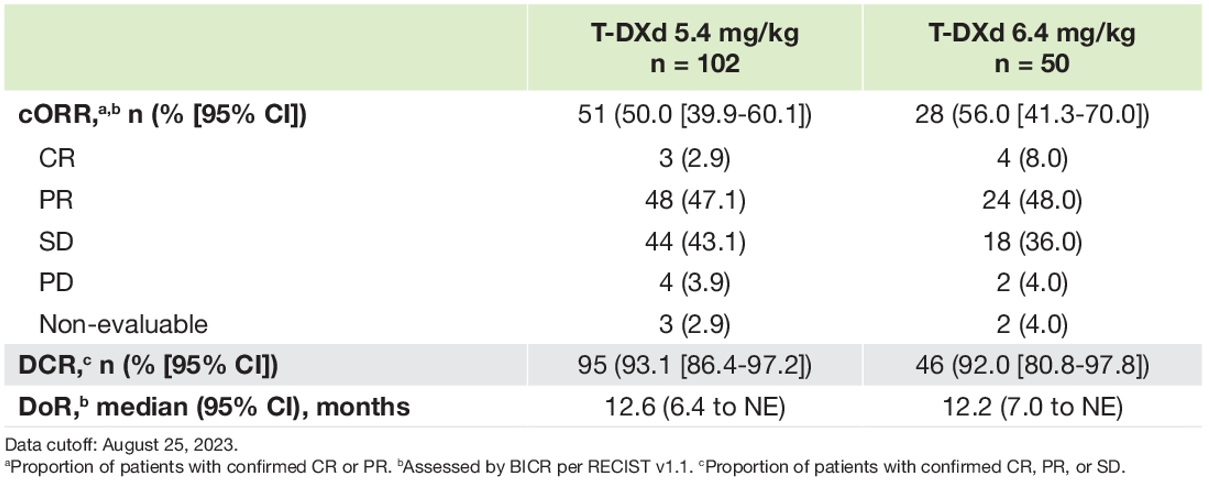
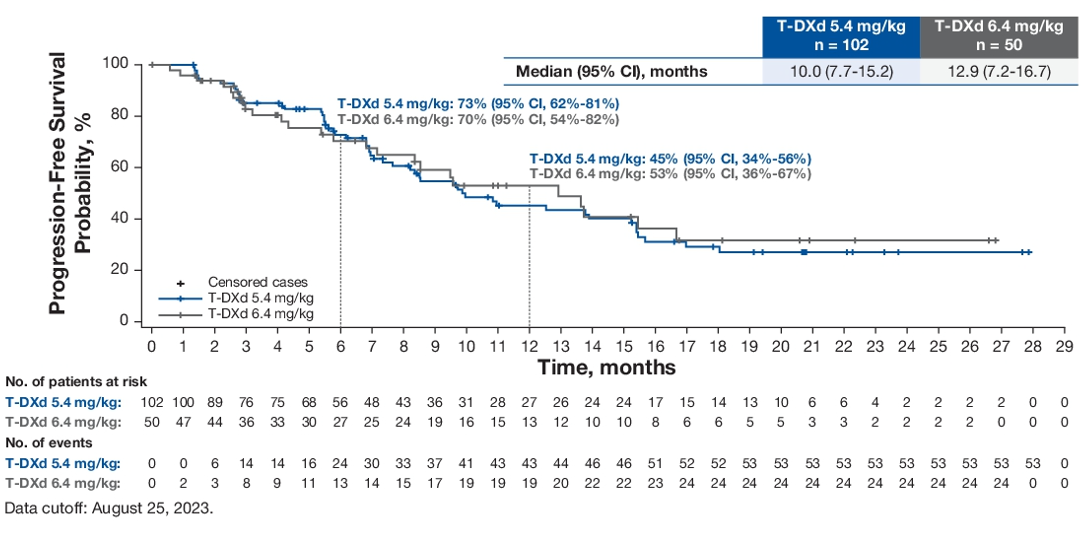
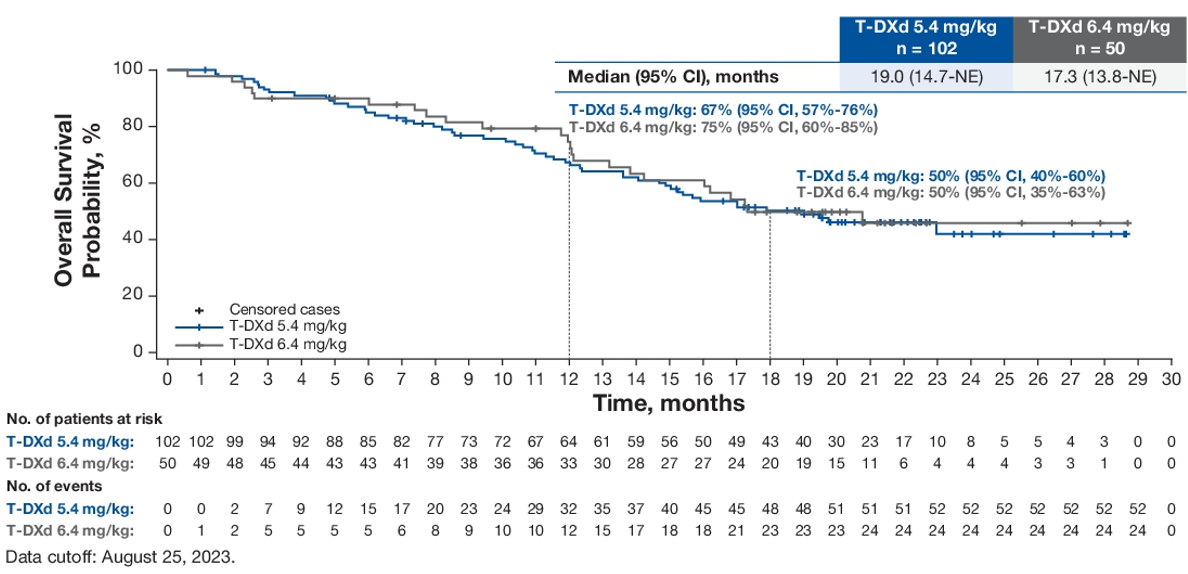 图5 DESTINY-Lung02最终分析疗效和生存结果
图5 DESTINY-Lung02最终分析疗效和生存结果
DESTINY-Lung02研究亚裔亚组:
已公布结果显示[7],5.4mg/kg德曲妥珠单抗组经确认的ORR为50.8%,中位DoR为16.8个月,中位PFS为10.8个月,12个月PFS率为45.5%,中位OS为19.5个月,12个月OS率为71.3%,研究结果与全球队列数据一致。
DESTINY-Lung01/02汇总分析:
在一项探索性分析中[8],与既往结果一致,5.4mg/kg德曲妥珠单抗确认的颅内ORR为50%,其中分别有21.4%、28.6%的患者达到完全缓解(CR)和部分缓解(PR)。中位颅内缓解持续时间为9.5个月。
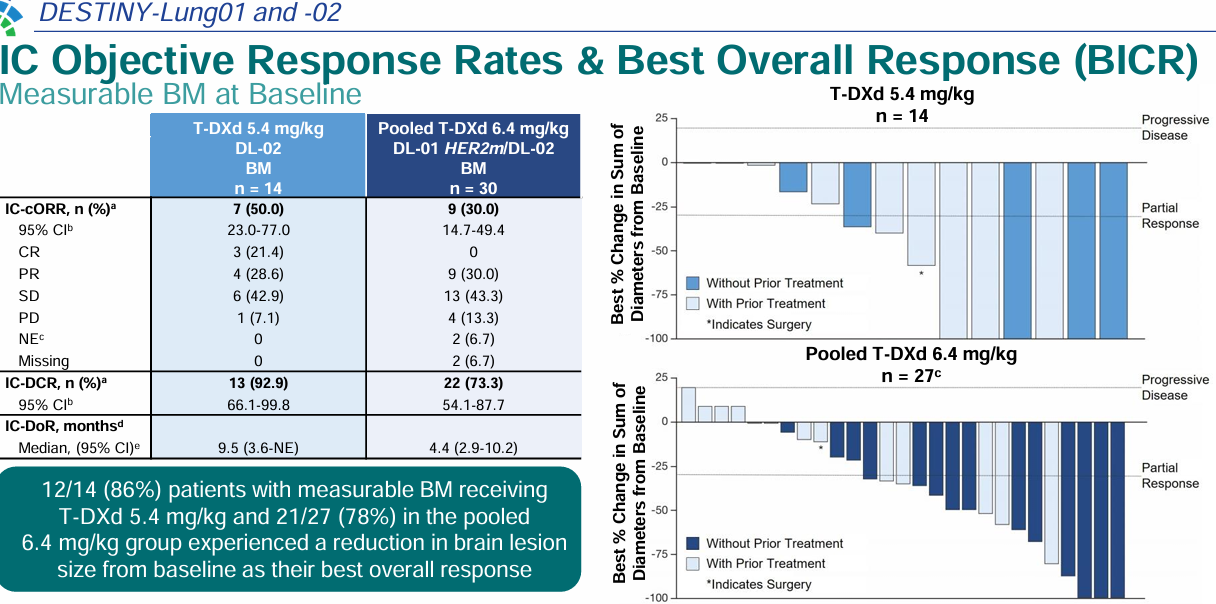 图6 颅内疗效分析
图6 颅内疗效分析
安全性分析显示,德曲妥珠单抗的主要不良事件有胃肠道或血液性毒性,常见的治疗期间不良事件(TEAE)有恶心、中性粒细胞减少症和和疲劳。除此之外,临床医生较关注的不良事件是间质性肺炎(ILD)的发生。经过前期DESTINY-Lung01和02的探索和证实,在5.4和6.4mg/kg德曲妥珠单抗疗效较一致的情况下,5.4mg/kg剂量组ILD发生率低。
DESTINY-Lung05研究:
DESTINY-Lung05是在中国经治HER2突变NSCLC人群中开展的单臂II期试验 [9],旨在评估5.4mg/kg德曲妥珠单抗在中国人群中的疗效和安全性。主要终点为由ICR评估确认的ORR,次要终点包括由研究者评估确认的ORR、ICR和研究者评估的DOR、DCR、PFS。从基线特征可见,分别有58.3%、41.7%的患者既往接受过2线及以上、1线治疗;分别有93.1%、90.3%、68.1%、68.1%的患者既往接受过细胞毒化疗、含铂化疗、免疫治疗、抗血管生成药物。
在入组的72例患者中,由ICR和研究者评估确认的ORR均达到58.3%,有效率高;ICR和研究者评估的中位至缓解持续时间短(即起效快),分别只有1.6个月、2.4个月。ICR评估的中位DoR仍未达到,意味着持续时间更长;研究者评估的中位DoR为9.0个月。中位PFS为10.8个月,而ICR评估的中位PFS仍未达到,意味着中位PFS会超过10.8个月。
治疗和相关检测均获得权威指南推荐:
基于上述研究结果,德曲妥珠单抗用于经治HER2突变NSCLC的治疗,已获得NCCN、CSCO、ASCO、ESMO等指南和共识的一致推荐。且国际/国内指南认为,HER2突变是晚期NSCLC的新兴生物标志物,是NSCLC的独立致癌驱动因素,精准筛选HER2突变人群,并实施分子标志物指导的精准治疗有望提高此类患者的疗效和生存获益。因此,国内外指南均推荐,晚期NSCLC进行包含HER2突变在内的多种致癌驱动基因的检测。在我国的临床实践中,基因检测推行有近10年时间,一次性检测多种致癌驱动基因变异,可以为患者节约检测样本、节省检测时间。
展望与总结
截止目前,德曲妥珠单抗已在HER2突变二线及以上治疗领域取得了突破性进展。除此之外,未来探索更关注于晚期NSCLC的一线及联合领域,相关临床研究包括DESTINY-Lung04、HUDSON Module 6、U106、DESTINY-Lung03等。其中DESTINY-Lung03已公布第1部分研究数据。初步结果显示,德曲妥珠单抗在HER2过表达晚期NSCLC中亦显示出较好的疗效,与既往DESTINY-Lung01队列1结果较一致。期待德曲妥珠单抗与免疫疗法或靶向疗法联合的更多研究与探索,以及未来更多临床试验结果的公布。
总体而言,基于DESTINY-Lung 02/05研究结果,FDA和NMPA已先后批准德曲妥珠单抗用于经治HER2突变NSCLC后线治疗的适应症,使得德曲妥珠单抗已在中国临床可及,为HER2突变晚期NSCLC带来了新选择。期待未来临床实践中德曲妥珠单抗能为中国HER2突变晚期NSCLC带来更优临床获益。
[1]Shitara K, Bang YJ, Iwasa S, et al. N Engl J Med. 2020;382(25):2419-2430.
[2]Sara A Hurvitz et al; Lancet. 2023 Jan 14;401(10371):105-117
[3]Nakada T, et al. Chem Pharm Bull (Tokyo). 2019;67(3):173-185.
[4]Ogitani Y, et al. Clin Cancer Res. 2016;22(20):5097-5108.
[5]Yoko Nagai et al. XENOBIOTICA, 2019, VOL. 49, NO. 9, 1086–1096
[6]Li BT, Smit EF, Goto Y, et al Trastuzumab Deruxtecan in HER2-Mutant Non-Small-Cell Lung Cancer. N Engl J Med. 2022 Jan 20;386(3):241-251. doi: 10.1056/NEJMoa2112431.
[7]Trastuzumab deruxtecan (T-DXd) in Asian patients (Pts) with human epidermal growth factor receptor 2 (HER2; ERBB2)-mutant (HER2m) metastatic non-small cell lung cancer (mNSCLC): Subgroup analysis of DESTINY–Lung02(DL-02). 2023 ESMO Asia 510MO.
[8]Trastuzumab Deruxtecan in Patients With HER2 (ERBB2)-Mutant Metastatic Non–Small Cell Lung Cancer With and Without Brain Metastases: Exploratory Pooled Analyses From DESTINY-Lung01 and DESTINY-Lung02.2023 ESMO, Abstract 1321MO.
[9]Trastuzumab deruxtecan (T-DXd) in Chinese patients (pts) with previously treated HER2 mutant non-small cell lung cancer (NSCLC): primary analysis from the Phase 2 DESTINY-Lung05 (DL-05) trial. Abstract CT248/7,2024 AACR.
排版编辑:肿瘤资讯-Ale











 苏公网安备32059002004080号
苏公网安备32059002004080号


