国家癌症中心在2024年最新发布的《2022年中国恶性肿瘤流行情况分析》报告中指出[1],肺癌已成为中国发病率和死亡率最高的恶性肿瘤,对公共卫生构成巨大挑战。非小细胞肺癌(NSCLC)患者在肺癌中占比高达80%~85%,且存在多种驱动基因突变。间质上皮转化因子(MET)外显子14跳跃突变(简称METex14跳突)是关键驱动基因之一,已被证实是非小细胞肺癌的独立致癌因素,然而传统治疗手段如化疗、免疫治疗效果有限。
目前,已有多款MET抑制剂在我国陆续获批上市,显著改善了METex14跳突NSCLC患者的生存状况。2024年6月11日,国家药品监督管理局(NMPA)批准卡马替尼上市[2],用于未经系统治疗的携带间质上皮转化因子(MET)外显子14跳跃突变的局部晚期或转移性NSCLC成人患者。卡马替尼是一款具有高度选择性和强效抑瘤效力的MET抑制剂,其一线治疗的疾病控制率(DCR)可高达98.3%,且中位无进展生存(PFS)超过1年[3]。此外,在安全性方面,卡马替尼还具有外周水肿发生率低、肝毒性低,且口服便利、不受餐食影响等多重优势。
卡马替尼在中国的获批上市,不仅为晚期METex14跳突NSCLC患者提供了更多样化的治疗选择,也为他们带来了新的治疗希望。
卡马替尼为METex14跳突NSCLC患者带来新的治疗选择
卡马替尼是一种高选择性的特异性MET受体酪氨酸激酶抑制剂,可抑制MET及MET介导的下游信号蛋白的磷酸化,从而抑制c-MET依赖性肿瘤细胞的增殖和迁移,并诱导细胞凋亡。卡马替尼对METex14跳突肿瘤细胞的半数抑制浓度(IC50)值仅为0.6nM[4],在同类MET抑制剂中最低,提示对MET具有极强的抑制活性。
卡马替尼的全球批准是基于GEOMETRY mono-1研究的结果[3],这是一项国际多中心、非随机、多队列参与的II期临床试验,其结果曾刊登于《新英格兰医学杂志》(NEJM)。该研究纳入了不同MET变异类型的NSCLC,其中队列4、5b、6、7分别纳入了经治及初治的METex14跳突患者。研究结果显示,METex14跳突初治患者(队列5b和7,n=60)接受卡马替尼治疗的客观缓解率(ORR)为68.3%,DCR为98.3%,中位无进展生存期(PFS)达12.5个月,中位OS达25.5个月。无论从短期病灶缓解到长期生存获益,卡马替尼都展现出了极佳的令人惊艳的疗效。
基于GEOMETRY mono-1研究成果,卡马替尼相继获得美国食品药品监督管理局(FDA)突破性疗法认证、孤儿药、加速审批及优先审评认定,于2020年5月获加速批准上市,并基于验证队列的一致数据于2022年8月获得完全批准[5]。卡马替尼是FDA批准的首个特异性MET抑制剂,开启了METex14跳突的靶向治疗时代。
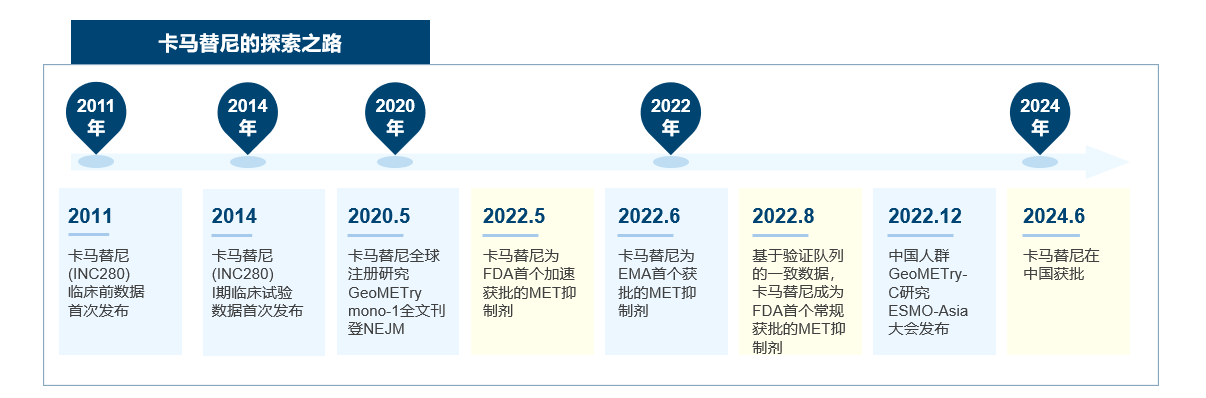
在GEOMETRY mono-1最新的随访报道中,卡马替尼在METex14跳突的NSCLC患者中展现出了持续的疗效。这项研究的最终结果发表在了《Lancet Oncology》上 [6],是继2020年在NEJM上发表的初期分析之后,该研究第二次在顶级期刊上发表。值得注意的是,这是目前所有针对METex14跳突NSCLC的临床研究中随访时间最长的。疗效数据显示,与既往报道一致,一线治疗队列(n=60)中,ORR为68%,DCR高达98%,中位缓解持续时间(DOR)为16.6个月,中位PFS为12.5个月。这些数据进一步证实了卡马替尼在治疗METex14跳突的NSCLC患者中的潜力和效果。
除全球人群之外,卡马替尼进一步开展了针对中国人群的多中心、单臂II期注册临床研究(GeoMETry-C研究)[7]。此项研究旨在评价卡马替尼在中国患者人群中治疗METex14跳突晚期NSCLC患者中的有效性。在初治队列的可评估人群中(N=13),盲态独立评审委员会(BIRC)评估的ORR为61.5%,研究者(INV)评估的ORR达69.2%,PFS和OS数据尚未成熟。这些结果与全球研究数据一致,进一步显示了卡马替尼对中国患者群体的获益,为其在中国的METex14跳突晚期NSCLC患者中的应用提供了科学依据。
卡马替尼高效透脑,半数颅内病灶可达完全缓解
在晚期METex14跳突患者中,约37%的患者存在脑部转移[8],并且对生存质量和预后产生不良影响。因此,针对脑转移的治疗成为了临床研究的新焦点。卡马替尼作为一种小分子MET抑制剂,能高效通过血脑屏障,控制并缓解颅内病灶。
在最新随访的GEOMETRY mono-1研究中,28名有可测量颅内靶病灶的脑转移患者接受了卡马替尼治疗[6]。研究结果显示,在所有颅内病灶可评估的患者中,卡马替尼的颅内客观缓解率(iORR)为57%,颅内完全缓解(iCR)率达到了32%,其中5/9的患者iCR的持续时间超过了6个月。对于那些既往未接受过脑部放疗的患者(N=15),卡马替尼的疗效数据与既往研究一致,iORR为67%,iCR为33%。作为衡量颅内肿瘤缩小效果的关键指标,iCR越高,则代表更多患者的颅内病灶完全消失,而该研究结果也充分展示了卡马替尼在颅内抑制肿瘤生长方面的卓越效力。
此外,在中国的注册临床研究GeoMETry-C中[7],也同样观察到了卡马替尼突出的颅内疗效,一线初治队列中4名脑转移患者有2名颅内病灶完全缓解,iCR高达50%,iDCR为100%。这意味着有一半的患者颅内病灶完全消失,而全部患者的颅内病灶均未进展。
此外,在一项大样本的专门针对脑转移患者真实世界回顾性研究中[9],55例METex14跳突阳性的脑转移患者接受一线卡马替尼治疗后全身病灶真实世界客观缓解率(rwORR) 为90.9%,真实世界疾病控制率(rwDCR)为96.4%,iORR达87.3%;iDCR达96.4%。如此惊艳的数据,再次验证了卡马替尼与临床研究一致的对脑转移患者颅内病灶和全身病灶的强大控制。以上所有证据都再次提示卡马替尼应成为METex14跳突患者的一线首选治疗。
真实世界证据充分验证,卡马替尼获多项指南推荐
作为FDA首个获批上市的特异性MET抑制剂,卡马替尼在真实世界中积累了丰富的数据。多项研究观察到卡马替尼在真实世界中的疗效和临床研究高度一致。来自美国的一项真实世界研究回顾性对比了卡马替尼与其他治疗方案的临床疗效[10],其中146名患者一线接受了卡马替尼治疗。研究结果显示,卡马替尼治疗的rwORR高达73.4%,rwDCR达到95%,18个月的PFS率和OS率分别达到了68%和92.6%,显著优于其他治疗组。
今年WCLC大会上公布的一项MAIC研究显示,在一线治疗METex14跳突的晚期NSCLC患者中,卡马替尼相较于其他MET抑制剂,展现出了更优的OS获益趋势。在安全性方面,卡马替尼在亚洲患者群体中的治疗相关不良事件(TRAEs)发生率显著较低[11]。
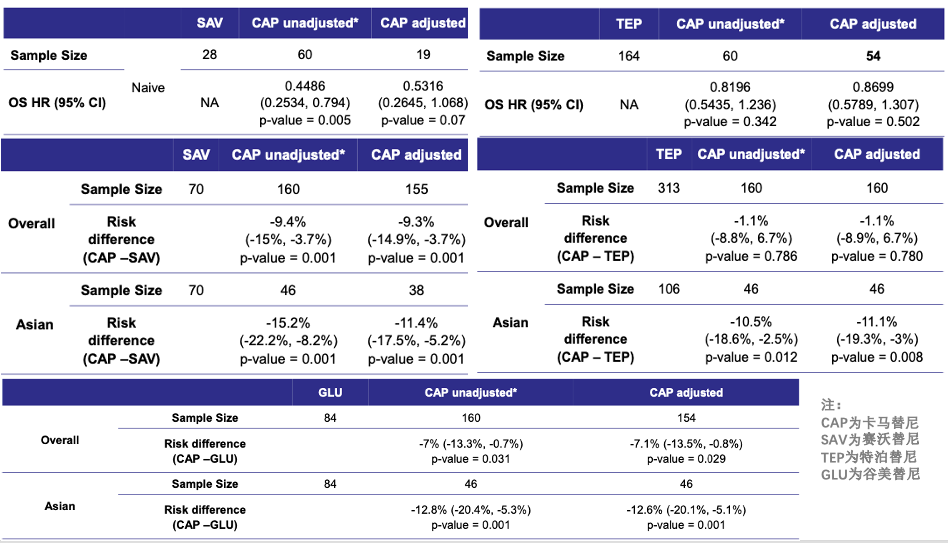
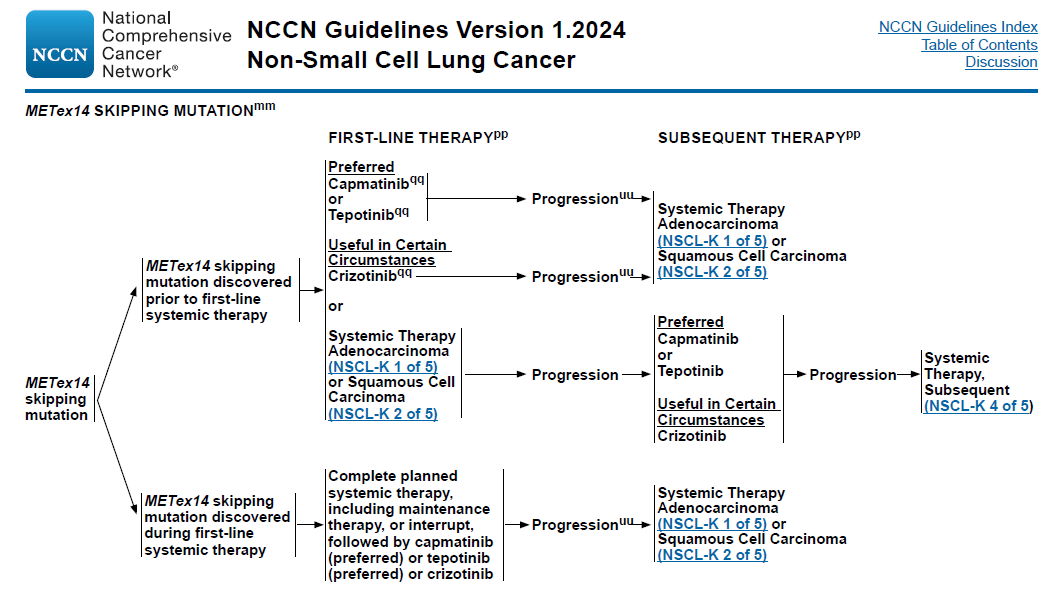
因此根据临床试验和真实世界研究数据,国际多项治疗指南,包括美国国家综合癌症网络(NCCN)、美国临床肿瘤学会(ASCO)、欧洲肿瘤医学学会(ESMO),已将卡马替尼列为METex14跳突NSCLC的一线治疗首选药物[12-14]。
卡马替尼安全低毒,降低临床管理负担,提高患者生活质量
METex14跳突患者多为老年患者,平均年龄为65~76岁,因此对于药物使用的便捷性和安全性有着更高的需求。《MET14外显子跳跃突变NSCLC靶向治疗专家共识》[15]中指出:外周水肿是各种MET-TKIs较为常见的不良反应,总体发生率为50%~63%,3级以上发生率为1%~11%。而肝毒性则是MET抑制剂另一个备受关注的安全性问题。一方面是因为METex14跳突患者多为老年人,基线合并肝功能不全的患者比例增高。另一方面是肺癌患者接受多种抗肿瘤治疗均有肝损伤的风险,比如几乎所有化疗药物都能够引起药物性肝损伤。
来自临床研究的安全性数据[5,7]显示,卡马替尼整体安全性良好,不良反应发生率低,严重程度低,且消退快。在中国人群中3/4级TRAEs的发生率仅为20%,且无致死性TRAEs。没有因不良事件导致研究停药。对于目前MET抑制剂常见的不良反应,卡马替尼的水肿发生率显著低于其他MET抑制剂,中国人群中治疗相关所有级别水肿发生率仅为26.7%,且无3/4级发生。卡马替尼的肝毒性也较低,是目前唯一一个有证据支持可在重度肝损患者中使用的MET抑制剂。轻、中、重度肝损患者使用卡马替尼的初始剂量均无需调整。
除水肿和肝毒性外,卡马替尼的安全性优势还体现在心脏毒性、血液毒性等多方面。目前,卡马替尼在临床研究中并未见治疗相关的血液毒性(如贫血)和心脏毒性(如QT间期延长)等不良反应的发生。
另外值得一提的是,临床研究显示[16],卡马替尼在体内的吸收代谢不受空腹或进食状态影响。因此卡马替尼的服用方式灵活,与食物同服或不同服均可,有助于提高患者的用药依从性。
结语
面对老龄化背景下METex14跳突NSCLC治疗的挑战,卡马替尼在中国的上市为晚期METex14跳突NSCLC患者延长生存和预后提供新的解决方案。
展望未来,我们期待卡马替尼能够在更广泛的患者群体中得到应用,并进一步验证其疗效和安全性。同时,也希望能有更多的研究探索卡马替尼与其他治疗手段的联合应用,以期为患者带来更深层次的个体化治疗策略。
1. 郑荣寿, 陈茹 等. 2022年中国恶性肿瘤流行情况分析. 中华肿瘤杂志, 2024, 46(3):221-231
2. 国家药品监督管理局.2024年06月18日药品批准证明文件送达信息. https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20240618120418177.html
3. Wolf J, Seto T, Han JY, et al. Capmatinib in MET Exon 14-Mutated or MET-Amplified Non-Small-Cell Lung Cancer. N Engl J Med. 2020;383(10):944-957.
4. Fujino T, et al. Sensitivity and Resistance of MET Exon 14 Mutations in Lung Cancer to Eight MET Tyrosine Kinase Inhibitors In Vitro. J Thorac Oncol. 2019 Oct;14(10):1753-1765.
5. FDA approves capmatinib for metastatic non-small cell lung cancer https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-capmatinib-metastatic-non-small-cell-lung-cancer
6. Wolf J, Hochmair M, Han JY, et al. Capmatinib in MET exon 14-mutated non-small-cell lung cancer: final results from the open-label, phase 2 GEOMETRY mono-1 trial. Lancet Oncol. 2024 Oct;25(10):1357-1370.
7. Wu YL, et al. ESMO ASIA. 2022; poster 388.
8. Awad MM, Leonardi GC, Kravets S, et al. Impact of MET inhibitors on survival among patients with non-small cell lung cancer harboring MET exon 14 mutations: a retrospective analysis. Lung Cancer. 2019;133:96-102. doi:10.1016/j.lungcan.2019.05.011
9. Paik PK, et al. Real-world outcomes in non-small-cell lung cancer patients with MET Exon 14 skipping mutation and brain metastases treated with capmatinib. Future Oncol. 2023 Jan;19(3):217-228.
10. Furqan M, Karanth S, Goyal RK, et al. Effectiveness of standard treatments in non-small-cell lung cancer with METexon14 skipping mutation: a real-world study. Future Oncol. Published online April 17, 2024. doi:10.2217/fon-2023-1064
11. Yi-long Wu, et al. Matching-Adjusted Indirect Comparison (MAIC) of overall survival (OS) and treatment related adverse events (TRAE) comparing Capmatinib (CAP) with other Mesenchymal-epithelial transition (MET) Inhibitors for treatment of advanced non-small cell lung cancer (aNSCLC) with MET Exon 14 skipping mutations. 2024 WCLC. EP.12D.05.
12. NCCN Guidelines Version 5.2022 Non-Small Cell Lung Cancer.
13. Dwight H. Owen et al., Therapy for Stage IV Non–Small Cell Lung Cancer With Driver Alterations: ASCO Living Guideline, Version 2024.1. JCO 0, JCO.24.00762.
14. Hendriks, L.E. et al.Annals of Oncology, Volume 34, Issue 4, 339 – 357.
15. 中国老年保健协会肺癌专业委员会. MET 14外显子跳跃突变NSCLC靶向治疗专家共识. 中国肺癌杂志, 2023, 26(6): 416-428.
Moreno V, et al. Pharmacokinetics and safety of capmatinib with food in patients with MET-dysregulated advanced solid tumors. Clin Ther. 2021 Jun;43(6):1092-1111.
审批码TAB0033367-77481,有效期为2024-10-31至2025-10-30,资料过期,视同作废
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


