
神经营养性酪氨酸受体激酶(NTRK)基因融合是多种儿童和成人肿瘤的致癌驱动因子,这种融合在我国实体瘤总体人群中较为罕见,患病率仅0.4%[1],但在特定的癌症类型,如5岁以下儿童肿瘤及甲状腺癌中,其发病率相对较高,分别达到了2.28%[2]和3.1%[1]。拉罗替尼是一种首创的、高选择性的、能够穿过中枢神经系统的口服TRK抑制剂,目前已被批准用于成人和儿童TRK融合癌症患者,标志着“广谱抗癌时代”的来临。
在第56届国际儿科肿瘤学会(SIOP)年会和2024年美国甲状腺学会(ATA)年会上,两项关于拉罗替尼治疗原发性CNS和非原发性CNS儿童TRK融合肿瘤及TRK融合甲状腺癌的相关数据分析公布,研究者基于SCOUT和NAVIGATE两项关键性研究数据,进一步更新了临床对拉罗替尼疗效和安全性的认识。本文将详细介绍这两项研究,并邀请多学科专家对这些研究结果进行深入点评。
2024 SIOP:拉罗替尼治疗原发性CNS和非原发性CNS儿童TRK融合肿瘤的长期疗效和安全性
研究背景
拉罗替尼是一种针对TRK融合癌症的高选择性、中枢神经系统活性的口服TRK抑制剂,已被批准用于成人和儿童患者。本研究旨在进一步评估拉罗替尼在儿童患者中,特别是那些患有原发性中枢神经系统(CNS)和非原发性CNS TRK融合肿瘤患者中的长期疗效和安全性。
研究方法
研究纳入NAVIGATE和 SCOUT两项临床研究中137例患有TRK融合肿瘤的儿童患者(年龄小于18岁)。拉罗替尼的剂量为100 mg/m2,每日两次(最大剂量为100 mg,每日两次)。主要终点是独立审查委员会(IRC)根据RECIST v1.1/RANO评估的客观缓解率(ORR)。次要终点包括反应持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)和安全性。
研究结果
患者中位年龄4岁,男性患者75例,女性患者62例;原发性CNS肿瘤和非CNS肿瘤患者分别为38例和99例;多数患者(63%)入组前已接受过系统治疗。分析共发现了43种独特的基因融合,其中ETV6::NTRK3(36%)和TPM3::NTRK1(25%)最为常见。
结果显示,非CNS肿瘤患者(N=99)的ORR为86%,中位DoR为43个月,中位PFS为40个月,中位OS尚未达到,60个月的OS率为88%(图1、图2)。在非CNS肿瘤患者中,有51例被纳入“等待观察(wait-and-see)”分析,患者在暂停治疗前的平均治疗时间为16个月。在暂停治疗期间,中位持续时间为22个月。在退出“等待观察”期的28例患者中,17例患者因疾病进展而恢复治疗,恢复治疗后有5例完全缓解(CR)、6例部分缓解(PR)、5例疾病稳定(SD)以及1例不可评估。
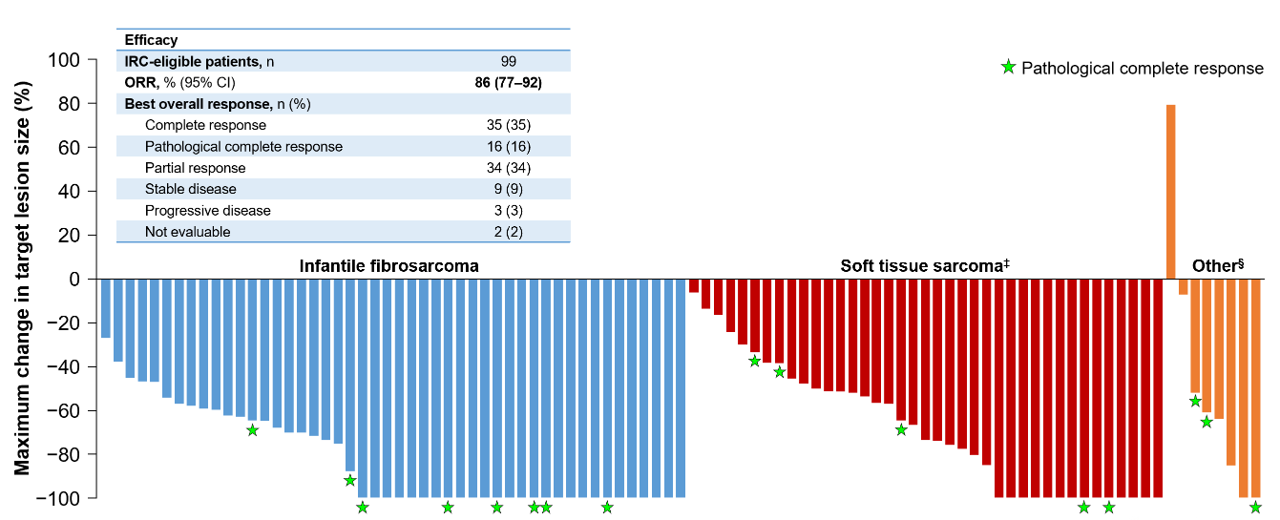
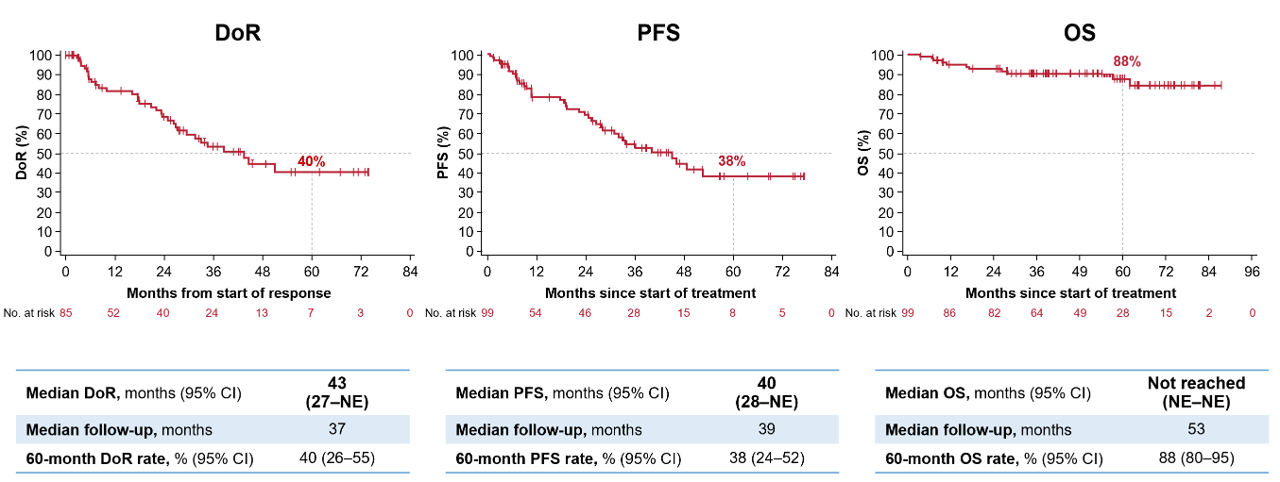
原发性CNS肿瘤患者(N=38)的ORR为37%,中位DoR为17个月,中位PFS为20个月,中位OS尚未达到,48个月的OS率为59%(图3)。4例低级别胶质瘤(LGG)和1例高级别胶质瘤(HGG)患者进入了“wait-and-see”分析,中位“等待观察”持续时间为20个月。1例LGG患者因未遵守医嘱退出“wait-and-see”期,其他患者在数据截止时均未观察到疾病进展,且都还存活。
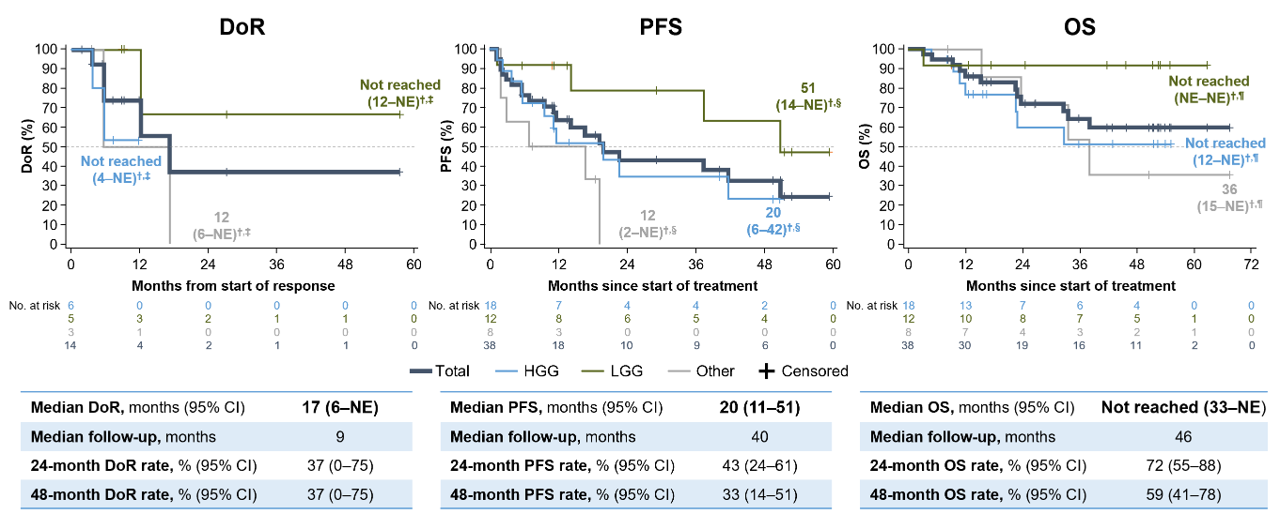
在安全性方面,所有患者的治疗相关不良事件(TRAEs)主要是1/2级。3/4级TRAEs发生率为28%,最常见的是中性粒细胞计数减少和ALT升高。三名患者因TRAEs停止治疗,但没有患者因TRAEs死亡。
研究结论
拉罗替尼在儿童患者中显示出良好的安全性,并且在原发性和非原发性CNS TRK融合肿瘤中均显示出快速且持久的治疗应答。即使在停止治疗后,肿瘤进展也可以通过再次治疗获得高缓解率。该结果支持更广泛地采用包括NTRK基因融合的下一代测序(NGS)测试,用于患有实体恶性肿瘤的儿童,包括CNS肿瘤。
2024 ATA:拉罗替尼治疗TRK融合型甲状腺癌(TC)患者的疗效、安全性和基因组数据
研究背景
早期研究显示,拉罗替尼治疗TRK融合TC患者的ORR为63%。本次分析报告了增加一年随访后,拉罗替尼治疗TRK融合TC患者更新的疗效、安全性和基因组数据。
研究方法
研究纳入NAVIGATE和 SCOUT两项临床研究中年龄≥18岁的31例TRK融合TC患者。主要终点是由IRC根据RECIST v1.1评估的ORR;次要终点包括DoR、PFS、OS和安全性。
研究结果
患者中位年龄为60岁,71%为女性,多数患者为ECOG 0分或1分(81%)。患者的肿瘤组织学类型多为分化型(77%),已知CNS转移的患者占13%。所有患者均接受了手术,77%接受了放疗,74%接受了放射性碘治疗,45%接受了系统治疗。在TRK基因融合方面,有8种独特的基因融合,其中ETV6::NTRK3最为常见。
研究共随访84个月,分析结果显示,在肿瘤反应方面,所有患者的ORR为65%,分化型TC(DTC)患者的ORR为79%,而间变性TC(ATC)患者的ORR为14%;中位DoR为41个月,中位PFS为44个月,中位OS未达到(图4、图5)。
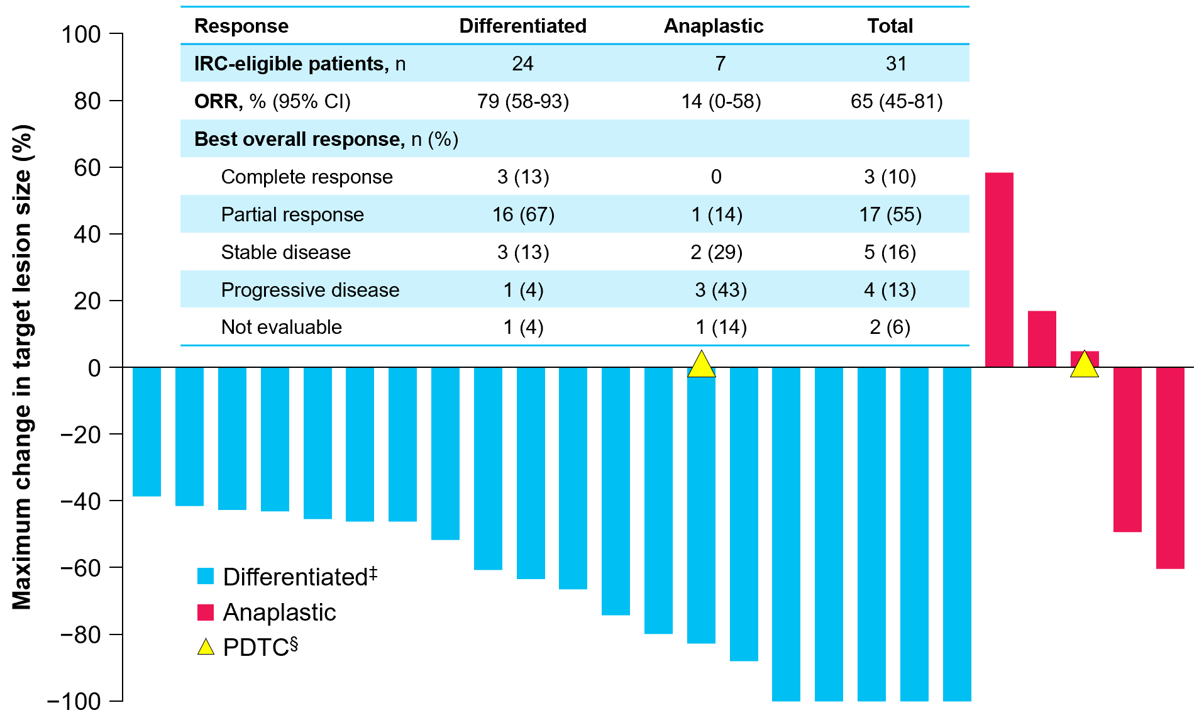

在安全性方面,TRAEs主要是1/2级,3例(10%)患者出现3级/4级TRAEs,包括贫血、淋巴细胞计数减少和肝细胞溶解,无患者因TRAEs中断治疗。
研究结论
在更新的数据集中,拉罗替尼在TRK融合DTC患者中继续显示出快速和持久的反应、延长的生存期和良好的安全性,而在ATC中的活性有限。这些结果支持使用NGS检测TC患者的NTRK基因融合,以识别可能从靶向治疗中受益的患者。
专家点评
儿童肿瘤科主任
华南肿瘤学国家重点实验室 PI
国家卫健委儿童血液病恶性肿瘤专家委员会 副主任委员
国家卫健委儿童血液病恶性肿瘤专家委员会 实体肿瘤内科专委会 主任委员
中国抗癌协会血液病转化研究专业委员会 副主任委员
中国研究型医院协会儿童肿瘤专业委员会 副主任委员
中国抗癌协会儿童肿瘤专委会 常委
CSCO 中国抗淋巴瘤联盟 常委
CSCO中国抗淋巴瘤联盟 儿童及青少年学组 常务副组长
中国抗癌协会血液肿瘤专业委员会 常委 (第三、第四届)
广东省抗癌协会小儿肿瘤专委会 候任主委
广东省精准医学应用学会 儿童肿瘤分会 主任委员
张翼鷟教授:CNS肿瘤是14岁及以下儿童最常见的实体瘤之一,其年发病率稳居儿童恶性肿瘤的第二位,且近十年来CNS肿瘤的预后并未显著改善。这一现状亟需引起重视,以推动更有效的治疗策略和研究进展。随着NTRK基因融合的发现以及TRK抑制剂的问世,原发性CNS肿瘤儿童患者也迎来了新的治疗希望。
拉罗替尼作为含新生儿适应症的NTRK融合跨越多瘤种的靶向药,不仅在成人患者中显示出良好的抗肿瘤活性,更为儿童NTRK融合实体瘤患者带来治疗希望。2024 SIOP年会上发布的研究显示,拉罗替尼在原发性CNS和非原发性CNS儿童TRK融合肿瘤患者中展现出强劲实力。疗效结果显示,拉罗替尼在非CNS肿瘤患者中的优异疗效,ORR达到了86%,PFS和OS获益显著;在原发性CNS肿瘤患者中,同样显示出了积极的效果,ORR近40%,中位PFS达到了20个月,48个月的OS率为59%,这些研究数据非常令人鼓舞。此外,研究还对”wait-and-see”策略进行了分析,该策略允许在没有疾病进展的情况下暂停治疗,有助于减少长期副作用,提高患者的生活质量。两组患者在”wait-and-see”分析均表现优异,暂停治疗的中位时间均超20个月,且在暂停治疗期间,大多数患者没有出现疾病进展。在安全性方面,拉罗替尼展现出了良好的耐受性,这对于需要长期治疗的儿童患者来说尤为重要。后续期待更多长期随访数据的积累,能够指导临床应用拉罗替尼在改善儿童NTRK融合肿瘤患者的预后方面发挥更大的作用。
以上表明,拉罗替尼治疗NTRK融合儿童肿瘤患者表现出快速且持久的缓解,延长了患者的生存获益,进一步支持拉罗替尼在儿童NTRK融合肿瘤中的优选地位。据最新医保目录,拉罗替尼纳入2025年国家医保目录,填补了12岁以下儿童NTRK融合实体瘤患者治疗空白,减轻病患家庭压力和社会负担。
中山大学肿瘤中心核医学科主任
广东省核医学专业质控中心主任
中国抗癌协会肿瘤核医学专委会前任主委
中华医学会核医学分会委员兼肿瘤学组副组长
中国核学会核医学分会常务理事
中国淋巴瘤质控中心专家委员会委员
广东省医院协会核医学管理专委会主委
《中华核医学与分子影像》杂志编委
《肿瘤影像学》杂志主编
樊卫教授:甲状腺癌是最常见的内分泌系统恶性肿瘤,其发病率在近年来不断上升,成为了一个全球性的公共卫生问题。传统治疗方法虽然在一定程度上改善了患者的生存状况,但对于部分难治性或晚期患者,尤其是那些对放射性碘治疗无反应的患者,治疗效果并不理想。这些患者迫切需要新的治疗选择。在这种情况下,拉罗替尼的出现无疑为NTRK基因融合的甲状腺癌患者带来了新的希望。
在2024年ATA年会上公布的这项研究中,患者接受拉罗替尼治疗,尽管这些患者既往均接受了多种治疗,包括手术、放疗、放射性碘治疗和系统治疗,但拉罗替尼仍然显示出了显著的疗效。研究结果显示,DTC患者的客观反应率高达79%。此外,研究还观察到了较长的反应持续时间和总生存期,这些都是评估抗癌治疗疗效的重要指标。在安全性方面,拉罗替尼同样展现了良好的耐受性,这对于需要长期治疗的甲状腺癌患者来说尤为重要,因为它意味着患者可以在保持生活质量的同时接受治疗。
目前,拉罗替尼已在中国获批,用于治疗NTRK基因融合的甲状腺癌患者。随着临床经验的积累和高质量循证医学证据的增加,预计拉罗替尼在NTRK基因融合TC患者中的应用将更加广泛。
广东省人民医院(广东省医学科学院)病理科 副主任医师 博士
美国纪念斯隆凯特琳癌症中心(MSKCC)访问学者
国际肺癌研究协会(IASLC)会员
全国医用临床检验实验室和体外诊断系统标准化技术委员会(SAC/TC136)委员
中国研究型医院学会分子诊断医学专委会青委
中国抗癌协会肿瘤病理学专委会肺癌病理学组委员
中国抗癌协会肿瘤分子医学专委会委员
中国抗癌协会肿瘤标志专委会委员
广东省医学会病理学分会青委
广东省医学会病理学分会数字与分子学组委员
颜黎栩专家:NTRK基因融合作为一种关键的致癌驱动因素,在多种肿瘤中的存在为患者提供了潜在的治疗靶点。然而,目前NTRK检测率较低,这限制了精准靶向治疗的应用。不同肿瘤NTRK基因融合率不同,要求我们采取更为敏感和全面的检测策略。
目前,NTRK基因融合的检测方法包括FISH、IHC、RT-PCR和基于DNA或RNA的NGS等,每种方法都有其有点和局限性。NGS检测能够发现已知和未知的NTRK融合,是检测的首选方法。FISH可以用于检测特定基因融合,对于NGS检测结果不确定的情况,可以作为补充检测手段。
为了提高NTRK基因融合的检测率,我们需要改进当前的检测流程,优化检测方法,并在临床上推广这些检测。这不仅能够为患者提供更精准的治疗选择,还能促进新型靶向治疗药物的研发和应用。随着检测技术的不断进步和成本的降低,我们有望在未来实现对更多患者的精准治疗。
1、NPJ Precis Oncol. 2023 Aug 11;7(1):75.
2、拉罗替尼治疗TRK融合儿童肿瘤中国专家共识[J].中国肿瘤临床, 2023, 50:998.
审批号:MA-LAR-CN-0269-1
排版编辑:肿瘤资讯-Zika











 苏公网安备32059002004080号
苏公网安备32059002004080号


