
在精准治疗时代,靶向治疗是炙手可热的精准疗法之一, 研究者也在不断探索新的靶点并开发相应的新疗法。HER2突变是晚期非小细胞肺癌(NSCLC)的重要生物标志物,与患者预后差相关。一直以来,由于缺乏有效的靶向治疗方案,HER2突变患者只能参考无驱动基因突变晚期NSCLC的治疗选择。随着DESTINY-Lung02和DESTINY-Lung05取得突破,10月9日,NMPA批准了抗体偶联药物(ADC)德曲妥珠单抗用于HER2突变晚期NSCLC后线治疗的适应症,为患者带来了新的治疗选择。
【肿瘤资讯-HER2学社】第十期特邀湖南省第二人民医院杨农教授回顾并深入解析HER2突变NSCLC的治疗现状。
主任医师 博导
海南热带肿瘤研究所、海南省肿瘤医院、海南成美医院长聘专家
2017-2023七届全国“年度好大夫”
第六届 国之名医·优秀风范
国家科技重大专项首席专家
国家肿瘤质控中心肺癌质控专委会委员
中国医药教育协会肿瘤免疫治疗专委会副主任委员
中国医药教育协会肿瘤临床科研创新发展专委会副主任委员
中国临床肿瘤学会理事及肿瘤免疫治疗、非小细胞肺癌、药物研发专委会委员
中国抗癌协会抗肿瘤药物专委会常委、肺癌专委会委员
中国医师协会肿瘤学分会委员
湖南省抗癌协会肿瘤精准医学专委会主任委员
湖南省老年医学学会临床肿瘤学分会主任委员
肺癌精准诊疗湖南省重点实验室主任
湖南省呼吸肿瘤临床医学研究中心主任
面临挑战:HER2突变晚期NSCLC预后差,
治疗需求未被满足
2004年,科学家在NSCLC中首次发现了发生于HER2基因酪氨酸激酶结构域内的激活突变[1],后续开展的体外和体内研究证实了HER2突变的致癌潜力[2-4]。HER2突变肺腺癌一般与女性、亚洲地区、从不吸烟者相关;HER2突变可鉴定出一种独特的肺腺癌亚群,是晚期NSCLC的重要生物标志物。HER2突变与晚期NSCLC预后差相关,且易出现脑转移;在疾病过程中约有50%的HER2突变NSCLC患者可能发生脑转移,分别约有19%、28%的HER2突变NSCLC在诊断时和治疗过程中可能出现脑转移[5]。
相比其他地区(1-3%),亚洲地区患者HER2突变的发生率略高,约为1.4-6.7%[6],HER2突变在晚期肺腺癌中国人群中的发生率约为2-4%[7],一项纳入7395例中国患者的研究显示,HER2突变的发生率为5.4%[8]。在所有恶性肿瘤中肺癌发生率高居榜首,例如中国每年约有106万新发病例[9],因此每年约有3.3万新发HER2突变肺癌病例。近20年来,这部分患者无有效的精准靶向疗法可用,我国HER2突变NSCLC的一线治疗选择主要参考驱动基因阴性NSCLC的治疗方案,即化疗±免疫治疗。整体而言,此类患者存在较大未被满足的治疗需求,亟需更开发更有效的新型疗法。
遭遇瓶颈:
传统药物、新型药物有效率难以突破约30%
研究者既往在HER2突变NSCLC中探索过多种传统治疗药物的有效性。例如一项多中心、随机双盲III期试验评估了多西他赛在此类患者中的疗效。此研究纳入一线含铂化疗方案治疗期间或之后进展的鳞状或非鳞状NSCLC,1253例患者被随机分配接受多西他赛75mg/m2±雷莫西尤单抗或安慰剂治疗,直至患者疾病进展、或出现不可接受的毒性、停药或死亡。结果显示,625例接受多西他赛治疗的HER2突变NSCLC的中位生存期(OS)仅为 9.1个月,中位无进展生存期(PFS)仅为3.0个月[10]。且有研究显示,HER2突变NSCLC从培美曲塞治疗中的获益低于ALK/ROS1融合患者,中位PFS分别为5.1 vs 9.2个月(P=0.004)[11]。
有研究显示免疫治疗在经治晚期NSCLC总人群中的疗效优于化疗,但HER2突变患者并不能从免疫单药中获益,HER2突变接受免疫单药的客观缓解率(ORR)为7%,低于KRAS、BRAF、ROS1和EGFR变异患者[11]。一项随机、开放标签的III期临床试验纳入经治IIIB或IV期鳞状或非鳞状NSCLC。1225例患者按1:1随机分配接受阿替利珠单抗或多西他赛治疗。结果显示,阿替利珠单抗二线治疗HER2突变NSCLC疗效不佳,ORR仅14%,中位PFS仅2.8个月[12]。
HER2与EGFR属于同家族成员,但相关探索显示,不同类型小分子EGFR-TKI在HER2突变NSCLC中均表现不佳。例如NICHE试验显示,阿法替尼在经化疗治疗进展的HER2突变NSCLC中仅展现8%的ORR,中位PFS只有15.9周[13] ,一项前瞻性、多中心、开放标签II期研究中评估了吡咯替尼用于经治HER2突变晚期NSCLC患者的疗效和安全性。结果显示,吡咯替尼组的ORR为30%,中位PFS为6.9个月[14]。其他小分子例如达可替尼在II期研究中的ORR仅约10%[15]。
大分子单克隆抗体在HER2突变NSCLC中也显示较差的疗效。一项多中心、非随机II期研究,前瞻性评估了曲妥珠单抗联合帕妥珠单抗用于经铂类化疗进展后HER2突变晚期NSCLC的疗效。结果显示,帕妥珠单抗+曲妥珠单抗治疗HER2突变NSCLC的ORR为28.9%,中位PFS为6.8个月[16]。总之,既往研究显示传统疗法包括化疗、免疫治疗、小分子TKI、大分子抗体等,在HER2突变NSCLC中的疗效难以令人满意,有效率难以突破30%。
闪耀新星:
德曲妥珠单抗引领HER2 ADC治疗新时代
继靶向/免疫疗法之后,新一代的ADC药物异军突起,成为近年来的闪耀新星。ADC药物能克服传统疗法局限性,集大分子与小分子的特性于一身,协同发挥“精准”靶向作用和“高效” 杀伤肿瘤细胞的作用,真正意义上实现了精准靶向地给予化疗。临床前研究显示,ADC对HER2突变肿瘤细胞有效,随后开展的临床研究亦在不同瘤种取得成功。
在肺癌领域,DESTINY-Lung02是一项多中心、全球化、剂量盲法、非对照II期临床研究,经治HER2突变晚期NSCLC患者按2:1比例随机分配接受5.4mg/kg和6.4mg/kg(Q3W)德曲妥珠单抗。基线特征显示,5.4mg/kg和6.4mg/kg组中亚裔人群分别占比61.8%、60%,分别有73.5%、78%的患者既往接受过PD-1/PD-1单抗,分别有67.6%、62%的患者接受过一线或二线治疗,分别有32.4%、38%的患者既往接受过3线及以上的治疗,基线伴中枢神经系统(CNS)转移患者分别占比34.3%、44%。
最终分析时,5.4mg/kg组和6.4mg/kg组分别有12.9%、12.0%的患者仍在接受德曲妥珠单抗治疗;两组的中位随访时间分别为15.8个月、16.5个月,两剂量组显示出相当的疗效和获益,且更长随访时间时,5.4mg/kg剂量组仍显示出良好的耐受性。疗效数据显示,5.4mg/kg德曲妥珠单抗确认的客观缓解率(ORR)为50%,有2.9%的患者达到完全缓解,有47.1%的患者达到部分缓解,疾病控制率(DCR)为93.1%,中位缓解持续时间(DoR)为12.6个月。5.4mg/kg剂量组的中位无进展生存期(PFS)为10.0个月,中位总生存期(OS)为19个月。结果显示,在经过多线治疗、70%以上患者接受过免疫治疗的情况下,德曲妥珠单抗仍显示出优异的抗肿瘤疗效、良好的耐受性和生存获益
基于DESTINY-Lung02结果,德曲妥珠单抗于2022年获得FDA批准用于HER2突变NSCLC的后线治疗,且获得NCCN/CSCO/ASCO/ESMO指南的持续推荐。
NCCN/CSCO/ASCO/ESMO指南中
HER2突变NSCLC的治疗推荐
HER2突变晚期NSCLC的一线治疗选择主要参考驱动基因阴性患者的治疗方案。在后线治疗领域,基于近两年来DESTINY-Lung系列研究的优异结果,德曲妥珠单抗成为全新的精准靶向治疗方案,并持续获得国内外权威指南的推荐。
在2024版NCCN非小细胞肺癌指南中[17],HER2突变NSCLC一线治疗需要参考“腺癌、大细胞癌、非特指性非小细胞肺癌(NSCLC NOS)和鳞状细胞癌”患者的治疗。HER2突变晚期NSCLC一线治疗进展后的后线方案中,德曲妥珠单抗是截止目前唯一的优选推荐方案。
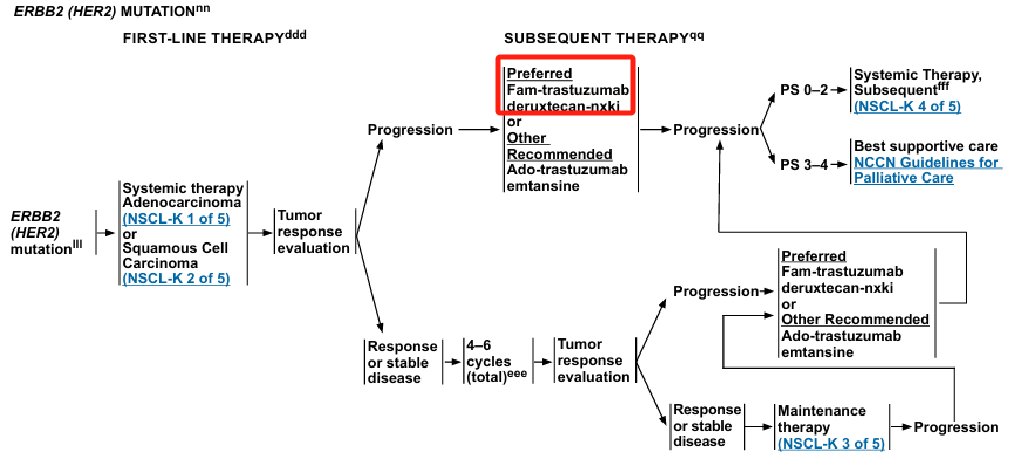 图1 2024版NCCN非小细胞肺癌指南
图1 2024版NCCN非小细胞肺癌指南
在2024版CSCO非小细胞肺癌诊疗指南中[18],HER2突变IV期NSCLC的一线治疗选择无分级推荐,主要参考“无驱动基因NSCLC的一线治疗”。此类患者的后线治疗有分级推荐,其中I级推荐“参考驱动基因阴性患者的后线治疗”; II级推荐只有德曲妥珠单抗,且是目前唯一一种被推荐的ADC药物。
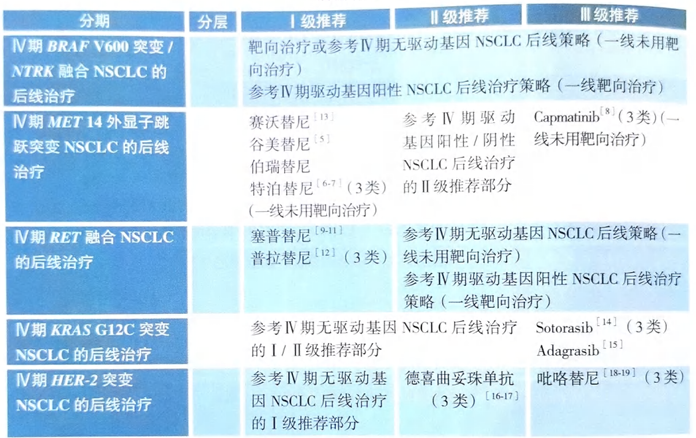 图2 2024版CSCO非小细胞肺癌诊疗指南推荐
图2 2024版CSCO非小细胞肺癌诊疗指南推荐
2023.V3版ASCO驱动基因阳性IV期NSCLC指南显示[19],德曲妥珠单抗是HER2变异IV期NSCLC二线及后线治疗方案中唯一一种治疗推荐(强烈推荐)。指南指出,由于潜在靶点耐药机制的发展,应尽力通过组织和/或血液NGS检测是否存在新的变异。若患者已接受所有靶向治疗,或无可用靶向疗法,临床医生可以参照无驱动变异IV期NSCLC指南给予标准治疗方案。
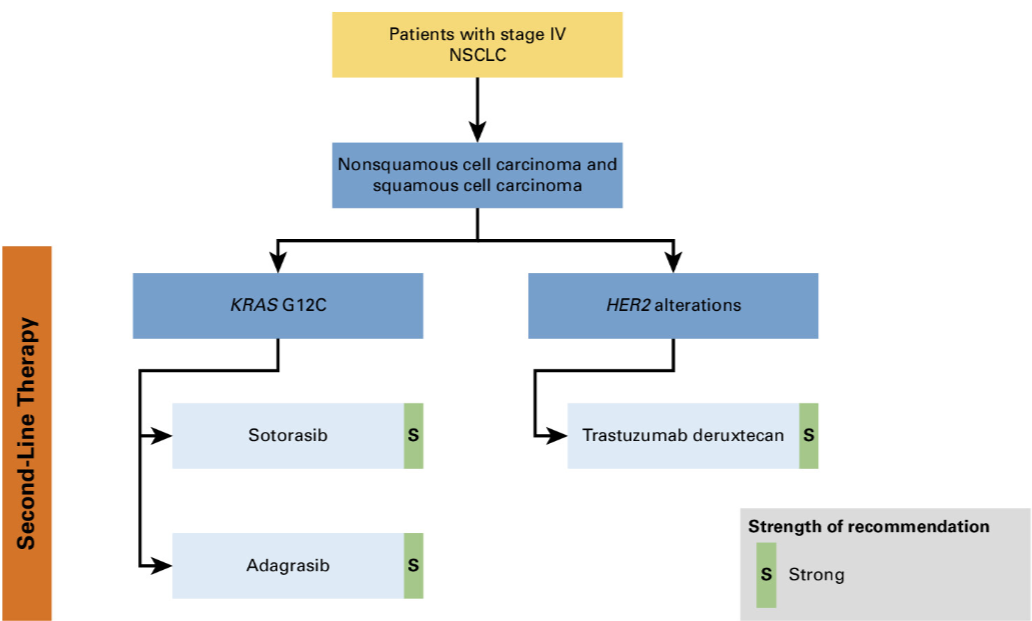 图3 2023版ASCO驱动基因阳性IV期NSCLC指南
图3 2023版ASCO驱动基因阳性IV期NSCLC指南
在2023版ESMO致癌驱动基因转移性NSCLC指南中[20],对于既接受过一线治疗的HER2 20外显子突变患者,如果药物可及,建议给予德曲妥珠单抗。
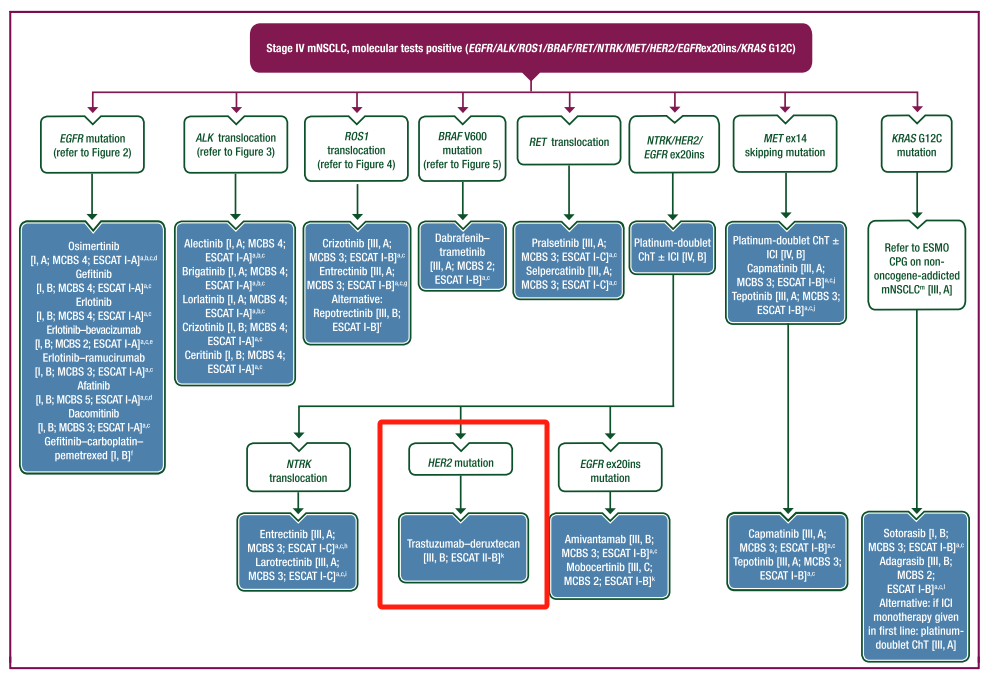 图4 2023版ESMO致癌驱动基因转移性NSCLC指南
图4 2023版ESMO致癌驱动基因转移性NSCLC指南
总结
自HER2突变被发现的近20年来,研究者一直在探索新型的疗法,以期满足HER2突变NSCLC临床上面临的治疗需求。遗憾的是,随着研究的推进,人们逐渐认识到HER2突变NSCLC不同于其他瘤种,更加难治;既往传统疗法均难以在NSCLC中发挥抗肿瘤作用。研究者采用独特设计开发出了新一代ADC药物,在各个肿瘤领域相继取得优异结果,亦为HER2突变NSCLC带来首次重大突破,开启了此类NSCLC治疗的新纪元。期待未来德曲妥珠单抗在NSCLC不同治疗领域更多研究结果的公布,为临床应用提供丰富循证依据,造福更多肺癌患者。
[1]Stephens P, Hunter C, Bignell G, et al. Lung cancer: intragenic ERBB2 kinase mutations in tumours. Nature. 2004 Sep 30;431(7008):525-6. doi: 10.1038/431525b. PMID: 15457249 10.1158/1078-0432.CCR-12-0912
[2]Wang SE, Narasanna A, Perez-Torres M, Xiang B, Wu FY, Yang S, et al HER2 kinase domain mutation results in constitutive phosphorylation and activation of HER2 and EGFR and resistance to EGFR tyrosine kinase inhibitors. Cancer Cell 2006;10:25–38.
[3]Perera SA, Li D, Shimamura T, Raso MG, Ji H, Chen L, et al HER2YVMA drives rapid development of adenosquamous lung tumors in mice that are sensitive to BIBW2992 and rapamycin combination therapy. Proc Natl Acad Sci U S A 2009;106:474–9.
[4]Shimamura T, Ji H, Minami Y, Thomas RK, Lowell AM, Shah K, et al Non-small-cell lung cancer and Ba/F3 transformed cells harboring the ERBB2 G776insV_G/C mutation are sensitive to the dual-specific epidermal growth factor receptor and ERBB2 inhibitor HKI-272. Cancer Res 2006;66:6487–91.
[5]Offin M, Feldman D, Ni A, et al. Frequency and outcomes of brain metastases in patients with HER2-mutant lung cancers. Cancer. 2019 Dec 15;125(24):4380-4387. doi: 10.1002/cncr.32461. Epub 2019 Aug 30. PMID: 31469421; PMCID: PMC6891113.
[6]Trastuzumab Deruxtecan in Asian Patients With Human Epidermal Growth Factor Receptor 2 (HER2; ERBB2)-Mutant Metastatic Non–Small Cell Lung Cancer: Subgroup Analysis of DESTINY-Lung02. 2023 ESMO ASIA
[7]Jebbink M, et al. Cancer Treat Rev, 2020, 86:101996
[8]Si X, Pan R, Ma S, et al. Genomic characteristics of driver genes in Chinese patients with non-small cell lung cancer. Thorac Cancer. 2021 Feb;12(3):357-363. doi: 10.1111/1759-7714.13757. Epub 2020 Dec 9. PMID: 33300283; PMCID: PMC7862783.
[9]郑荣寿等. 中华肿瘤杂志,2024,46(03):221-231.
[10]Garon EB, et al. Lancet. 2014;384(9944):665-673
[11]Ren S, Wang J, Ying J, et al. Consensus for HER2 alterations testing in non-small-cell lung cancer. ESMO Open. 2022 Feb;7(1):100395. doi: 10.1016/j.esmoop.2022.100395. Epub 2022 Feb 8. Erratum in: ESMO Open. 2022 Jun;7(3):100482. PMID: 35149428; PMCID: PMC8844658.
[12]Rittmeyer A, et al. Lancet. 2017;389(10066):255-265.
[13]Dziadziuszko, R. Smit, E.F. Dafni, U.et al. Afatinib in NSCLC with HER2Mutations: Results of the Prospective, Open-Label Phase II NICHE Trial of European Thoracic Oncology Platform (ETOP). J. Thorac. Oncol. 2019, 14, 1086–1094.
[14]Zhou C, et al. Journal of Clinical Oncology, 2020, 38(24): 2753-2761.
[15]Kris, M.G. Camidge, D.R. Giaccone, G.et al.Targeting HER2 aberrations as actionable drivers in lung cancers: Phase II trial of the pan-HER tyrosine kinase inhibitor dacomitinib in patients with HER2-mutant or amplified tumors. Ann. Oncol. 2015, 26, 1421–1427.
[16]Mazieres J, et al. Journal of Clinical Oncology, 2022, 40(7): 719-728.
[17]NCCN Non-Small Cell Lung Cancer Version 8.2024-August 23, 2024
[18]24版CSCO非小细胞肺癌诊疗指南
[19]Ishmael A. Jaiyesimi et al., Therapy for Stage IV Non–Small Cell Lung Cancer With Driver Alterations: ASCO Living Guideline, Version 2023.3. JCO 42, e1-e22(2024).DOI:10.1200/JCO.23.02744
[20]Oncogene-addicted metastatic non-small-cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-upHendriks, L.E. et al.Annals of Oncology, Volume 34, Issue 4, 339 - 357
排版编辑:肿瘤资讯-Ale











 苏公网安备32059002004080号
苏公网安备32059002004080号


