颈段食管癌的发病较为少见,约占食管癌总体的5%。颈段食管癌毗邻诸多重要的颈部解剖结构,从器官保留的角度考虑,根治性放化疗(dCRT)是目前治疗颈段食管癌的首选方案。然而dCRT治疗疗效并不令人满意,远期生存率仅30%左右。此次分享一例局部晚期颈段食管鳞癌患者采用免疫联合化疗筛选治疗2个周期后达到显著缓解,接受dCRT后采用免疫维持治疗并获得长期临床完全缓解(cCR)的病例。
患者基本情况及入院检查
◆ 患者,男,71岁,2023年1月因“进食梗阻”就诊。外院病理示鳞状细胞癌;外院PET-CT:C7-T4椎体水平段食管壁增厚伴条块灶,FDG代谢异常增高,考虑食管癌伴管腔狭窄,局部累及外膜;左锁骨上窝、纵隔主动脉弓下增大淋巴结,FDG代谢异常增高,考虑转移。
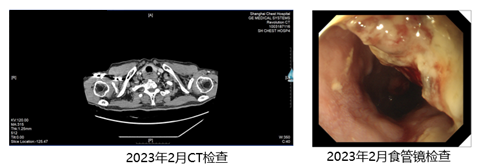
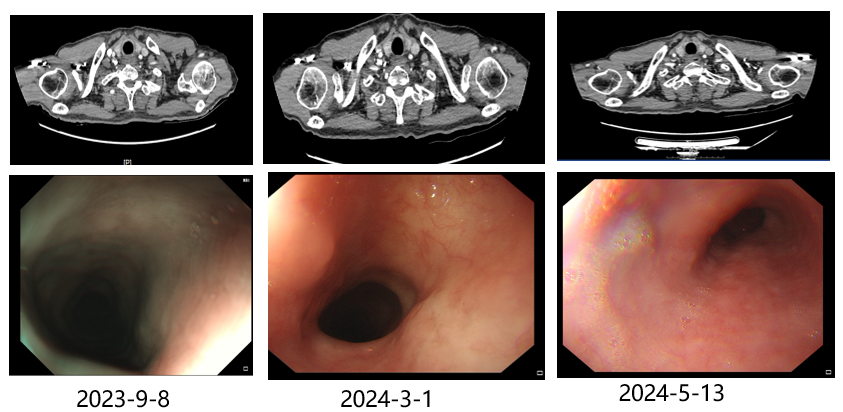
◆ 2023年2月我院CT示:食管上段管壁增厚,管腔狭窄,两侧颈部未见明显肿大淋巴结;食管镜检查示:食管距门齿17~25cm见新生物,占2/3周,不规则隆起,中央溃疡,接触性出血。
◆ 临床分期:cT3N1M0,III期。
治疗过程
◆ 患者颈段食管癌诊断明确,符合本中心开展的“免疫联合化疗诱导后筛选分层治疗局限期颈段食管鳞癌的II期多中心干预性研究”入组条件,经与患者及家属沟通后同意入组。
◆ 2023年2月15日、2023年3月8日分别行2次新辅助免疫联合化疗,具体为替雷利珠单抗200mg d1联合白蛋白紫杉醇148mg d1, d8, d15+卡铂 515mg d1, q3w。
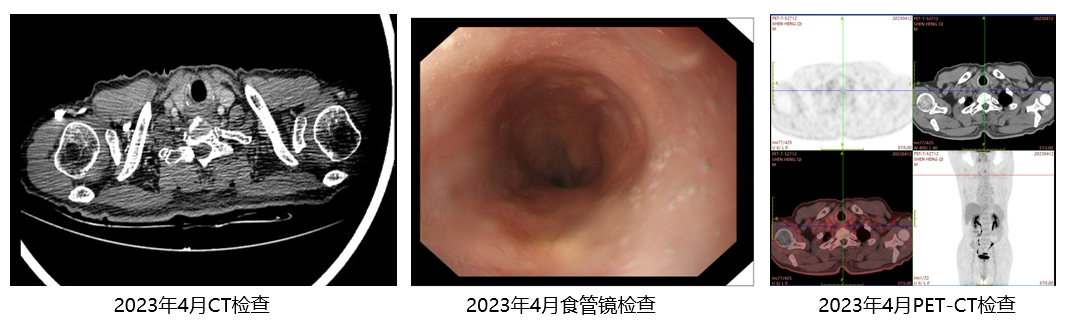
◆ 2023年4月13日CT:双侧颈部未见明显肿大淋巴结,颈部CT增强扫描未见明显异常。食管上段癌,较前范围缩小;食管镜报告:原肿瘤基本消退,未见明显残留病灶;PET CT示:治疗后改变,管壁略增厚,局部FDG代谢轻度增高,较前病灶范围明显缩小。
◆ 临床评价为显著缓解(RR),拟行根治性同步放化疗
◆ 2023年4月24日起,对双锁骨上区+食管病灶+中上纵隔行IMRT放疗, 1.8Gy*28fr,分别于4月27日、5月6日、5月13日、5月20日行周方案TC(力朴素+CBP)方案静脉滴注化疗;因末次化疗骨髓抑制明显,5月20日化疗减量。
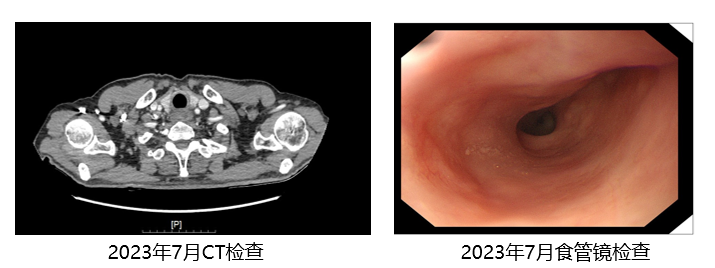
◆ 2023年7月3日CT报告:未见明显异常,食管镜报告:符合内科治疗后改变,疗效评价持续显著缓解(RR)。
◆ 2023年7月4日起至2024年5月27日止,给予替雷利珠单抗免疫维持治疗,200mg q3w,共行15个周期,免疫治疗满1年后停止治疗,目前患者规律随访中。
本期特邀专家——李春光 教授
医学博士 ,上海市胸科医院 副主任医师
兼任上海市中西医结合学会胸外科专业委员 青年委员
中华胸部外科电子杂志青年编委,擅长食管癌、肺部结节的外科治疗
主持国家级课题1项、省部级课题1项,获得上海市医苑新星青年人才项目资助
以第一作者或通讯发表SCI论文20篇,累计影响因子超过80分,参编著作1本
专家点评
颈段食管是指从食管入口到胸骨切迹的一段食管,长约5cm。位于颈段食管的恶性肿瘤即为颈段食管癌,病理类型以鳞状细胞癌为主[1]。单纯的颈段食管癌并不多见,其范围往往延伸侵犯下咽或胸上段食管。由于其所处解剖位置复杂,加之颈部淋巴的引流丰富,颈段食管癌易发生淋巴结转移,因此大部分颈段食管癌患者在就诊时已处于局部晚期[2]。从保留器官的角度考虑,国内外指南均推荐颈段食管癌进行根治性放化疗(dCRT),但颈段食管癌的总体预后仍不理想,长期生存率仅30%左右[3-5]。此外,dCRT后局部控制失败率很高,挽救性手术的实施难度大、术后并发症多,患者的生活质量不尽如人意[6]。
随着外科微创技术的进步,使得越来越多的颈段食管癌患者可以接受微创手术和保喉手术。回顾性研究发现,以手术为中心的综合治疗模式的优化可显著改善颈段食管癌的生存获益[7],这提示外科手术在颈段食管癌的治疗方面仍有一席之地。
我们认为,局部晚期颈段食管癌的治疗不应是“一刀切“的治疗模式,更应该根据患者实际情况、肿瘤特性来区别对待,选择个体化的治疗方案,既保证患者良好的远期生存,又兼顾其生活质量。免疫治疗在晚期转移性食管鳞癌中取得令人欣喜的疗效,极大推动了其向食管癌围术期的应用。为此,我院牵头发起了一项”免疫联合化疗诱导后筛选分层治疗局限期颈段食管鳞癌的II期多中心干预性研究“,旨在探索化免诱导筛选分层策略的有效性和安全性。
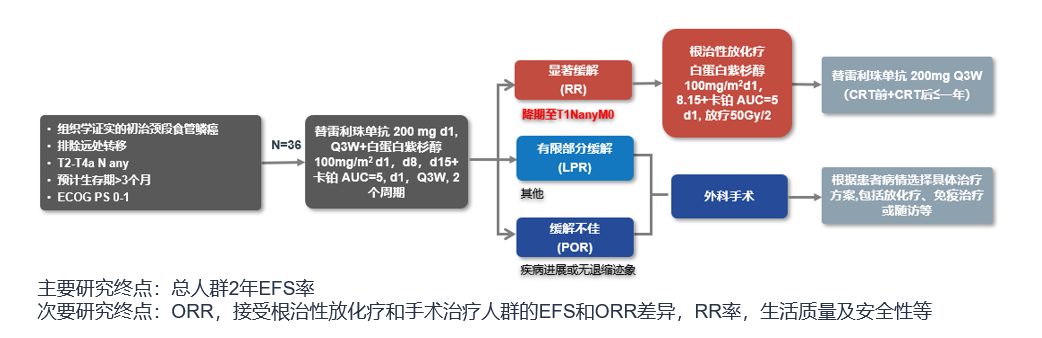
该研究计划纳入36例未经治疗的颈段食管癌患者,分期为T2-4aNanyM0,诱导治疗方案为替雷利珠单抗(200mg d1,Q3W)联合白蛋白紫杉醇(100mg/m2 d1, d8, d15, Q3W)和卡铂(AUC=5 d1,Q3W),共2个周期。治疗完成后进行疗效评估,对于肿瘤退缩至T1达到显著缓解(RR)的患者,继续接受dCRT序贯免疫维持治疗,对于有限缓解(LPR)或缓解不佳(POR)的患者,及时给予手术治疗,术后由主诊医生确定辅助治疗方案。研究主要终点为总人群2年无事件发生率,次要终点包括客观缓解率、总生存期、生活质量及安全性等。研究于2022年7月启动,截至2024年9月,已完成40例患者的入组,目前仍在生存随访中。
本项研究设计颇具匠心:1)诱导及巩固治疗方案选择:本研究采用替雷利珠单抗联合化疗作为诱导治疗方案、替雷利珠单抗作为dCRT后巩固方案,可充分其发挥高效缩瘤,安全耐受性高的优势。在RATIONALE-306研究中,替雷利珠联合化疗在晚期转移性食管鳞癌一线治疗中实现超长生存获益。全球人群中位总生存(mOS)17.2个月,中位无进展生存(mPFS)达7.3个月,客观缓解率(ORR)较化疗提高21.2%[8]。RATIONALE-302研究也证实,替雷利珠单抗单药在晚期食管癌二线治疗中疗效不俗,安全性良好[9]。2)放疗剂量选择:尽管多项研究支持,50.4Gy放疗与61.2Gy放疗的治疗疗效相当,但有部分诊疗中心仍采用61.2Gy放疗作为局部晚期不可手术患者的根治性治疗剂量,高剂量照射后组织黏连、水肿严重,复发后挽救性手术难度和风险大大提升。出于联合免疫治疗的安全性考虑,本研究的放射治疗按照50.4Gy/1.8Gy剂量实施,很好地平衡了根治性放疗的疗效和挽救性手术开展的安全性。3)外科手术的及时干预及个性化的辅助治疗:对于化免诱导治疗未达到理想退缩状态的患者,及时手术有助于降低患者的肿瘤负荷,避免放化疗无效带来肿瘤进展的风险。同时,根据术后病理情况和患者自身耐受情况,考虑给予术后辅助放疗或联合其他药物治疗。希望通过本研究的探索,为局部进展期颈段食管癌的个体化治疗提供更多循证依据。
[1] Lee DJ, Harris A, Gillette A, et al. Carcinoma of the cervical esophagus: diagnosis, management, and results. South Med J, 1984,
77(11): 1365-1367.
[2] Ajani JA, D'Amico TA, Bentrem DJ, et al. Esophageal and esophagogastric junction cancers, version 2. 2019, NCCN clinical
practice guidelines in oncology. J Natl Compr Canc Netw, 2019,
17(7): 855-883.
[3] Burmeister BH, Dickie G, Smithers BM, et al. Thirty-four patients
with carcinoma of the cervical esophagus treated with chemoradiation therapy. Arch Otolaryngol Head Neck Surg, 2000, 126(2): 205-208.
[4]Yamada K, Murakami M, Okamoto Y, et al. Treatment results of
radiotherapy for carcinoma of the cervical esophagus. Acta Oncol,
2006, 45(8): 1120-1125.
[5]Huang SH, Lockwood G, Brierley J, et al. Effect of concurrent high-dose cisplatin chemotherapy and conformal radiotherapy on cervical esophageal cancer survival. Int J Radiat Oncol Biol Phys,
2008, 71(3): 735-740.
[6] Takebayashi K, Tsubosa Y, Kamijo T, et al. Comparison of Salvage Total Pharyngolaryngectomy and Cervical Esophagectomy Between Hypopharyngeal Cancer and Cervical Esophageal Cancer. Ann Surg Oncol. 2017 Mar;24(3):778-784.
[7]Xu L, Chen XK, Xie HN, et al. Treatment and Prognosis of Resectable Cervical Esophageal Cancer: A Population-Based Study. Ann Thorac Surg. 2022 Jun;113(6):1873-1881.
[8] XU J, KATO K, RAYMOND E, et al. Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first-line treatment for advanced or metastatic oesophageal squamous cell carcinoma (RATIONALE-306): a global, randomised, placebo-controlled, phase 3 study. Lancet Oncol, 2023, 24(5): 483-95.
[9] SHEN L, KATO K, KIM S B, et al. Tislelizumab Versus Chemotherapy as Second-Line Treatment for Advanced or Metastatic Esophageal Squamous Cell Carcinoma (RATIONALE-302): A Randomized Phase III Study. J Clin Oncol 2022;40(26): 3065-76.
排版编辑:肿瘤资讯-高惠
下期预告
肠癌后线RAS野生型患者经过替雷利珠单抗联合西妥昔单抗和伊立替康治疗后达到PR,疗效明确
往期回顾:
【食管癌】有一种爱,是我陪你一起抗癌:一例晚期食管鳞癌患者多线免疫治疗病例分享
【食管癌】局部晚期不可手术切除食管鳞癌经放化疗联合替雷利珠单抗治疗后成功转化手术并获得长期生存病例
【食管癌】替雷利珠单抗联合同步放化疗为不可手术的局部晚期食管鳞癌老年患者带来新希望
【食管癌】局部晚期不可切除食管鳞癌患者接受替雷利珠单抗联合治疗,生存获益超过20个月
【食管癌】基于PRO评估后局部晚期食管鳞癌患者术前免疫联合短程放化疗新辅助治疗,OS超过21个月











 苏公网安备32059002004080号
苏公网安备32059002004080号


