2024年欧洲肿瘤内科学会(ESMO)年会已经顺利落下帷幕,多项肿瘤领域重磅研究公布,为临床实践带来最新风向标。部分研究还于《新英格兰医学杂志》(NEJM)同期发表,体现了研究重要性。【肿瘤资讯】特将这些同期发表的消化道肿瘤相关研究进行分享。
TOPGEAR:可切除胃癌,围手术期化疗 vs 化放疗孰优孰劣?
2024年ESMO会议公布了TOPGEAR研究最终结果。既往MAGIC、FLOT4等研究证实围手术期化疗的作用,而INT0116、CRITICS等研究显示术后化放疗(CRT)较单纯手术改善患者生存。那么将术前CRT加入围手术期化疗是否可改善胃癌患者生存?TOPGEAR Ⅲ期研究带来循证证据。
研究入组ⅠB~ⅢC期可切除胃或胃食管结合部(GOJ)腺癌患者,随机接受围手术期化疗或术前CRT及术后化疗。主要终点是总生存(OS)(图1)。
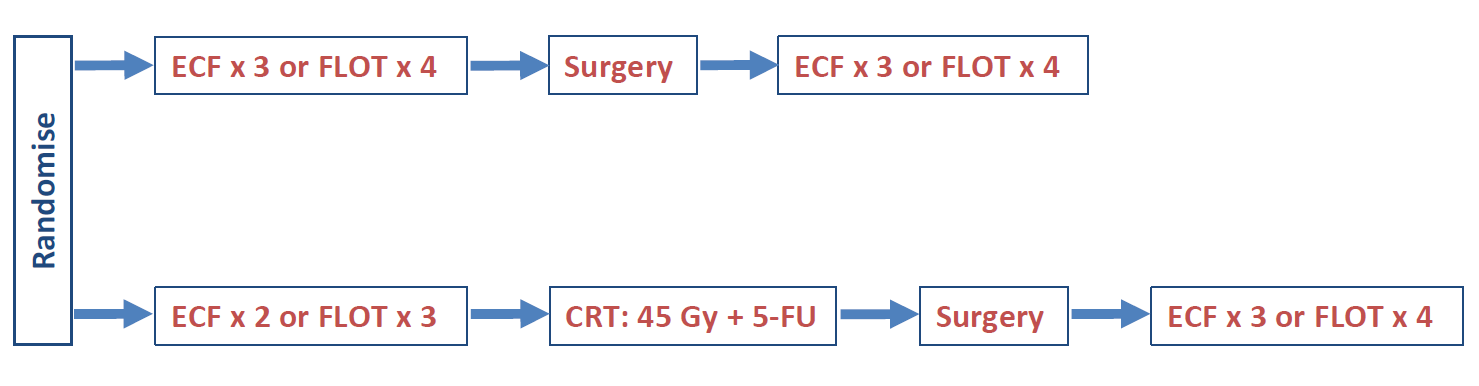
共574例患者随机,术前CRT组和围手术期化疗组分别是286例和288例。结果显示术前CRT显著提高病理完全缓解(pCR)率,两组分别是16.8% vs 8.0%(P<0.0001)。但是两组OS无显著差异,分别是46.4个月 vs 49.4个月,5年OS率分别是44.4% vs 45.7%(图2)。两组中位无进展生存期(PFS)分别是31.4个月 vs 31.8个月,5年PFS率分别是39.7% vs 40.1%。血液学和胃肠道毒性以及手术并发症发生率类似。
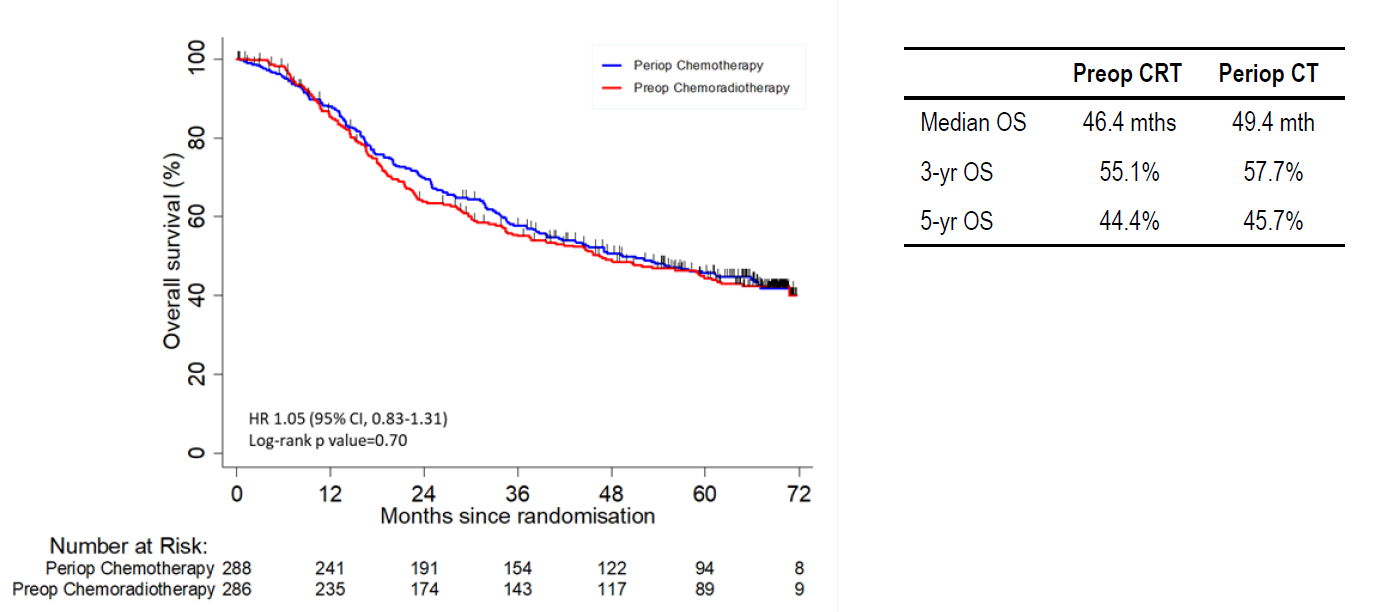
TOPGEAR研究显示术前CRT可增加pCR率和肿瘤降期,但是未改善OS,不影响根治性切除率,也不增加毒性或手术并发症。因此临床中,可以根据患者治疗目标进行方案选择。
NEJM同期发表研究结果和ESMO会议公布结果数据一致,但增加更多研究细节。具体可以移步官网阅读(图3):https://www.nejm.org/doi/full/10.1056/NEJMoa2405195

KEYNOTE-811公布最终生存结果,夯实HER2+胃癌靶免治疗地位
KEYNOTE-811研究探索了免疫治疗加入曲妥珠单抗+化疗治疗HER2+胃癌的表现。基于前期分析结果,帕博利珠单抗的加入可显著改善PD-L1 CPS≥1患者的客观缓解率(ORR,74% vs 52%)和PFS(10.8个月 vs 7.2个月,HR 0.70)。因此,帕博利珠单抗联合曲妥珠单抗和化疗已经获批成为PD-L1阳性HER2+晚期胃癌的一线治疗。
2024年ESMO会议公布最终OS结果,确立抗HER2治疗联合免疫治疗在HER2+胃癌一线治疗中的作用。研究显示意向治疗(ITT)人群中,帕博利珠单抗组和安慰剂组的中位OS分别是20.0个月 vs 16.8个月(HR 0.80,P=0.0040),中位PFS分别是10.0个月 vs 8.1个月(HR 0.73),ORR分别是72.6% vs 60.1%。CPS≥1的患者中,两组中位OS分别是20.1个月 vs 15.7个月(HR 0.79),中位PFS分别是10.9个月 vs 7.3个月(HR 0.72),ORR分别是73.2% vs 58.4%(图4)。
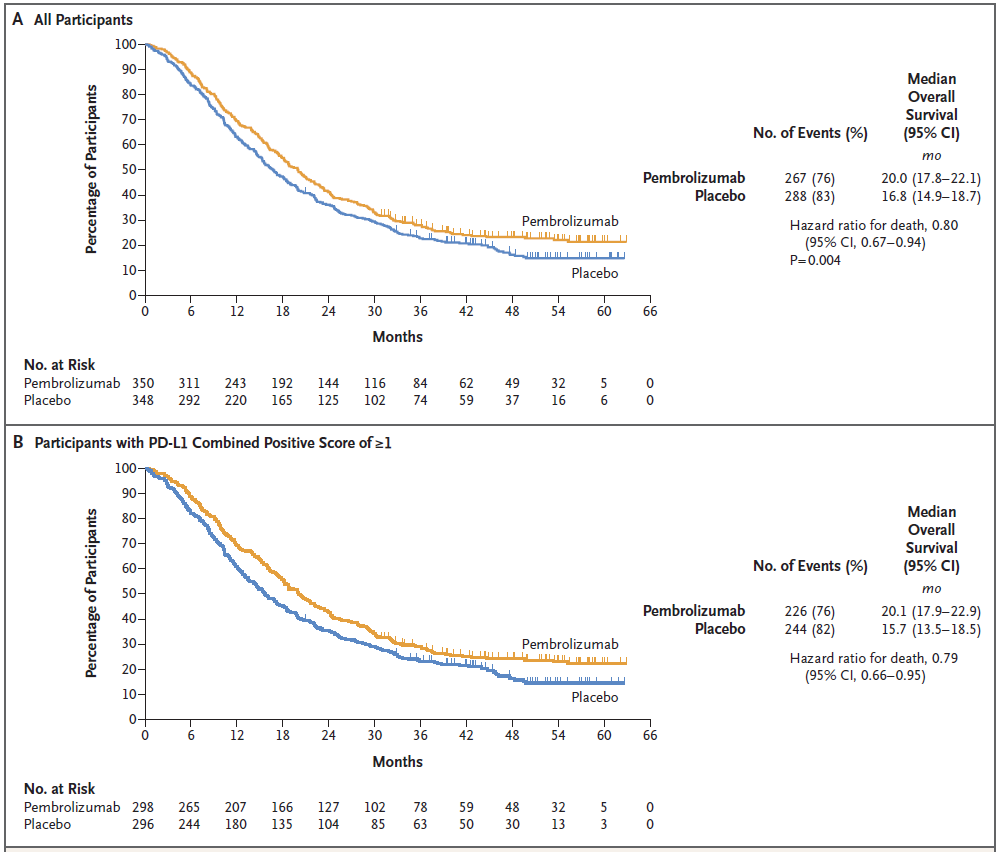
因此,帕博利珠单抗的加入为HER2+患者带来有统计学意义及临床意义的OS改善,进一步确定了免疫治疗在此类患者中的作用。
研究同期在NEJM以通讯形式发表(图5),研究详情见:https://www.nejm.org/doi/full/10.1056/NEJMc2408121

联合分析证实Zolbetuximab在CLDN18.2+胃癌中的作用
Claudin 18.2(CLDN18.2)是胃癌中的新兴靶点。SPOTLIGHT和GLOW研究均证实抗CLDN18.2药物Zolbetuximab的作用。2024年ESMO会议公布了SPOTLIGHT和GLOW研究联合分析结果。
结果显示Zolbetuximab依旧可带来PFS(9.2个月 vs 8.2个月,HR 0.71)和OS(16.4个月 vs 13.7个月,HR 0.77)的显著改善(图6)。
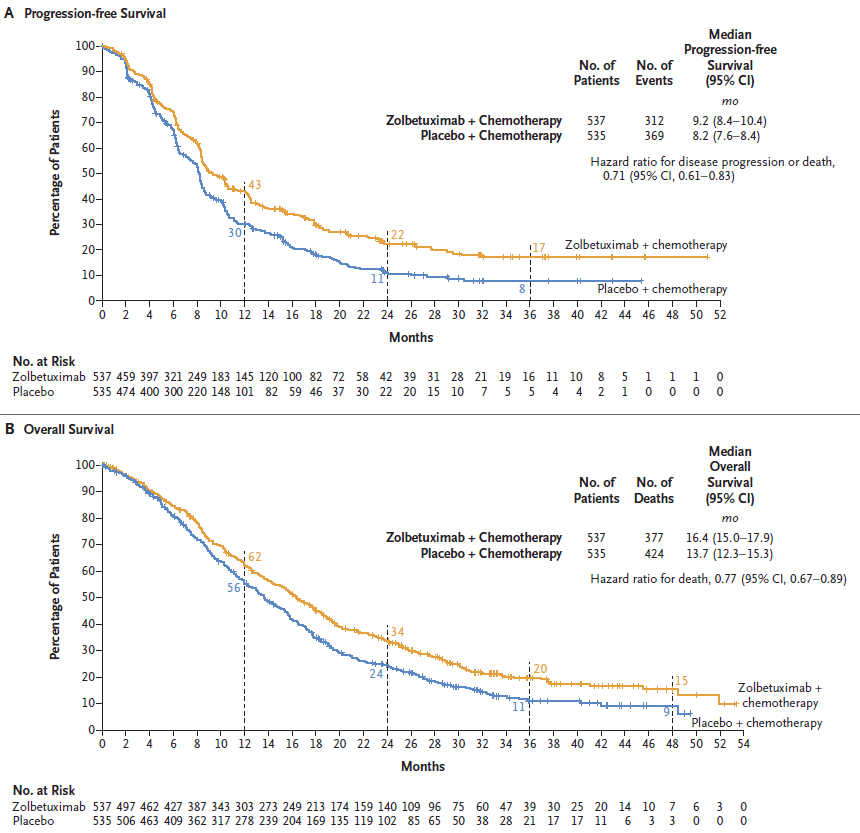
因此,Zolbetuximab联合化疗可显著改善CLDN18.2+、HER2-胃癌患者的结局,应作为此类患者的标准一线治疗。
研究同期在NEJM以通讯形式发表(图7),研究详情见:https://www.nejm.org/doi/full/10.1056/NEJMc2409512

图7. Zolbetuximab联合分析发表于NEJM
CABINET数据更新:再证卡博替尼治疗神经内分泌肿瘤的有效性
CABINET是一项探索卡博替尼治疗经治胰腺外(epNET)和胰腺神经内分泌肿瘤(pNET)患者疗效的Ⅲ期研究。2023年ESMO会议公布了研究PFS结果,本次会议中数据进行更新。
结果显示epNET队列中,卡博替尼和安慰剂组的中位PFS分别是8.4个月 vs 3.9个月(HR 0.38,P<0.0001),中位OS分别是21.9个月 vs 19.7个月(HR 0.86),ORR分别是5% vs 0(图8);pNET队列中,两组中位PFS分别是13.8个月 vs 4.4个月(HR 0.23,P<0.0001),中位OS分别是40.0个月 vs 31.1个月(HR 0.95),ORR分别是19% vs 0(图9)。
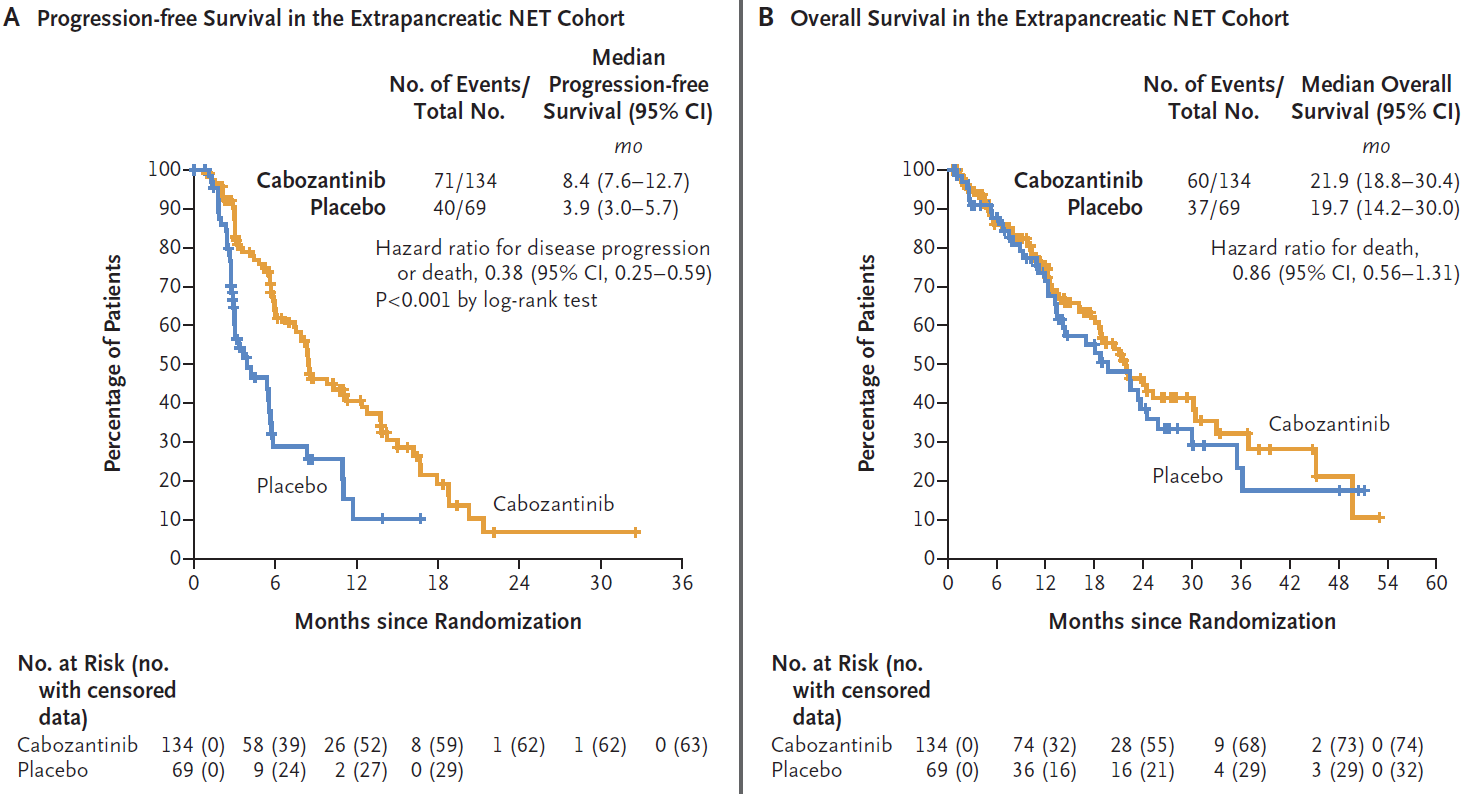
图8. epNET患者疗效(A)PFS;(B)OS
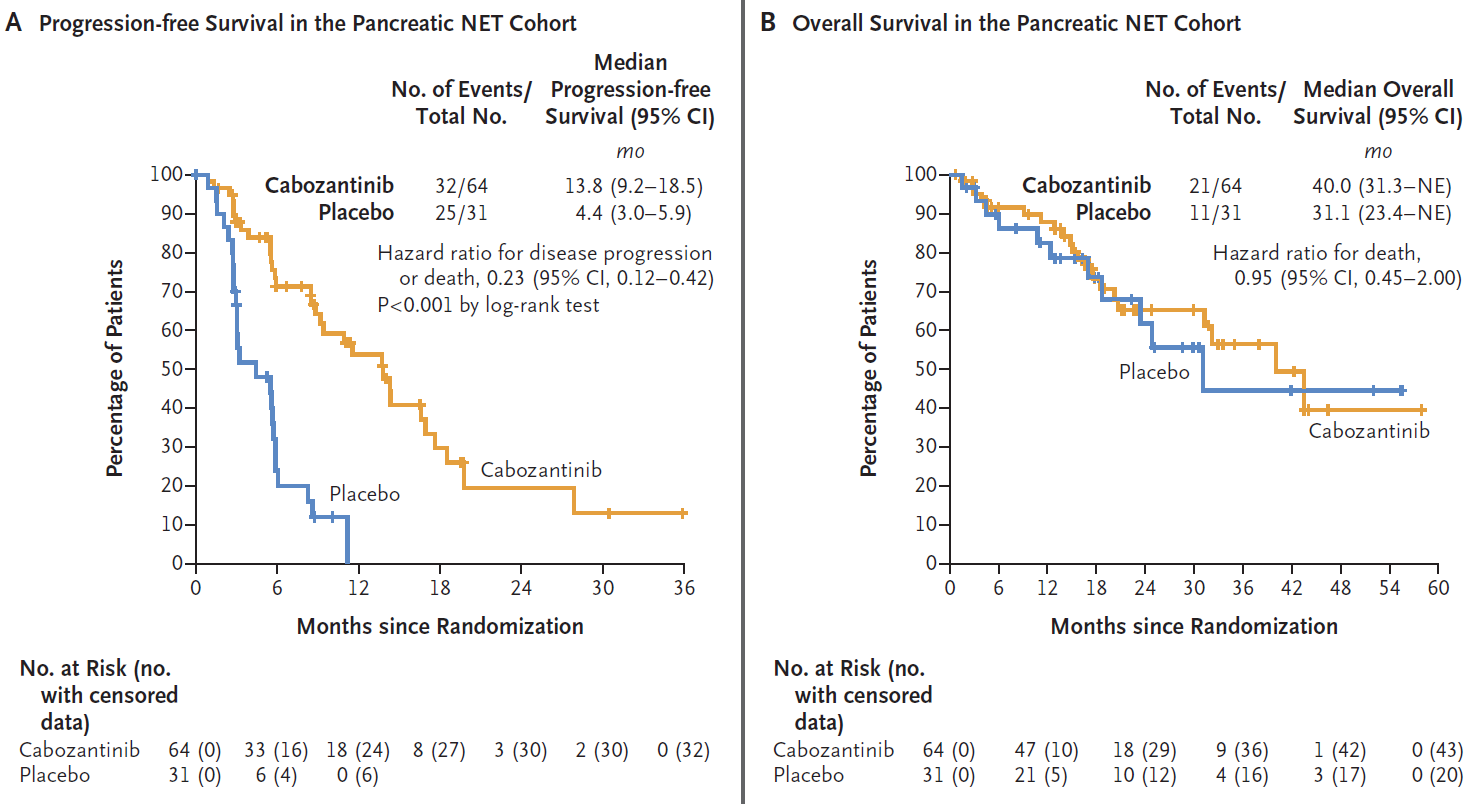
图9. pNET患者疗效(A)PFS;(B)OS
研究是首个评估在肽受体放射性核素疗法和/或靶向治疗后患者中药物疗效的随机对照研究之一,证实卡博替尼是经治NET患者的新兴有效治疗选择。目前研究全文已经在NEJM发表,可在官网查看(图10):https://www.nejm.org/doi/full/10.1056/NEJMoa2403991

Ponsegromab——治疗恶病质的成功GDF-15抗体
恶病质是临床中极为棘手的癌症并发症,有研究显示生长分化因子15(GDF-15)在其发病中起到重要作用。Ponsegromab是一种强力高选择性抑制GDF-15的单克隆抗体。2024年ESMO公布了Ponsegromab治疗癌症恶病质的随机Ⅱ期研究结果。
恶病质定义为6个月内体重下降>5%(如果BMI<20 kg/m2则2%)。研究纳入具有恶病质的非小细胞肺癌、胰腺癌或结直肠癌患者,随机接受不同剂量的Ponsegromab或安慰剂治疗。结果显示Ponsegromab显著增加12周体重,100 mg、200 mg、400 mg剂量组的安慰剂调整中位体重增加分别是1.33 kg、2.08 kg和3.00 kg(图11)。400 mg剂量组较安慰剂将12周体重增加超过5%。药物整体安全性良好,不良事件发生率和安慰剂组类似。
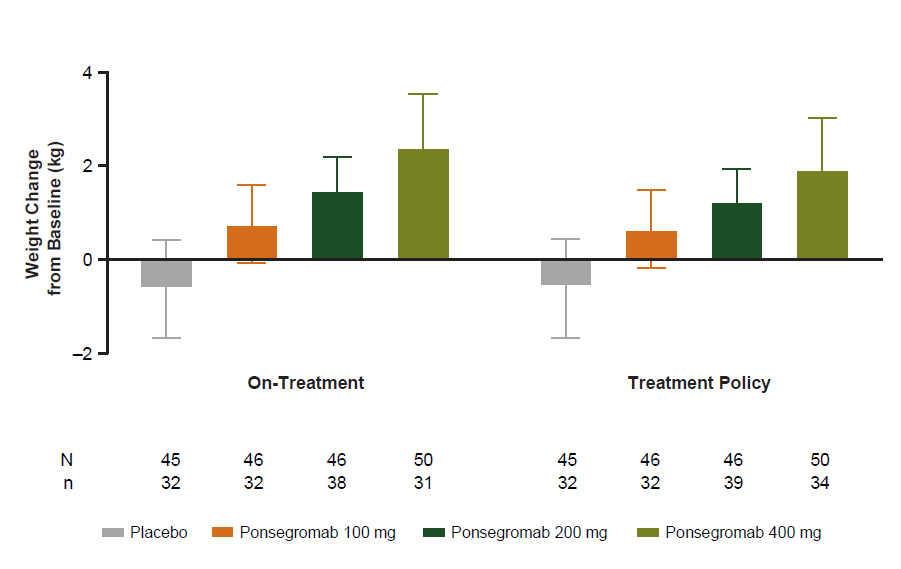
研究显示Ponsegromab可改善体重,食欲和恶病质症状,体力活动,骨骼肌量,安全性类似于安慰剂。恶病质终于迎来有效治疗药物。
目前研究全文已发表于NEJM(图12),详情可见:https://www.nejm.org/doi/full/10.1056/NEJMoa2409515

图12. Ponsegromab研究发表于NEJM
[1] Leong T, et al. A randomized phase III trial of perioperative chemotherapy (periop CT) with or without preoperative chemoradiotherapy (preop CRT) for resectable gastric cancer (AGITG TOPGEAR): Final results from an intergroup trial of AGITG, TROG, EORTC and CCTG. 2024 ESMO LBA58.
[2] Leong T, et al. Preoperative Chemoradiotherapy for Resectable Gastric Cancer. N Engl J Med. 2024 Sep 14.
[3] Lonardi S, et al. Final overall survival for the phase III, KEYNOTE-811 study of pembrolizumab plus trastuzumab and chemotherapy for HER2+ advanced, unresectable or metastatic G/GEJ adenocarcinoma. 2024 ESMO 1400O.
[4] Janjigian YY, et al. Pembrolizumab in HER2-Positive Gastric Cancer. N Engl J Med. 2024 Sep 14.
[5] Kang YK, et al. First-line (1L) zolbetuximab + chemotherapy in patients (pts) with claudin 18.2 (CLDN18.2) +, HER2-, locally advanced (LA) unresectable or metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma: A pooled final analysis of SPOTLIGHT + GLOW. 2024 ESMO 1438P.
[6] Shitara K, et al. Zolbetuximab in Gastric or Gastroesophageal Junction Adenocarcinoma. N Engl J Med. 2024 Sep 16.
[7] Chan J, et al. Cabozantinib versus placebo for advanced neuroendocrine tumors (NET) after progression on prior therapy (CABINET Trial/Alliance A021602): Updated results including progression free-survival (PFS) by blinded independent central review (BICR) and subgroup analyses. 2024 ESMO 1141O.
[8] Chan JA, et al. Phase 3 Trial of Cabozantinib to Treat Advanced Neuroendocrine Tumors. N Engl J Med. 2024 Sep 16.
[9] Crawford J, et al. Efficacy and safety of ponsegromab, a first-in-class, monoclonal antibody inhibitor of growth differentiation factor 15, in patients with cancer cachexia: A randomized, placebo-controlled, phase II study. 2024 ESMO LBA82.
[10] Groarke JD, et al. Ponsegromab for the Treatment of Cancer Cachexia. N Engl J Med. 2024 Sep 14.
排版编辑:肿瘤资讯-HYF











 苏公网安备32059002004080号
苏公网安备32059002004080号


