激素受体阳性(HR+)的Luminal型患者是乳腺癌中最常见的分子亚型,其中,对于HR+/HER2低表达的晚期患者,目前已经形成了CDK4/6抑制剂联合内分泌治疗的标准治疗模式。然而,对于一线CDK4/6抑制剂治疗失败的患者,虽然有多种治疗方案可选,但患者获益都较为有限,未能形成标准治疗模式。2024年4月,随着DESTINY-Breast06研究重磅报阳,这类患者终于迎来了全新的治疗选择。【肿瘤资讯】特别邀请到来自辽宁省肿瘤医院的孙涛教授,就2024 ASCO 乳腺癌领域更新内容进行深度解读,并就乳腺癌诊疗的未来进行展望。
特邀专家
辽宁省肿瘤医院乳腺内科主任、博导
国务院特殊津贴专家、二级教授
辽宁青年名医
中国临床肿瘤学会(CSCO)乳腺癌专委会 常委
中国临床肿瘤学会(CSCO)肿瘤心脏病学专委会 副主委
中国抗癌协会肿瘤异质性与个体化治疗专委会 副主委
中国抗癌协会肿瘤标志物专委会 副主委
中国抗癌协会肿瘤靶向治疗专业委员会 常委
中国抗癌协会多发和不明原发肿瘤专委会 常委
中国医药教育协会乳腺疾病专业委员会 副主委
中国研究型医院精准医学与肿瘤MDT专委会 副主委
辽宁省抗癌协会肿瘤标志物专委会 主任委员
辽宁省抗癌协会化疗专委会 (候任)主任委员
辽宁省药学会抗肿瘤药物专业委员会 主任委员
辽宁省药学药物临床评价研究专业委员会 副主委
后CDK4/6抑制剂时代,
HER2将成为突破口?
此前,在乳腺癌的分子分型中,通常将HER2划分为阳性(IHC 3+或IHC2+/ISH+)或阴性(IHC 2+/ISH-,IHC 1+或IHC 0)两类情况,基于此划定了HR+、HER2+以及三阴型三大分型。其中,对于HER2阳性、阴性的划分主要旨在提示患者对于曲妥珠单抗的治疗是否敏感。对于HR+患者,IHC 2+/ISH-和IHC 1+通常按照HER2阴性划分为HR+/HER2-,这类患者是内分泌治疗的获益人群。
然而,对于接受一线或二线内分泌治疗后进展的晚期HR+患者,考虑患者已经对多种内分泌治疗耐药,如果不存在其他可以指导治疗的基因改变(如PIK3CA突变),那么通常只可选择化疗药物,如卡培他滨、紫杉醇或白蛋白结合型紫杉醇等,这类方案为患者带来的获益较为有限。尽管一些研究显示了CDK4/6抑制剂经治患者跨线使用CDK4/6抑制剂仍能带来PFS获益,例如2024年ASCO大会中报告的postMONARCH研究便显示,CDK4/6抑制剂跨线联合氟维司群可延长患者PFS,但中位PFS为6.0个月,较对照组仅延长0.7个月,获益仍较为有限,亟需探索更有效的治疗方案。
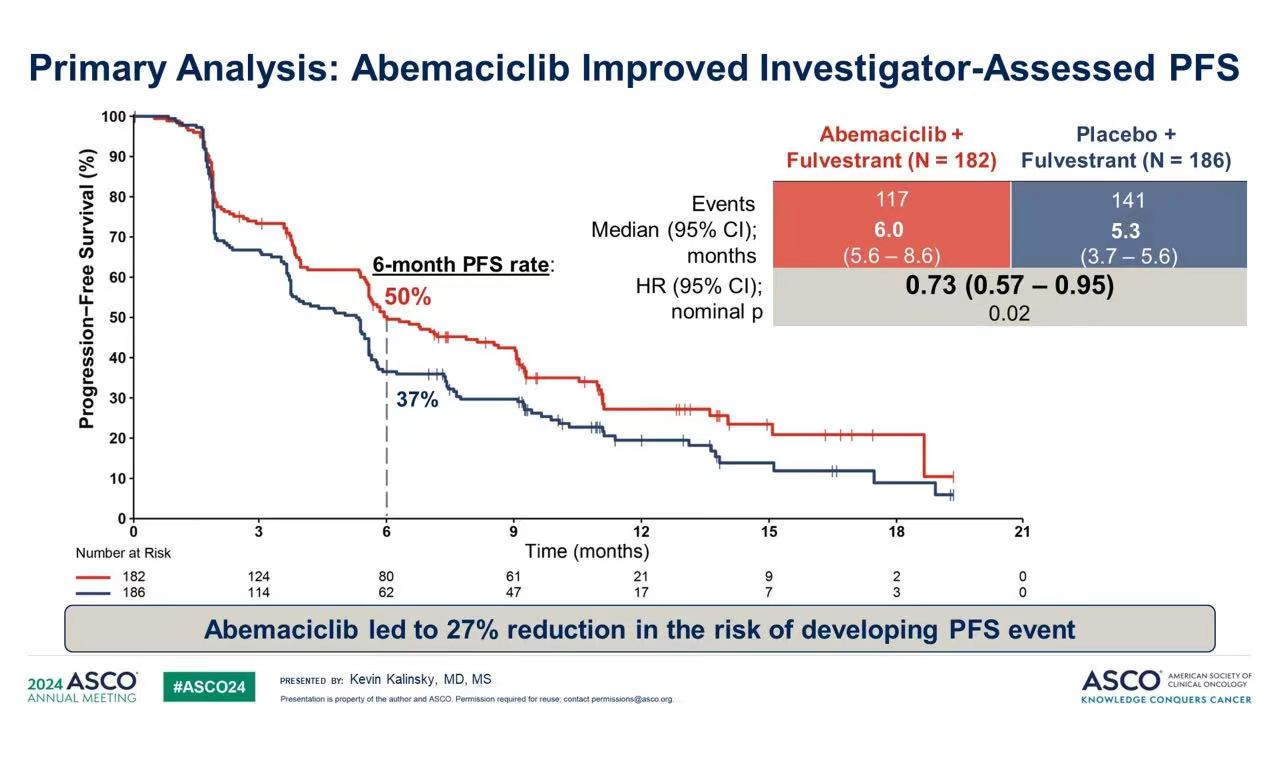 图1.postMONARCH研究主要分析PFS曲线
图1.postMONARCH研究主要分析PFS曲线
靶向HER2的抗体偶联药物(ADC)的发展带来了转机,德曲妥珠单抗(DS-8201,T-DXd)在DESTINY-Breast04研究中,针对HER2低表达的晚期乳腺癌患者(无论患者HR表达状态),对比医生选择的化疗方案带来了无进展生存期(PFS)和总生存期(OS)的改善,基于此,2024年4月更新的《CSCO乳腺癌诊疗指南》中,正式将HER2低表达列入独立章节,并推荐德曲妥珠单抗作为HR+/HER2低表达患者晚期一线治疗后的优选方案。
上周成功报阳的DESTINY-Breast06研究则再次为ADC在HER2低表达患者中的应用增添了重要的循证,并再次将应用范围扩展至HER2超低表达(IHC 0伴有膜染色:即IHC >0且IHC<1+)。
DESTINY-Breast06:
再次突破HER2的“边界线”
DESTINY-Breast06 是一项全球性、随机、开放标签的 III 期试验,旨在评估德曲妥珠单抗 (5.4 mg/kg) 与研究者选择的化疗(卡培他滨、紫杉醇或白蛋白结合型紫杉醇,TPC)对 HR 阳性/HER2 低表达(IHC 1+ 或 2+/ISH-)及 HER2超低表达(IHC 0伴有膜染色:即IHC >0且ICH<1+)的晚期或转移性乳腺癌患者的疗效和安全性研究纳入未曾接受过晚期阶段化疗,且在开始使用内分泌疗法联合CDK4/6抑制剂一线治疗后6个月内病情进展,或在晚期阶段接受过至少两线内分泌治疗的患者。
研究设置的主要终点是由盲法独立中央审查 (BICR) 评估的HR +/HER2 低表达人群的 PFS,关键次要终点包括 HER2 低表达患者的 OS 以及意向治疗人群(包含HER2低表达和 HER2超低表达)中由 BICR评估的 PFS 以及OS。其他次要终点则包括客观缓解率(ORR)、缓解持续时间(DoR)、首次后续治疗或死亡时间、第二次后续治疗或死亡时间以及安全性。
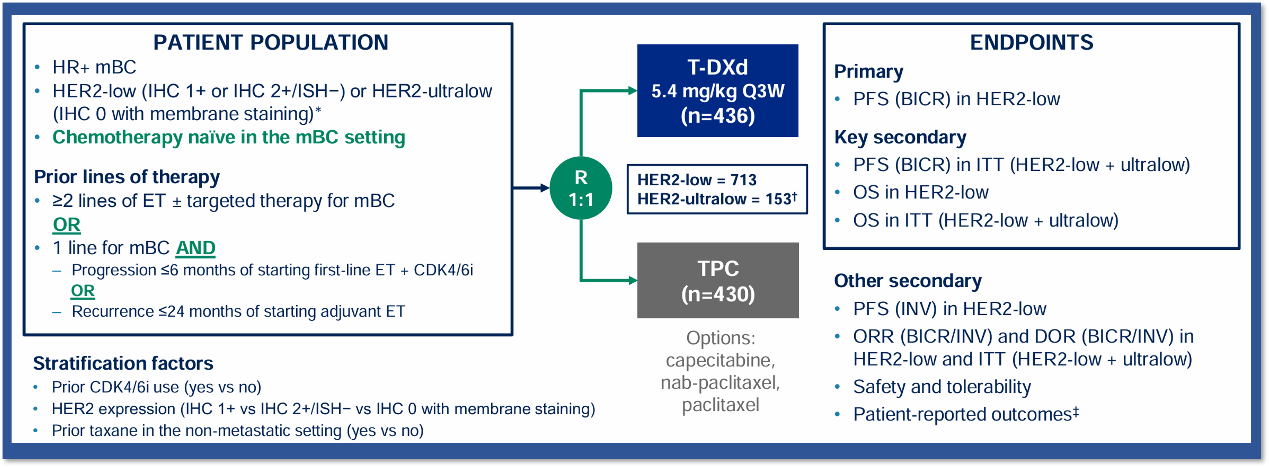 图2. DESTINY-Breast06研究设计
图2. DESTINY-Breast06研究设计
研究总计纳入了来自亚洲、欧洲、北美和南美多个中心的866名患者(HER2低表达组 713 名,HER2超低表达组 153 名),其中65%的患者既往接受两线内分泌治疗后进展,接近20%的患者在一线内分泌治疗后进展。
研究结果显示,对比标准化疗,德曲妥珠单抗的治疗提供了前所未有的疗效,数据截止2024年3月18日,ITT人群的中位随访时间为18.2个月,HER2低表达患者中德曲妥珠单抗组的中位PFS达到了13.2个月,对比TPC组的8.1个月改善了5.1个月,降低了38%的疾病进展或死亡风险(HR 0.62,95%CI 0.51-0.74;P<0.0001),显示出具有临床意义和统计学意义的PFS改善;在总体人群中,德曲妥珠单抗组的中位PFS同样达到了13.2个月,较TPC组的8.1个月改善了5.1个月,降低了37%的疾病进展或死亡风险(HR 0.63,95%CI 0.53-0.75;P<0.0001),同样显示出具有临床意义和统计学意义的PFS改善。
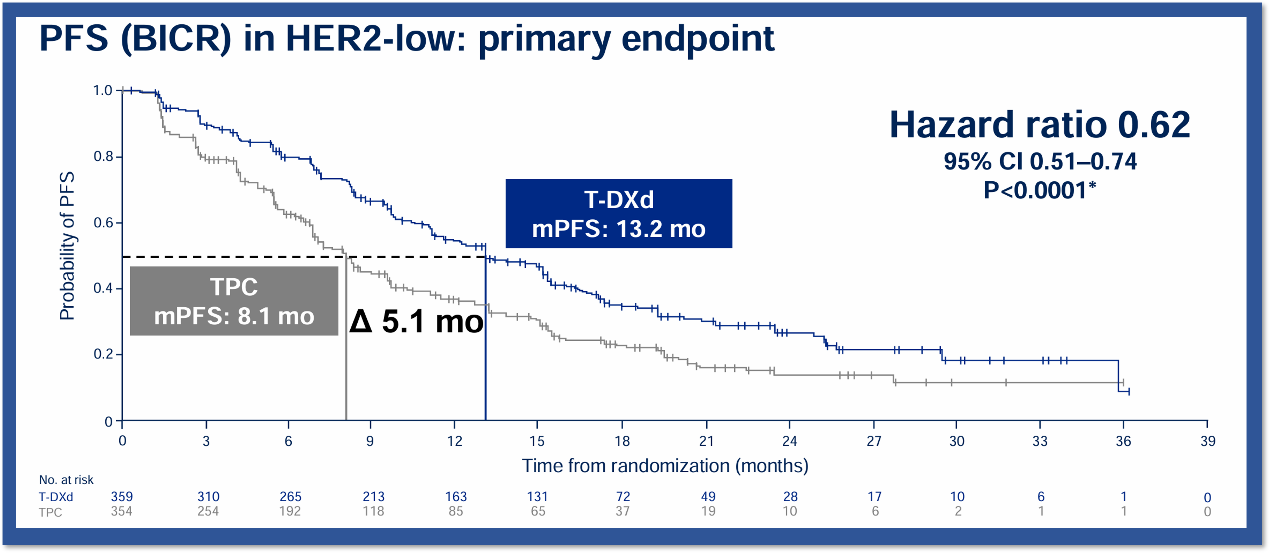 图3. DESTINY-Breast06研究中HER2低表达人群PFS
图3. DESTINY-Breast06研究中HER2低表达人群PFS
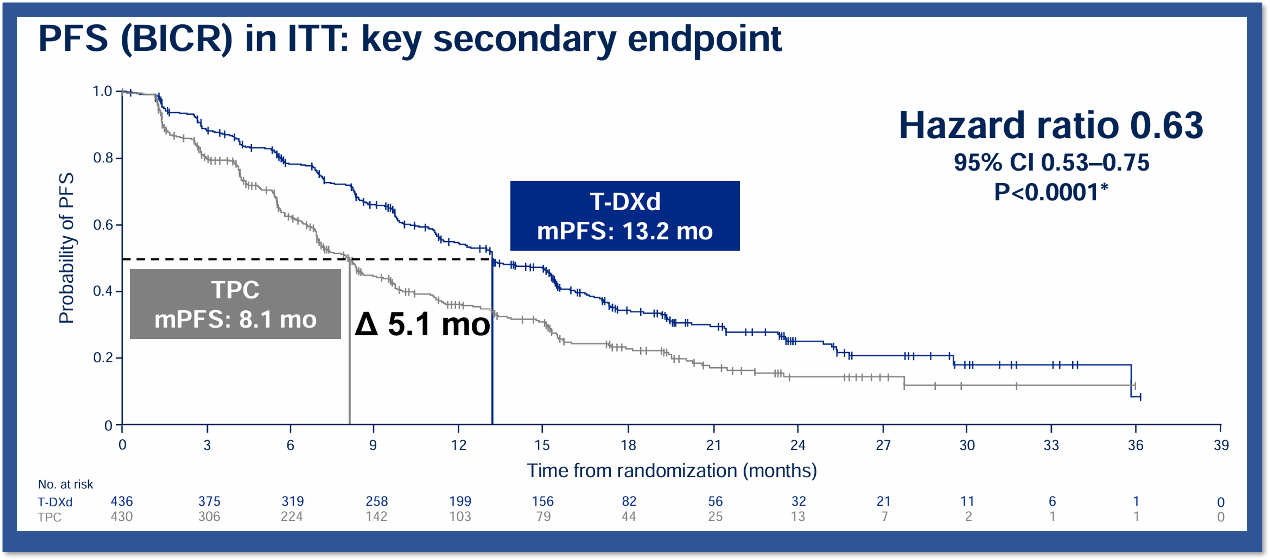 图4. DESTINY-Breast06研究中ITT人群PFS
图4. DESTINY-Breast06研究中ITT人群PFS
OS方面,在HER2低表达及总体人群中,德曲妥珠单抗组的1年OS率分别为87.6%和87.0%,对比TPC组降低了17%和19%的死亡风险。
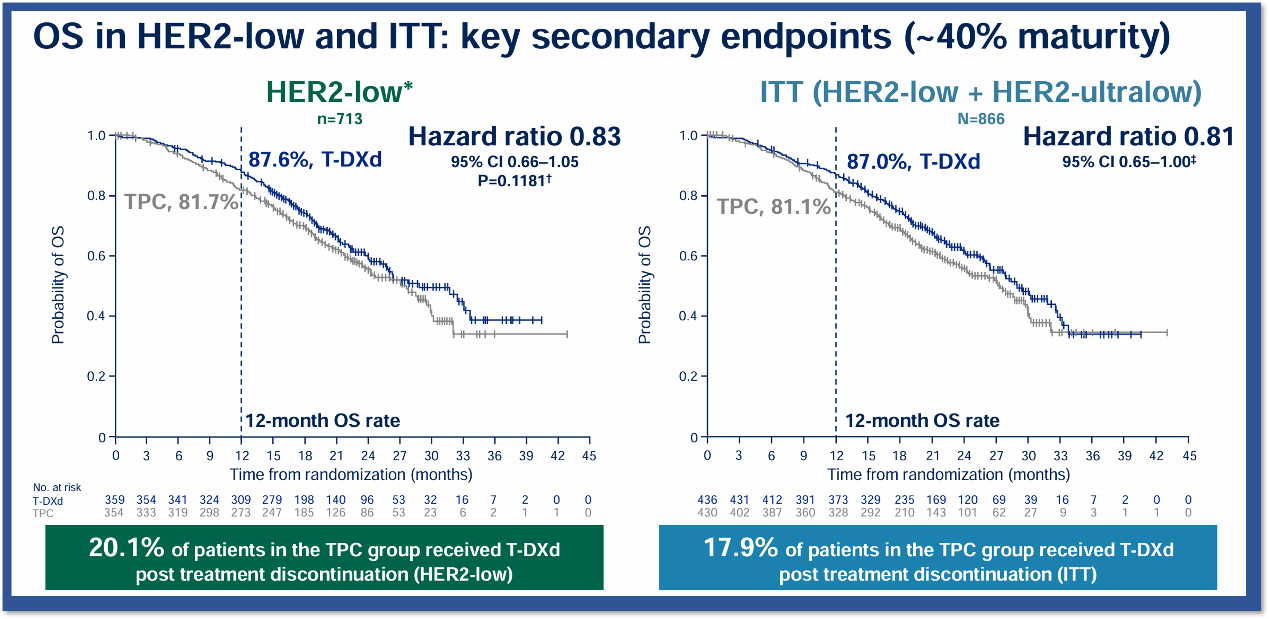
图5.DESTINY-Breast06研究中HER2低表达人群和ITT人群的OS曲线
而在HER2超低表达患者中,德曲妥珠单抗对比TPC显示出与在HER2低表达患者中一致的PFS获益,中位PFS达到13.2个月,对比提高了4.9个月(HR 0.78,95%CI 0.50-1.21)。
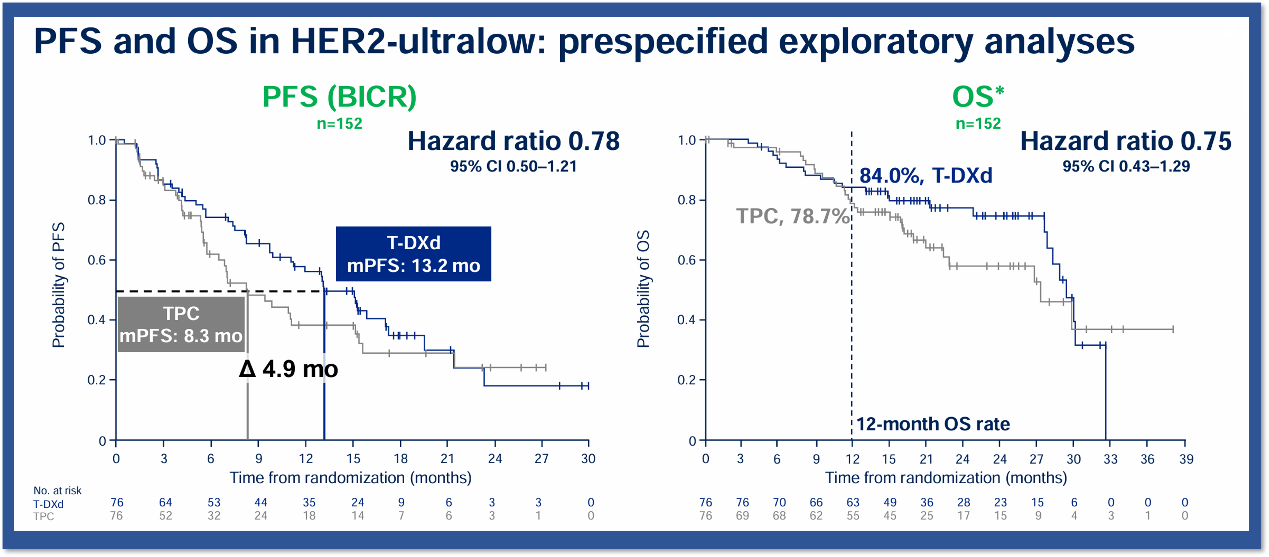 图6. DESTINY-Breast06研究中HER2极低表达人群PFS及OS曲线
图6. DESTINY-Breast06研究中HER2极低表达人群PFS及OS曲线
HER2低表达患者中的亚组分析如下图所示:
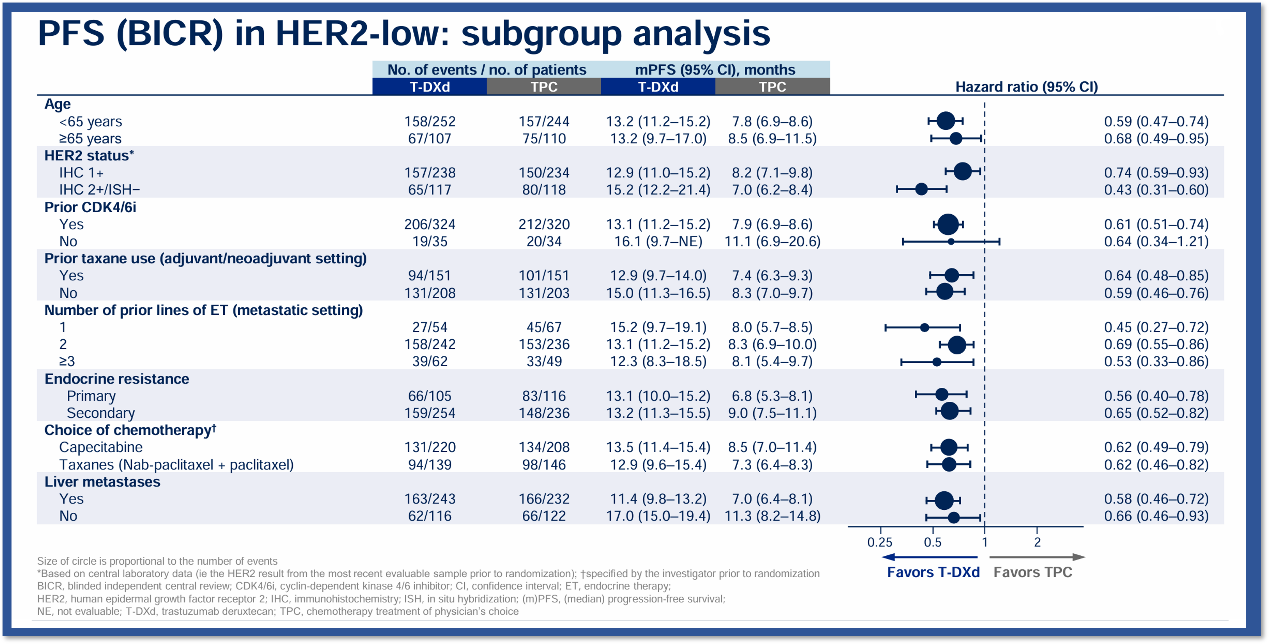 图7. DESTINY-Breast06研究中HER2低表达人群亚组分析
图7. DESTINY-Breast06研究中HER2低表达人群亚组分析
肿瘤缓解方面,总体人群中,德曲妥珠单抗组和TPC组的ORR分别为57.3%和31.2%,HER2低表达患者中则为56.5%和32.2%,HER2超低表达患者中则为61.8%和26.3%。
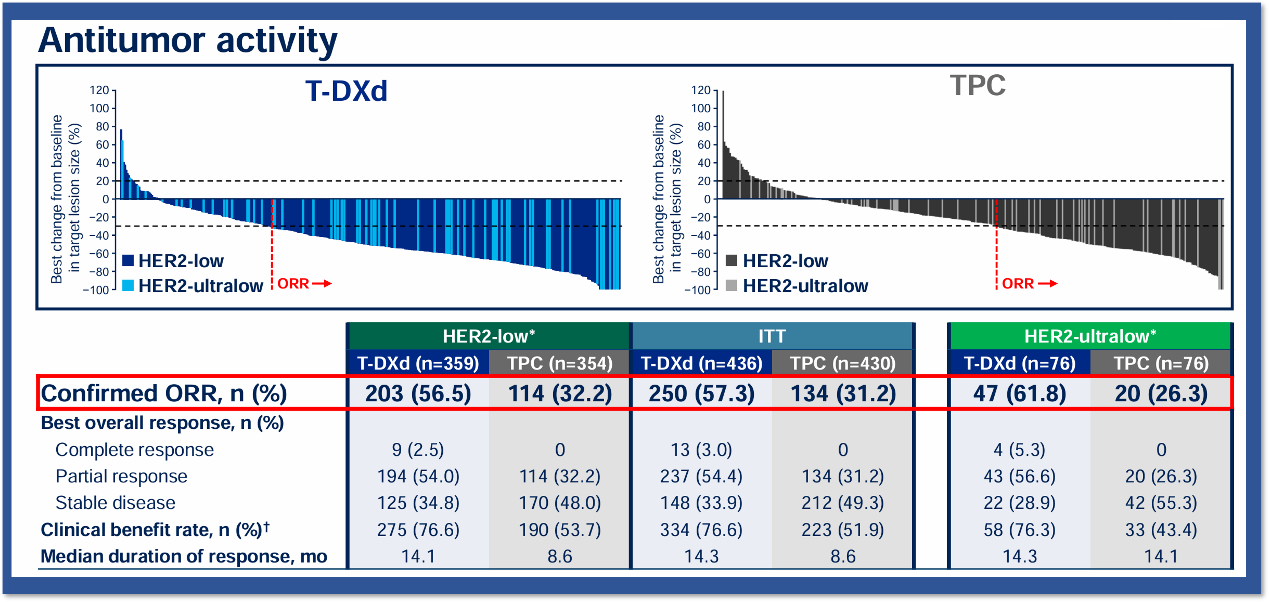 图8. DESTINY-Breast06研究中肿瘤缓解表现
图8. DESTINY-Breast06研究中肿瘤缓解表现
总体安全性表现如下图所示,德曲妥珠单抗组和TPC组≥3级治疗相关的不良反应发生率分别为40.6%和31.4%,严重不良反应发生率分别为20.3%和16.1%。
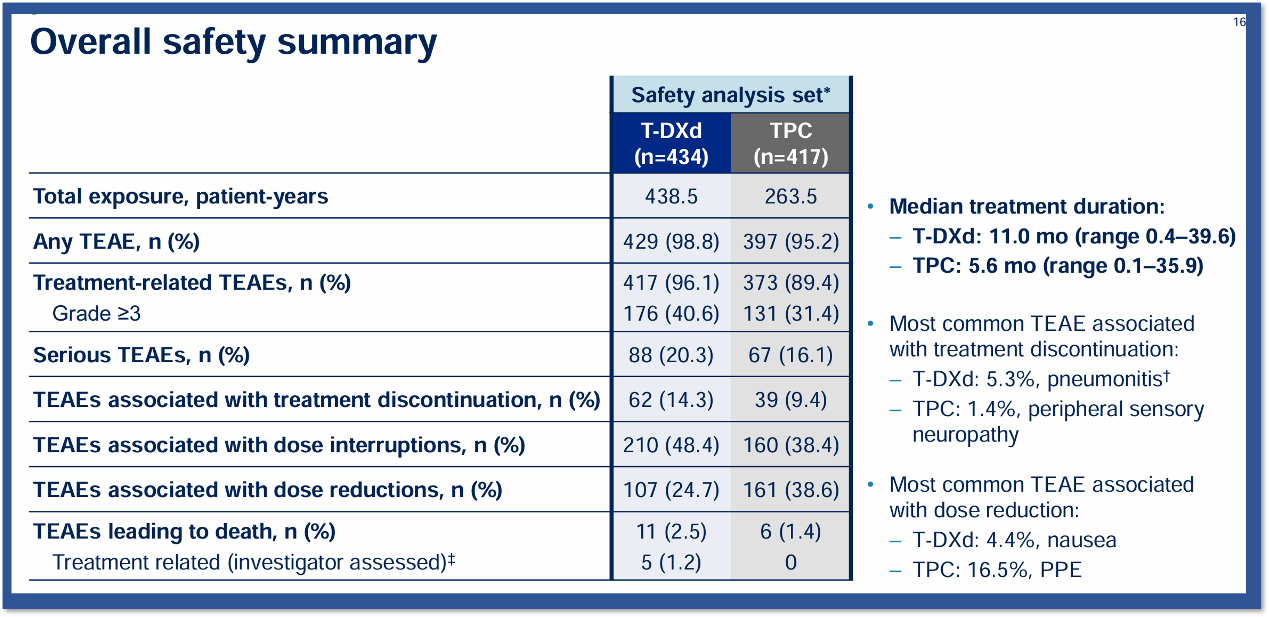 图9. DESTINY-Breast06研究中总体安全性表现
图9. DESTINY-Breast06研究中总体安全性表现
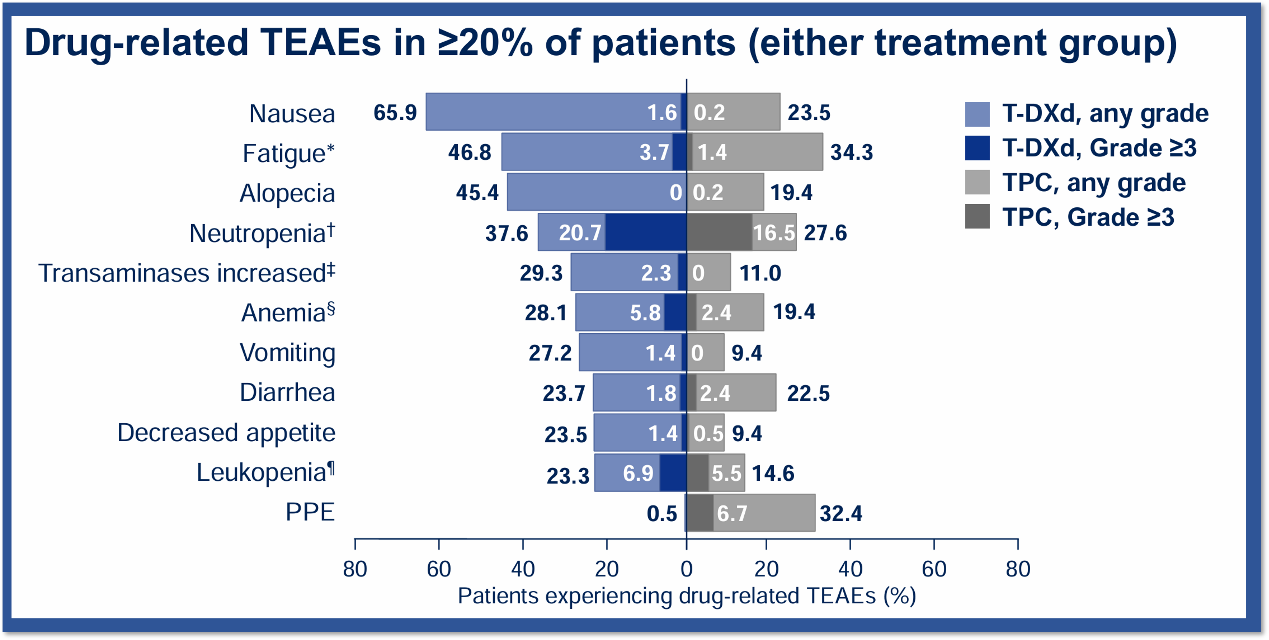 图10. DESTINY-Breast06研究中发生率≥20%的药物相关不良反应
图10. DESTINY-Breast06研究中发生率≥20%的药物相关不良反应
基于这一结果,德曲妥珠单抗也成为了首个且唯一证实在至少一线标准内分泌治疗进展的HR+/HER2低表达和HER2超低表达患者中疗效显著优于化疗的ADC。研究结果在为HR+/HER2低表达患者中进一步支持德曲妥珠单抗作为内分泌治疗进展后的治疗选择的同时,也进一步细分出了HER2超低表达患者,这一在临床实践中占比不低的特殊人群,并提示了对于这部分患者带来的获益。德曲妥珠单抗再次拓展了抗HER2治疗的边界线,持续拓宽着在HER2表达(IHC >0)人群中的疗效,也让人更加期待其未来更多的临床探索。
“命运”延续,下一曲从何而起?
DB06研究表明:T-DXd再次探索HER2低表达的下限,并持续拓宽在HER2表达(IHC>0)人群中的获益边界,有望取代化疗,成为≥1线标准内分泌治疗进展的HR+/HER2低表达和HER2-ultralow晚期乳腺癌的优选方案。也让人更加期待其未来更多的临床研究。
排版编辑:肿瘤资讯-Ale











 苏公网安备32059002004080号
苏公网安备32059002004080号


