2024美国临床肿瘤学会(ASCO)年会已圆满落幕。在肺癌领域,抗体偶联药物(ADC)相关重磅研究进展尤为引人注目。基于DESTINY-Lung02研究结果,德曲妥珠单抗(DS-8201,T-DXd)惊艳问世,并开创了HER2(ERBB2)突变晚期NSCLC患者治疗的新时代,今年ASCO大会上DESTINY-Lung02最终分析结果为德曲妥珠单抗(DS-8201,T-DXd)的卓越疗效再次提供新证据。基于已取得的优异结果,未来德曲妥珠单抗(DS-8201,T-DXd)将布局更多临床研究。
【肿瘤资讯】特邀深圳市人民医院许瑞莲教授解读ADC发展以及德曲妥珠单抗(DS-8201,T-DXd)的最新进展和未来方向。
专家简介
深圳市人民医院肿瘤内科主任、深圳市肿瘤研究所副所长
中国医药教育协会腹部肿瘤医学综合康复分会 副主任委员
中国医师协会结直肠肿瘤专业委员会内科治疗专业委员会委员
CSCO结直肠癌专家委员会委员、胆道肿瘤专家委员会委员
广东省医师协会肿瘤内科医师分会副主任委员
广东省女医师协会消化道肿瘤专委会副主任委员、肺癌专委会副主任委员
广东省医学教育协会肿瘤学专业委员会副主任委员
广东省抗癌协会靶向与个体化治疗专业委员会常委
广州抗癌协会靶向专业委员会副主任委员
深圳市医学会腹部肿瘤MDT专委会主任委员
深圳市抗癌协会秘书长、大肠癌专业委员会主任委员
深圳市健康管理协会肿瘤专业委员会主任委员
ADC突破化疗局限性,为HER2(ERBB2)突变晚期NSCLC带来全新选择
ADC成为抗肿瘤领域的新生力量
化疗是一种经典抗肿瘤疗法,但剂量限制性毒性限制了它发挥更大的抗肿瘤作用。1913年德国医学家Paul Ehrlich教授首次提出了“魔法子弹”ADC的概念,即通过靶向特异性抗原将细胞毒药物选择性递送至肿瘤细胞,以期精准给予靶病灶细胞毒药物,以最大程度地提高疗效并减少细胞毒性。历经了约90年的发展,科学家们将ADC的概念变成了现实,20世纪80至90年代期间,研究者从早期失败临床研究中吸取经验教训,不断优化ADC结构,解决了相关异质性、不稳定性、安全性等问题。经过后续第二/三发展阶段的发展,ADC药物的研发已进入成熟阶段。如今针对不同靶点的新型ADC陆续获批上市进入临床应用,已然成为抗肿瘤领域的新生力量。
德曲妥珠单抗(DS-8201,T-DXd)开辟HER2(ERBB2)突变晚期肺癌治疗新时代
在HER2(ERBB2)突变肺癌领域,既往相关的新药探索包括大分子抗体、小分子TKI等都未能取得较大突破,始终面临着较大未必满足的临床需求。而ADC相关临床研究提示,HER2(ERBB2)ADC德曲妥珠单抗显示出有希望的抗肿瘤疗效,提示了ADC在该领域的应用潜力。德曲妥珠单抗(DS-8201,T-DXd)是一种基于DXd-ADC平台设计的新型ADC,具有良好的结构优势,由肿瘤选择性可裂解连接子将曲妥珠单抗与高活性细胞毒载药拓扑异构酶I抑制剂DXd偶联而成。
在首个人体试验中,德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变晚期NSCLC患者中展现出非常惊艳的抗肿瘤活性,客观缓解率(ORR)达到72.7%,后续DESTINY-Lung01研究结果重磅刊登NEJM[1]。DESTINY-Lung01结果显示,6.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)在经治HER2(ERBB2)突变NSCLC患者中的ORR达到55%,中位缓解持续时间(DoR)达到9.3个月,中位无进展生存期(PFS)和中位总生存期(OS)分别为8.2个月和17.8个月。DESTINY-Lung02进一步评估了低剂量德曲妥珠单抗(DS-8201,T-DXd)的疗效和安全性,在初步疗效分析人群中,德曲妥珠单抗(DS-8201,T-DXd)确认的ORR为58%(5.4mg/kg),中位DoR为8.7个月。基于5.4mg/kg与6.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)相当的疗效 和更优的安全性,2022年FDA批准了德曲妥珠单抗(DS-8201,T-DXd)用于HER2(ERBB2)突变晚期NSCLC患者后线治疗的适应症,开启了此类患者精准治疗的新时代。
DESTINY-Lung02最终分析持续验证德曲妥珠单抗(DS-8201,T-DXd)的优异疗效
今年ASCO大会上,DESTINY-Lung02公布最终分析结果。最终分析时截止日期为2023年8月25日,5.4mg/kg组和6.4mg/kg组分别有12.9%、12.0%的患者接受德曲妥珠单抗(DS-8201,T-DXd)治疗[2]。基线特征显示,5.4mg/kg和6.4mg/kg组中亚裔人群分别占比61.8%、60%,分别有73.5%、78%的患者既往接受过PD-1/PD-1单抗,分别有67.6%、62%的患者接受过一线或二线治疗,分别有32.4%、38%的患者既往接受过3线及以上的治疗,基线伴CNS转移患者分别占比34.3%、44%(表1)。
表1 基线特征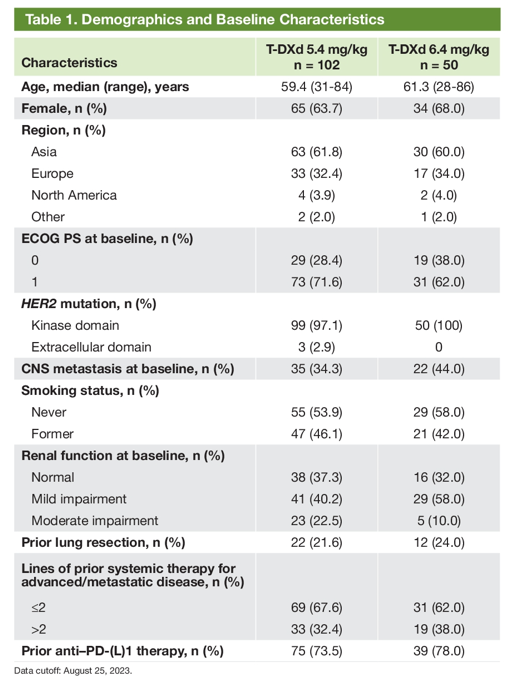
最终分析时,5.4mg/kg、6.4mg/kg组的中位随访时间分别为15.8个月、16.5个月,5.4mg/kg、6.4mg/kg组确认的ORR分别为50%、56%,分别有2.9%、8%的患者达到完全缓解,分别有47.1%、48%的患者达到部分缓解。5.4mg/kg、6.4mg/kg组确认的中位DoR分别为12.6个月、12.2个月。两组的疾病控制率(DCR)分别为93.1%、92%(表2)。
表2 疗效分析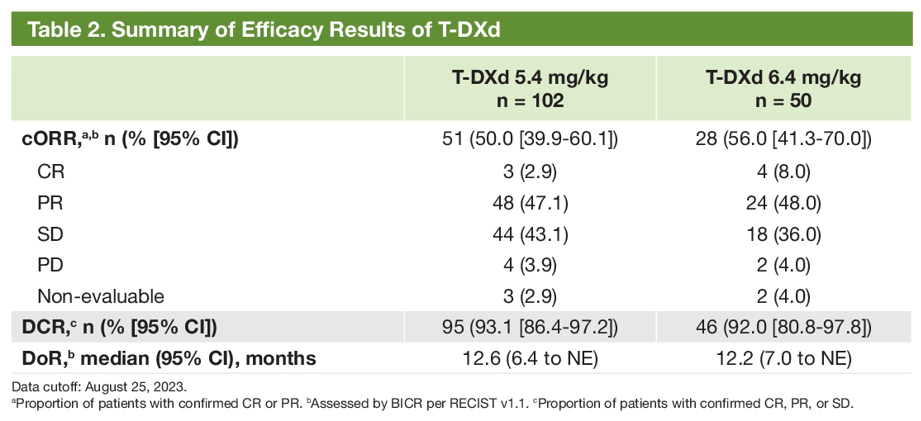
5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)亚组分析显示,既往和未接受PD-L1/PD-1单抗患者的ORR为45.1%、58.3%,既往接受过一线、二线、三线及以上患者确认的ORR分别为43.2%、46.9%、60.6%,基线伴脑转移和无脑转移患者确认的ORR分别为60%、44.8%。5.4mg/kg、6.4mg/kg组患者的中位PFS分别为10.0个月、12.9个月,两组中位OS分别为19个月、17.3个月(图1、图2)。
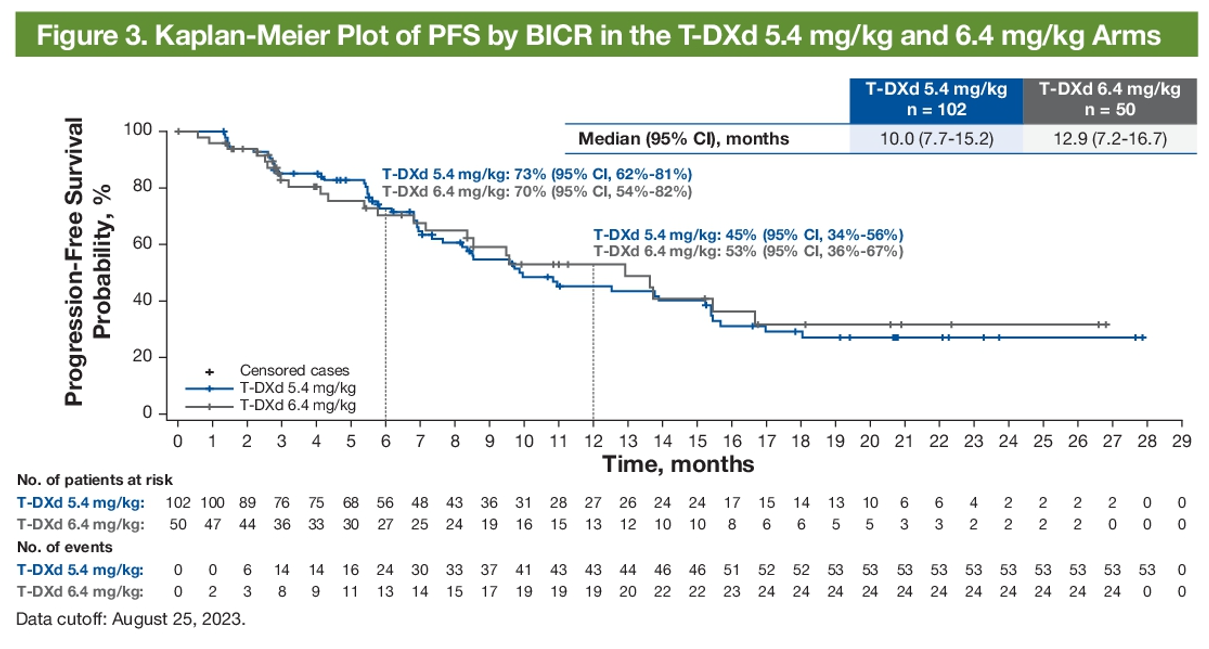
图1 PFS结果
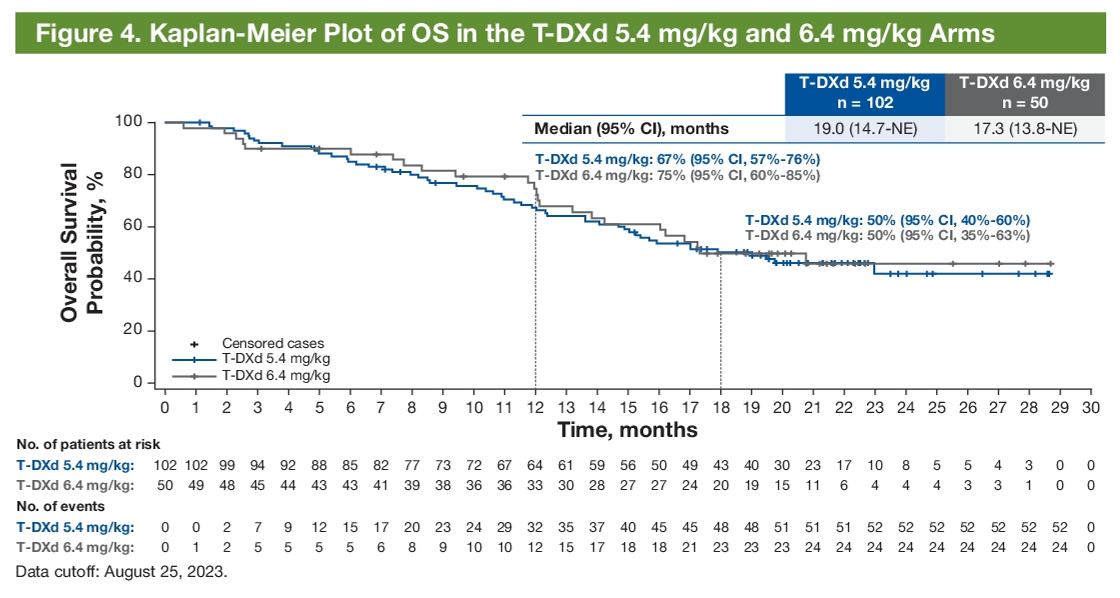 图2 OS结果
图2 OS结果
DESTINY-Lung02最终分析结果仍然非常亮眼,经过更长随访时间时,5.4mg/kg和6.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)在经治HER2(ERBB2)突变晚期NSCLC患者中仍展现出优异的疗效、持久的疗缓解持续时间和更优的生存期,最终分析带来了更有力的研究证据,并再次重现和验证了德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变晚期NSCLC全球人群中的疗效和安全性。
德曲妥珠单抗(DS-8201,T-DXd)在中国人群中同样疗效优异,期待尽早中国上市
DESTINY-Lung05是一项开放标签、单臂、II期临床研究,旨在评估德曲妥珠单抗(DS-8201,T-DXd)用于至少一线治疗期间或治疗进展后HER2(ERBB2)突变转移性NSCLC中国患者的疗效和安全性。关键入组标准包括病理学确认的非鳞状转移性NSCLC患者、至少接受过一种抗肿瘤全身治疗、经FFPE肿瘤组织检测为HER2(ERBB2)突变、WHO或ECOG评分为0或1、按RECIST 1.1标准经研究者至少有一个可测量病灶。主要终点经ICR评估确认的ORR,次要终点包括由研究者评估确认的ORR、以及ICR和研究者评估的DoR、DCR、PFS。
2024 AACR大会上DESTINY-Lung05研究首次公布5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)在中国HER2(ERBB2)突变晚期NSCLC患者中的结果[3]。中位随访9.8个月时,有72例HER2(ERBB2)突变晚期NSCLC患者至少接受1剂5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)治疗。结果显示,由ICR评估的确认的ORR为58.3%,其中1.4%的患者达到完全缓解,56.9%的患者达到部分缓解,中位DoR未达到,DCR为91.7%(表3),中位PFS未达到,12个月PFS率为55.1%。
表3 疗效分析
值得关注的是,德曲妥珠单抗(DS-8201,T-DXd)已被纳入CDE优先评审。DESTINY-Lung05研究中可见,德曲妥珠单抗(DS-8201,T-DXd)在中国HER2(ERBB2)突变晚期NSCLC患者中同样具有卓越的疗效。非常期待德曲妥珠单抗(DS-8201,T-DXd)能在中国尽早上市,以造福中国肺癌患者。
一线治疗领域和HER2(ERBB2)过表达领域是未来重要研究方向
德曲妥珠单抗(DS-8201,T-DXd)已在HER2(ERBB2)突变晚期NSCLC领域取得重大突破,我们更期待德曲妥珠单抗(DS-8201,T-DXd)在更广阔的肺癌治疗领域开展临床研究,其中在一线治疗领域和HER2(ERBB2)过表达领域具有较大的探索空间,是值得关注的研究方向。DESTINY-Lung04是一项开放标签、多中心III期临床研究,旨在评估德曲妥珠单抗(DS-8201,T-DXd)对比帕博利珠单抗+含铂双药化疗用于初治HER2(ERBB2)突变不可切除局部晚期或转移性非鳞状NSCLC患者一线治疗的疗效和安全性。期待德曲妥珠单抗(DS-8201,T-DXd)能在一线治疗领域取得进展。
既往研究显示,德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)过表达晚期NSCLC患者中显示出初步疗效,临床价值和疗效同样值得进一步探索。DESTINY-Lung03研究正在开展中,旨在探索一线德曲妥珠单抗(DS-8201,T-DXd)+免疫治疗±化疗治疗转移性HER2(ERBB2)过表达非鳞状NSCLC患者的疗效和安全性。期待研究数据的公布能为德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)过表达晚期NSCLC患者提供循证依据。
结语
基于DESTINY-Lung02研究结果,FDA加速批准德曲妥珠单抗(DS-8201,T-DXd)上市,为HER2(ERBB2)突变晚期NSCLC患者带来了全新的治疗选择。DESTINY-Lung02最终分析结果再增添了新的研究证据,更有力的证实了德曲妥珠单抗(DS-8201,T-DXd)在此类患者中的优异疗效。德曲妥珠单抗(DS-8201,T-DXd)在中国人群中同样展现出令人鼓舞的卓越疗效,期待德曲妥珠单抗(DS-8201,T-DXd)尽早在中国上市,造福中国肺癌患者。同时期待更多研究能为HER2(ERBB2)突变晚期NSCLC患者带来新的希望和曙光。
[1] Goto K, Goto Y, Kubo T, et al. Trastuzumab Deruxtecan in Patients With HER2-Mutant Metastatic Non-Small-Cell Lung Cancer: Primary Results From the Randomized, Phase II DESTINY-Lung02 Trial. J Clin Oncol. 2023 Nov 1;41(31):4852-4863. doi: 10.1200/JCO.23.01361. Epub 2023 Sep 11. Erratum in: J Clin Oncol. 2024 Feb 1;42(4):485. PMID: 37694347; PMCID: PMC10617843.
[2]Trastuzumab deruxtecan (T-DXd) in patients with HER2-mutant metastatic non–small cell lung cancer (mNSCLC): Final analysis results of DESTINY-Lung02. Abstract 8543. 2024 ASCO.
[3]Trastuzumab deruxtecan (T-DXd) in patients with HER2-mutant metastatic non–small cell lung cancer (mNSCLC): Final analysis results of DESTINY-Lung02. Abstract 8543. 2024 ASCO.
排版编辑:肿瘤资讯-Rex











 苏公网安备32059002004080号
苏公网安备32059002004080号


