2024年美国临床肿瘤学会(ASCO)年会已于当地时间5月31日-6月4日在美国芝加哥盛大召开。在5月31日下午转移性非小细胞肺癌专场中,全球共入选8项口头报告,令人惊喜的是,其中有2项均来自中国同一个团队——中山大学肿瘤防治中心张力教授团队。本年度,他们继续以中国好研究,在这场肿瘤界的“奥斯卡”中,唱响了“中国好声音”。
两项口头报告中,HARMONi-A试验为肺癌EGFR +肺癌患者建立了免疫治疗新方案;而OptiTROP-Lung01研究则为野生型肺癌患者探索了新型trop-2- ADC联合免疫治疗新方法。【肿瘤资讯】特对两项研究详细内容做以整理,以飨读者。
研究一:依沃西单抗联合化疗用于EGFR酪氨酸激酶抑制剂(HARMONi-A)治疗进展的EGFR突变非鳞状非小细胞肺癌:一项随机、双盲、多中心、3期试验(Abstarct#8508)
除了在ASCO上荣光闪耀外,该试验同步被国际顶尖权威期刊《美国医学会杂志》(Journal of the American Medical Association, JAMA)在线发表。基于此试验的积极结果,今年5月,依沃西单抗也被国家药品监督管理局(NMPA)批准上市,用于联合化疗治疗EGFR-TKI治疗进展的EGFR突变的局部晚期或转移性nsq-NSCLC,从而惠及更多患者。并且这项来自中国自主研发的创新研究,有望改写全球EGFR-TKI耐药的EGFR突变nsq-NSCLC的治疗格局。


图:张力教授
研究背景
EGFR-TKI是EGFR突变NSCLC的标准一线治疗,但获得性耐药不可避免。目前临床上EGFR-TKI尤其是第三代TKI治疗进展患者,最佳的治疗选择仍然有限。HARMONi-A(AK112-301)研究是一项双盲、安慰剂对照、随机III期研究,旨在评估依沃西单抗联合化疗对比化疗在EGFR-TKI 经治失败EGFR突变转移性NSCLC患者的疗效和安全性。
研究方法
III期HARMONi-A研究在中国55个中心开展,共纳入322例EGFR-TKI治疗失败的NSCLC,随机(1:1)接受依沃西单抗(n=161)或安慰剂(n=161)联合培美曲塞+卡铂Q3W 4个周期治疗,随后接受依沃西单抗+培美曲塞或安慰剂+培美曲塞的维持治疗。主要终点是根据RECIST v1.1标准由独立放射学评审委员会(IRRC)评估的意向治疗(ITT)人群的无进展生存期(PFS)。
研究结果
PFS结果显示,中位随访7.9个月时,依沃西单抗联合化疗组和对照组的中位PFS分别为7.1个月和4.8个月,疾病进展或死亡风险显著降低54%(HR=0.46,P<0.001)。PFS亚组分析显示,除部分患者人数较少的亚组外,几乎所有亚组都观察到与总人群一致的PFS获益,并具有显著统计学意义,尤其是临床上备受关注的EGFR敏感突变亚组和脑转移亚组。如下图所示,在不论既往接受三代EGFR-TKI或一/二代EGFR-TKI、不论EGFR敏感突变类型、无论是否脑转移等关键亚组均观察到PFS的明显获益。
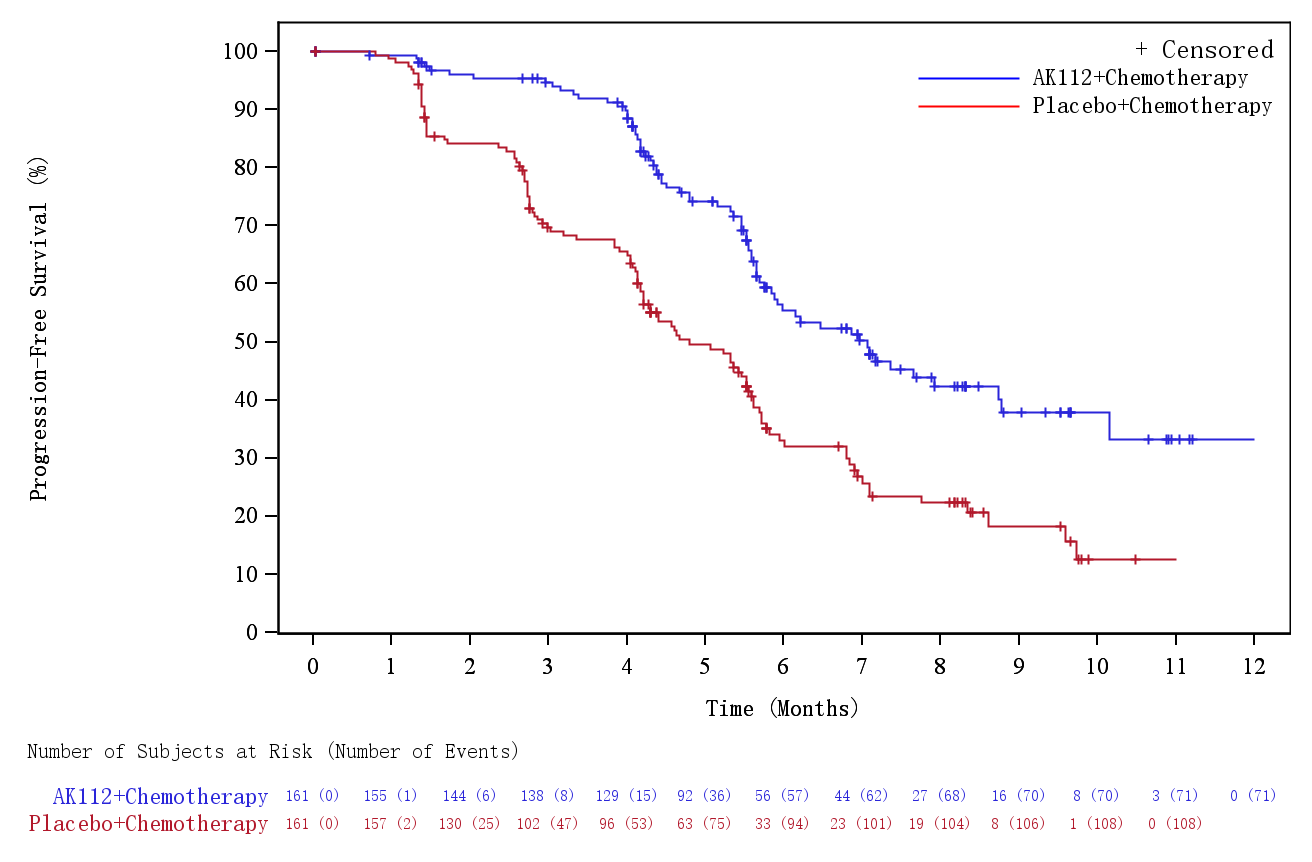 图:ITT人群的PFS
图:ITT人群的PFS
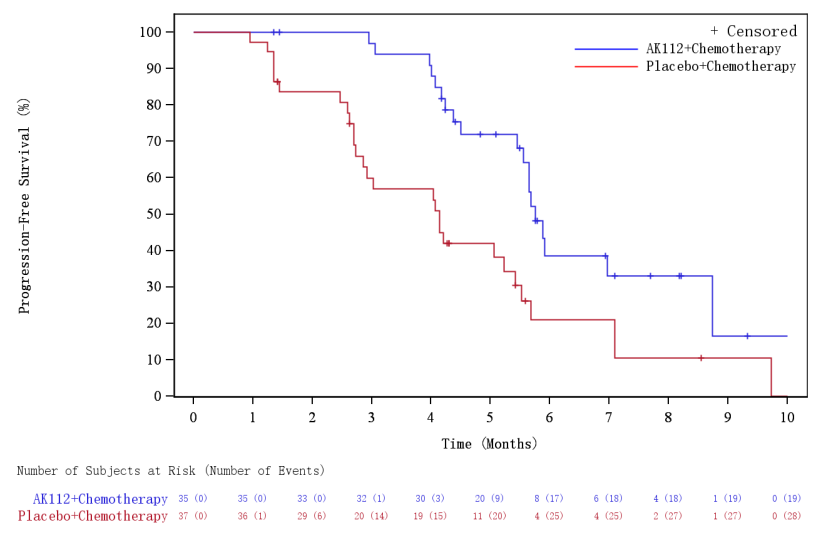 图:脑转移患者的PFS
图:脑转移患者的PFS
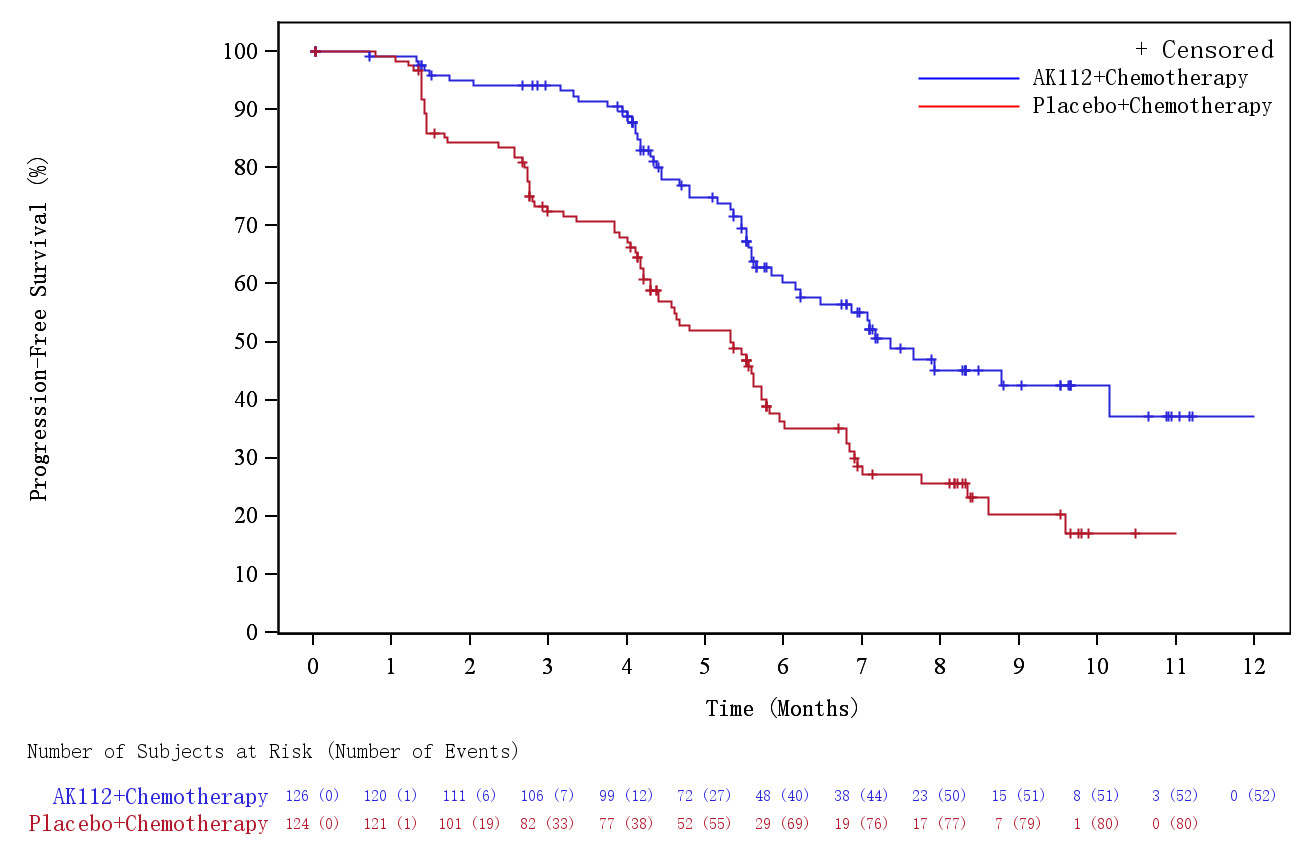 图:不伴有脑转移患者的PFS
图:不伴有脑转移患者的PFS
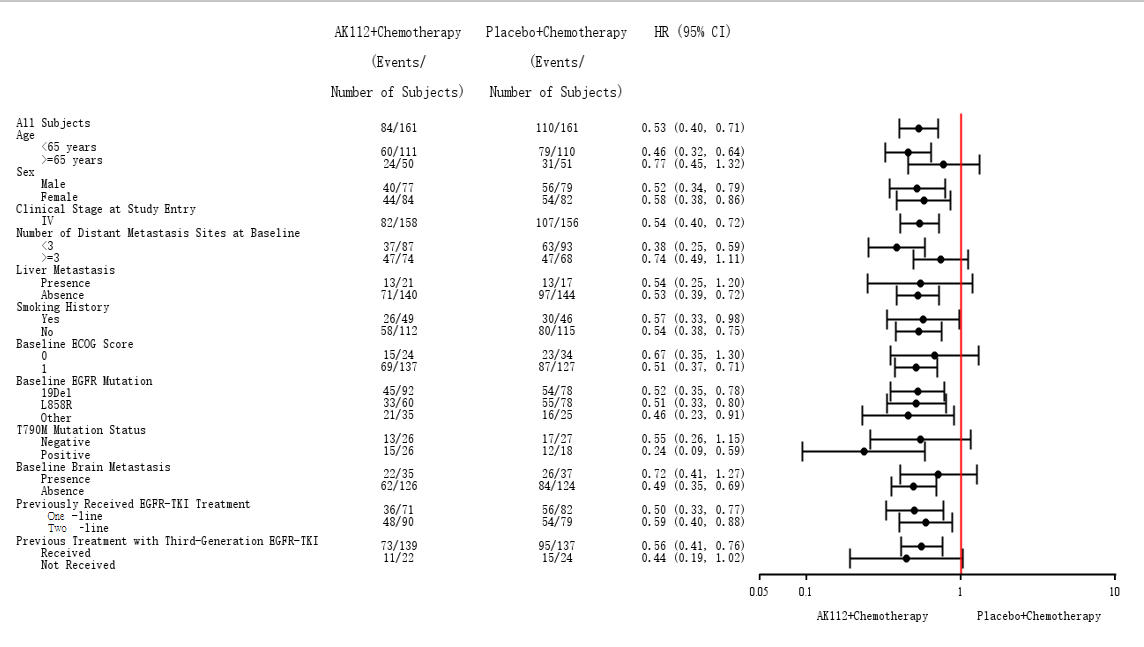 图: IRRC评估的PFS Kaplan-Meier曲线
图: IRRC评估的PFS Kaplan-Meier曲线
OS结果显示,HARMONi-A是在本领域取得OS明显获益趋势的一项关键III期临床研究。中位随访17.6个月时,试验组和对照组的中位OS分别为17.1个月 vs 14.5个月,依沃西单抗可降低患者死亡风险20%(HR=0.8)。排除免疫治疗经治患者的敏感性分析显示,依沃西单抗联合组观察到OS明显延长的趋势,降低死亡风险23%(HR=0.77)。
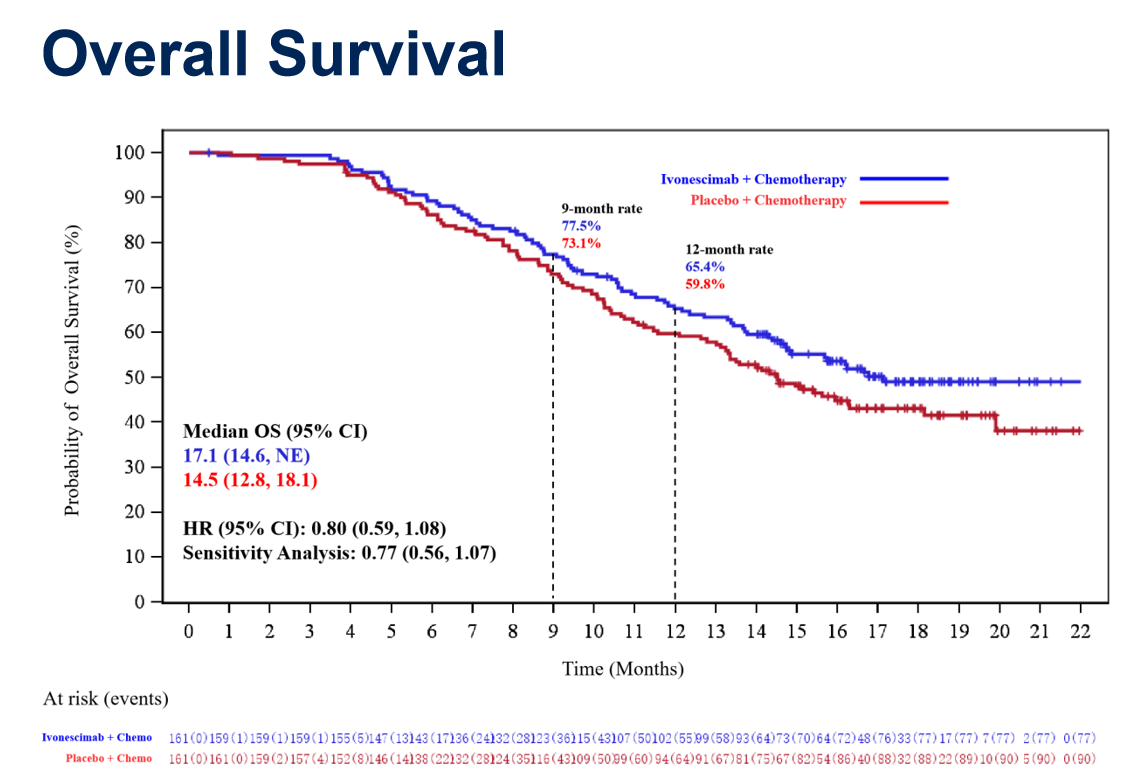 图:OS曲线
图:OS曲线
安全性方面,依沃西单抗联合化疗不良事件发生率与对照组相当,整体安全可控,两组中≥3级治疗相关不良事件(TRAE)发生率分别为54% vs 42.9%。除中性粒细胞减少以及肝酶提升外,其他≥3级TRAE在两组间无显著差异。研究中不良事件主要以血液学毒性为主,与化疗相关,免疫相关不良事件发生率较低。总体上,依沃西单抗可同时靶向两个靶点,但并没有增加不良事件发生风险,临床应用中利于提高患者用药的依从性。
研究结论
总之,依沃西单抗联合化疗对比化疗明显改善EGFR-TKI经治失败晚期NSCLC患者的PFS,并可见OS获益趋势,且安全性可控并利于提高患者用药的依从性。
研究意义
基于这项研究的积极结果,依沃西单抗于5月被国家药品监督管理局(NMPA)批准上市。同时,依沃西单抗联合化疗用于经第三代EGFR-TKI治疗进展的EGFR突变、局晚期或转移性nsq-NSCLC的国际多中心III期HARMONi研究已经在高效开展中,这项来自中国自主研发的创新方案有望改写全球EGFR-TKI耐药的EGFR突变nsq-NSCLC的治疗格局,彰显了中国学者在肿瘤免疫治疗临床研究领域的引领地位。
研究二:芦康沙妥珠单抗 (SKB264/MK-2870)联合KL-A167(PD-L1单抗)一线治疗晚期NSCLC II期OptiTROP-Lung01研究(Abstract# 8502)
OptiTROP-Lung01研究突破了以往标准治疗的限制,为多类患者提供了新的治疗选择。其成功无疑会给更多的研究者对这种联合方案进行更多更深入的探索带来信心,从而让更多的患者从治疗中获益。

方文峰教授
研究背景
在免疫治疗时代,驱动基因阴性晚期NSCLC患者的一线治疗主要以免疫联合化疗为主,患者的5年生存率得到了显著改善,但尽管如此,仍有相当一部分患者对现在治疗方案应答有限,迫切需要更加有效的治疗方案来改善其预后及生活质量,满足其临床治疗需求。
是否可以将芦康沙妥珠单抗与免疫检查点抑制剂联合,用于一线治疗驱动基因阴性NSCLC,让更多的患者达到肿瘤缓解,延长生存时间?基于此,研究团队开展了OptiTROP-Lung01研究,旨在探索芦康沙妥珠单抗联合PD-L1单抗KL-A167一线治疗驱动基因阴性晚期NSCLC患者的疗效和安全性。
研究方法
OptiTROP-Lung01研究是一项多中心的II期研究,未曾接受过治疗的晚期无驱动基因突变 NSCLC患者入组并按非随机方式每3周接受一次5 mg/kg剂量的芦康沙妥珠单抗(sac-TMT)加每3周接受一次1200 mg剂量的KL-A167治疗(1A队列)或每2周接受一次5 mg/kg剂量的芦康沙妥珠单抗(sac-TMT)加每2周接受一次900 mg剂量的KL-A167治疗(1B队列),直至疾病进展或发生不可耐受毒性。截至2024年1月2日,1A队列和1B队列分别入组40名及63名患者。中位年龄为63/63岁(1A/1B队列);97.5%/85.7%患者的美国东部肿瘤协作组体能状态(ECOG PS)评分为1分 ;根据IHC 22C3 pharmDx测定法,分别有30.0%/33.3%、32.5%/30.2%及37.5%/36.5%的患者肿瘤细胞的程序性死亡配体1(PD-L1)表达为< 1%、1%-49%及≥ 50%。
研究结果
在本次ASCO会议中, 方文峰教授代表研究团队以Oral presentation的形式公布了该研究的阶段性数据。1A队列经过为期14.0个月的中位随访后,ORR为48.6%(18/37, 2例待确认),疾病控制率(DCR)为94.6%,中位PFS为15.4个月(95% CI: 6.7, NE),6个月PFS率为69.2%。1B队列经过为期6.9个月的中位随访后,ORR为77.6%(45/58, 5例待确认),DCR为100%,未达到中位PFS,6个月的中位PFS率为84.6%。1B队列的亚组分析提示,无论患者PD-L1的表达水平如何,也无论患者是非鳞癌或鳞癌,芦康沙妥珠单抗+KL-A167 Q2W方案均展示出疗效:
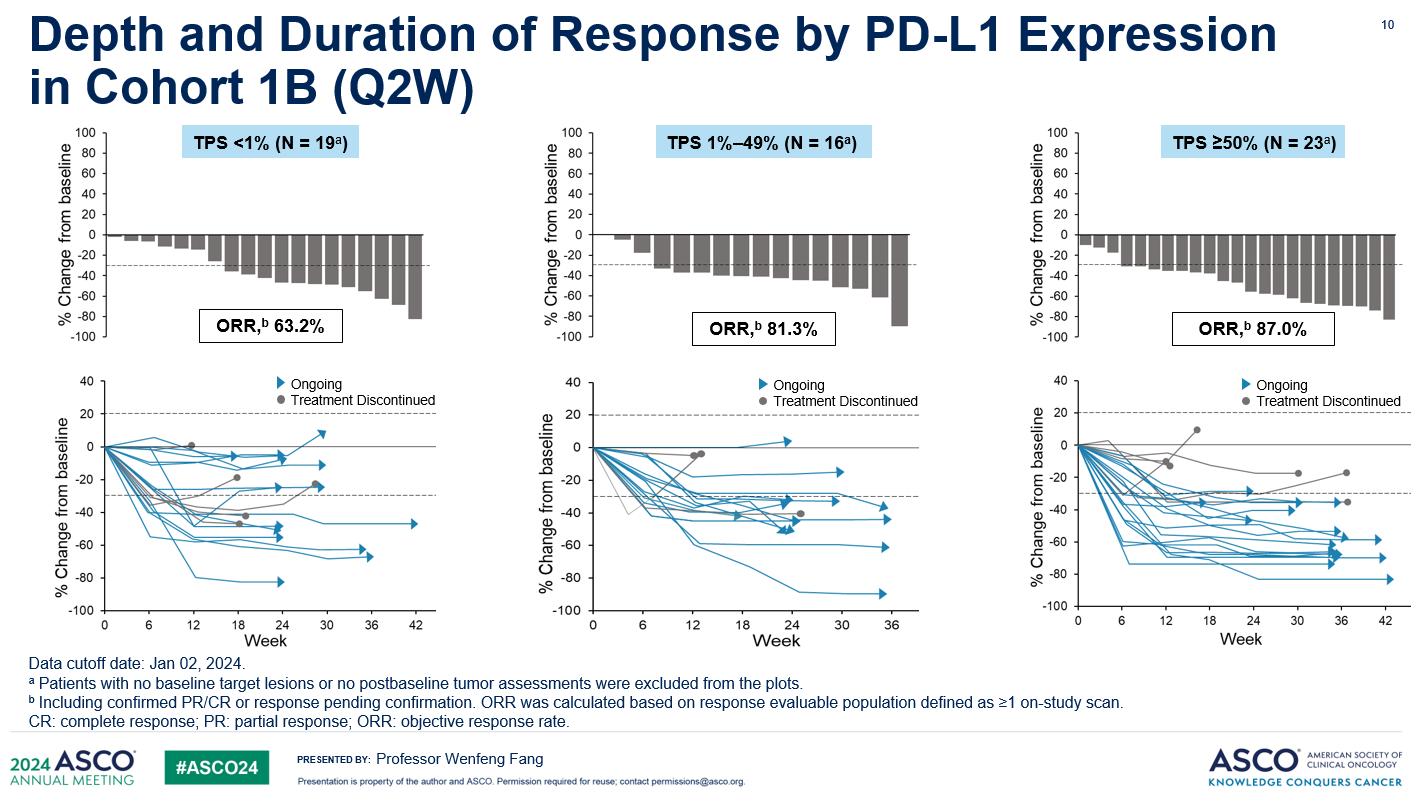
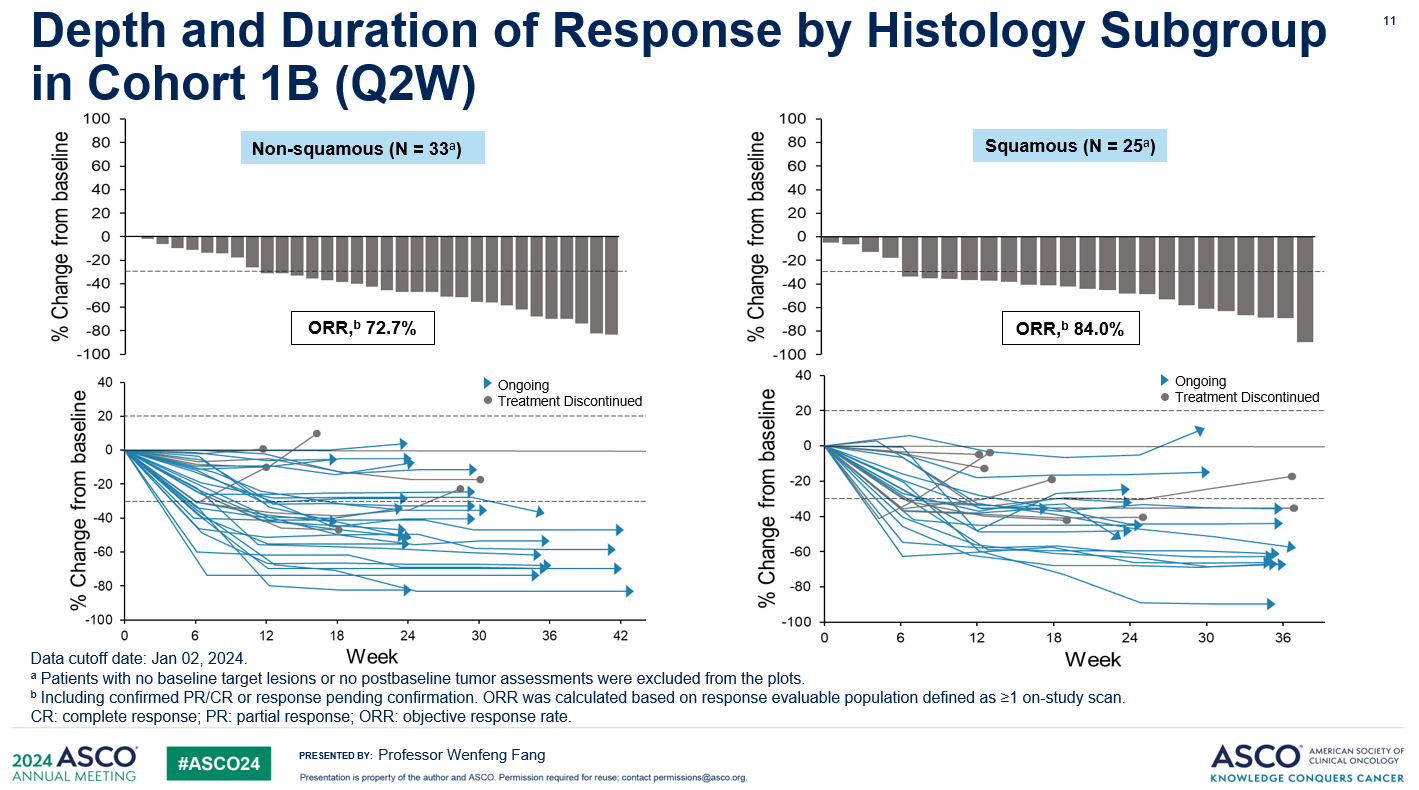
在1A和1B队列中,最常见的≥3级TRAE为中性粒细胞计数降低(30.0%/30.2%)、WBC降低(5.0%/17.5%)、贫血(5.0%/15.9%)、皮疹(5.0%/6.3%)及药疹(7.5%/0)。曾发生1B队列的1名患者因出现超敏反应导致停用芦康沙妥珠单抗(sac-TMT)的治疗相关不良事件,但并无出现治疗相关死亡事件。
研究结论
芦康沙妥珠单抗+KL-A167治疗NSCLC一线患者显示出令人鼓舞的抗肿瘤活性。无论患者PD-L1的表达水平如何,也无论患者是非鳞癌或鳞癌,芦康沙妥珠单抗+KL-A167 Q2W方案均展示出疗效。联合方案安全谱与两个单药既往已知的安全谱一致,未观察到新的安全性信号或毒性的叠加。
研究意义
基于该研究结果,芦康沙妥珠单抗联合PD-1/L1将继续开展和推进多项NSCLC领域的III期研究。目前多个TROP2 ADC均开展了联合PD-1/L1±含铂化疗在一线驱动基因阴性NSCLC的临床研究,并发布了积极数据,这一联合方案有望为患者带来更多临床获益。
专家简介
中山大学肿瘤防治中心,内科主任,博导,肺癌首席专家
中国抗癌协会癌症康复与姑息治疗专业委员会 主任委员
中国抗癌协会肿瘤药物临床研究专业委员会 副主任委员
中国抗癌协会肿瘤防治科普专业委员会 副主任委员
中国临床肿瘤学会(CSCO) 常务理事
CSCO-免疫治疗专家委员会 候任主委
广东省医学会临床研究学分会 主任委员
广东省临床医学学会精准医疗专业委员会 主任委员
广东省医学领军人才、“特支计划”杰出人才(南粤百杰)
中山大学附属肿瘤医院
“国家高层次人才项目青年人才”
“广东省特支计划百千万工程青年拔尖人才”
“广东省杰出青年医学人才”
“广州市珠江科技新星”
CSCO非小细胞肺癌专业委员会委员
CSCO鼻咽癌专业委员会委员
中国抗癌协会肺癌专业委员会委员
广东省抗癌协会鼻咽癌专业青年委员会副主任委员
广东省医学会精准医学与分子诊断专业委员会副主任委员
广东省临床医学会真实世界临床研究专业委员会副主任委员
研究方向:肺癌及鼻咽癌的靶向治疗及免疫治疗的临床及转化研究
主要课题:主持国家重大研发计划(子课题)、国自然(6项)
代表论著:JAMA、Cancer Cell、JCO、Lancet Oncology(2篇,2021,2018)、STTT、 Molecular Cancer、 Nature Communications、J Thorac Oncol、Clinical Cancer Research、JITC等
排版编辑:肿瘤资讯-tcz











 苏公网安备32059002004080号
苏公网安备32059002004080号


