2024美国临床肿瘤学会(ASCO)年会于当地时间2024年5月31日~6月4日在美国芝加哥盛大召开。会议期间有数项改变临床实践的重磅研究以及最前沿科研成果亮相。在肺癌领域,针对HER2(ERBB2)、TROP2靶点的抗体偶联药物(ADC)有多项重磅研究公布或更新结果。基于DESTINY-Lung02研究,FDA已于2022年批准德曲妥珠单抗(DS-8201,T-DXd)用于HER2突变晚期非小细胞肺癌(NSCLC)患者的后线治疗,德曲妥珠单抗因此成为肺癌领域目前为止首个且唯一获批的ADC。在今年ASCO大会上,DESTINY-Lung02研究公布最终分析结果。【肿瘤资讯】特邀武汉大学人民医院宋启斌教授分析治疗现状,解读最新进展。
武汉大学人民医院肿瘤中心 主任 兼肿瘤学教研室主任、学科带头人、首席专家
欧洲自然科学院院士
第五届“国之名医”—卓越建树专家
国家卫健委医政医管局《肺癌诊疗指南》专家组成员
国家癌症中心肺癌质控专家
中国医师协会第五届理事会 理事
中国医师协会肿瘤多学科诊疗专业委员会副主任委员兼总干事
世界华人肿瘤医师协会常委兼胸部肿瘤分会副主任委员
中国医促会胸部肿瘤分会 副主任委员
中国临床肿瘤学会(CSCO)常务理事
CSCO老年肿瘤专委会副主委
肺癌、大数据专委会常委
中国抗癌协会肺癌、肿瘤多学科诊疗专委会常委
湖北省临床肿瘤学会(ESCO)理事长兼肺癌专委员会主任委员
武汉医学会放射肿瘤治疗学分会主任委员
HER2突变晚期NSCLC治疗需求未满,CSCO/NCCN指南推荐见证德曲妥珠单抗不凡治疗地位
HER2是早在1985年被发现的关键致癌驱动基因,且很快被发现可作为乳腺癌治疗的重要疗效预测因子,开启了乳腺癌治疗的新篇章。后续的多项研究表明HER2可促进肿瘤发生发展,在多种实体瘤组织中高表达,并与多种实体瘤的预后差相关。
临床困局
在晚期NSCLC中,HER2突变的发生率约为2%-4%,常见于腺癌或腺鳞癌、从不吸烟者和女性患者。过去二十年间,研究者一直在评估和探索针对HER2靶点的靶向治疗药物,包括大分子单克隆抗体曲妥珠单抗、帕妥珠单抗,以及小分子TKI类药物包括阿法替尼、达可替尼、来那替尼、吡咯替尼等在HER2突变晚期NSCLC中的价值。尽管一些小分子TKI类药物显示出一定的临床疗效,但迄今为止这两大类药物在该领域都没有取得变革性的结果。因此十多年来,含铂为基础的化疗方案仍是HER2突变晚期NSCLC患者的标准疗法,临床上始终有较大未被满足的临床治疗需求。
从2024版《CSCO非小细胞肺癌诊疗指南》中可见[1],目前此类经治晚期NSCLC患者的治疗选择仍然非常有限,IV期HER2突变NSCLC的一线治疗仍需参考“IV期无驱动基因NSCLC患者的一线治疗”部分;后线治疗I级推荐也需要参考“IV期无驱动基因NSCLC后线治疗的I级推荐”部分。
新突破
值得关注的是,德曲妥珠单抗是目前为止唯一一种获得CSCO指南推荐的ADC,且新版指南中的推荐级别从III级推荐上升为II级推荐[1]。而在2024版NCCN指南中,德曲妥珠单抗是截止目前HER2突变晚期NSCLC后线治疗选择中唯一的优选推荐。总体而言,自德曲妥珠单抗首次打破HER2突变晚期NSCLC领域治疗格局,到后续获得NCCN指南的优选推荐和新版CSCO指南的升级推荐,德曲妥珠单抗展现出不凡的治疗地位,有望弥补此类患者的临床治疗需求。
DESTINY-Lung02最终分析,为德曲妥珠单抗填补治疗空白提供新证据
DESTINY-Lung02是一项多中心、随机双盲、剂量优化、非对照研究,旨在评估两剂量德曲妥珠单抗(5.4mg/kg和6.4mg/kg)用于经治HER2突变不可切除或转移性NSCLC患者的疗效。该研究结果多次在ESMO/ASCO/WCLC等学术会议上公布和更新结果。
在2023 WCLC大会上,DESTINY-Lung02研究曾以口头汇报形式公布更新结果,并同步发表于临床肿瘤学杂志(JCO)[2]。数据截止时的疗效分析结果显示,5.4mg/kg和6.4mg/kg组的中位随访时间分别为11.5个月和11.8个月,分别有102例和50例患者分配至5.4mg/kg和6.4mg/kg组。德曲妥珠单抗在总人群中的客观缓解率(ORR)分别为49%、56%,疾病控制率(DCR)分别为93.1%、92%(表1),中位无进展生存期(PFS)分别为9.9个月、15.4个月,中位总生存期(OS)分别为19.5个月、NE。在安全性方面,德曲妥珠单抗显示出与既往研究一致的安全谱特征,其中5.4mg/kg德曲妥珠单抗具有更优的安全性。
表1 DESTINY-Lung02研究疗效分析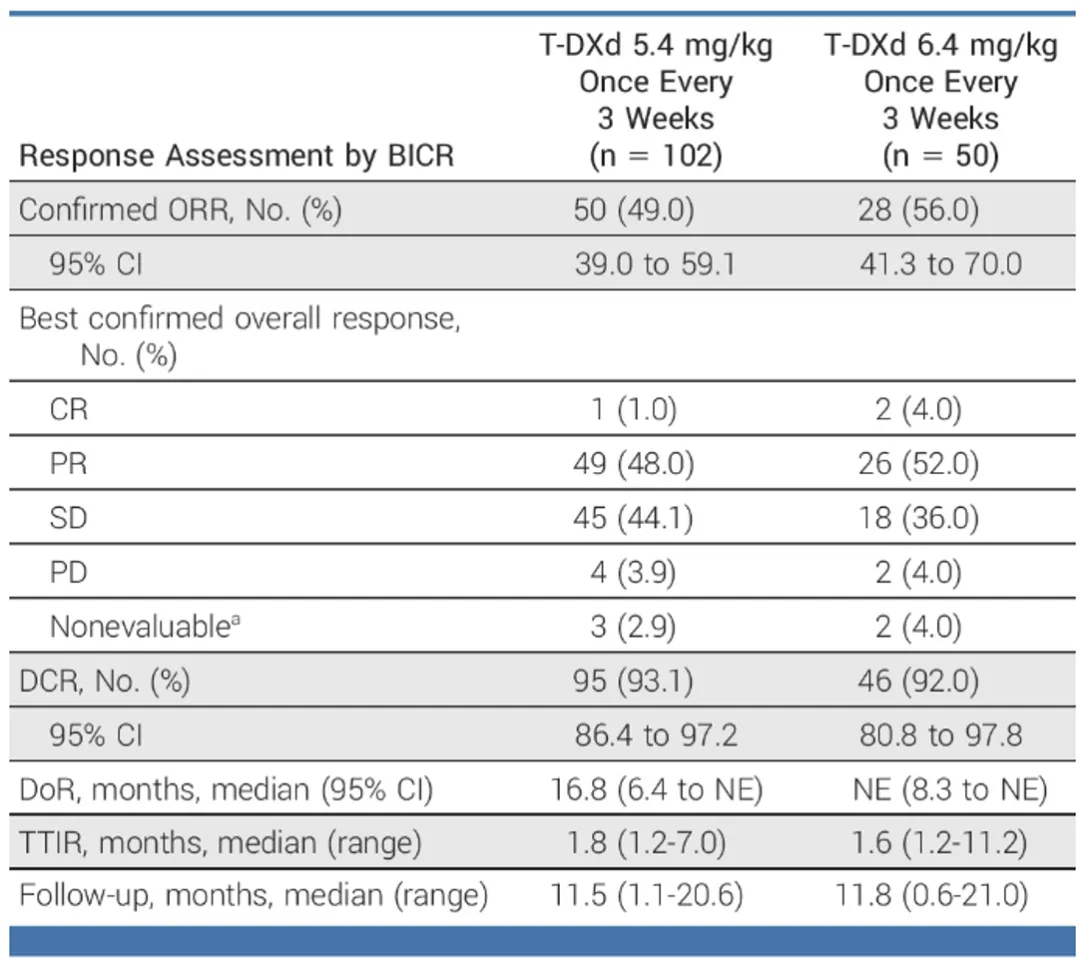
在2024 ASCO大会上,DESTINY-Lung02研究公布最终分析结果[3]。入组的HER2突变经治晚期NSCLC,按2:1比例随机分配接受5.4mg/kg和6.4mg/kg(Q3W)德曲妥珠单抗。基线特征显示,5.4mg/kg和6.4mg/kg组亚裔人群分别占比61.8%、60%,分别有73.5%、78%的患者既往接受过PD-1/PD-1单抗,基线伴CNS转移患者分别占比34.3%、44%(表2)。
表2 5.4mg/kg和6.4mg/kg组患者基线特征
最终分析截至2023年8月25日,5.4mg/kg、6.4mg/kg组的中位随访时间分别为15.8个月、16.5个月,5.4mg/kg、6.4mg/kg德曲妥珠单抗确认的ORR分别为50%、56%;5.4mg/kg、6.4mg/kg组的中位缓解持续时间(DoR)分别为12.6个月、12.2个月,两组的DCR分别为93.1%、92%(表3)。
表3 DESTINY-Lung02最终疗效分析结果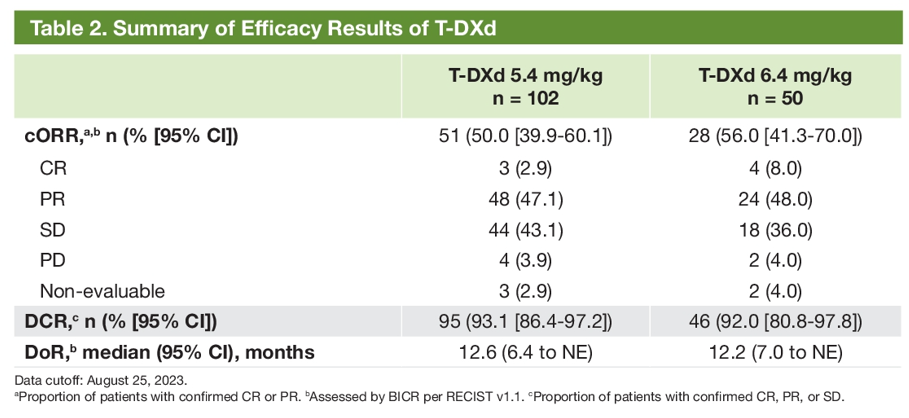
5.4mg/kg、6.4mg/kg德曲妥珠单抗亚组分析显示,伴脑转移患者确认的ORR分别为60%、45.5%(表4)。
表4 5.4mg/kg、6.4mg/kg组德曲妥珠单抗亚组分析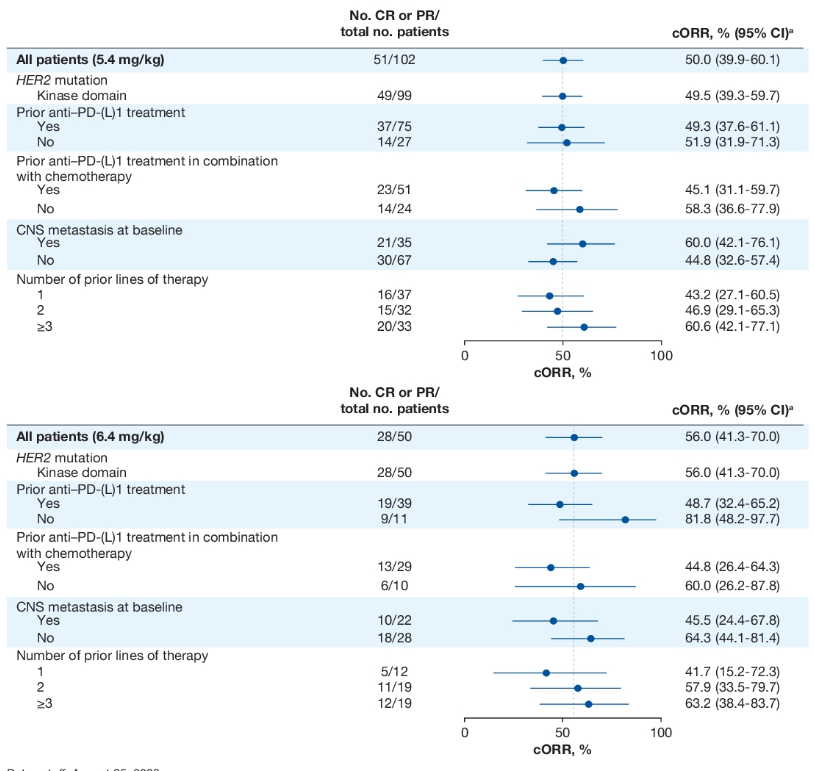
5.4mg/kg、6.4mg/kg组患者的中位PFS分别为10.0个月、12.9个月,两组中位OS分别为19个月、17.3个月。安全性方面,且未出现新的安全性信号,低剂量组安全性更优。两剂量组德曲妥珠单抗仍然显示出与既往研究一致的优异且持久的抗肿瘤疗效。
多次披露的研究结果提示,不论在中期分析还是最终分析中,DESTINY-Lung02研究持续不断验证着德曲妥珠单抗的卓越疗效、肿瘤应答的持久性,良好的安全性以及优异的PFS和OS结果。本次最终分析结果的公布再次为指南推荐提供了研究数据支持,同时为德曲妥珠单抗填补此类患者的治疗需求提供了新证据。
德曲妥珠单抗在脑转移人群和中国人群均展现卓越疗效
令人鼓舞的是,DESTINY-Lung02关键亚组分析结果可见,不论是否有脑转移,德曲妥珠单抗均显示出优异的颅内疗效。2023 WCLC大会公布的结果中,5.4mg/kg德曲妥珠单抗用于有CNS转移和无CNS转移HER2突变晚期NSCLC患者的ORR分别为60%和43.3%。本次最终分析中,5.4mg/kg德曲妥珠单抗用于基线有CNS转移和无CNS转移HER2突变晚期NSCLC患者的ORR分别为60%和44.8%。
同样,2023 ESMO大会上公布的DESTINY-Lung01和DESTINY-Lung02汇总分析结果同样提示,不论基线是否有CNS转移,德曲妥珠单抗均显示良好的疗效[4]。5.4mg/kg和6.4mg/kg组患者确认的颅内ORR(IC-cORR)分别为50%和30%,两组患者的颅内疾病控制率(IC-DCR)分别为92.9%和73.3%,两组患者的中位颅内缓解持续时间(IC-DoR)分别为9.5个月和4.4个月(表5)。总体而言,两剂量组德曲妥珠单抗在伴脑转移HER2突变转移性NSCLC患者中均显示出良好的颅内活性,而5.4mg/kg德曲妥珠单抗的颅内疗效更优。
表5 汇总分析颅内疗效分析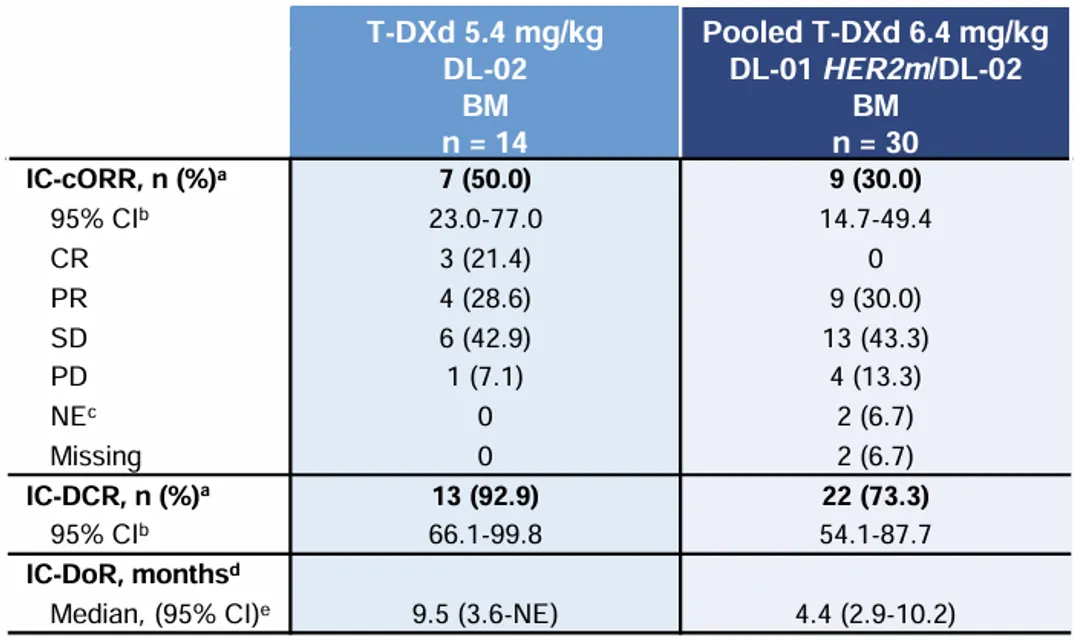
在今年4月结束的2024 AACR大会上,DESTINY-Lung05研究首次披露了5.4mg/kg德曲妥珠单抗在中国HER2突变晚期NSCLC患者中的疗效[5]。截至2023年9月23日数据分析时,中位随访时间为9.8个月,有72例HER2突变晚期NSCLC患者至少接受1剂5.4mg/kg德曲妥珠单抗治疗。结果显示,由ICR评估的确认的ORR为58.3%,其中1.4%的患者达到完全缓解,56.9%的患者达到部分缓解,中位DoR未达到,DCR为91.7%(表6),中位PFS未达到,12个月PFS率为55.1%。由研究者评估确认的ORR为58.3%,中位DoR为9个月,DCR为93.1%,中位PFS为10.8个月,12个月PFS率为39.7%。安全性结果方面,德曲妥珠单抗显示出与总人群一致的不良事件,未出现新的安全性信号。德曲妥珠单抗的中位暴露时间为7.9个月,3级及以上药物相关不良事件(AE)发生率为51.4%。最常见(≥5%)药物相关≥3级AE为中性粒细胞减少症(26.4%)、血小板减少症(18.1%)和白细胞减少症(11.1%)和淋巴细胞减少症(6.9%)。
表6 DESTINY-Lung05疗效分析
结语
在HER2突变晚期NSCLC后线治疗领域,德曲妥珠单抗是NCCN指南的优选推荐;在新版《CSCO非小细胞肺癌诊疗指南》中,德曲妥珠单抗被纳入此类患者后线治疗的II级推荐。本次会议上公布的DESTINY-Lung02最终分析结果显示,随着随访时间的延长,德曲妥珠单抗仍可得到同样优异的ORR、DoR、PFS和OS结果及良好的安全性结果。此外,德曲妥珠单抗更是伴脑转移HER2突变晚期NSCLC患者的福音和新希望,亦在中国人群中展现同样卓越的疗效。简言之,德曲妥珠单抗为HER2突变晚期NSCLC带来了新选择,而随着指南推荐的升级和研究结果的更新,德曲妥珠单抗有望造福更多患者,将HER2突变晚期NSCLC带进ADC精准治疗的新时代。目前德曲妥珠单抗已被纳入CDE优先评审,期待德曲妥珠单抗NSCLC适应证早日在中国获批,以造福广大中国患者。
[1]中国临床肿瘤学会指南工作委员会. CSCO非小细胞肺癌诊疗指南(2024版)
[2]Goto K, Goto Y, Kubo T, et al. Trastuzumab Deruxtecan in Patients With HER2-Mutant Metastatic Non-Small-Cell Lung Cancer: Primary Results From the Randomized, Phase II DESTINY-Lung02 Trial. J Clin Oncol. 2023 Nov 1;41(31):4852-4863. doi: 10.1200/JCO.23.01361. Epub 2023 Sep 11. Erratum in: J Clin Oncol. 2024 Feb 1;42(4):485. PMID: 37694347; PMCID: PMC10617843.
[3] Trastuzumab deruxtecan (T-DXd) in patients with HER2-mutant metastatic non–small cell lung cancer (mNSCLC): Final analysis results of DESTINY-Lung02. Abstract 8543. 2024 ASCO.
[4] Li BT, et al. Trastuzumab deruxtecan (T-DXd) in patients (pts) with HER2(ERBB2)-mutant (HER2m) metastatic nonesmall cell lung cancer (NSCLC) with and without brain metastases (BMs):Pooled analyses from DESTINY-Lung01 and DESTINYLung02. 2023 ESMO 1321MO.
[5] Trastuzumab deruxtecan (T-DXd) in Chinese patients (pts) with previously treated HER2 mutant non-small cell lung cancer (NSCLC): primary analysis from the Phase 2 DESTINY-Lung05 (DL-05) trial. Abstract CT248/7,2024 AACR.
排版编辑:肿瘤资讯-Rex











 苏公网安备32059002004080号
苏公网安备32059002004080号


