食管癌是我国常见的消化道恶性肿瘤之一,早期食管癌通过手术治疗可获得明显效果,但对于可切除的局部晚期/局部进展期食管癌患者来说,单纯手术的效果并不理想,临床上多采取术前新辅助化疗、放疗或联合放化疗或术后辅助化疗、放疗等综合治疗模式1。
目前,免疫治疗已开启食管癌治疗的新篇章。已有临床研究探索了免疫在食管癌术前新辅助治疗以及在晚期食管癌一线治疗中的获益情况。基于此,本文特分享一例ⅣA期食管癌综合治疗病例,期望能给临床带来更多思考与启示。
病例介绍
基本情况
患者男性,56岁。于2019-11-18因“进食梗阻3月余,确诊食管癌20余天”入院。
既往史:肺结核病史,8年前于当地医院行“阑尾切除术”。
个人史:无吸烟习惯,饮酒30年,每天白酒100ml。
一般情况:意识清晰;体温36.5 ℃;脉搏76次/分;呼吸17次/分;血压 128/83mmHg/L;体位:自主体位;病容:无;体重:56kg;身高:165cm;
查体:双锁骨上未及明显肿大淋巴结。
辅助检查
2019-10-25于桐乡市当地医院行胃镜:食管隆起,Ca可能,慢性萎缩性胃炎伴糜烂。我院病理会诊:(食管)低分化鳞状细胞癌。
2019-11-7 我院院前胸腹部增强CT检查:
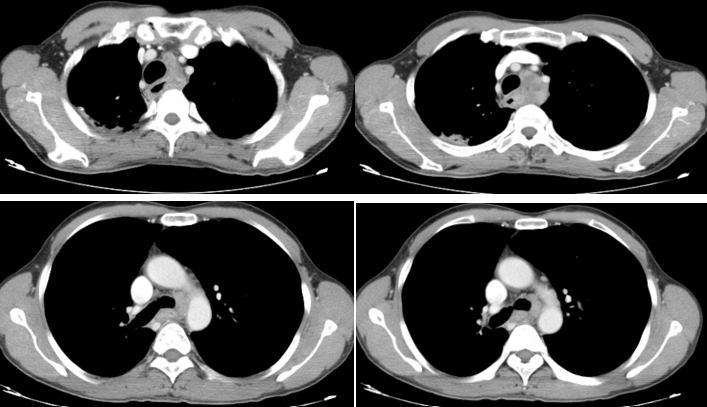
初步诊断
食管中上段恶性肿瘤(cT4aN1-2M0 ⅣA期)
肺结核个人史
阑尾炎术后
治疗经过
新辅助治疗:
2019.11.19、2019.12.19、2020.01.13、2020.02.26行4周期免疫联合化疗方案治疗,具体为:PD-1抑制剂 静滴 d1 Once+白蛋白紫杉醇 180mg 静滴 d1,d8 Once+卡铂 550mg 静滴 d1 Once Q3W。
用药后疗效评估:
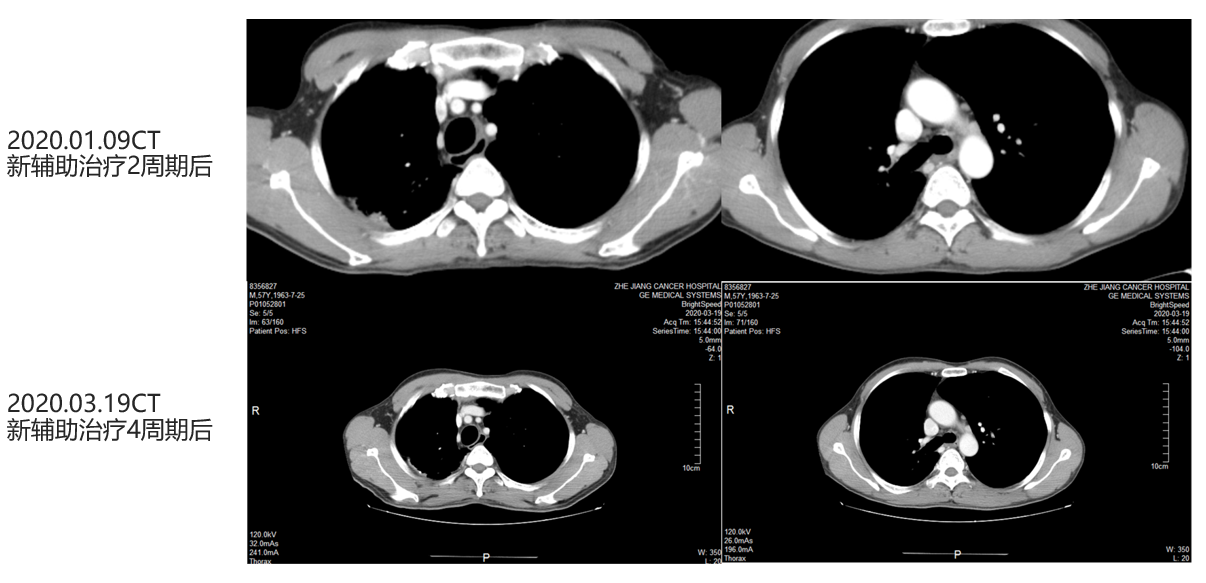
手术治疗:
排除手术禁忌症后,患者于2020.4.2在全麻下行全腔镜食管癌根治术(Mckeown),手术过程顺利,术后无吻合口瘘及肺部并发症,术后恢复可。
术后病理:
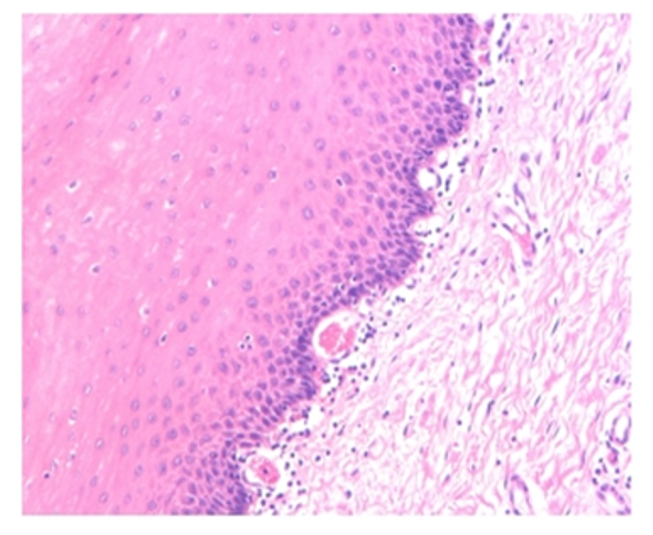
食管恶性肿瘤综合治疗后:
食管粘膜慢性炎伴部分区鳞状上皮增生,粘膜下至肌层见炎性肉芽组织形成及灶性淋巴细胞浸润(符合治疗后反应,0级)。
(食管周)1只、(胃周)9只、(右喉返神经旁)2只、(隆突下)4只、(肝总动脉旁)2只,淋巴结慢性炎。
部分胃粘膜慢性炎
网膜纤维、脂肪组织。
术后影像学检查:
CT检查诊断结果:
食管癌术后,比较2020.03.19CT:
吻合口壁未见异常增厚;左侧锁骨上小淋巴结显示。
右肺上叶慢性炎症或陈旧性病灶考虑,较前大致相仿。
肝脏多发小囊肿考虑,较前相仿,建议随访;原肝脏动脉期散在强化影此次扫描显示不清,建议复查。
脾脏右缘斑片状低密度影,脾梗死可能,建议复查;双肾多发小囊肿。
胸骨局部骨质密度增高,较前新出,转移可能,建议结合ECT。
MR检查:
影像所见:
胸骨柄局部骨质信号异常,平扫T1低信号,T2高信号,边缘不清,临近未见软组织肿胀。矢状位见胸骨体下部局限性片状异常信号,横断位信号可疑增高,余扫及骨未见异常信号:
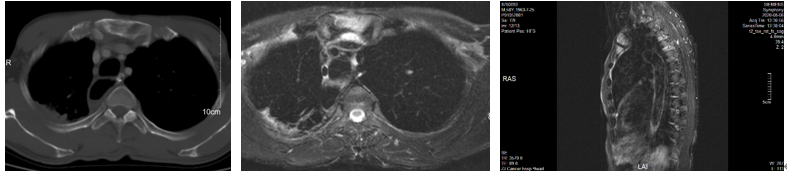
诊断结果:
胸骨柄局部骨质信号异常,考虑转移:胸骨体下部局部信号异常,请复查除外转移。
PET-CT检查诊断意见:
食管癌术后改变,吻合口区未见明显复发征象。
胸骨柄骨质密度异常伴FDG代谢轻度增高,倾向骨转移;余骨未见明显骨质密度异常及FDG代谢增高,建议随诊。
双颈部、双侧锁骨上多发淋巴结伴FDG代谢增高,炎性考虑。
双侧扁桃体炎症。
右肺上叶条片灶,无明显FDG代谢增高,倾向炎性陈旧性病变。
肝脏多发小囊肿;前列腺区钙化灶。
术后辅助治疗:
术后3月余胸骨转移转内科治疗,于2020-08-18、2020-09-08、2020-09-28、2020-10-21予以行4周期GP方案化疗,具体用药:吉西他滨,1.4g d1、8;顺铂,30mg d1-3;
2020.11.28起转放疗科行胸骨骨转移处姑息放疗,靶区包括:胸骨骨转移处;
放疗结束后患者定期复查。
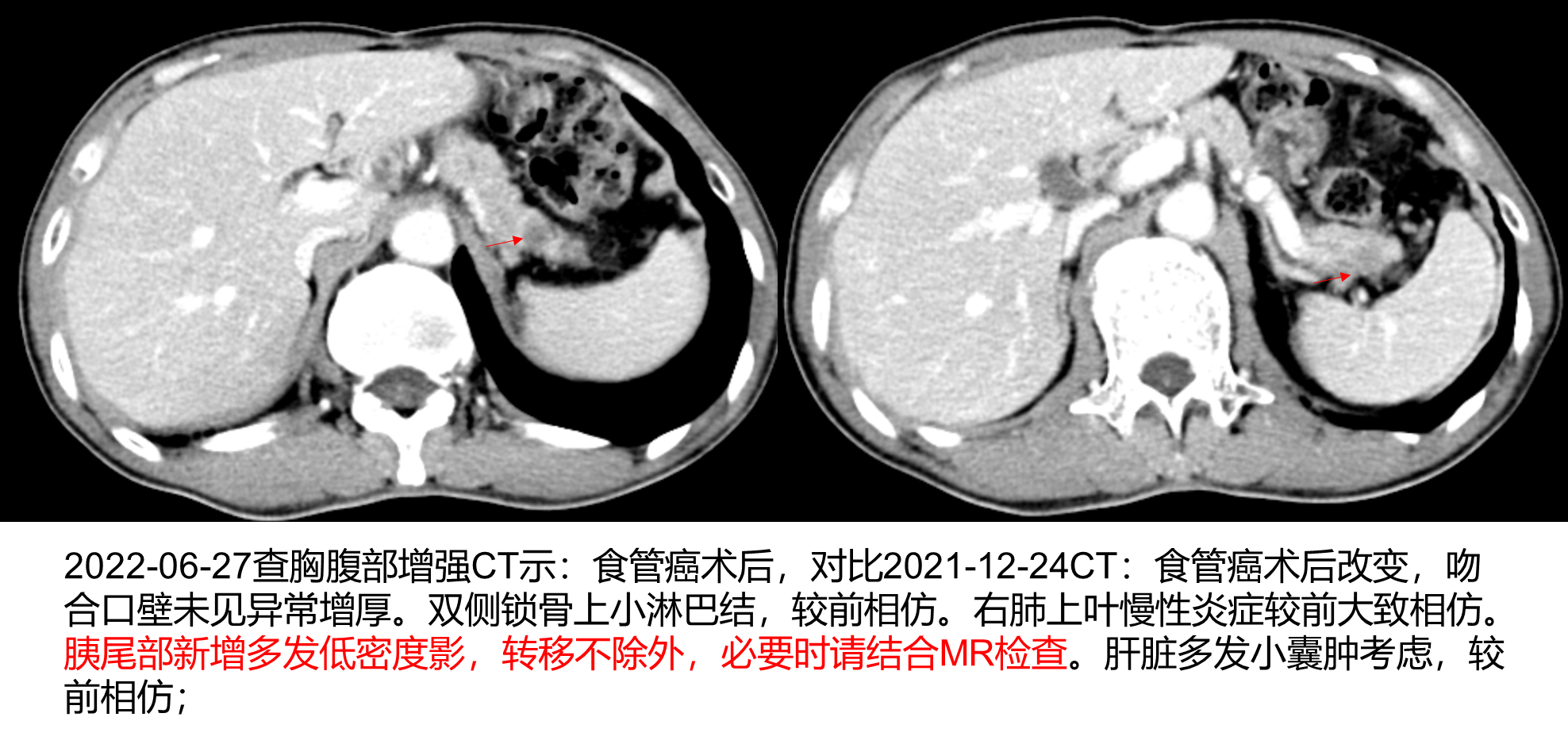
2022-06-27查胸腹部增强CT示:
食管癌术后,对比2021-12-24CT:食管癌术后改变,吻合口壁未见异常增厚。双侧锁骨上小淋巴结,较前相仿。右肺上叶慢性炎症较前大致相仿。胰尾部新增多发低密度影,转移不除外,必要时请结合MR检查。肝脏多发小囊肿考虑,较前相仿。
2022-07-12查上腹部增强MR示:
胰腺体尾部异常信号影,约4.1*1.4cm,不均匀强化;结合病史,考虑转移瘤。
进展后治疗:
食管癌术后胸骨及胰腺转移后治疗:2022-08-15~2022-11.7行第1-6周期化疗联合免疫治疗,具体方案:奥沙利铂180mg d1,PD-1抑制剂 d1,口服替吉奥40mg bid d1-14。
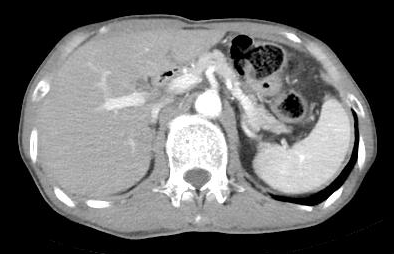
2022.10.15CT:
食管癌术后,对比2022-08-26CT:食管癌术后改变,吻合口未见明显占位。胰尾部片状低密度影,范围较前缩小,建议复查。肝脏多发小囊肿考虑,较前相仿;右肝局部灌注异常可能,较前相仿。脾脏右缘斑片状低密度影,脾梗死可能,较前大致相仿。双肾多发小囊肿。
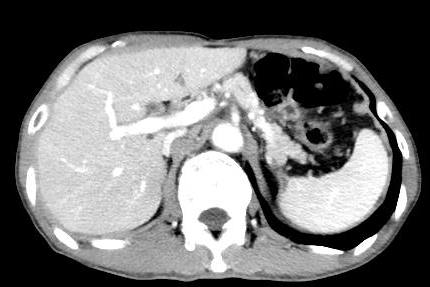
2022.11.30CT:
食管癌术后,对比2022-10-14CT:食管癌术后改变,吻合口未见明显占位。双侧锁骨上小淋巴结,较前大致相仿。右肺上叶慢性炎症,较前大致相仿。前片示“胰尾部片状低密度影”,本次显示不明确,建议复查。肝脏多发小囊肿考虑,较前相仿;右肝局部灌注异常可能,较前不明显。脾脏右缘斑片状低密度影,脾梗死可能,较前大致相仿。
复查评估胰腺病灶退缩。2022-12-06开始予斯鲁利单抗+替吉奥维持治疗。未诉明显不适,继续维持治疗中。
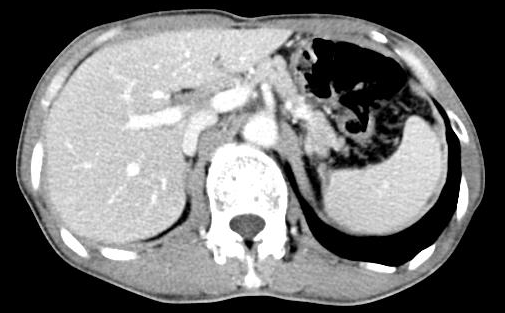
2023.4.12CT:
食管癌术后复查,对照2023-02-28 CT:食管癌术后改变,吻合口未见明显占位。双侧锁骨上小淋巴结,较前大致相仿。右肺上叶慢性炎症,较前大致相仿;右肺中叶胸膜下少许炎症,与前相仿。肝脏多发小囊肿考虑,较前相仿,请随诊;右肝局部灌注异常考虑,较前相仿。
患者结局及治疗经过:
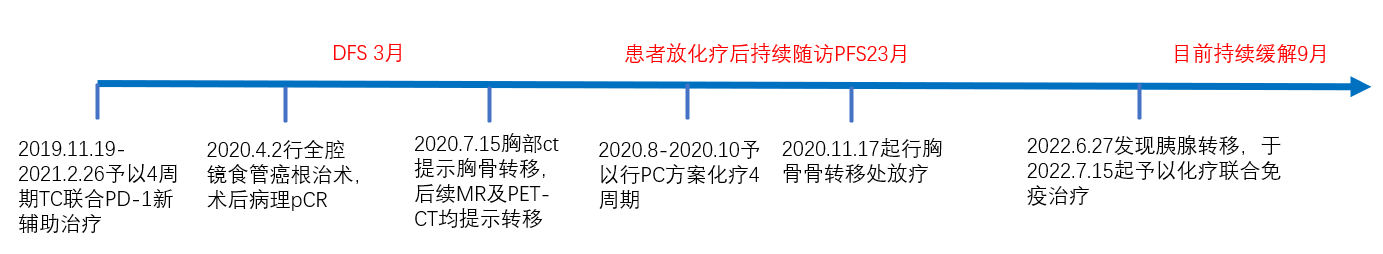
该患者初诊为食管中上段恶性肿瘤(cT4aN1-2M0 ⅣA期)。根据《2023年CSCO食管癌诊疗指南》2,对于T4a(肿瘤累及胸膜、心包或膈膜)的患者是可切除的,应考虑新辅助治疗+食管切除术,并优先推荐参加临床研究,如新辅助免疫治疗。此患者在予以4周期TC联合PD-1新辅助治疗后,行Mckeown术式(经腹+经右胸+颈部吻合术)后病理pCR。但2020.07.15胸部CT提示存在胸骨转移,后续MR及PET-CT均提示转移,随后予以PC方案化疗4周期,后行胸骨骨转移处放疗。2022.06.27又发现胰腺转移,于2022.07.15起予以化疗联合免疫治疗,后CT提示胰腺病灶退缩;2022.12.06开始予以斯鲁利单抗+替吉奥维持治疗。未诉明显不适,继续维持治疗已达9月。
讨论
目前,对于经外科评估可切除的局部进展期食管癌,新辅助免疫治疗已在一些I期和Ⅱ期临床研究中显示出安全性和初步疗效3-6,故《2023年CSCO食管癌诊疗指南》优先推荐患者参加新辅助免疫治疗临床研究2。但目前尚缺乏大型III期随机对照研究证据,因此,免疫治疗能否会成为新辅助治疗的主角目前证据依旧不足。
本案例患者尽管在新辅助免疫治疗后行Mckeown术式实现了病理pCR(病理学完全缓解),但术后仅3月余就出现复发,这不禁让人对pCR这个指标产生了怀疑。一方面,在pCR率增加的基础上推广“新治疗方案”可能会导致批准增加毒性而不改善生存的治疗;另一方面,基于未能改善pCR 而拒绝“新治疗方案”,则可能会导致放弃本可带来有利生存结果的治疗。基于此,对于其他指标在局部晚期食管癌新辅助化疗联合免疫治疗疗效预测价值的探索,比如与pCR、总生存期(OS)可能相关的血液、组织生物标记物等的探索,可能有助于更好地预测新辅助免疫治疗的疗效,从而为患者制定更加有效的新辅助治疗方案。
此外,免疫治疗在晚期食管癌领域已取得了重要进展和突破。多项免疫联合化疗与单纯化疗对比的临床研究表明,相较于单纯化疗,免疫联合化疗显著延长了晚期食管癌患者的生存期,给那些濒临困境的患者带来了巨大希望7-9。现在,免疫联合化疗已经成为我国晚期食管癌患者的一线治疗新标准方案,意义重大2。
在本案例患者出现了胰腺转移并予免疫治疗联合化疗方案后,CT提示胰腺病灶出现了退缩,这表明本案例患者能从免疫治疗联合化疗中获益,随后予斯鲁利单抗+替吉奥维持治疗,未诉明显不适。
ASTRUM-007研究显示,斯鲁利单抗联合化疗一线治疗晚期食管癌患者,显著延长了总生存期和无进展生存期,尤其在CPS≥10的患者中,总生存期长达18.6个月,较单纯化疗约长5个月。此外,在客观缓解率和缓解持续时间方面,斯鲁利单抗联合化疗都展示出明显优势,其抗肿瘤活性更强,同时安全性良好10。本案例患者使用的斯鲁利单抗,已于2023年9月22日正式获得中国国家药品监督管理局(NMPA)批准上市,用于联合化疗一线治疗局部晚期/转移性食管鳞癌(ESCC)患者,这进一步提高了肿瘤免疫治疗的可及性,给晚期食管癌患者带来了免疫治疗新手段11。
随着免疫治疗在食管癌中的探索,相信未来会有更多相关研究数据以及真实世界数据为临床用药提供支持,从而进一步改变可切除食管癌患者及晚期食管癌的治疗理念和格局。
中国科学院大学附属肿瘤医院(浙江省肿瘤医院) 胸部肿瘤外科 主治医师 博士
从事胸部肿瘤外科的临床、科研及教学工作
擅长肺癌、食管癌、纵隔肿瘤的综合治疗与个体化治疗
主要致力于局部晚期食管癌综合诊疗及临床转化研究,参与多项研究者发起食管癌免疫新辅助治疗研究,参与国际多中心食管癌免疫辅助治疗研究
博士课题主要围绕食管癌免疫微环境对免疫新辅助治疗疗效的影响
主持浙江省医药卫生科技面上项目1项
主持浙江省医药青年创新人才支持计划1项
参与国家青年科学基金及多项省级以上课题
第一作者发表SCI论文7篇,中华系列杂志医学论文2篇
中华医学会杂志社主办"集思探新,与食俱进"食管癌临床研究方案征选南部总决赛冠军
第五届“钱潮杯”肿瘤微创手术视频精英赛(肺叶组)第二名
1. 国家癌症中心,中国医师协会胸外科医师分会,中华医学会胸心血管外科学分会,等. 中国可切除食管癌围手术期诊疗实践指南(2023版).中华医学杂志,2023,103(33) : 2552-2570.
2. 中国临床肿瘤学会(CSCO).食管癌诊疗指南2023.
3. Ge F, Huo Z, Cai X, et al. Evaluation of Clinical and Safety Outcomes of Neoadjuvant Immunotherapy Combined With Chemotherapy for Patients With Resectable Esophageal Cancer: A Systematic Review and Meta-analysis. JAMA Netw Open. 2022;5(11):e2239778.
4. Xu L, Wei XF, Li CJ, et al. Pathologic responses and surgical outcomes after neoadjuvant immunochemotherapy versus neoadjuvant chemoradiotherapy in patients with locally advanced esophageal squamous cell carcinoma. Front Immunol. 2022;13:1052542.
5. Zhu J, Leng X, Gao B, et al. Efficacy and safety of neoadjuvant immunotherapy in resectable esophageal or gastroesophageal junction carcinoma: A pooled analysis of prospective clinical trials. Front Immunol. 2022;13:1041233.
6. Yang Y, Tan L, Hu J, et al. Safety and efficacy of neoadjuvant treatment with immune checkpoint inhibitors in esophageal cancer: real-world multicenter retrospective study in China. Dis Esophagus. 2022;35(11):doac031.
7. Janjigian YY, Shitara K, Moehler M, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. Lancet. 2021;398(10294):27-40.
8. Luo H, Lu J, Bai Y, et al. Effect of Camrelizumab vs Placebo Added to Chemotherapy on Survival and Progression-Free Survival in Patients With Advanced or Metastatic Esophageal Squamous Cell Carcinoma: The ESCORT-1st Randomized Clinical Trial. JAMA. 2021;326(10):916-925.
9. Doki Y, Ajani JA, Kato K, et al. Nivolumab Combination Therapy in Advanced Esophageal Squamous-Cell Carcinoma. N Engl J Med. 2022;386(5):449-462.
10. Song Y, Zhang B, Xin D, et al. First-line serplulimab or placebo plus chemotherapy in PD-L1-positive esophageal squamous cell carcinoma: a randomized, double-blind phase 3 trial. Nat Med. 2023;29(2):473-482.
11. https://www.nmpa.gov.cn/
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


