2024年CSCO指南大会由中国临床肿瘤学会(CSCO)和北京市希思科临床肿瘤学研究基金会联合主办。
4月26日下午在泉城济南市香格里拉大酒店齐鲁厅免疫治疗专场隆重召开,该领域的专家学者齐聚一堂,聚焦最新研究进展,共议临床实践热点。会议由解放军第960医院王宝成教授、中山大学肿瘤防治中心张力教授和陆军军医大学新桥医院朱波教授担任主持,山东第一医科大学第一附属医院王俊教授、武汉大学人民医院章必成教授、北京大学肿瘤医院斯璐教授分别就2024 CSCO免疫检查点抑制剂临床应用指南更新部分进行解读。
2024 CSCO免疫检查点抑制剂临床应用指南更新解读(上)
讲者:山东第一医科大学第一附属医院王俊教授
总体而言,2024年指南中,肿瘤种类没有太多变化。王俊教授结合相关研究,对免疫检查点抑制剂在八大瘤种临床应用的重点内容进行了简要介绍。
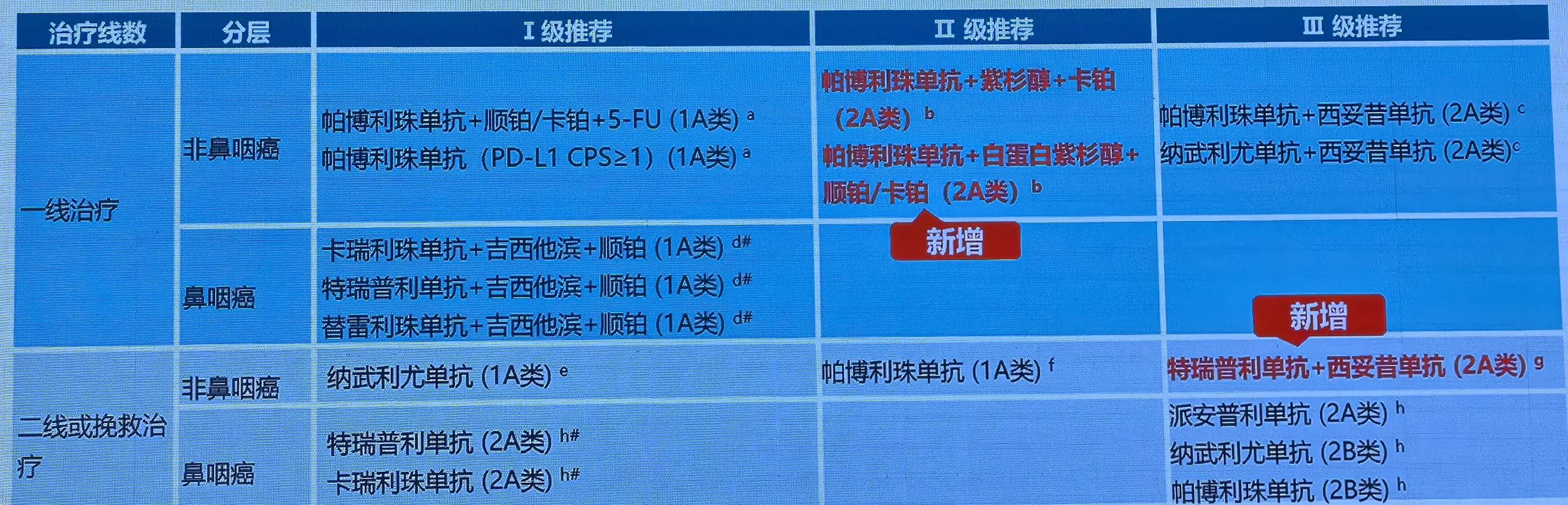
复发或转移性头颈部鳞癌:更新要点
帕博利珠单抗+紫杉醇+卡铂用于R/M HNSCC一线治疗IV期研究,结果显示,治疗ORR为42.7%,DCR为58.5%,中位DOR为5.5个月,治疗相关严重AE发生率为17.4%,整体安全性良好,将该方案新增为非鼻咽癌一线治疗Ⅱ级推荐。特瑞普利单抗联合西妥昔单抗治疗铂类难治性R/M HNSCC的Ib/II期临床研究数据显示ORR为60%,DCR为80%,中位DOR为17.9个月,中位PFS为9.9个月,中位OS为15.4个月,将该方案新增为非鼻咽癌二线或挽救治疗Ⅲ级推荐。
食管癌:更新要点
舒格利单抗联合化疗对比化疗一线治疗无法切除的局部晚期、复发或转移性试管鳞癌患者的III期临床研究提示舒格利单抗联合化疗组的中位PFS为6.2个月(对照组5.4个月),中位OS为15.3个月(对照组11.5个月),因此指南更新“舒格利单抗+顺铂+5-FU”为晚期一线治疗Ⅰ级推荐。

非小细胞肺癌:更新要点
无驱动基因突变的非鳞非小细胞肺癌
这部分改动较多,多项临床试验为指南更新提供医学证据:Neotorch研究通过特瑞普利单抗+含铂化疗新辅助+辅助治疗NSCLC III期研究,结果提示疾病进展风险降低60%,死亡风险降低38%; RATIONALE-315研究提示替雷利珠单抗+含铂化疗新辅助+辅助治疗NSCLC III期,疾病进展风险/复发风险降低44%,死亡风险降低38%;KEYNOTE-671研究提示帕博利珠单抗+含铂化疗新辅助+辅助治疗NSCLC III期研究mEFS HR为0.58,mOS HR为0.72;AEGEAN研究提示度伐利尤单抗+含铂化疗新辅助+辅助治疗NSCLC III期研究mEFS HR为0.68;CheckMate-77T研究提示纳武利尤单抗+含铂化疗新辅助+辅助治疗NSCLC III期研究mEFS HR为0.58。
基于以上研究将“特瑞普利单抗+含铂化疗新辅助+辅助治疗”增为围手术期治疗Ⅰ级推荐,新增“帕博利珠单抗、替雷利珠单抗或卡瑞利珠单抗+含铂化疗新辅助+辅助治疗”为围手术期治疗Ⅱ级推荐,将“度伐利尤单抗或纳武利尤单抗+含铂化疗新辅助+辅助治疗”为围手术期治疗Ⅲ级推荐。

驱动基因突变阳性的非鳞非小细胞肺癌
2023年5月9日,NMPA基于ORIENT-31研究批准信迪利单抗联合贝伐珠单抗及化疗治疗经EGFR-TKI治疗失败的EGFR基因突变阳性的局部晚期或转移性非鳞状NSCLC,将“信迪利单抗+贝伐珠单抗类似物+化疗”升级为晚期二线及以上治疗Ⅰ级推荐。
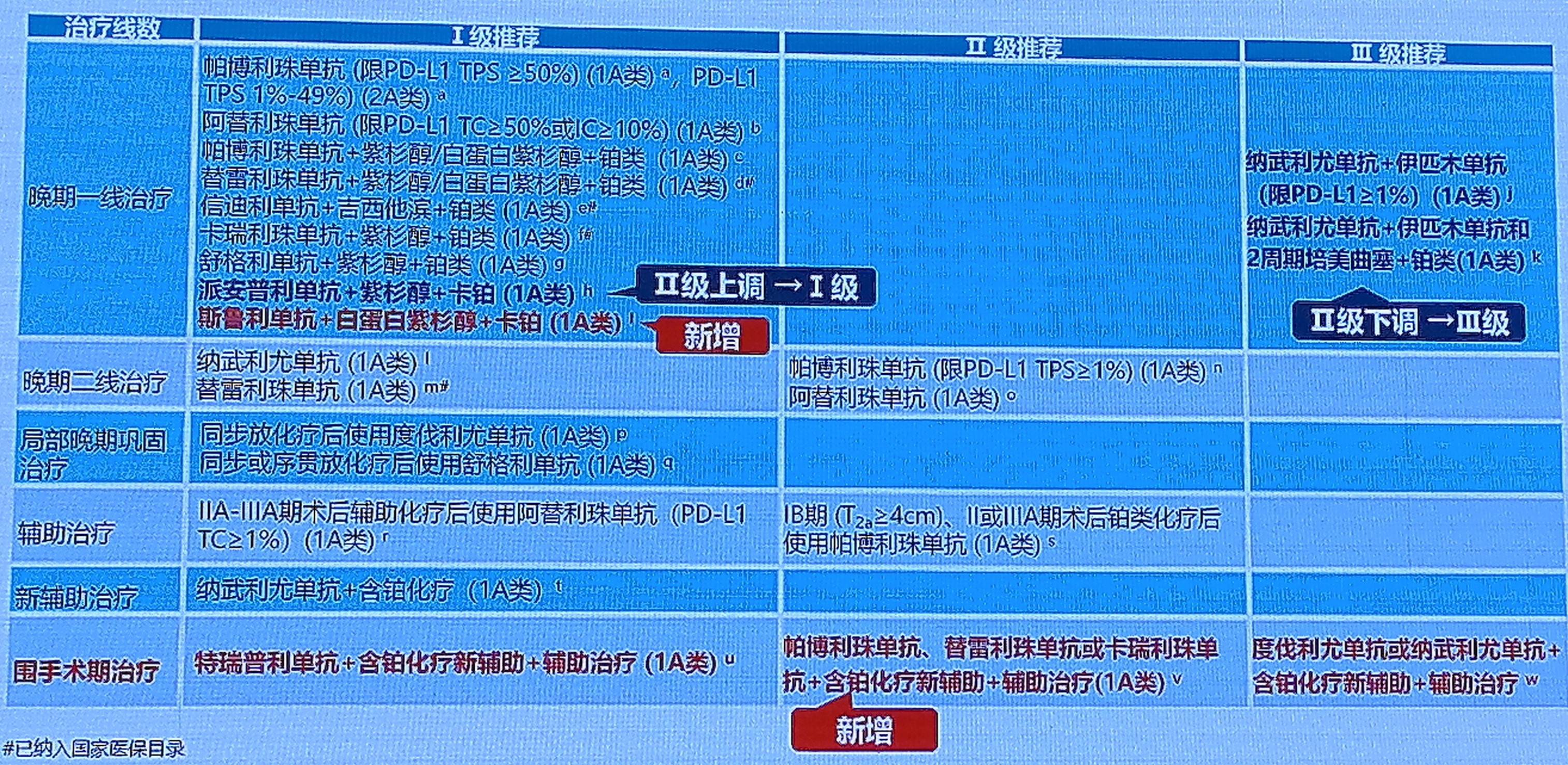
鳞状非小细胞肺癌
基于AK105-302研究,2023年1月13日,NMPA批准斯派安普利单抗联合紫杉醇和卡铂一线用于局部晚期或转移性鳞状NSCLC,将“派安普利单抗+紫杉醇+卡铂”升级为晚期一线治疗Ⅰ级推荐。基于ASTRUM-004研究,2022年11月1日,NMPA批准斯鲁利单抗联合白蛋白紫杉醇和卡铂一线用于局部晚期或转移性鳞状NSCLC,新增“斯鲁利单抗+白蛋白紫杉醇+卡铂”为晚期一线治疗Ⅰ级推荐。
广泛期小细胞肺癌:更新要点
RATIONALE-312研究提示替雷利珠单抗+依托泊苷+卡铂或顺铂一线治疗ES-SCLC III期研究中位OS延长至15.5个月,3年OS率达到25%。EXTENTORCH研究提示特瑞普利单抗+依托泊苷+卡铂或顺铂一线治疗ES-SCLC III期中位PFS为5.8个月,中位OS为14.6个月,故新增“特瑞普利单抗+依托泊苷+卡铂或顺铂”、“替雷利珠单抗+依托泊苷+卡铂或顺铂”作为一线治疗Ⅱ级推荐。
晚期恶性胸膜间皮瘤:更新要点
新指南将原指南中标题“晚期胸膜间皮瘤”改为“晚期恶性胸膜间皮瘤”。并根据帕博利珠单抗+培美曲塞+顺铂/卡铂一线治疗晚期恶性胸膜间皮瘤II/III期研究结果(中位OS延长至17.3个月,3年OS率达到25%)将“帕博利珠单抗+培美曲塞+顺铂/卡铂”列为一线治疗Ⅰ级推荐。

乳腺癌:更新要点
CheckMate7FL研究提示纳武利尤单抗用于HR+/HER2-乳腺癌新辅助和辅助治疗III期显著提高其pCR率。KEYNOTE-756研究提示帕博利珠单抗用于HR+/HER2-乳腺癌新辅助和辅助治疗III期显著提高其pCR率。TORCHLIGHT研究提示特瑞普利单抗联合白蛋白紫杉醇一线治疗晚期TNBC III期OS 32.8个月。综合以上研究结果,指南将以上方案更新,并做出不同等级推荐。

晚期胃癌:更新要点
值得一提的是,KEYNOTE-895研究,帕博利珠单抗联合化疗一线治疗HER2阴性晚期GC/GEJC III期临床研究,在ITT人群中mOS达12.9个月,在CPS≥10人群中mOS达15.7个月;GEMSTONE-303研究提示舒格利单抗联合化疗一线治疗HER2阴性、PD-L1 CPS≥5晚期GC/GEJC,mOS达15.64个月,mPFS达7.62个月。基于以上研究,将 “XELOX/FP+帕博利珠单抗(PD-L1 CPS≥10)”、“XELOX+舒格利单抗(PD-L1 CPS≥5)”新增为一线治疗(HER2阴性)Ⅰ级推荐。

肝细胞癌:更新要点
将标题由“中晚期肝细胞癌”改为“肝细胞癌”。
新增“阿替利珠单抗+贝伐珠单抗”为术后辅助治疗Ⅰ级推荐。
2024 CSCO 免疫检查点抑制剂临床应用指南更新解读(中)
讲者:武汉大学人民医院章必成教授
晚期胆道恶性肿瘤:更新解读
KEYNOTE-966研究,提示了帕博利珠单抗在治疗晚期胆道恶性肿瘤的成功,其将OS延长至12.7个月(对照组10.9个月),PFS延长至6.5个月(对照组为5.6个月),ORR均为29%。2023年10月31日,FDA批准帕博利珠单抗联合化疗一线治疗局部晚期不可切除或转移性胆道癌。故此次指南更新将 “吉西他滨+顺铂+帕博利珠单抗” 新增为一线治疗Ⅰ级推荐。

结直肠癌:更新解读
结直肠癌分为两部分:非转移性结直肠癌和转移性结直肠癌,但均限定在dMMR/MSI-H人群中。在非转移性结直肠癌方面,可根治切除的患者首要需求是器官功能保护,可直接选择PD-1/PD-L1单抗药物治疗;在不可根治切除的患者中根据2023年9月8日NMPA批准的药物适应症将Ⅱ级推荐中“PD-1/PD-L1单抗”具体改为“恩沃利单抗、斯鲁利单抗、替雷利珠单抗或普特利单抗”。在转移性结直肠癌方面,主要的变动在于考虑到双单抗方案药物副作用较大,故将原有的“纳武利尤单抗+伊匹木单抗”方案从二线治疗Ⅱ级推荐降级为Ⅲ级推荐。值得关注的是更新指南将以往笼统的“PD-1/PD-L1单抗”具体更新为“恩沃利单抗、斯鲁利单抗、替雷利珠单抗、普特利单抗”这4种药物,均基于药物的II期临床研究数据和NMPA批准的适应症。


肾癌:更新解读
在肾透明细胞癌部分,新指南在新辅助、辅助及二线治疗以上未做改动,主要在一线治疗新增了Ⅰ级推荐。RENOTORCH研究(特瑞普利单抗联合阿西替尼体像治疗晚期肾细胞癌的III期研究)结果提示PFS可提升至18个月(对照组9.8个月),ORR为56.7%(对照组为30.8%),并且2024年4月7日,该方案获得NMPA批准用于中高危的不可切除或远处转移性肾细胞癌患者一线治疗,是国内首个获批适应症的ICIs。

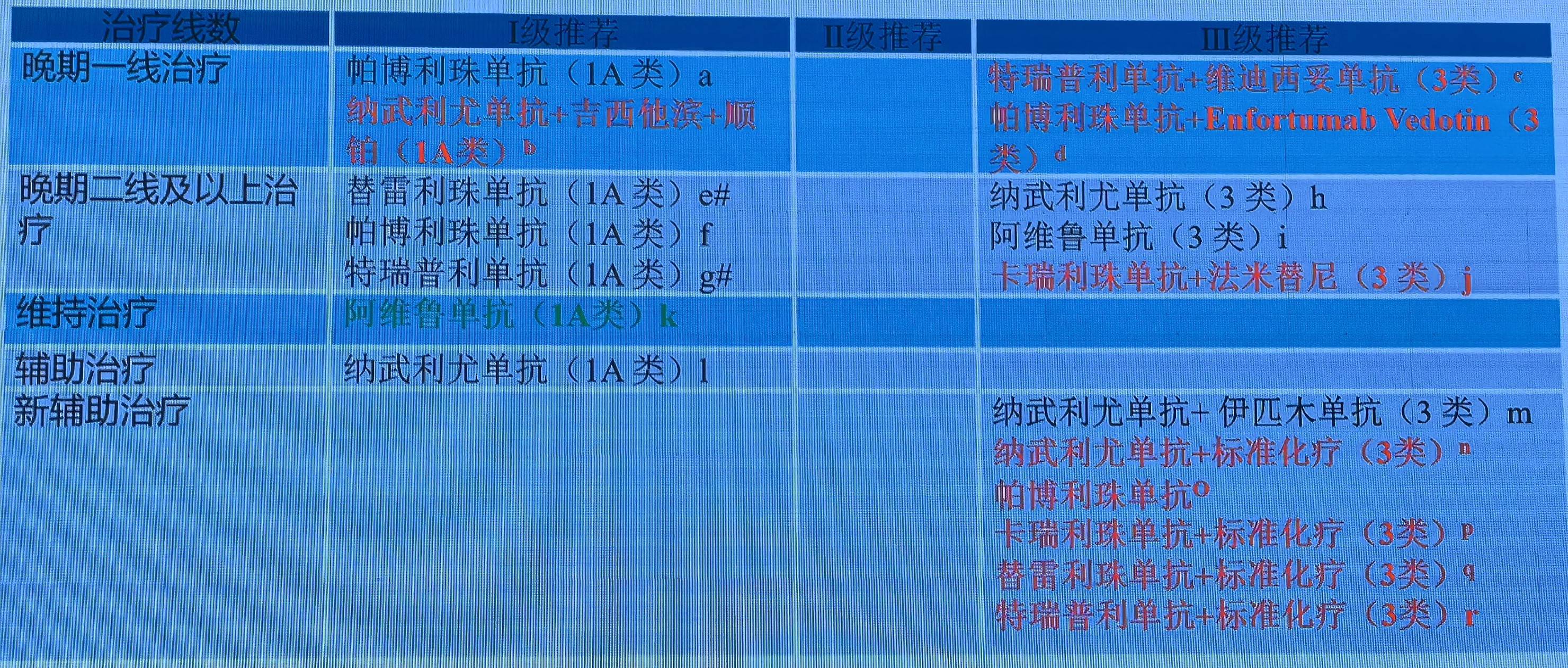
尿路上皮癌:更新解读
纳武利尤单抗+GP成为一线新标准,III期研究CheckMate901研究中的双免队列失败,但免疫+化疗队列达到终点。纳武利尤单抗成为近30余年来首个对比标准化疗可带来显著生存获益的ICIs。
基于III期ELIN Bladder 100研究,阿维鲁单抗获得FDA批准适应症,且2023年7月公布的≥2年的随访结果提示标准化疗结束以后以ICIs维持,阿维鲁单抗,独此一家。
此外,新辅助治疗方面再添5项Ⅲ级推荐。
宫颈癌:更新解读
2023年,赛帕利单抗获批用于治疗既往接受含铂化疗治疗失败的复发或转移性且PD-L1表达阳性(CPS≥1)的宫颈癌患者,故新增“赛帕利单抗(限PD-L1表达阳性患者)”为晚期二线及以上治疗Ⅱ级推荐。
复发或转移性子宫内膜癌:更新解读
新增“帕博利珠单抗+卡铂+紫杉醇(癌肉瘤除外)”为初治FIGO Ⅲ~Ⅳ期子宫内膜癌一线治疗Ⅰ级推荐。
新增“帕博利珠单抗+卡铂+紫杉醇(癌肉瘤除外)”为一线治疗Ⅰ级推荐。
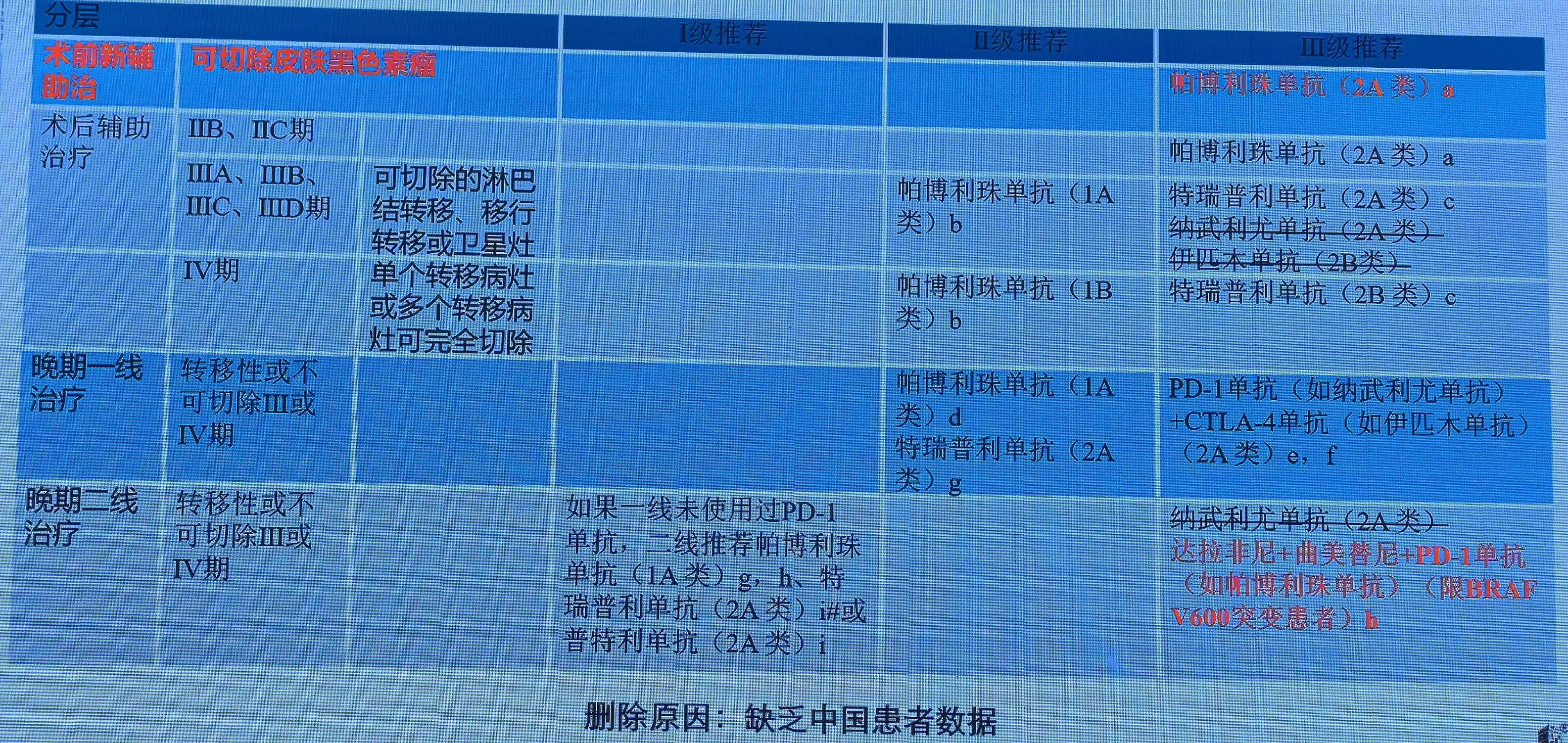
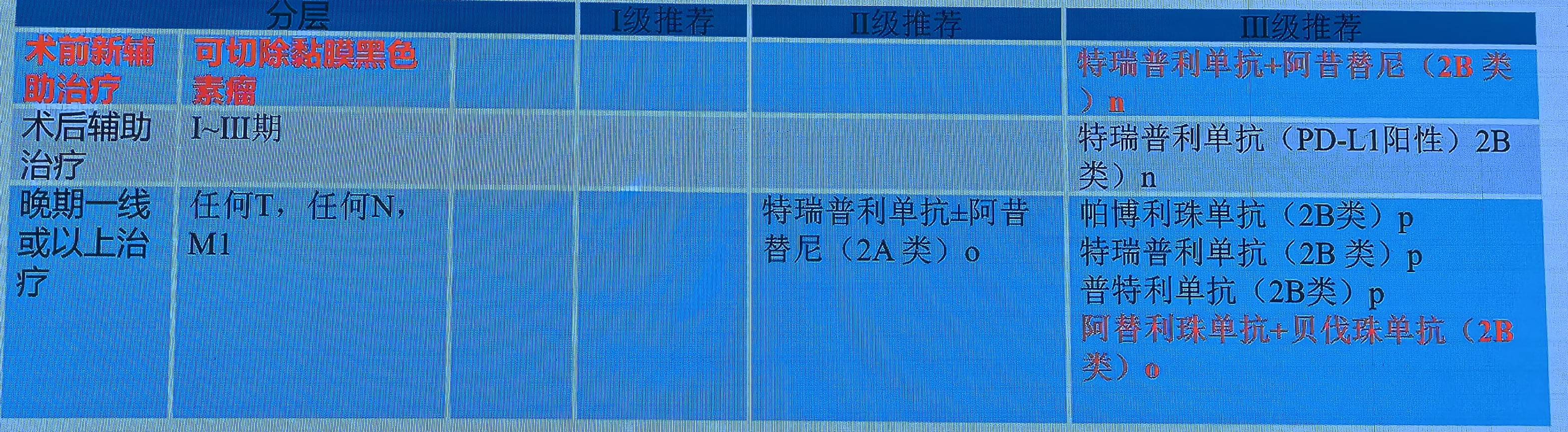
黑色素瘤:更新解读
皮肤黑色素瘤方面:一项皮肤黑色素瘤Ib期研究的5年随访将新辅助推入推荐行列。研究结果显示30例患者术前三周接受一剂帕博利珠单抗,随后是一年辅助帕博利珠单抗,中位随访时间可达61.9个月。MPR或pCR的患者无死亡(n=8),而其余患者5年OS事为72.8%;8例pCR或MPR患者中有2例复发。病理肿雇残留>10%患者中,有8例(36%)复发;病理肿瘤残留≤10%患者的中位复发时间为3.9年,>10%的患者为0.6年。故新指南将 “帕博利珠单抗” 新增为皮肤黑色素瘤新辅助治疗Ⅲ级推荐。
肢端黑色素瘤方面:晚期一线的三联组合“替莫唑胺+阿帕替尼+卡瑞利珠”的II期临床研究结果显示OPR为64%,DOR为17.5个月,DCR为88%, mPFS预计为18.4个月,成为“替莫唑胺+阿帕替尼+卡瑞利珠单抗”为肢端黑色素瘤晚期一线治疗Ⅱ级推荐证据。

黏膜黑色素瘤方面:新辅助在一项II期研究中表现良好,结果提示中位EFS为11.1个月;手术后,8例(33.3%)实现了病理缓解,其中4例(16.7%)达到pCR,4例(16.7%)达到pPR,成为“特瑞普利单抗+阿昔替尼”新增为黏膜黑色素瘤新辅助治疗Ⅲ级推荐的有力证据。
复发/难治性恶性淋巴瘤:更新解读
最主要的更新是,结外NK/T细胞淋巴瘤有了Ⅰ级推荐。GEMSTONE-201研究结果提示舒格利单抗用于治疗复发或难治性结外NKTCL患者ORR为44.9%,CR率为35.9%,12个月缓解率可达82.5%,基于此结果,2023年10月27日,NMPA批准舒格利单抗用于治疗复发或难治性结外NKTCL患者。

皮肤癌(非黑色素瘤):更新解读
皮肤癌方面改动较少,默克尔细胞的新辅助治疗研究显示36例手术患者47.2%获得pCR,故新增“纳武利尤单抗”为默克尔细胞癌新辅助治疗Ⅲ级推荐。

2024 CSCO免疫检查点抑制剂临床应用指南更新解读(下)
讲者:北京大学肿瘤医院斯璐教授
斯璐教授对免疫检查点抑制剂临床应用指南(附录部分)的更新进行了阐述,介绍了附录部分新增的免疫治疗的非典型反应特征和免疫检查点抑制剂治疗预测标志物,以及NMPA批准的免疫检查点抑制剂适应症的更新。
新增附录1:免疫治疗的非典型反应特征
免疫治疗独特的作用机制,导致其应答不同于传统化疗和靶向治疗,具有非典型反应特征,包括:延迟反应、假性进展、分离反应和超进展。

KEYNOTE-189研究、RATIONALE-304研究、III期POSEIDON研究等多项免疫治疗研究中观察到延迟反应,表现为免疫起效/缓解时间具有较大的个体差异。针对NSCLC免疫治疗可能出现的延迟反应特征,2023年11月,CSCO免疫治疗专家委员会联合领域专家共同制定《“拯救生命的另一半”肺癌免疫治疗持续用药规范化白皮书》中倡议:对于首次疗效评估为SD的患者推荐继续治疗,4周期导入治疗后再评估才能更准确判断患者免疫治疗是否获益,应充分了解免疫反应的个体化差异,提前终止免疫治疗潜在影响患者免疫治疗的获益。
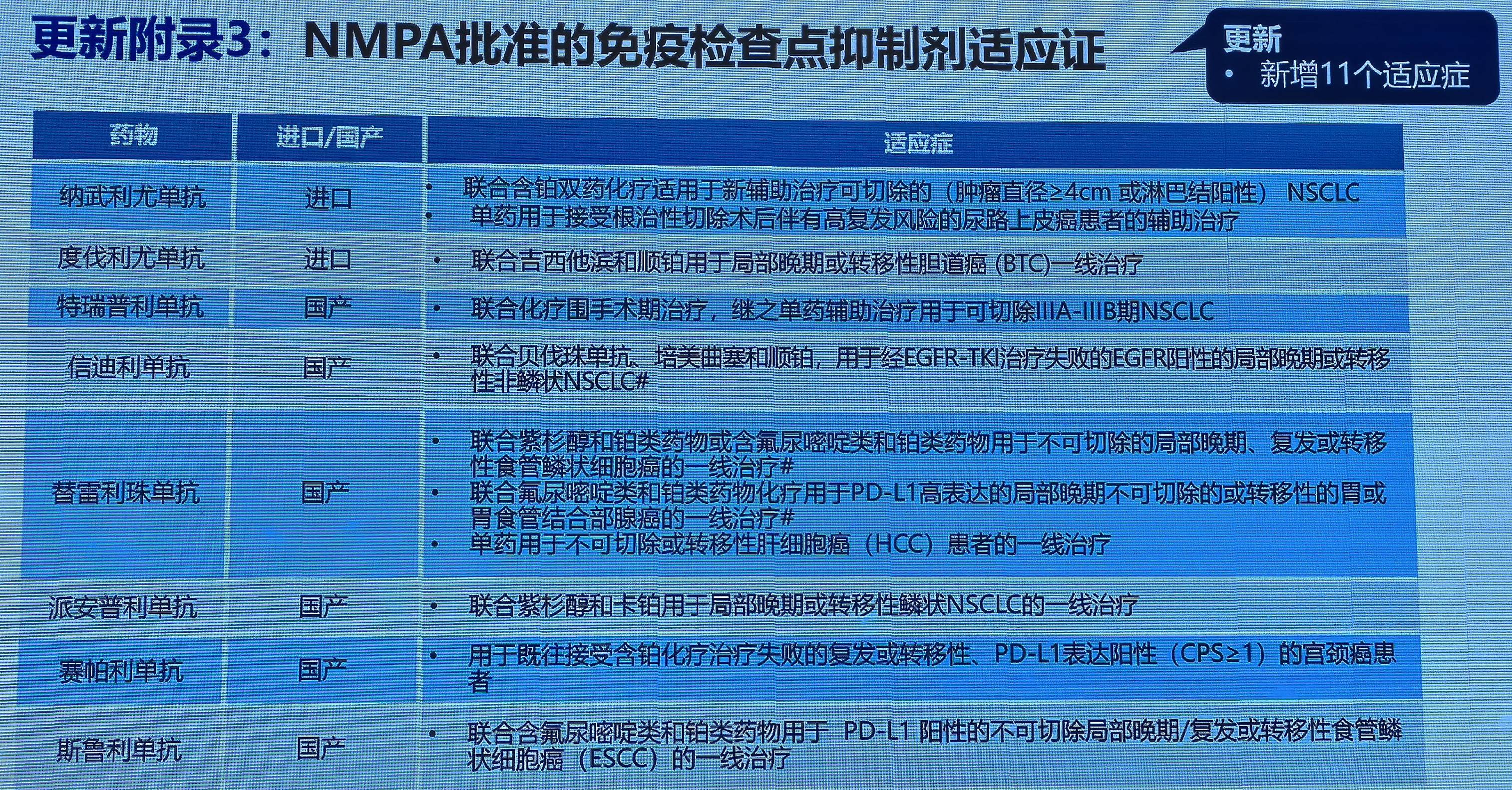
更新附录3:NMPA批准的免疫检查点抑制剂适应症
替雷利珠单抗新增3个适应症,纳武利尤单抗新增2个适应症,度代利尤单抗、特瑞普利单抗、信迪利单抗、派安普利单抗、赛帕利单抗、斯鲁利单抗各新增1个适应症。
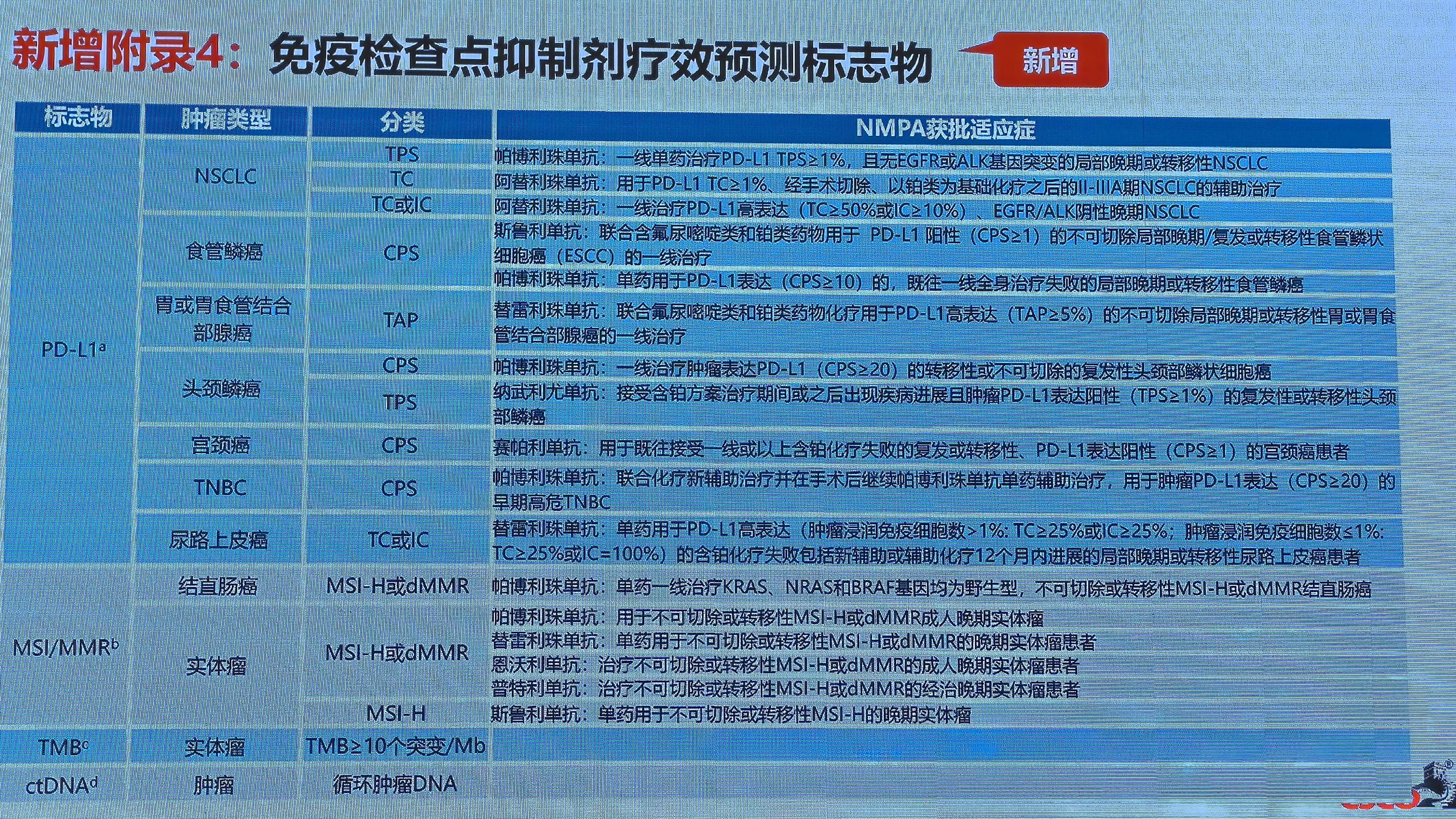
新增附录4:免疫检查点抑制剂治疗预测标志物
多项研究及检测显示出免疫检查点抑制剂治疗预测标志物对相对应的肿瘤类别预测的重要价值,可供临床参考及查阅。
排版编辑:肿瘤资讯-Nydia
阅读推荐
2024 CSCO指南会 | 与时俱进,前瞻未来:结直肠癌诊疗指南更新要点速览
2024 CSCO指南会 | 杨宏英教授详解子宫内膜癌新进展











 苏公网安备32059002004080号
苏公网安备32059002004080号


