中年男性患者,诊断“左肺鳞癌伴左侧锁骨上淋巴结转移(cT2N3M0,IIIB)”,PS评分0-1分。一线使用“K药+化疗”治疗8.5个月后进展;二线更换化疗药物,未见良好响应,于2周期后再次进展。三线使用“卡度尼利单抗+安罗替尼”治疗,1个月达PR,后持续稳定,PFS已超过16个月。
病例分享专家
副主任医师 医学博士 硕士生导师 副教授
CSCO血管靶向治疗专家委员会委员
中国抗癌协会恶性间皮瘤专业委员会委员
浙江省抗癌协会肿瘤内科专委会青委副主委
中国医药教育协会肺癌医学教育委员会委员
浙江省预防医学会肺癌预防与控制专委会委员
浙江省免疫学会肿瘤免疫与生物治疗专委会青年委员
主要从事胸部肿瘤治疗与肿瘤微环境的信号通路及分子机制研究
作为项目负责人支持国家自然科学基金、浙江省自然科学基金等多项课题,在Oncogene、EMBO Rep、Nat Commun、Cell Death&Dis等国际知名杂志发表论文多篇。
病史回顾
【患者】男,58岁
【主诉】以“发热伴咳嗽1周”为主诉入院。
【病例特点】患者于2021年11月24日因“发热伴咳嗽”于外院就诊,查PET-CT提示“左肺下叶中央型肺癌伴阻塞性肺不张,左侧肺门及纵膈,左侧锁骨上多发淋巴结转移”,外院纤维支气管镜检查示“左下叶开口新生物”,左下肺刷检+快速细胞学诊断示“鳞状细胞癌”;为进一步诊治,转诊浙江省肿瘤医院。PS评分1分。
【辅助检查】
(2021-11-24)外院PET-CT:1、左肺下叶中央型肺癌伴阻塞性肺不张,左侧肺门及纵膈,左侧锁骨上多发淋巴结转移;2、肺气肿,右肺中叶、左肺舌段少许纤维灶;3、前列腺轻度增生伴少许钙化。
外院纤维支气管镜检查:左下叶开口新生物。病理:(左下肺新生物活检)送检物均为坏死组织。左下肺刷检+快速细胞学诊断:鳞状细胞癌。
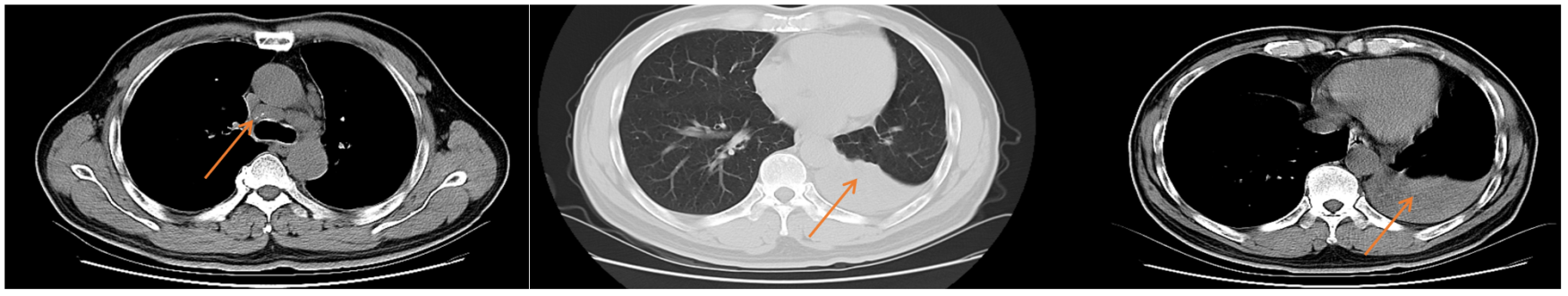
(2021-11-26)我院CT:1、左肺下叶中央型肺癌(3.8x2.7cm)伴阻塞性肺不张;2、左侧锁骨上、纵隔、左肺门多发肿大淋巴结,考虑转移;3、两肺慢支肺气肿;4、双肺多枚粟粒灶;5、左侧胸腔少许积液;
病理会诊:(左肺刷检)找到非小细胞癌细胞,细胞形态考虑鳞癌。
颅脑MRI未见异常。
诊断
1、左肺鳞癌伴左侧锁骨上淋巴结转移(cT2N3M0,IIIB)
治疗
【一线治疗】
2021年12月01日至2022年02月10日:予“免疫+化疗”方案治疗4周期,具体为:(白蛋白结合型)注射用紫杉醇 0.18g d1+顺铂注射液 40mg d1-3+帕博利珠单抗注射液 200mg d1。
治疗1个月后,复查CT提示病灶较前明显缩小,肿瘤标志物较前降低,疗效评价为PR。
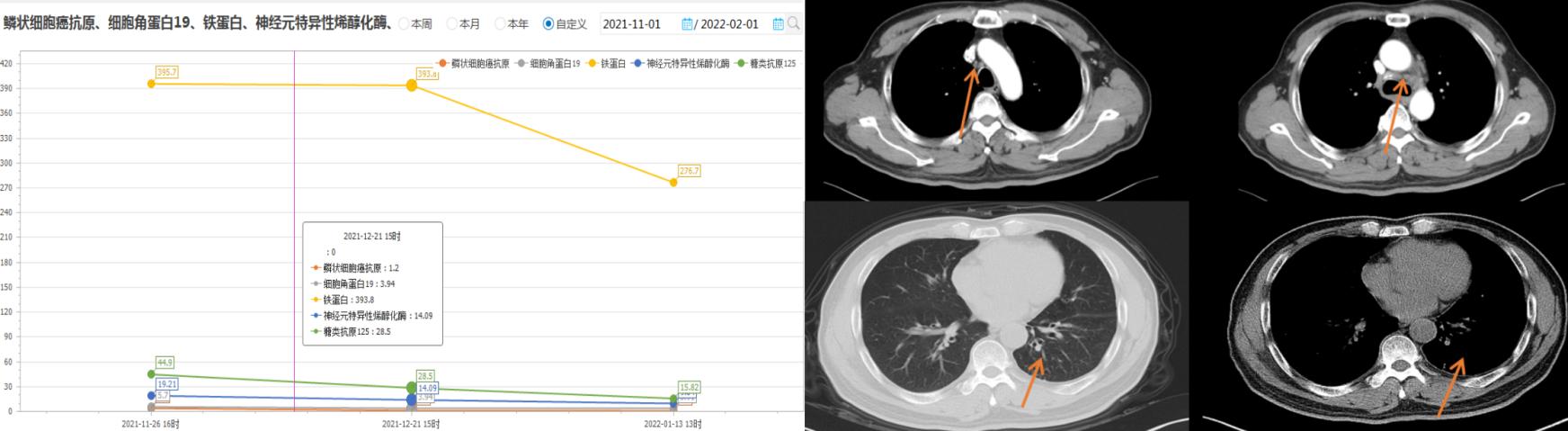
2022年03月11日:复查PET-CT提示仍有肿瘤残留,故加用局部放疗,于2022-03-18至2022-04-28行胸部调强放疗,照射肺部原发灶及纵膈阳性淋巴结区,95%PTV体积剂量为6000cGy/30F QD。
2022年06月08日起:予免疫单药维持治疗2周期。
2022年08月22日:患者诉胸闷气急、咳嗽咳痰加重,伴痰中带血、声嘶,反复发热,最高体温:38℃。复查CT提示:左肺门区软组织增厚伴结节,较前明显,伴左下肺支气管闭塞,左肺下叶远端少许阻塞性肺不张。
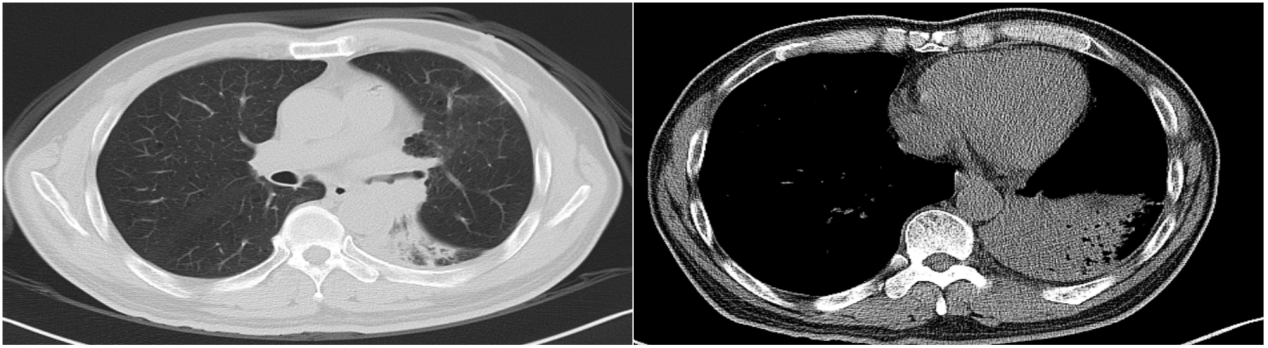
查肺部肿瘤标志物:糖类抗原125:36.77↑U/ml,鳞状细胞癌抗原:2.20↑ng/mL均较前升高。
血气分析:酸碱度:7.41,氧分压:69↓mmHg,血氧饱和度:94%,二氧化碳分压:42mmHg,标准碳酸氢根:26.2↑mmol/L,乳酸:1.4mmol/L。
超敏C反应蛋白:76.48↑mg/L。
结核菌涂片组套、隐球菌染色组套、痰液培养未见阳性结果。
2022年08月25日:行“内镜下肿物切除+止血封堵术”,术中见:左主支气管远端菜花样隆起新生物,表面粗糙,左肺下叶完全阻塞,左肺上叶管腔通畅。
术后患者症状好转,炎症指标较前明显下降,超敏C反应蛋白:24.16↑mg/L。
病理活检:(左主支气管)鳞状细胞癌。考虑疾病进展。一线PFS为8.5个月。
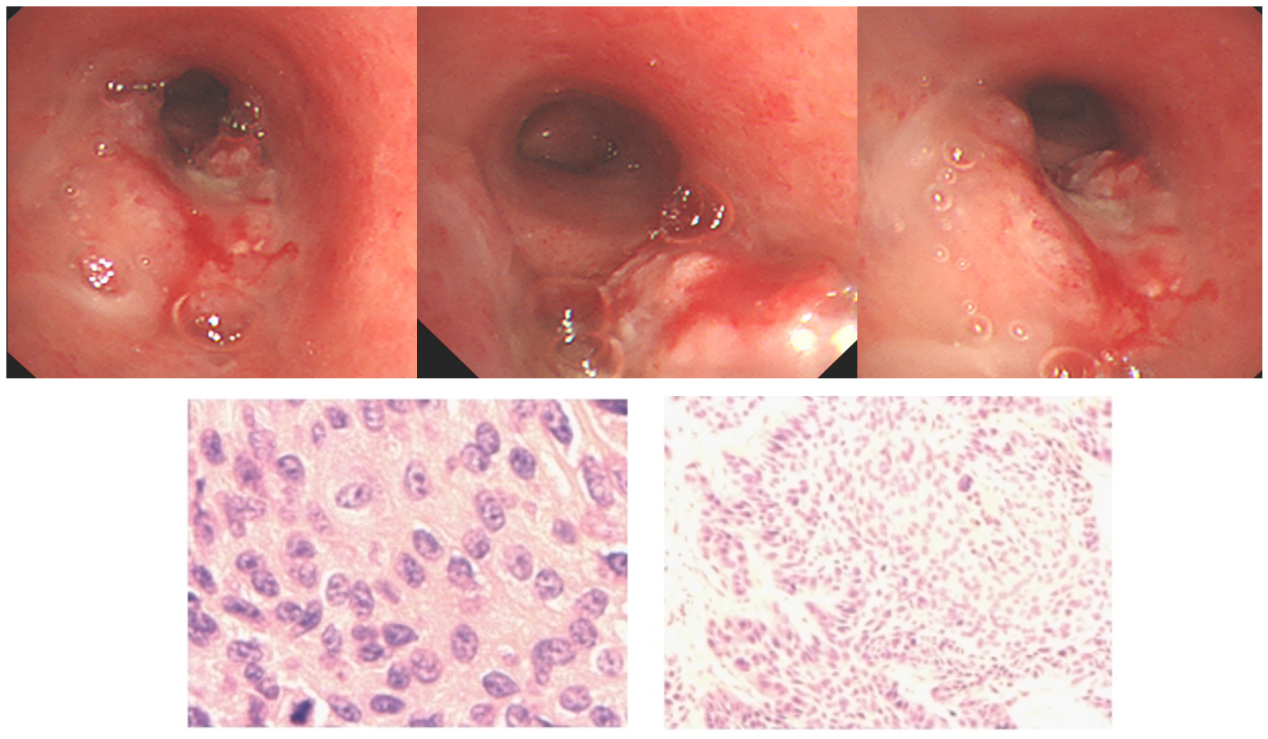
【二线治疗】
患者拒绝临床研究筛选。
2022年09月14日至2022年10月12日:予更换化疗药物,行“免疫+化疗”治疗,具体为:吉西他滨+帕博丽珠单抗。
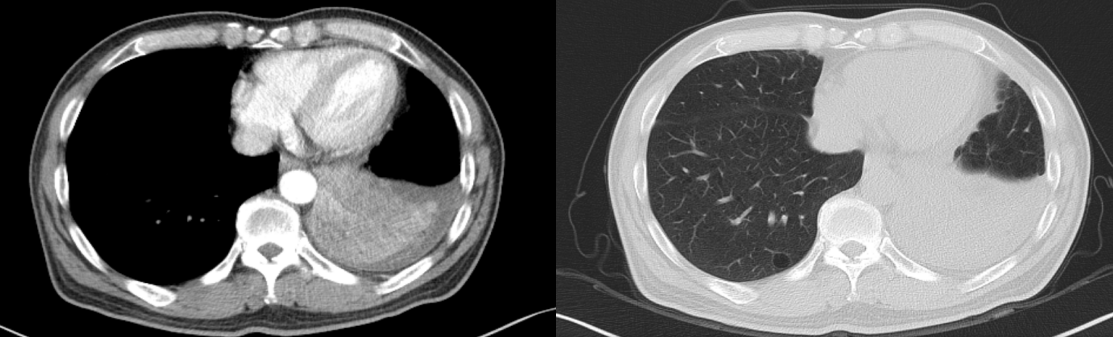
2022年11月02日:治疗2周期后,复查CT提示:1、左肺门软组织肿块(3.8x2.5cm),伴左下肺支气管阻塞,左下叶阻塞性肺不张,较前明显;左侧少量胸腔积液,左上肺炎症较前吸收;2、左侧锁骨上、纵隔、左肺门多发增大淋巴结,较前明显;3、两肺慢支伴肺气肿,双肺多枚粟粒灶,较前大致相仿。
疗效评价为PD。
【三线治疗】
患者仍拒绝筛选临床研究。
2022年11月09日起:予“卡度尼利单抗+抗血管”方案治疗,具体为:卡度尼利单抗625mg/d1+安罗替尼12mg/d1-14
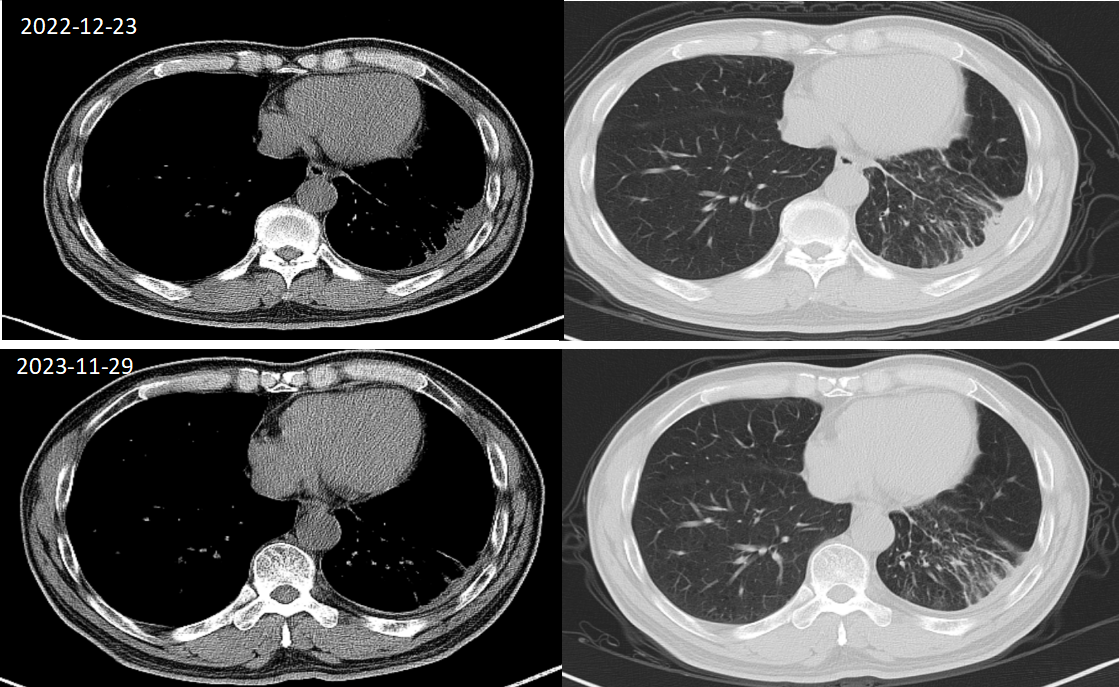
2022年12月23日:治疗1个月后,复查CT提示:1、左肺门区软组织肿块(2.5x2.2cm),较前明显退缩,左侧少量胸腔积液;2、左侧锁骨上、纵隔、左肺门多发增大淋巴结,较前相仿;3、两肺慢支伴肺气肿,双肺多枚粟粒灶,较前大致相仿。
疗效评价为PR。
继续该方案治疗,后规律复查,疗效稳定,未见明显不良反应。三线PFS已超16个月。
病例点评专家
副主任医师 博士 硕士生导师 副教授
浙江省卫生高层次人才培养对象
浙江大学药学院研究生校外导师
CSCO非小细胞肺癌专家委员会委员
CSCO青年专家委员会委员
中国抗癌协会第二届肿瘤药物临床研究专委会委员
中国抗癌协会肿瘤支持治疗专业委员会委员
中国医药教育协会肿瘤转移专业委员会委员
浙江省抗癌协会肿瘤内科专委会委员兼秘书
浙江省抗癌协会肺癌专业委员会青年委员
获2021浙江省科学技术进步二等奖(第二完成人)
主持国家自然科学基金、浙江省自然科学基金、浙江省医药卫生科技计划面上项目,人才振兴“40”计划项目等6项;发表SCI论文近40篇
免疫治疗已经极大地改变了无驱动基因突变的晚期非小细胞肺癌的治疗前景,为许多患者带来了生存获益。然而,即使是初治有效的患者,继发性耐药亦不可避免。正如此病例中,晚期肺鳞癌患者一线使用“免疫+化疗”治疗后达到PR,实现了8.5个月的PFS,但随后则发生疾病进展。免疫耐药后的有效治疗策略是临床上的重点、难点问题。
该患者二线治疗时选择延用原有免疫治疗药物,重启化疗并更换化疗方案,并未起到良好响应,2周期后就再次进展。可见,目前临床实践中常见的“化疗+继续免疫治疗”的方案并不能满足目前的临床需求,我们仍需进行个体化的探索。
那么,对于免疫继发性耐药的人群,有什么方法可以使其再次获益呢?实际上,联用免疫检查点抑制剂的免疫再挑战方案,是克服耐药的有效选择。从机制上看,抗CTLA-4与抗PD-(L)1协同作用于肿瘤免疫循环的不同阶段,并且PD-1和CTLA-4在肿瘤浸润淋巴细胞中高度共表达,为联用提供了基础[1]。
相较于双免联合的方案,双特异性抗体更是低毒高效的新选择。卡度尼利单抗“一药双靶”的特点,使其一方面能同时具备抗PD-1和抗CTLA-4的生物学活性,另一方面通过Fc段改造减少了不良反应的发生率[2],有利于提高依从性,为联合治疗提供了空间。
在AK104-208研究中,卡度尼利单抗联合安罗替尼治疗PD-(L)1抑制剂耐药的NSCLC患者,DCR高达100%。本文中,患者三线治疗也选用了该方案,在用药1个月后即达PR,疗效显著,且PFS已超过16个月。卡度尼利单抗为该患者带来了明确的生存获益,也提高了患者的生活质量,让我们看到了双抗在非小细胞肺癌免疫耐药后治疗中的曙光和希望。
综上,临床中对于免疫治疗后耐药的非小细胞肺癌患者,需要进行精准的个体化治疗。当前,在化疗和单免治疗难以克服免疫耐药的情况下,卡度尼利单抗不失为免疫再挑战的有效选择。
1.Chen, D. S., & Mellman, I. 2013, Immunity, 39(1), 1–10.
2.Pang X, et al. Cadonilimab, a tetravalent PD-1/CTLA-4 bispecific antibody with trans-binding and enhanced target binding avidity. MAbs. 2023;15(1):2180794.
3.2021 ESMO Abstract#1300P
排版编辑:肿瘤资讯-Rex











 苏公网安备32059002004080号
苏公网安备32059002004080号


