关注专题,查看全系列精要解读
随着肿瘤精准分型及药物研发的飞速发展,晚期乳腺癌的诊疗研究也在不断取得新的突破。为了帮助大家更好地了解这一领域的最新进展,【肿瘤资讯】特别邀请复旦大学附属肿瘤医院王碧芸教授,对2023年不同分型晚期乳腺癌的诊疗进展进行了深入的梳理和解读。
复旦大学附属肿瘤医院乳腺及泌尿肿瘤内科
中国临床肿瘤学会CSCO 青委会 主任委员
中国临床肿瘤学会CSCO 患教专家委员会 常务委员
中国临床肿瘤学会CSCO 乳腺癌专家委员会 委员
上海抗癌协会癌症康复与姑息治疗专委会CRPC 副主任委员兼秘书长,候任主委,青委主任委员
上海市抗癌协会乳腺癌专业委员会 常务委员
上海市抗癌协会青年理事会 常务理事
HR阳性乳腺癌的研究进展
CDK4/6抑制剂一线治疗的最新进展
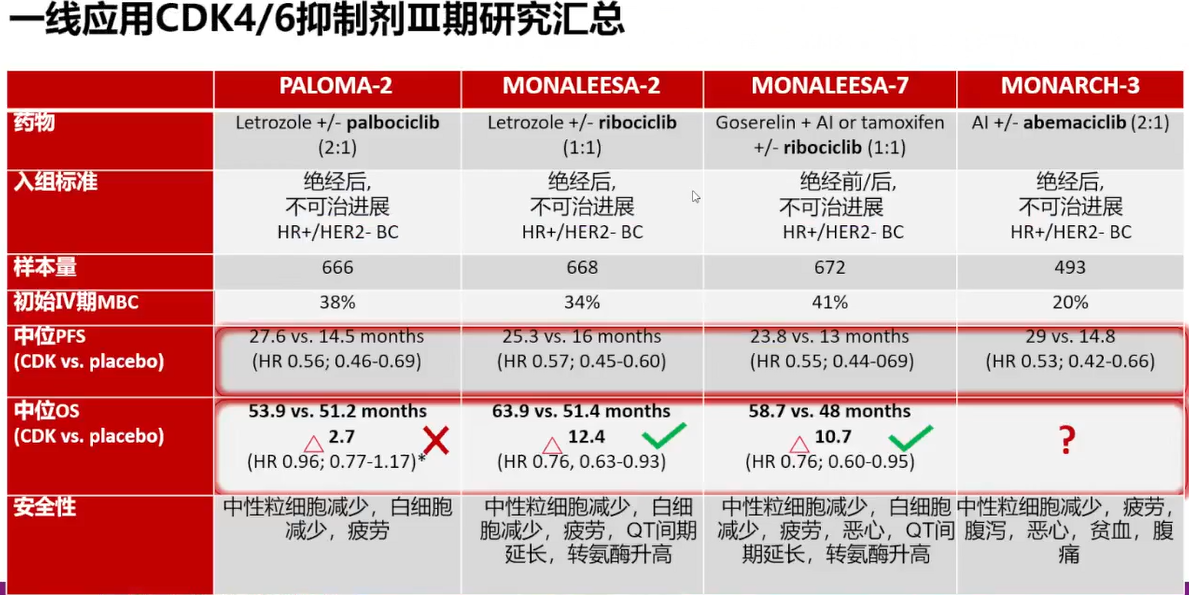
在CDK4/6抑制剂作为一线治疗的Ⅲ期研究中,PALOMA-2(哌柏西利)、MONALEESA-2和MONALEESA-7(瑞波西利)和MONARCH-3(阿贝西利)均取得了中位无进展生存期(PFS)的显著获益,但在总生存期(OS)方面呈现出不同的结果。在MONALEESA-2和MONALEESA-7研究中,观察到OS的显著提升,两个研究的风险比(HR)均为0.76[1,2]。然而,PALOMA-2研究的OS结果并未显示出统计学上的显著差异(HR=0.96)[3]。同样,在2023年圣安东尼奥乳腺癌研讨会(SABCS),MONARCH-3研究的最终分析结果揭示了阿贝西利联合非甾体类芳香化酶抑制剂(NSAI)作为一线治疗晚期乳腺癌时,中位OS达到了66.8个月,相较于对照组延长了13.1个月(HR=0.804;95% CI: 0.637~1.015;P=0.0664),这一延长在临床上具有重要意义,尽管P值未能达到统计学上的显著性差异[4]。
表1 一线应用CDK4/6抑制剂Ⅲ期研究汇总
CDK4/6抑制剂的应用策略
在CDK4/6抑制剂进入临床一线以后,关于其应用策略的诸多问题仍待解答。今年的研究进展为这些问题提供了新的见解,包括研究结果差异的潜在原因、最佳治疗搭档的选择、一线治疗的适宜性以及疾病进展后的治疗方案。
在最佳治疗搭档的选择上,PARSIFAL研究的长期随访数据(中位随访59.7个月)揭示了新的视角。研究发现,在HR+/HER2-晚期乳腺癌的一线治疗中,哌柏西利联合氟维司群与哌柏西利联合来曲唑相比,患者的OS延长了近7个月,尽管两组间的差异在统计学上不显著[5]。这表明,与来曲唑的联合治疗有效,而与氟维司群的联合也是一个可行的选择。PARSIFAL研究中的一个显著发现是,对于治疗反应的预后预测。对于那些中位PFS<12个月的患者,其中位OS仅为24个月。相反,如果患者的PFS≥12,其中位OS可达81.5个月。这一发现为内分泌耐药的判断提供了新的标准。以往,我们通常将6个月作为判断内分泌耐药的界限,但CDK4/6抑制剂的应用使得12个月成为了一个更为合理的界限。这一界限对于评估患者的长期预后以及指导后续内分泌治疗的选择具有重要意义。对于PFS超过12个月的患者,其预后通常较好,这可能对后续治疗决策产生积极影响。
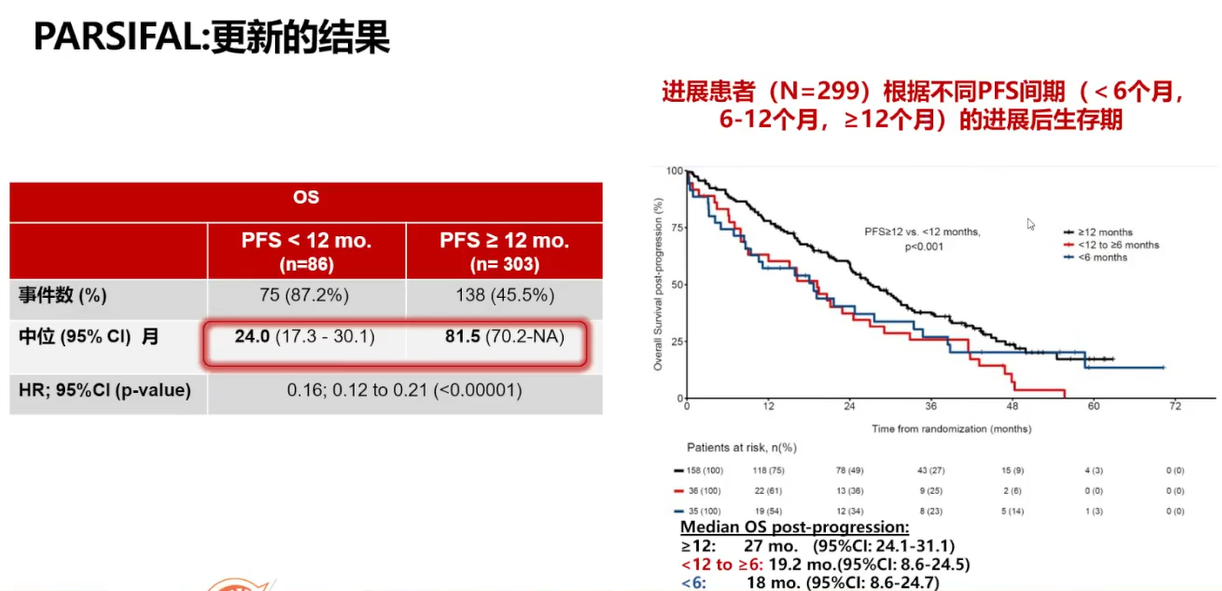
图1 PARSIFAL研究根据PFS界限分析的OS结果
关于是否所有的患者都需要一线就接受CDK4/6抑制剂,SONIA研究结果提供了参考。该研究发现,一线使用CDK4/6抑制剂的患者与二线使用该类药物的患者相比,中位PFS2分别为31.0个月和27.8个月(HR=0.87; 95%CI: 0.74~1.03; P=0.1) [6]。这一结果表明,尽管一线使用CDK4/6抑制剂能带来约4个月的PFS2延长,但这种延长是以较长时间使用CDK4/6抑制剂和随之而来的更大毒性为代价的。研究中,3级以上不良事件增加了42%。因此,SONIA研究提示我们,在决定是否在一线治疗中使用CDK4/6抑制剂时,可能需要根据患者的个体情况,权衡疗效与毒性之间的关系。
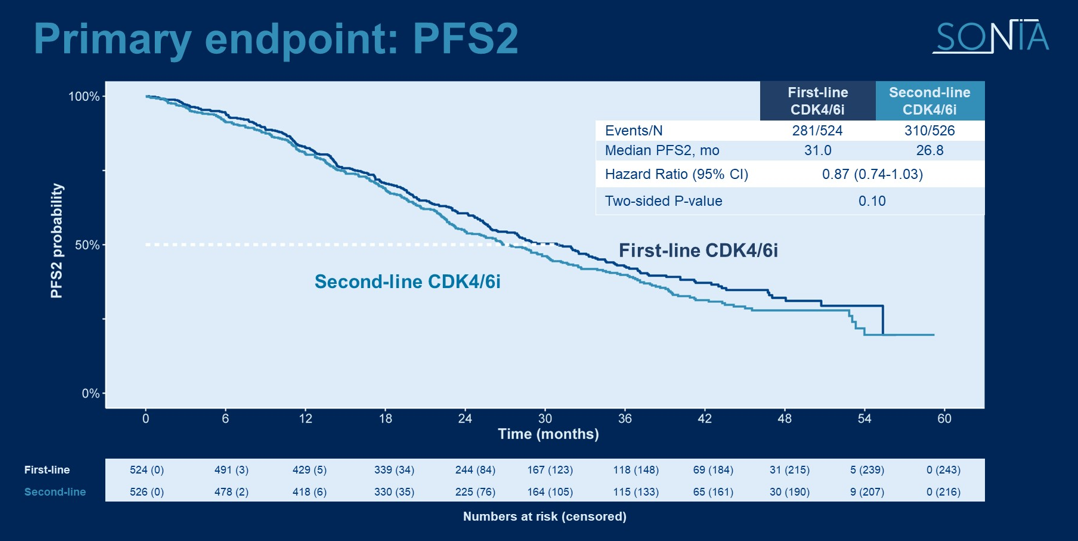
图2 一线CDK4/6抑制剂和二线CDK4/6抑制剂治疗的PFS2
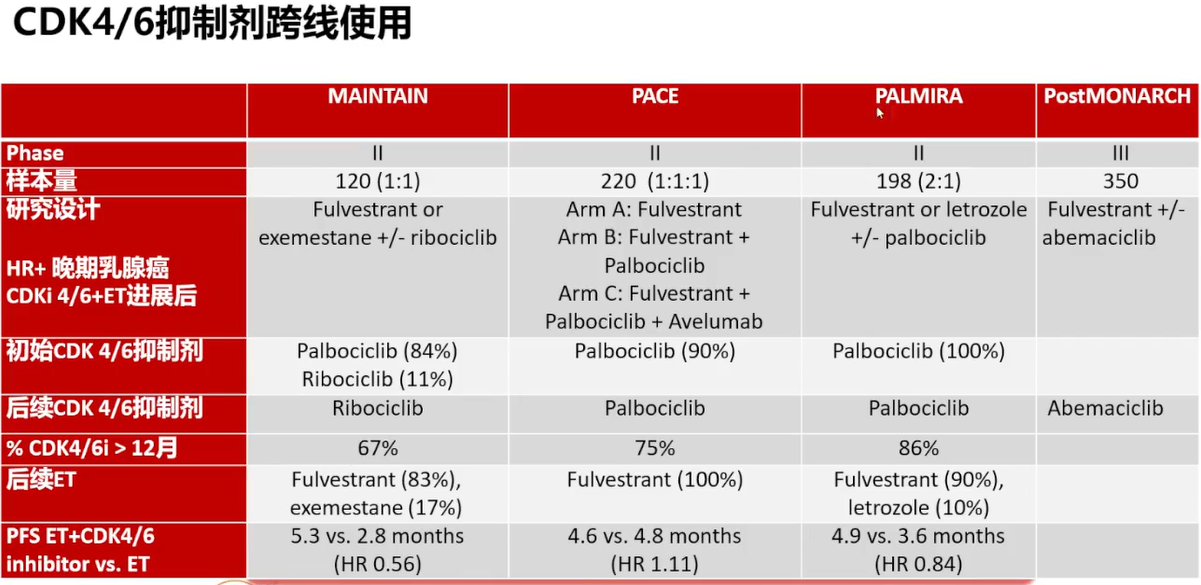
在晚期乳腺癌治疗中,面对疾病进展后的挑战,一些研究采用了跨线治疗的策略。MAINTAIN研究虽然在小样本中显示了一定的疗效,但其结果仍需进一步验证。备受期待的III期PostMONARCH研究将为我们提供更多关于跨线治疗的深入见解。在临床实践中,医生在选择跨线治疗时会综合考虑疗效、药物可及性以及经济负担等因素。至于联合治疗方案,INAVO120研究中的PI3Kα抑制剂Inavolisib与哌柏西利和氟维司群的联合应用,在治疗PIK3CA突变的HR+/HER2-局晚期或转移性乳腺癌患者时,显示出显著的PFS获益。然而,这种联合治疗也伴随着较高的毒副作用[7]。在慢性病管理的整体理念下,如何在确保疗效的同时平衡毒性,仍是临床实践中需要进一步探讨和验证的问题。
表2 CDK4/6抑制剂跨线使用的研究
新药研发进展
在新药研发领域,elacestrant基于EMERALD研究的成果,在2023年1月获得了FDA的批准,成为首个口服选择性雌激素受体降解剂(SERD),用于治疗携带ESR1突变的ER+/HER2-晚期乳腺癌患者。同年11月,AKT抑制剂capivasertib也获得FDA的批准,用于与氟维司群联合治疗携带PIK3CA/AKT1/PTEN基因变异的HR+/HER2-晚期或转移性乳腺癌患者。王碧芸教授对PI3KCA/AKT/mTOR通路抑制剂的最新研究进展进行了深入探讨。
在抗体偶联药物(ADC)领域,德曲妥珠单抗(T-DXd)的DESTINY-Breast04研究和戈沙妥珠单抗(SG)的TROPICS-02研究的最新数据在PFS和OS方面均取得了与先前报道一致的积极成果。并且新药Dato-DXd在TROPION-Breast01研究中展现出显著的PFS获益。在临床应用方面,T-DXd和Dato-DXd在化疗后的疗效得到了循证医学的支持。T-DXd较适用于HER2低表达患者,而SG的证据则支持其在2-4线化疗后的应用。尽管这些ADC药物的临床应用已经相当广泛,我们仍然期待更多前线研究数据的发布,以便更精确地确定其在治疗序列中的最佳定位。
三阴性乳腺癌的研究进展
在三阴性乳腺癌(TNBC)的治疗领域,王碧芸教授深入探讨了如何优化现有的以化疗和免疫治疗为基础的标准治疗方案,并分享了三种提高疗效的策略。首先,她分享了在免疫治疗基础上增加药物的三药联合策略。ATRACTIB研究评估了阿替利珠单抗、化疗和贝伐珠单抗联合作为一线治疗方案在mTNBC患者(不考虑PD-L1状态)中的安全性和疗效,结果显示中位mPFS为11个月,18个月 OS为69.4%[8]。FUTURE-C-PLUS研究在一线化疗和卡瑞利珠单抗的基础上增加了小分子TKI法米替尼,观察到的mPFS达到了13.6个月,这是目前报道中最长的mPFS[9]。KEYLYNK-009研究中,帕博利珠单抗、奥拉帕利和化疗的联合治疗组mPFS为5.5个月[10]。IPATunity170研究则探索了阿替利珠单抗联合AKT抑制剂Ipatasertib和化疗在晚期TNBC一线治疗中的疗效,结果显示mPFS为5.6个月[11]。
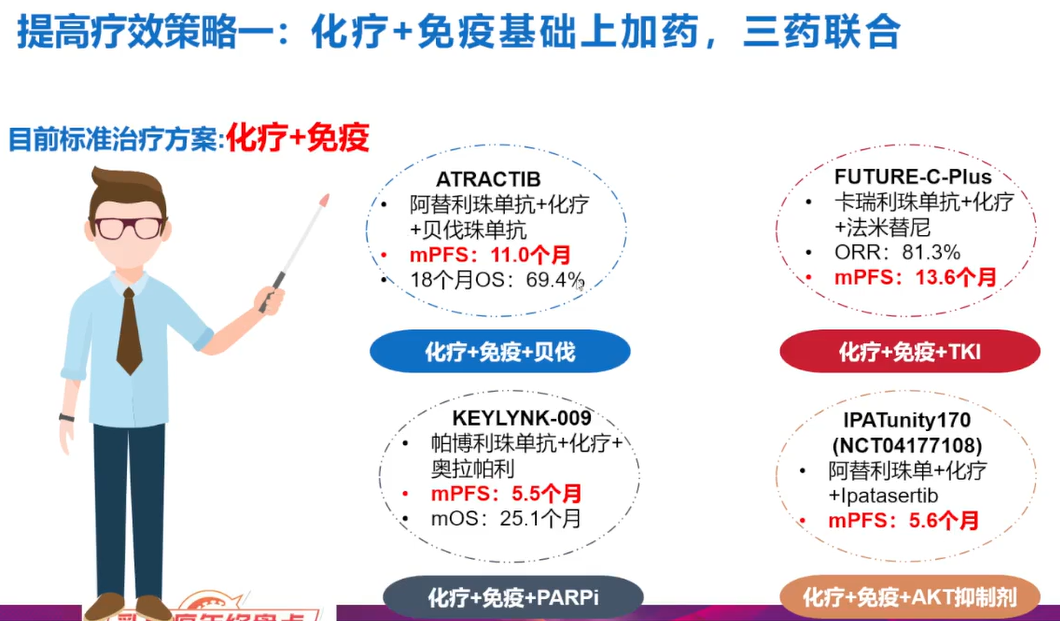
图3 三药联合策略
第二种策略,即ADC与免疫治疗的联合应用,已成为全球研究的热点。ASCENT-04/KEYNOTE-D19研究目前仍在进行中,其结果备受期待。BEGONIA研究的第7组初步数据显示,Dato-DXd联合度伐利尤单抗作为一线治疗mTNBC的mPFS达13.8个月[12],这一数据与FUTURE-C-PLUS研究中的三药联合治疗结果相一致,显示出较好的疗效。
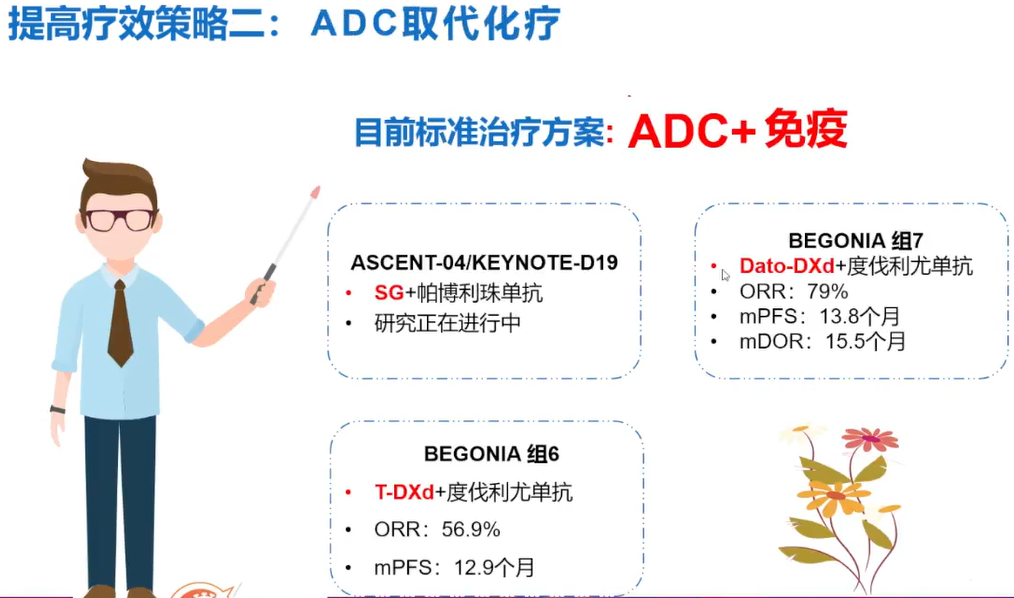
图4 ADC+免疫治疗策略
第三个策略是加强免疫治疗,然而这一领域仍处于早期探索阶段。

图5 加强免疫治疗策略
此外,王碧芸教授还提到了国内研究团队在免疫治疗领域的贡献,如江苏省人民医院殷咏梅教授领衔的SKB264用于后线TNBC治疗的研究,在2023SABCS年会更新了疗效数据,为TNBC的治疗提供了新的视角。
HER2阳性乳腺癌的研究进展
在HER2阳性乳腺癌的治疗领域,2023年SABCS会议上公布的HER2CLIMB-02研究结果显示图卡替尼联合T-DM1可显著延长既往经治HER2阳性转移性乳腺癌的PFS(HR=0.76),尤其是在脑转移患者中(HR=0.64)[13]。此外,HER2CLIMB-04研究也展示了ADC药物与小分子TKI联合治疗的潜力,这一联合治疗策略有望成为未来HER2阳性乳腺癌治疗的新方向。
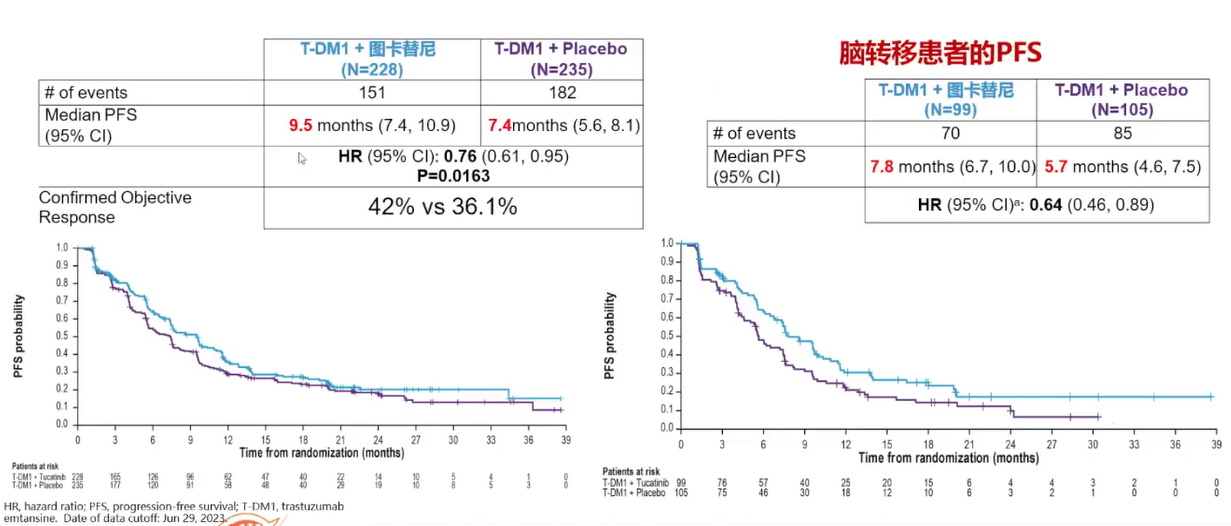
图6 HER2CLIMB-02研究PFS结局
小结
2023年的晚期乳腺癌研究进展为我们描绘了一个充满希望的未来,随着更多研究的深入和新药的不断涌现,我们期待能够为患者提供更加精准和有效的治疗方案。
[1] Hortobagyi GN, Stemmer SM, Burris HA, et al. Overall Survival with Ribociclib plus Letrozole in Advanced Breast Cancer. N Engl J Med. 2022 Mar 10;386(10):942-950. doi: 10.1056/NEJMoa2114663. PMID: 35263519.
[2] Lu YS, Im SA, Colleoni M, et al. Updated Overall Survival of Ribociclib plus Endocrine Therapy versus Endocrine Therapy Alone in Pre- and Perimenopausal Patients with HR+/HER2- Advanced Breast Cancer in MONALEESA-7: A Phase III Randomized Clinical Trial. Clin Cancer Res. 2022 Mar 1;28(5):851-859. doi: 10.1158/1078-0432.CCR-21-3032.
[3] Slamon DJ, Diéras V, Rugo HS, Harbeck N, Im SA, Gelmon KA, Lipatov ON, Walshe JM, Martin M, Chavez-MacGregor M, Bananis E, Gauthier E, Lu DR, Kim S, Finn RS. Overall Survival With Palbociclib Plus Letrozole in Advanced Breast Cancer. J Clin Oncol. 2024 Jan 22:JCO2300137. doi: 10.1200/JCO.23.00137.
[4] Matthew P, et al. MONARCH 3: Final overall survival results of abemaciclib plus a nonsteroidal aromatase inhibitor as first-line therapy for HR+, HER2- advanced breast cancer. 2023 SABCS abstract. GS01-12.
[5] Antonio Llombart-Cussac, José Manuel Pérez-García, Meritxell Bellet- Ezquerra, et al. PARSIFAL-LONG: Extended follow-up of hormone receptor-positive /HER2-negative advanced breast cancer patients treated with fulvestrant and palbociclib vs. letrozole and palbociclib in the PARSIFAL study. 2023 SABCS Abstract RF01-03.
[6] Gabe S. Sonke, Annemiek Van Ommen - Nijhof, Noor Wortelboer, et al. Primary outcome analysis of the phase 3 SONIA trial (BOOG 2017-03) on selecting the optimal position of cyclin-dependent kinases 4 and 6 (CDK4/6) inhibitors for patients with hormone receptor-positive (HR+), HER2-negative (HER2-) advanced breast cancer (ABC). 2023 ASCO abstract LBA1000.
[7] Komal L. Jhaveri. et al. lnavolisib or placebo in combination with palbociclib and fulvestrant in patients with PIK3CA-mutated,hormone receptor-positive,HER2-negative Iocally advanced or metastatic breast cancer:Phase Ill INAVO120 primary analysis. 2023 SABCS Abstract.
[8] A. Cortés Salgado, et al. ATRACTIB: A phase II trial of first-line (1L) atezolizumab (A) in combination with paclitaxel (P) and bevacizumab (B) in metastatic triple-negative breast cancer (mTNBC). 2022ESMO Abstract 205TiP.
[9] Li Chen, Shao Zhimin, Zhonghua Wang, et al. The overall survival analysis of FUTURE-C-PLUS: Combination of famitinib with camrelizumab plus nab-paclitaxel as first-line treatment for advanced, immunomodulatory triple-negative breast cancer—An open-label, single-arm, phase 2 trial. 2023 ASCO Annual Meeting. J Clin Oncol 41, 2023 (suppl 16; abstr 1086). DOI: 10.1200/JCO.2023.41.16_suppl.1086.
[10] Mark Robson, Seock-Ah Im, Florence Dalenc. et al. Pembrolizumab + Olaparib vs Pembrolizumab + Chemotherapy After Induction With Pembrolizumab + Chemotherapy for Locally Recurrent Inoperable or Metastatic TNBC: Randomized Open-Label Phase 2 KEYLYNK-009 Study. 2023SABCS abstract GS01-05.
[11] A Study Of Ipatasertib in Combination With Atezolizumab and Paclitaxel as a Treatment for Participants With Locally Advanced or Metastatic Triple-Negative Breast Cancer. https://clinicaltrials.gov/study/NCT04177108.
[12] P. Schmid, P.J. Wysocki, C.X. Ma, Y.H. Park, et al. Denduluri, Z. Nowecki. Datopotamab deruxtecan (Dato-DXd) + durvalumab (D) as first-line (1L) treatment for unresectable locally advanced/metastatic triple-negative breast cancer (a/mTNBC): Updated results from BEGONIA, a phase Ib/II study. 2023 ESMO Abstract 379MO.
[13] Sara Hurvitz,MD,FACP. HER2CLIMB-02: Randomized, Double-Blind Phase 3 Trial of Tucatinib and Trastuzumab Emtansine for Previously Treated HER2-Positive Metastatic Breast Cancer. 2023 SABCS GS01-10.
排版编辑:樊雅琦











 苏公网安备32059002004080号
苏公网安备32059002004080号


