关注专题,查看全系列精要解读
随着精准医疗时代的到来,乳腺癌的治疗已经从传统的统一治疗模式转变转变为个体化、靶向治疗。在这一转变中,新药的研发和应用成为了推动乳腺癌治疗进步的关键力量。在【肿瘤资讯】的“乳腺癌年终盘点”栏目中,我们特邀复旦大学附属肿瘤医院张剑教授,为我们深入解读了2023年国内外乳腺癌靶向治疗领域的最新科研成果。【肿瘤资讯】特此整理,以飨读者。
肿瘤内科主任医师、博导、一期临床研究病房医疗主任
复旦大学附属肿瘤医院福建医院
临床研究中心主任/肿瘤内科常务副主任
中国老年保健协会肿瘤防治与临床研究专业委员会 主委
长江学术带乳腺联盟 YBCSG主委
上海市抗癌协会肿瘤药物临床研究专业委员会候任主委
中国抗癌协会乳腺癌专业委员会常委
中国抗癌协会乳腺癌专业委员会青委会副召集人
中国研究型医院协会乳腺专业委员会青委会副主委
国家抗肿瘤药物临床应用监测青委会副主委
上海市抗癌协会肿瘤心脏病学专业委员会副主委
CSCO肿瘤支持与康复治疗专家委员会常委
中国康复医学会肿瘤康复专业委员会常委
CSCO青年专家委员会常委
CSCO乳腺癌专家委员会委员
中国抗癌协会肿瘤临床研究管理学专业委员会委员
上海“医苑新星”杰青人才获得者
国家食品药品监督管理总局CDE首批化药临床兼职审评员
获2023 十大医学先锋专家、2023“人民好医生”杰出贡献奖
第一/共一/通讯SCI论文71篇(Lancet Oncol、Ann Oncol、Nat Commun、Clin Cancer Res、J Hematol Oncol等)
张剑教授首先向我们介绍了乳腺癌临床领域的十大热点词汇,这些词汇是根据会议搜索、顶级期刊的关注度等多个因素综合评选出来的。在这些热点中,CDK4/6抑制剂、TROP2抑制剂、AKT抑制剂以及免疫治疗等关键词频繁出现,并在相关榜单中占据了重要位置。在药物分榜单中,新药的关注度非常高,这表明新药的创新和应用无疑是当前研究的热点。在2023年圣安东尼奥乳腺癌研讨会(SABCS)上,有9项乳腺癌新药研究受到了广泛关注。这些研究涉及人表皮生长因子受体2(HER2)、雌激素受体(ER)、雄激素受体(AR)成纤维细胞生长因子受体(FGFR)、磷脂酰肌醇3-激酶(PI3K)等多个关键靶点。
表1 2023年SABCS新药研究概要
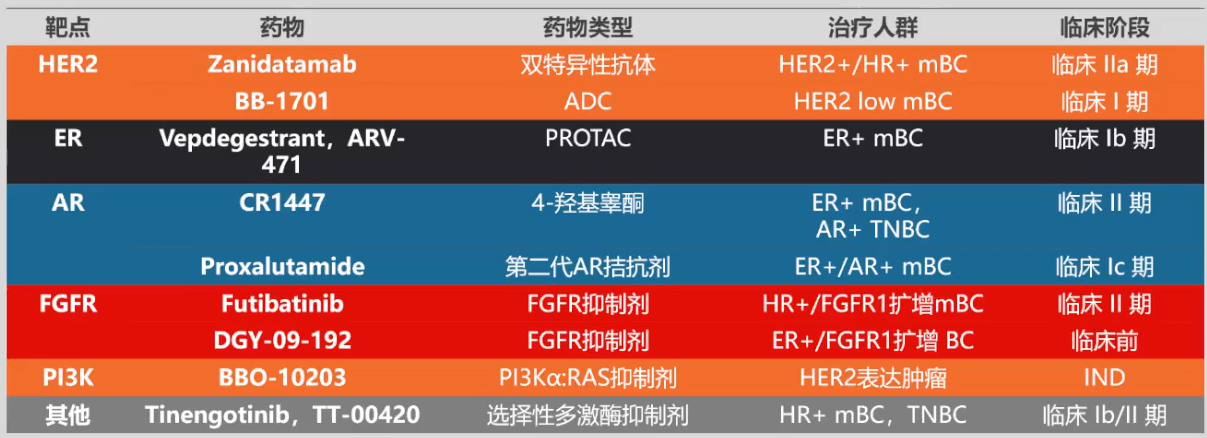
靶向HER2的新药
在HER2靶向治疗领域,Zanidatamab作为一种靶向HER2的双特异性抗体,其独特设计融合了曲妥珠单抗和帕妥珠单抗的双重优势,旨在通过这种协同作用显著提升治疗效果。在临床试验中,Zanidatamab常与多西他赛联用,而最新的研究显示,当与哌柏西利和氟维司群联合应用时,对于HER2阳性/激素受体阳性乳腺癌患者,6个月无进展生存期(PFS6)达到了67%,中位无进展生存期(mPFS)约为12个月[1]。尽管这一结果令人鼓舞,我们仍然期待进一步提高疗效。此外,研究还对比了HER2富集型、Luminal B型乳腺癌与Basal-like亚型之间的疗效差异。通过对29例患者进行PAM50亚型分析,结果显示,尽管Luminal B型与HER2富集型在中位PFS(11.7个月 vs 9.3个月;P=0.74)上的差异在数值上呈现,但统计学上并未达到显著性,且两种亚型的PFS6相似(66.7% vs 62.5%)。这一发现为未来的研究方向提供了新的视角。
双功能抗体,特别是针对HER2阳性乳腺癌的双功能抗体,正成为研究的热点。当前,除了HER2加HER2的双功能抗体外,HER2加CD47、HER2加CD73、HER2加CDK2A等不同组合的双功能抗体也在积极开发之中。
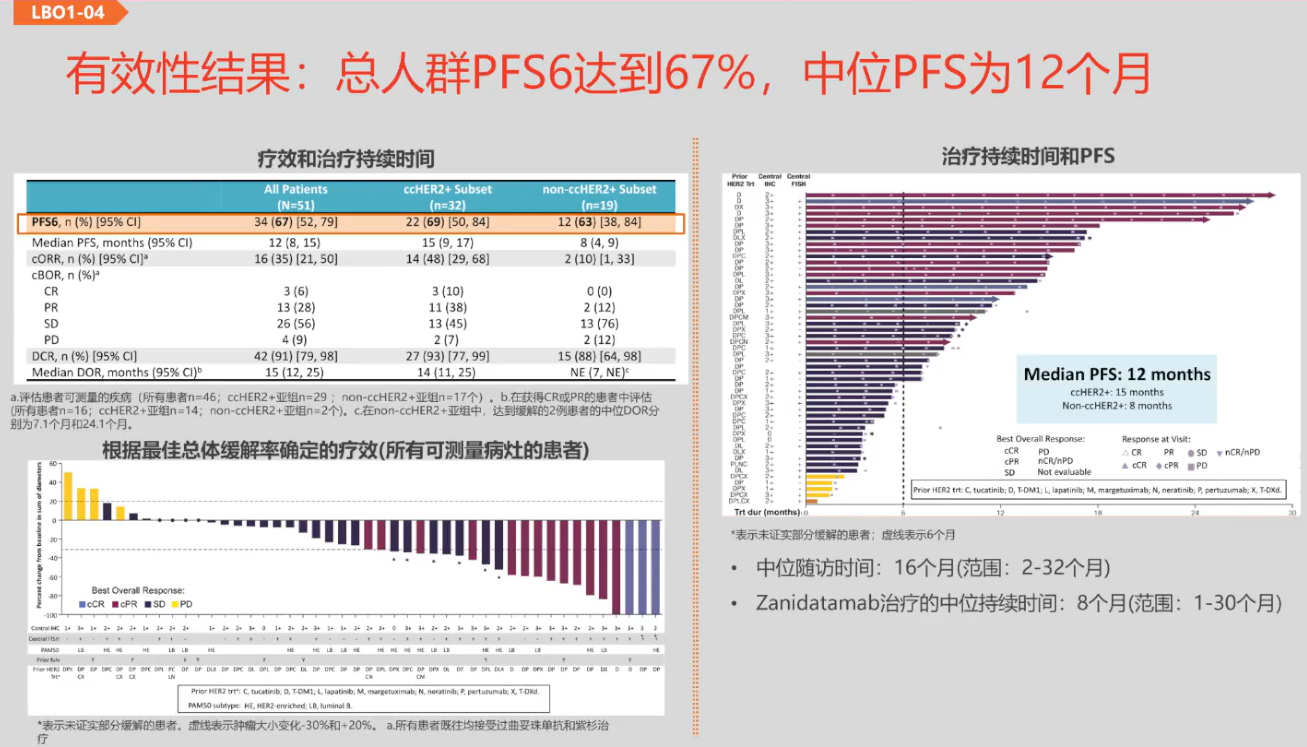
图1 Zanidatamab联合哌柏西利和氟维司群治疗HER2+/HR+乳腺癌的有效性结果
中国医学科学院肿瘤医院马飞教授及其团队在研究中报告了一项关于靶向HER2的新型抗体偶联药物(ADC)BB-1701在I期临床试验扩展队列的初步成果。这项针对HER2低表达乳腺癌患者的研究显示,BB-1701在治疗中表现出了初步的抗肿瘤活性。即便在曾经接受过其他抗HER2 ADC治疗的患者中,BB-1701同样显示出了潜在的治疗效果。这些发现为未来的研究和临床应用奠定了基础[2]。
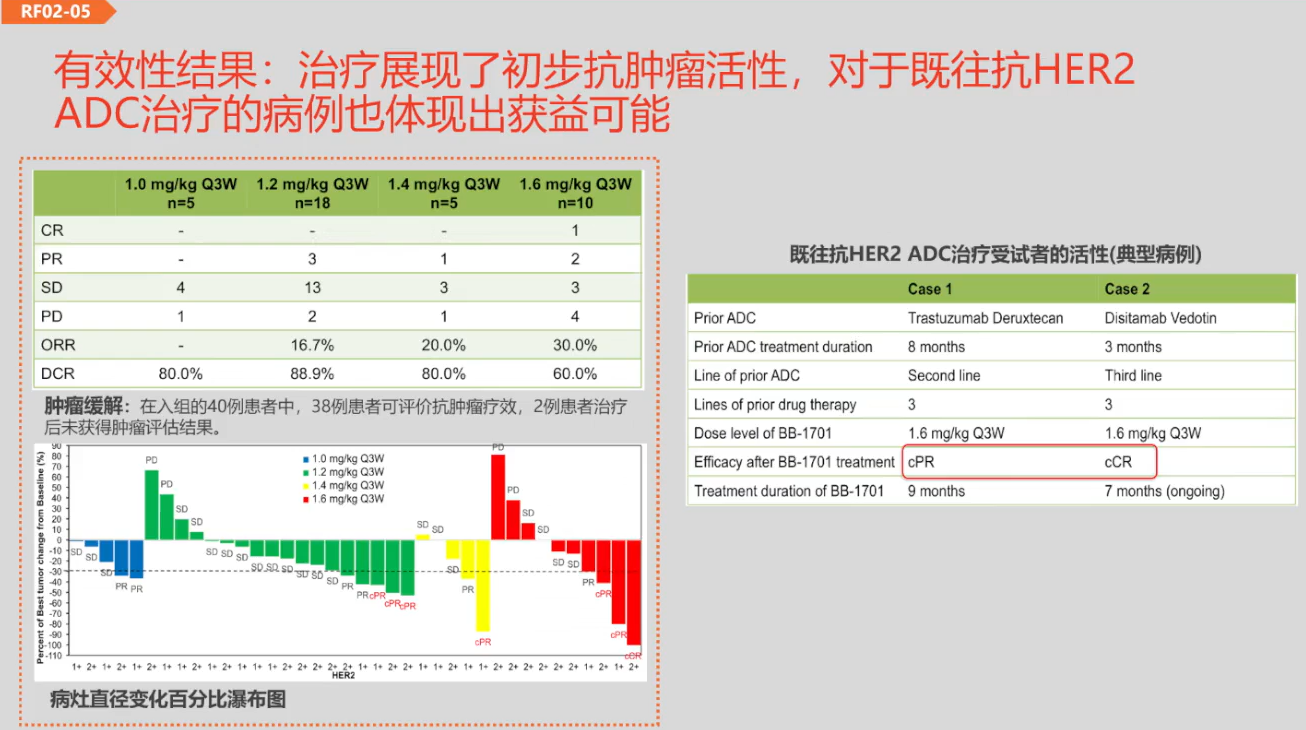
图2 BB-1701用于HER2低表达乳腺癌的有效性结果
靶向ER和AR的新药
在ER靶向治疗领域,vepdegestrant(ARV-471)是一种基于PROTAC(蛋白质降解靶向嵌合体)技术开发的创新药物,相关研究表明ARV-471在经过多线治疗的患者中依然能够提供显著的治疗效果。在一项针对ER+/HER2-晚期乳腺癌的Ⅰb期临床研究中,ARV-471与哌柏西利联合治疗的方案为经过多重治疗的患者带来了11.2个月的PFS[3]。这一结果不仅显示了其良好的疗效,也挑战了我们对于抗雌激素治疗失败后难以再次应用抗雌激素治疗的传统观念。在国内,除了PROTAC技术,分子胶技术也在积极研发中。
在激素受体阳性(HR+)乳腺癌的治疗领域,针对AR的靶向治疗正逐渐显现其治疗潜力。鉴于AR在这类乳腺癌中的高表达水平,研究者们正在探索一种创新的治疗方向:不依赖于传统的抗雄激素治疗,而是采用促进雄激素活性的策略,如新型4-羟基睾酮制剂[4]。在过去的SABCS上,专家们对这种促进雄激素活性的治疗方法进行了深入讨论,并初步证实了其在治疗中的实际效果。在这一研究方向上,已有临床研究取得积极进展。特别是在一线治疗失败的AR+/HR+/HER2-转移性乳腺癌患者中,Pruxelutamide(一种第二代AR拮抗剂)与氟维司群的联合治疗显示出了良好的安全性和显著的抗肿瘤活性。在该研究的PART2中,15例接受治疗时间≥2个月的患者,其mPFS达到了11个月[5]。这一成果预示着在HR+/HER2-乳腺癌的治疗策略中,雄激素相关治疗可能成为一个关键的治疗组成部分,为患者提供了除抗雌激素治疗之外的新选择。
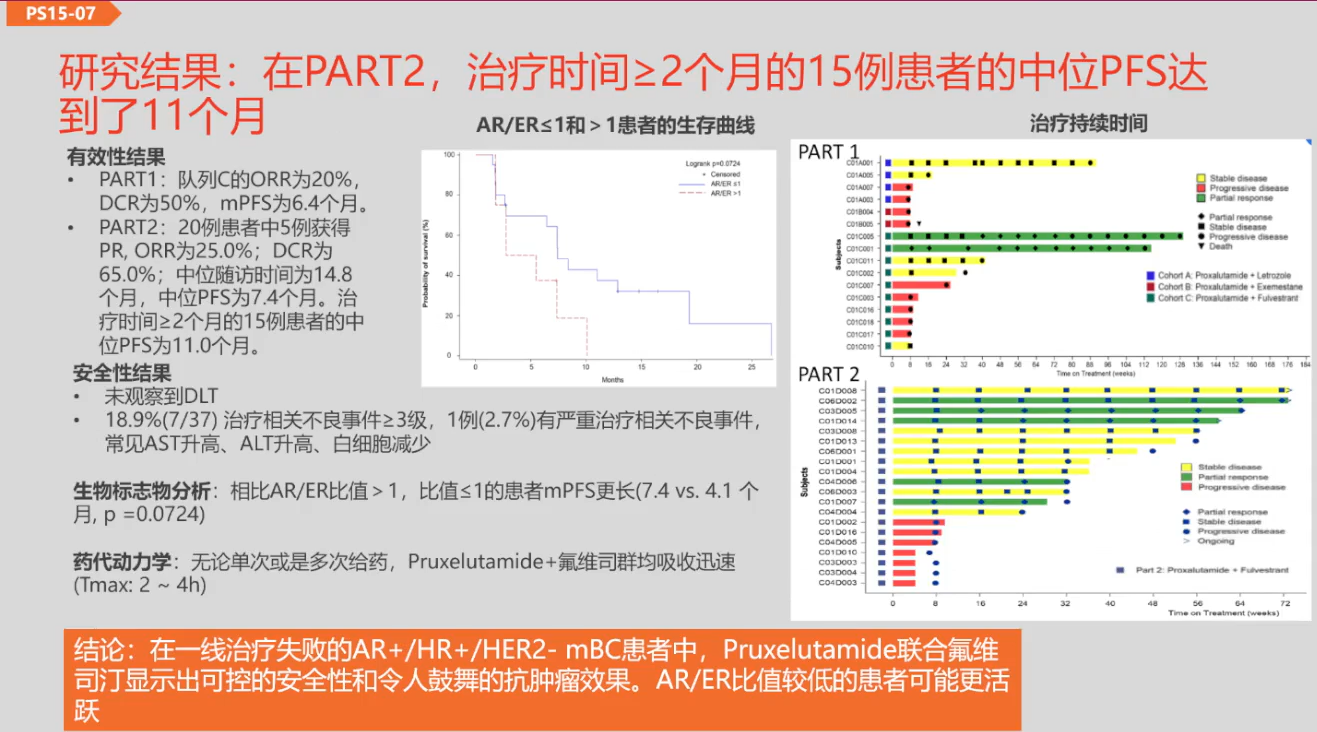
图3 Pruxelutamide联合氟维司群治疗AR+/HR+/HER2-转移性乳腺癌患者的疗效结果
靶向FGFR、PI3K及其他新药
在乳腺癌的治疗中,FGFR的靶向治疗正逐渐受到关注。Futibatinib与内分泌治疗的联合应用在临床试验中展现出了积极的效果,FGFR1 基因扩增HR+/HER2-晚期乳腺癌患者的PFS达到了7.2个月,有效率为18.2%[6]。这一发现启示我们针对FGFR扩增的乳腺癌患者,未来可能需要更精准的分类治疗策略,而不是对所有患者采用统一的治疗方案。特别是在CDK4/6抑制剂治疗后,FGFR扩增可能会更加显著,这为FGFR抑制剂的应用开辟了新的治疗领域。
在PI3K抑制剂的研究中,PI3Kα在乳腺癌中扮演着关键角色。一项关于BBO-10203的研究展示了在HR+乳腺癌患者中,联合使用PI3Kα抑制剂、CDK4/6抑制剂、氟维司群二线治疗的潜力[7]。尽管该研究主要关注的是毒副反应的控制,但研究结果表明,HER2表达的乳腺癌患者展现出了良好的抗肿瘤活性。这种活性的验证和进一步的临床研究将是未来工作的重点。这种药物之所以受到关注,在于BBO-10203不仅对PI3Kα具有特异性,还可阻断KRAS、NRAS和HRAS通路的激活。这种设计思路是创新的,因为它同时阻断了肿瘤生长的多条关键通路。然而,这种双重阻断策略是否会导致更多的毒副反应,例如皮疹和高血糖,以及其治疗效果如何,都需要在未来的研究中进行验证。尽管如此,这种新的理念为我们提供了新的治疗思路。
此外,多激酶抑制剂的研究也在不断进展。针对Aurora A/B、FGFR1/2/3、VEGFRs、JAK1/2以及CSF1R的抑制剂,已被发现能够调控上皮间质转换(EMT)和细胞周期,从而影响肿瘤的生长和扩散。多靶点抑制剂的优势在于其潜在的协同效应,尽管可能伴随较大的毒副反应,但这种效应可能增强治疗效果。以Tinengotinib为例,无论是作为单药治疗还是与其他药物联合使用,都显示出了一定的疗效[8]。然而,目前的研究规模尚有限,其在更大规模患者群体中的有效性和安全性仍需进一步验证。
国内乳腺癌研究进展
在国内乳腺癌治疗领域,我们目睹了一系列令人鼓舞的进展。LEORARDA-1研究中的新型CDK4/6抑制剂Lerociclib的亮相,以及靶向HER2的ADC药物ARX788和BB-1701的开发,还有针对HER2低表达乳腺癌的双抗JSKN003, TROP2抑制剂SKB264和新型B7-H4 ADC药物HS20089的研究,均在国际舞台上展示了中国科研团队的实力,并取得了显著的成果。此外,TORCHLIGHT研究中特瑞普利单抗在TNBC的应用,为我国临床实践提供了新的治疗视角。随后,张剑教授分享了其团队在2023 ESMO年会上的3项口头报告[9-11],以及在2023 SABCS年会上的3项壁报讨论研究[12-14],这些成就不仅彰显了中国在乳腺癌研究领域的贡献,也为全球乳腺癌治疗的进步做出了重要贡献。
在2023年,我们见证了国内外学者在新药和治疗方法上取得了令人瞩目的突破。展望未来,对新靶点的深入探索、药物的联合使用、创新治疗方案的研发将成为推动乳腺癌治疗领域不断前进的强大动力。
[1] Santiago Esc, Juan Mig, Emilio Alba, et al. Primary results from a phase 2a study of zanidatamab (zani) + palbociclib (palbo) + fulvestrant (fulv) in HER2+/HR+ metastatic breast cancer (mBC). 2023 SABCS Abstract LBO1-04.
[2] F. Ma, P. Munster, X. Guan, J et al. Report on Cohort Expansion of Phase I Study to Investigate the Safety, Tolerability, Pharmacokinetics and Antitumor Activity of BB-1701 in Patients with Locally Advanced/Metastatic HER2 Low Breast Cancer. 2023 SABCS Abstract, RF02-05.
[3] E. Hamilton, et al.Vepdegestrant, a PROteolysis TArgeting Chimera (PROTAC) estrogen receptor (ER) degrader, plus palbociclib in ER–positive/human epidermal growth factor receptor 2 (HER2)–negative advanced breast cancer: phase 1b cohort. 2023 SABCS Abstract, PS15-03.
[4] M. Vetter, et al. Final Overall Survival (OS) analysis of the SAKK 21/12 trial. CR1447 in HR+/HER2-metastatic breast cancer and androgen receptor positive triple negative breast cancer. 2023 SABCS Abstract, PS15-08.
[5] H. Li, et al.Proxalutamide plus Endocrine Therapies in Women with HR+/HER2-/AR+ Metastatic Breast Cancer: A Phase Ic Study. 2023 SABCS Abstract, PS15-07.
[6] Senthil Damodaran, Fabrice André, Nisha Unni, et al. Final results from the phase 2, open-label FOENIX-MBC2 study: efficacy and safety of futibatinib in adult patients with locally advanced/metastatic HR+/HER2− breast cancer harboring high-level FGFR1 gene amplification. 2023 SABCS Abstract RF01-04.
[7] P. Beltran, et al. BBO-10203, a first-in-class, orally bioavailable, selective covalent small molecule that inhibits RAS-driven PI3Kalpha activity without affecting glucose metabolism. 2023 SABCS Abstract RF02-02.
[8] Piha-Paul A. Sarina, et al. The efficacy and safety of tinengotinib in patients with advanced or metastatic HR+/HER2- breast cancer or TNBC. 2023 SABCS abstract RF01-07.
[9] J. Zhang, X. Hu, Y. Du, et al. A multicenter, open-label, dose escalation and expansion study of DP303c in patients with HER2-positive pre-treated advanced solid tumors. 2023 ESMO Abstract 385MO.
[10] J. Wu et al., First-in-human/phase I trial of HS-20089, a B7-H4 ADC, in patients with advanced solid tumors. 2023 ESMO abstract 381O.
[11] J. Zhang, et al. Preliminary results from a phase I/II study of 9MW2821, an antibody-drug conjugate targeting nectin-4, in patients with advanced solid tumors. 2023 ESMO abstract 659MO.
[12] J. Zhang, et al. BL-B01D1, a first-in-class EGFRxHER3 bispecific antibody-drug conjugate, in patients with Locally Advanced or Metastatic Breast Cancer and other Solid Tumor: Results from a phase 1 study. 2023 SABCS abstract PS08-07.
[13] J. Wu. et al. A Phase Ib/II Study to Assess the Safety and Efficacy of PM8002 (Anti-PD-L1 x VEGF-A Bispecific Antibody) in Combination with Nab-Paclitaxel for First Line Treatment of Locally Advanced or Metastatic Triple-Negative Breast Cancer. 2023 SABCS abstract PS08-06.
[14] J. Wu. et al. A first-in-human phase 1 study of SIM0270, a brain-penetrant oral selective estrogen receptor degrader (SERD), in patients with ER+/ HER2- locally advanced or metastatic breast cancer. 2023 SABCS abstract PS15-01.
排版编辑:樊雅琦











 苏公网安备32059002004080号
苏公网安备32059002004080号


