肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)由于发病隐匿、进展迅速,多数ICC患者初诊时就已进展至中晚期,失去了根治性手术机会[1,2]。而转化治疗有望帮助中晚期ICC实现降期后切除,或能为此类患者带来生存获益。在这个过程中,目前公认的治疗建议是:化疗联合靶向、免疫等多种治疗手段,针对患者进行个体化合理选择,并全程实施 MDT策略[1]。此外,即使行根治性切除术(R0切除),ICC术后仍然极易复发和转移[2],故ICC的术后辅助治疗一直备受关注,其中,靶免联合方案是热点方案之一。本期由武汉大学中南医院肝胆胰外科张中林、廖铂医生为大家分享并解读一则病例,该病例为3个周期“替雷利珠单抗+仑伐替尼”联合12个疗程放疗(采用IMRT)、3个疗程化疗(药物为卡培他滨),成功转化治疗Ⅲa期ICC实现R0切除,并在术后辅助治疗中使患者持久获益的真实案例,这一疗效显著、安全性高的抗癌方案为中晚期ICC的治疗提供了新选择,为患者带来了新希望。
点评专家
武汉大学中南医院
肝胆胰外科 副主任 主任医师
医学博士,硕士生导师
武汉大学中南医院肝胆胰外科副主任,肝脏外科临床亚专业组长
武汉大学中南医院肝胆胰疾病诊疗MDT团队专家及总执行人
香港大学玛丽医院肝胆与肝移植外科荣誉临床助理
美国芝加哥大学访问学者
湖北省医学会普通外科分会委员
湖北省医学会腔镜外科分会副主任委员
武汉市医学会腔镜外科分会委员兼秘书
武汉医学会机器人与腔镜外科分会肝胆胰外科学组委员
中国医疗保健国际委员会肝胆疾病分会委员
国际肝胆胰协会中国分会胆道结石专业委员会委员
中国医师协会外科医师分会门静脉高压症专家工作组专家委员
湖北省肝胆疾病学会常务理事
分享专家
武汉大学中南医院
肝胆胰外科 副主任医师 硕士生导师医学博士,中共党员
武汉大学中南医院肝胆胰外科党支部副书记
美国斯坦福大学访问学者,曾至法国南锡大学医学院交流学习
毕业于华中科技大学附属同济医院,师从于陈孝平院士
擅长于肝胆胰外科的微创手术治疗
获得“第三届APHAB腹腔镜肝切除手术菁英赛全国总决赛”三等奖
获批武汉大学中南医院优秀中青年技术人才培养计划
主持国自然青年基金项目及中央高校基本科研业务费专项资金各一项
在国内外期刊上已发表多篇学术论文,以第一/通讯作者身份发表SCI论文8篇
病例详情
01基本情况
患者男性,53岁。
主诉:发现肝内胆管癌伴梗阻性黄疸1月余,PTCD术后半月余。
现病史:患者约1个月前因突发尿黄、皮肤巩膜黄染、皮肤瘙痒等症状到当地卫生院就诊,行腹部彩超检查示:肝脏占位。遂进一步至仙桃市第一人民医院就诊,行腹部CT及MRI提示:肝占位性病变伴肝门侵犯,性质考虑为肝内胆管细胞癌,合并肝内胆管扩张。行超声引导下经皮肝穿刺活检,病检结果示:肝内胆管细胞癌。邀请我院进行多学科会诊(MDT),意见为:病灶暂时评估为初始不可切除,建议行减黄治疗、放化疗等治疗。约半个月前,当地医院给予超声引导下经皮肝胆管穿刺引流术(PTCD),引流管置入左肝管,治疗后黄疸有所减退,但肝酶及胆红素未降至正常,考虑后续治疗风险大,与家属沟通后决定转入我院进一步治疗。遂以“1、肝内胆管癌伴肝门侵犯;2、梗阻性黄疸”为诊断收入我院放化疗科。
既往史:既往体健。无高血压、糖尿病及心脏病病史,无乙肝、结核等传染病病史,无外伤手术输血史,无药物食物过敏史,无烟酒史。
家族史:否认家族遗传病及特殊病史。
体格检查:皮肤巩膜轻度黄染,余无特殊。
02辅助检查
入院(2022-11-05)实验室检查:
●肝功能:TBIL:103μmol/L;DBIL:47.7μmol/L;IBIL:55.3μmol/L;ALT:82IU/L;AST:57IU/L。
●肿瘤标志物:CA19-9:639.1U/mL;CEA:8.73ng/mL;AFP、CA12-5均正常。
2022-10外院腹部MRI增强扫描示:肝脏占位性病变伴肝门侵犯,考虑为肝内胆管癌,合并肝内胆管扩张。
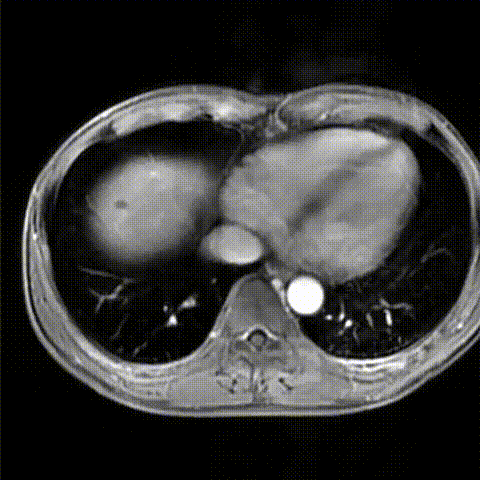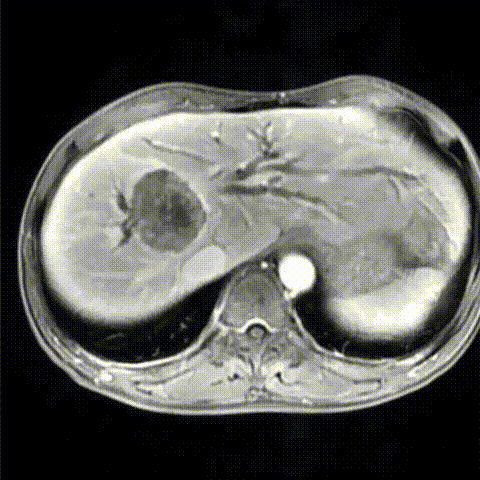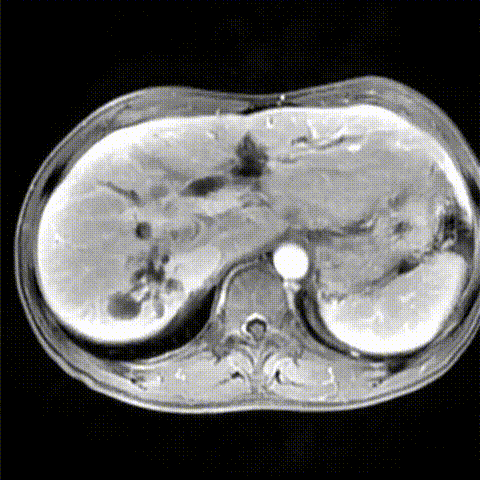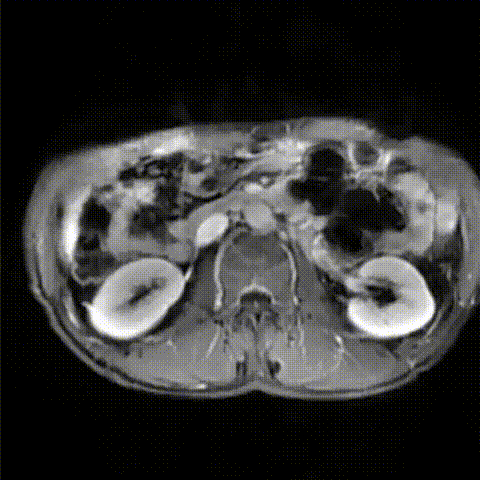 2022-10外院腹部MRI增强影像
2022-10外院腹部MRI增强影像
因患者黄疸症状较重,影像检查示左肝管扩张明显、右肝管不显现,外院予行PTCD术,将引流管置入左肝管,如下图所示。
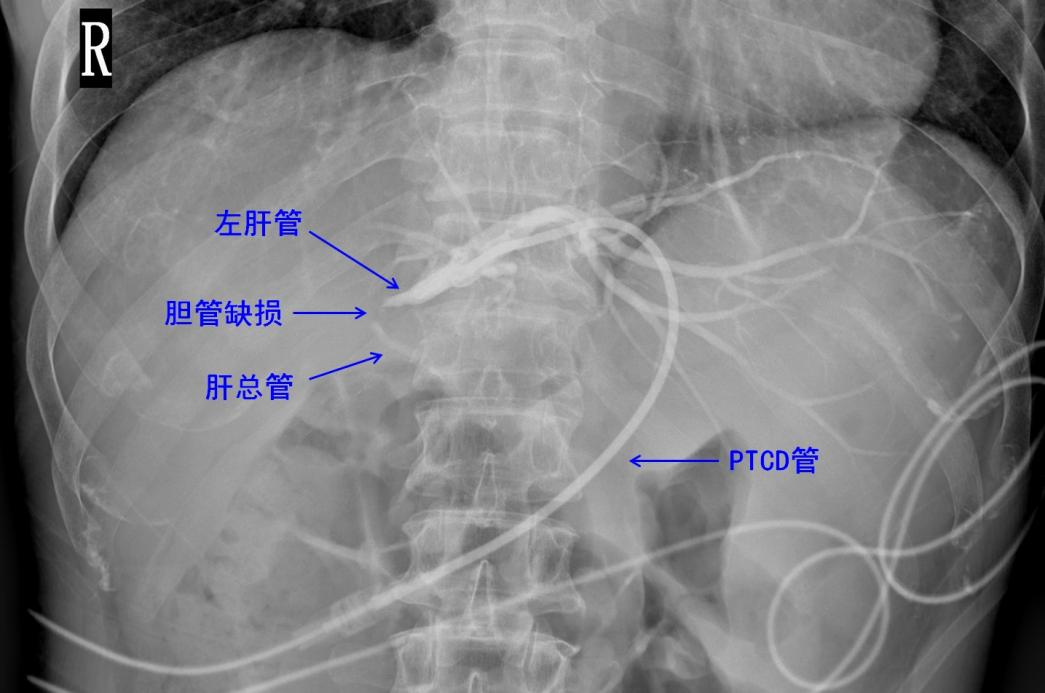 外院PTCD造影图像,见右肝管不显影,引流管置入左肝管
外院PTCD造影图像,见右肝管不显影,引流管置入左肝管
借阅外院肝占位穿刺活检病理切片,判定结果为:小块肝组织中见中分化管状腺癌;结合免疫组化,可符合肝内胆管细胞癌。
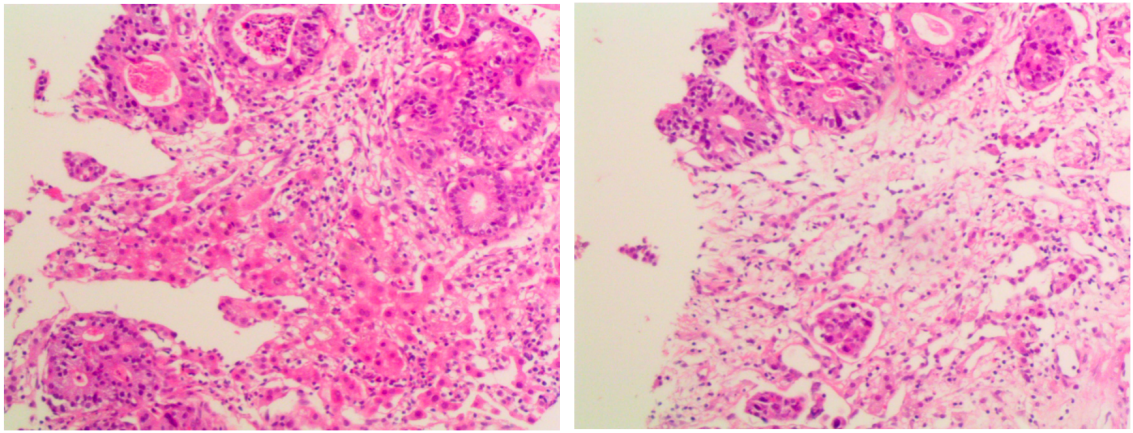 外院肝穿刺活检结果(镜下观)
外院肝穿刺活检结果(镜下观)
03临床诊断
肝内胆管癌伴肝门侵犯(Ⅲa期)
梗阻性黄疸
04治疗经过
根据先前MDT会议意见,结合目前患者胆道梗阻所致的皮肤巩膜黄染、瘙痒等症状仍然存在,决定予积极减黄的基础上,实施放疗、化疗、靶向治疗、免疫治疗等综合性治疗,以寻求根治性手术切除的机会,并积极采取术后辅助治疗来防范肿瘤复发。
1、综合性转化治疗
入院后检查见右侧胆管扩张,遂于2022-11-05行超声引导下PTCD术,引流管置入右肝内胆管,术程顺利,引流出胆汁。
于2022-11-06进行放疗定位,两天后开始进行肿瘤、肝胆管及门脉癌栓的三维适形调强放射治疗(IMRT),肿瘤靶区(GTV)剂量为:36GY/12F qd,d1-5 qw(即:每1周为一个周期,周一至周五每天放疗,然后周六周日休息)。直至2022-11-23放疗结束,一共进行了12个疗程。
同步予以化疗药物,具体方案为:卡培他滨片1000mg po bid,d1-14 q3w(即:每3周为一个周期,前两周用药,然后停药一周),共治疗三个疗程。
同期(于2022-11-18)给予靶向药物+免疫治疗,具体用药为:替雷利珠单抗200mg ivgtt q3w+仑伐替尼胶囊8mg po qd,共治疗3个周期(替雷利珠单抗最后一次用药为2023-01-04,仑伐替尼最后一次用药为2023-01-12)。
于2023-01-01在当地医院复查肿瘤标志物,结果示:CA19-9、CEA及AFP均正常。
2、根治性手术切除
于2023-1-28至我院肝胆胰外科就诊,入院后于次日行实验室检查,结果示:
l 肝功能:TBIL:30.5μmol/L;DBIL:12.7μmol/L;IBIL:正常;ALT:106IU/L;AST:80IU/L。
l 肿瘤标志物:CA19-9:正常;CEA:正常;AFP:正常。
于2023-01-29行全腹部CT示:肝右叶稍低密度影,邻近胆管壁增厚,远端胆管扩张,为肝内胆管癌治疗后表现,未见新增转移瘤灶;肝左叶引流管置入术后;肝周及胆囊周围少许积液。
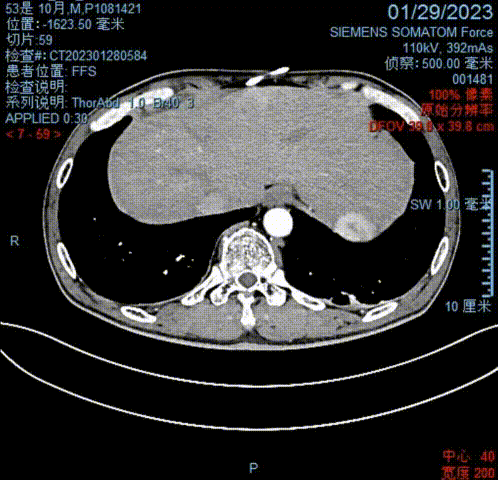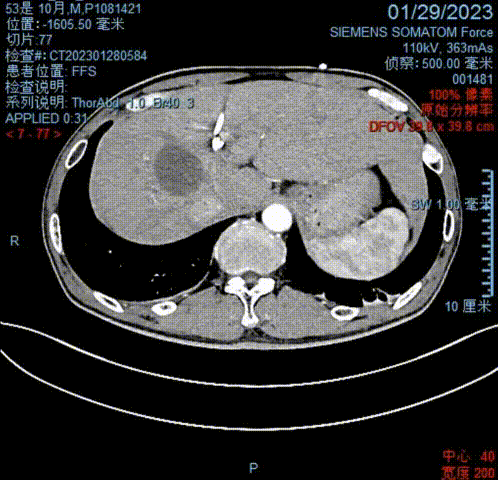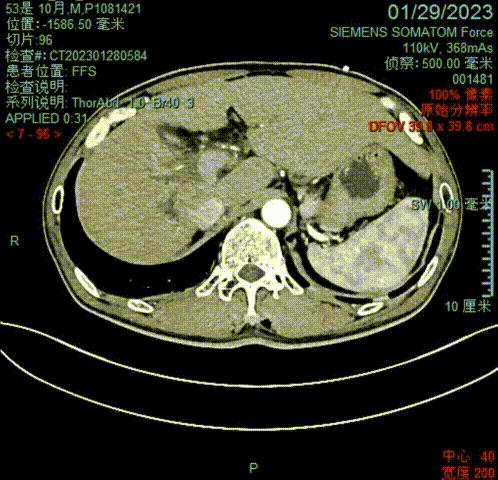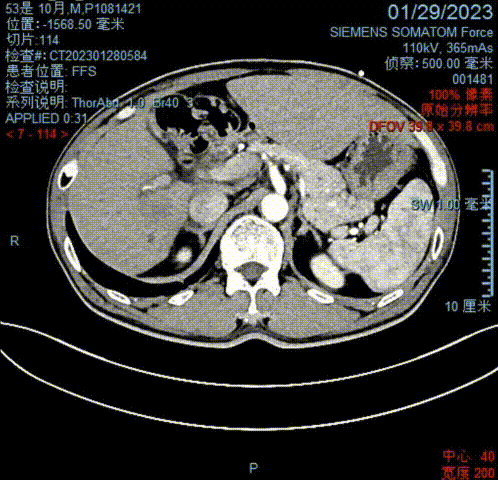 2023-01-29全腹CT影像
2023-01-29全腹CT影像
对比先前PTCD造影,转化治疗后右肝管已显影,见右肝管受侵并狭窄。
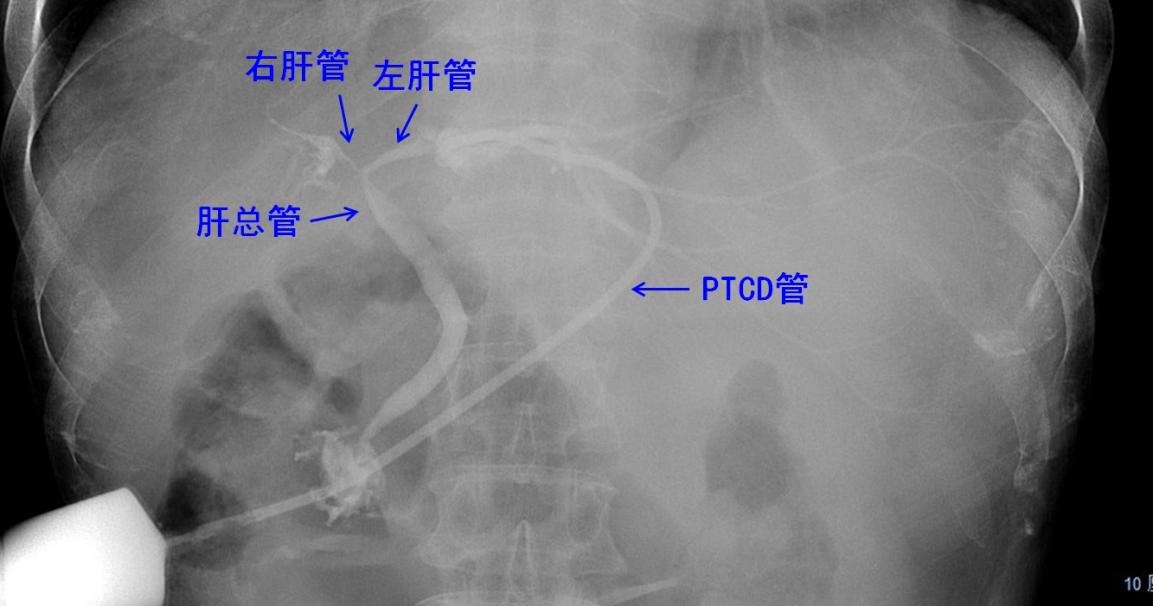
转化治疗后PTCD造影图像,见右肝管受侵并狭窄
术前可切除性评估结果为:功能残肝比:55.8%;ECOG-PS评分 1分;Child-Pugh评分 A级;ICG-R15:9.9%。符合实施根治性手术治疗的基本要求。
于2023-02-02在全麻下行“开腹胆囊切除+右半肝切除+尾叶切除+肝门淋巴结清扫+左肝管空肠吻合术”。
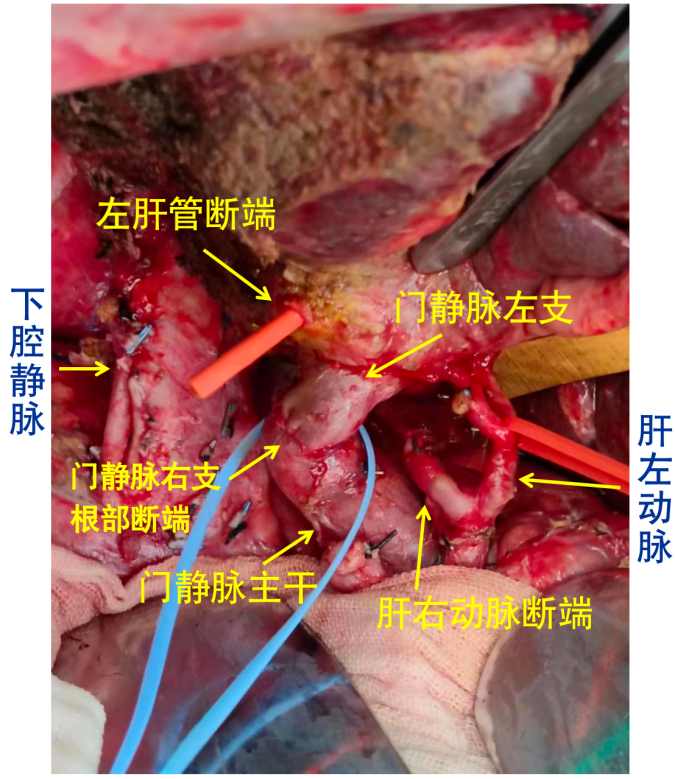 术中所见
术中所见
术中病理提示:(右半肝)肿物,大小约5cm×4.8cm×4cm,符合肝内胆管癌,肿瘤坏死百分率达95%;肿瘤局限于肝脏,未见脉管侵犯,局域淋巴结未见转移。
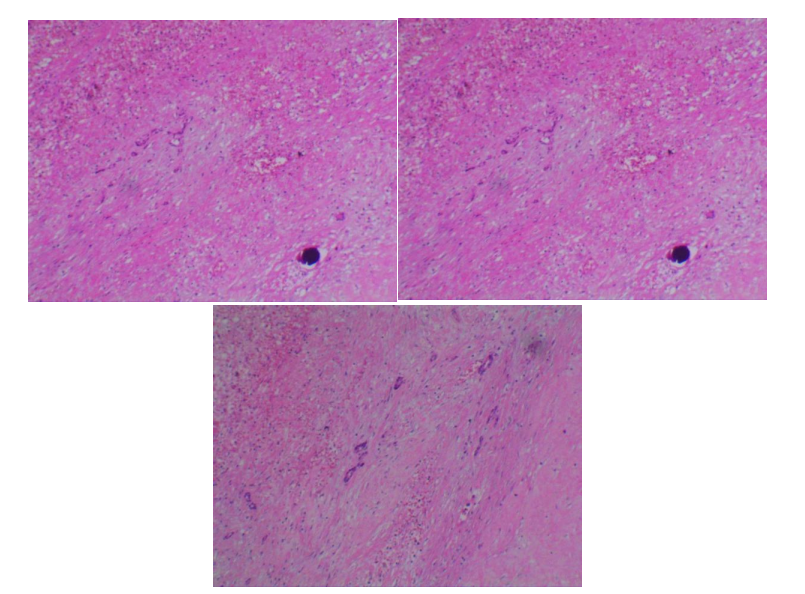 术后病理图片(镜下观)
术后病理图片(镜下观)
术后11天(2023-02-13)复查腹部CT示:原肿瘤切除彻底,未见复发或转移迹象;引流管位置适当。提示实现R0切除。
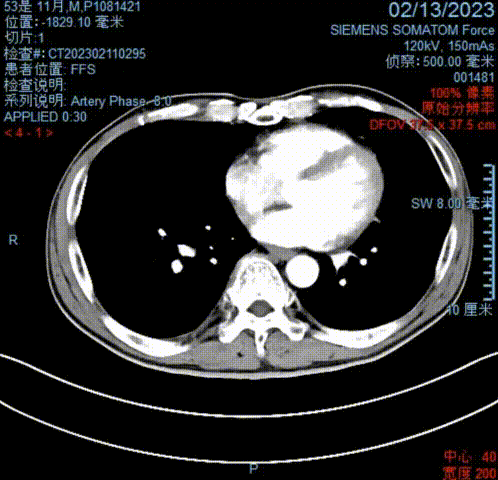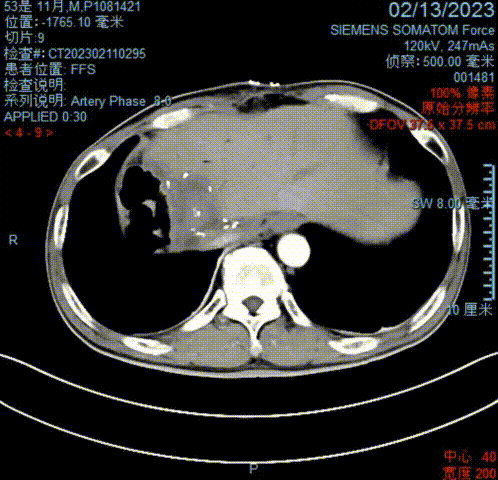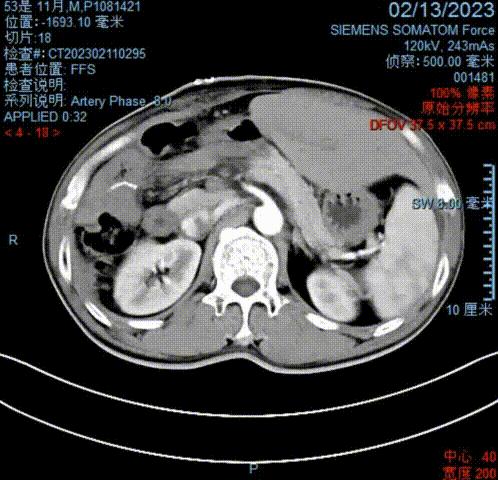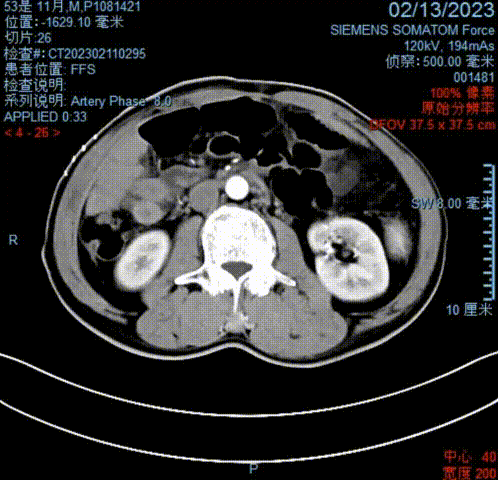 2023-02-13腹部CT影像
2023-02-13腹部CT影像
因见胆肠吻合口旁引流管引流出褐色胆汁,考虑出现胆漏,予延长引流管留置时间。术后40天见无引流液,遂拔管。
于2023-03-30返我院放化疗科复查,结果示:肝功能各指标(胆红素、ALT、AST等)及肿瘤标志物(CA19-9、CEA及AFP)均正常。
于2023-3-31采取靶免联合方案进行术后辅助治疗,具体用药为:替雷利珠单抗200mg ivgtt q3w+仑伐替尼胶囊8mg po qd。目前(截至2023-05)仍在继续靶免联合治疗,且未见任何复发转移迹象。
疗效评估:“替雷利珠单抗+仑伐替尼”联合放化疗成功转化治疗Ⅲa期ICC实现R0切除,并在术后辅助治疗中使患者持久获益。
不良反应:治疗期间未出现任何明显的药物相关不良反应,患者治疗依从性、耐受度良好。
病例总结
ICC是一种临床常见的胆道系统恶性肿瘤(BTC),由于多数患者初诊即晚期,缺乏有效的治疗手段,通常预后较差[2]。另外,有数据显示,ICC患者术后5年复发率高达60%~70%[1]。近年来,以免疫检查点抑制剂(ICI)为代表的免疫治疗时代的到来,彻底改变了晚期BTC治疗单一的格局,有望为患者带来更多生存获益[3]。研究发现,抗血管生成治疗和化疗均可与免疫治疗产生协同作用,以ICI为基础的联合化疗和(或)靶向药物治疗在晚期ICC治疗中表现出了良好的疗效和安全性[1]。鉴于此,对于本例伴肝门侵犯、合并梗阻性黄疸的晚期ICC患者,我们在积极减黄的基础上,实施了放疗、化疗、靶向治疗、免疫治疗等综合性治疗,以寻求根治性手术切除的机会,并积极采取术后辅助治疗来防范肿瘤复发。
在诸多ICI药物中,我们选择了国产PD-1抑制剂替雷利珠单抗,主要是因为该药不仅在一线联合治疗晚期ICC患者中表现突出,而且具有可及性高的优势。一项采用GEMOX联合多纳非尼和替雷利珠单抗一线治疗局部晚期或转移性BTC的前瞻性单中心探索性研究显示:患者的6个月总生存期(OS)率高达90.9%,III-IV期患者转化治疗成功率达到23.1%;且整个研究期间,3级或4级治疗相关不良事件发生率(TRAEs)仅为53.8%[4],这些数据彰显了替雷利珠单抗在联合治疗中强大的肿瘤控制能力。另一项采用替雷利珠单抗联合仑伐替尼和GEMOX治疗潜在可切除的局部晚期BTC的单臂、开放标签、II期研究结果表明:患者客观缓解率(ORR)可达56%,转化治疗成功率高达84%,约52%的患者实现了R0切除,其中1例(4%)患者达到病理学完全缓解(pCR),且所有患者术后均未发生严重并发症[5]。以上研究数据显示了替雷利珠单抗在中晚期BTC治疗中出色的疗效和可靠安全性。
基于上述研究证据,对于本例Ⅲa期ICC患者,我们在一线治疗中给予了3个周期“替雷利珠单抗+仑伐替尼”、12个疗程放疗(采用IMRT)、3个疗程化疗(药物为卡培他滨),结果经转化治疗成功实现R0切除,并在术后辅助治疗中继续应用“替雷利珠单抗+仑伐替尼”方案使患者持久获益。目前(截至2023-05)仍在继续靶免联合治疗,且未见任何复发转移迹象。且治疗期间患者未曾发生任何明显的药物相关不良反应,表明“替雷利珠单抗+仑伐替尼”靶免联合方案的安全性可靠。期待在后续的长期随访中见证患者更持久的获益,也希望替雷利珠单抗能够助力我国更多晚期ICC患者实现转化降期后切除和长期无复发生存。
[1]中国抗癌协会肝癌专业委员会胆管癌协作组. 原发性肝癌诊疗指南之肝内胆管癌诊疗中国专家共识(2022版)[J]. 中华消化外科杂志,2022,21(10):1269-1301.
[2]科技部传染病防治重大专项课题“病毒性肝炎相关肝癌外科综合治疗的个体化和新策略研究”专家组.肝内胆管癌外科治疗中国专家共识(2020版)[J].中华消化外科杂志, 2021, 20(1):1-15.
[3]施国明, 裴晏梓, 陆品相, 等. 胆道系统恶性肿瘤免疫检查点抑制剂治疗[J].临床肝胆病杂志, 2022, 38(5):998-1001.
[4]Lu Wang, et al. Efficacy and safety of sintilimab combined nab-paclitaxel and gemcitabine as first-line treatment for metastatic pancreatic ductal adenocarcinoma (PDAC): A retrospective analysis,2022 ESMO World GI ,p-110.
[5]Huikai Li, et al. A single-arm, open-label, Phase II study of tislelizumab combined with lenvatinib and GEMOX regimen for conversion therapy of potentially resectable locally advanced biliary tract cancers.2022 ESMO 65P.
排版编辑:肿瘤资讯-小瑜











 苏公网安备32059002004080号
苏公网安备32059002004080号


