原发性肝癌是我国目前第4位常见恶性肿瘤及第2位肿瘤致死病因,其中肝细胞癌(hepatocellular carcinoma,HCC)占75%-85%[1]。目前,肝切除术仍是HCC治疗最常用的潜在根治性治疗手段[2]。但由于HCC早期多无明显临床症状,大部分患者在初次诊断时已为晚期,错失了接受根治性手术切除的时机[1,3]。近年来,HCC的综合治疗取得了巨大进步,尤其是以靶向药物、免疫治疗为代表的系统治疗,联合肝动脉栓塞(TAE)、肝动脉灌注化疗(HAIC)等局部治疗,这种多模式的综合性治疗方案可有效控制肿瘤进展,为不可切除的肝癌转化治疗后行根治性切除、降低术后复发和改善预后提供更多可能[1,3]。本期由西安交通大学第一附属医院肝胆外科郭成、刘志奎医生为大家分享并解读一则病例,该病例为采用“替雷利珠单抗+多纳非尼”联合TAE、HAIC、放疗的综合性转化治疗方案,成功转化合并门静脉主干、左右分支癌栓的IIIa期HCC实现R0切除且达到主要病理学缓解(MPR),并在术后辅助治疗中使患者持续获益的真实案例,该案例为晚期HCC的治疗提供了一种新思路。
点评专家
西安交通大学第一附属医院
肝胆外科 副主任医师 医学博士
目前担任:
中国抗癌协会肝癌专业委员会委员
中国医师协会外科医师分会门静脉高压症专家工作组专家委员
中国研究型医院数字医学临床外科专业委员会 委员
中国研究型医院学会数字医学临床外科专业委员会数字化肝胆胰外伤学组 委员
陕西省国际医学交流促进会肝脏肿瘤MDT专委会 主任委员
西安市医学会腔镜外科分会 副主任委员
专业方向:
原发性肝癌以外科治疗为主的肝癌多学科综合治疗,特别是对于中晚期肝癌的转化治疗;肝转移癌的综合治疗,主要是结直肠癌肝转移及乳腺癌肝转移的外科治疗。
分享专家
西安交通大学第一附属医院
肝胆外科 副研究员 医学博士陕西省国际医学交流促进会 肝脏肿瘤MDT专委会秘书长。
西安交通大学博士研究生标兵。
2017-2018年受国家留学基金委资助至美国Mayo医学中心联合培养,主要研究方向是细胞微环境对肿瘤的影响。发表《Gastroenterology》《Hepatology》《Theranostics》等SCI论文45篇,其中第一或通讯20篇.《中国普通外科杂志》中青年编委。主持1项国家自然科学基金及多项陕西省科技项目。
病例详情
01基本情况
患者男性,53岁。
主诉:体检发现肝占位2天。
现病史:2023年1月3日入院。患者2天前体检时发现肝占位,无腹痛、腹胀,无恶心、呕吐,无乏力、纳差,无发热、寒战,全身皮肤巩膜无黄染。为求进一步诊治,特来我院就诊,门诊以“肝脏占位:恶性肿瘤?”为诊断收入。
既往史:既往患“乙肝”20余年,口服恩替卡韦抗病毒治疗。
个人史及家族史:无特殊。
体格检查:全身皮肤巩膜无黄染,腹平软,全腹无压痛、反跳痛,墨菲征阴性,肝区无叩痛,无肝掌、蜘蛛痣。
02辅助检查
入院(基线)实验室检查:
●凝血功能:无明显异常。
●肝肾功能:无明显异常。
● 肿瘤指标:甲胎蛋白:107ng/mL, 异常凝血酶原:29877.82mAu/mL。
●乙肝相关检查:乙肝表面抗原(+),e抗体(+),核心抗体(+);乙肝病毒DNA定量:8.23×103IU/mL。
入院时腹部增强CT示:肝左内叶及右叶块状异常强化病灶,门静脉主干及左右支栓子并显著强化,考虑肝癌伴门静脉、左右支癌栓形成;肝中、右静脉受侵可能,下腔静脉肝内段管径变细。肝硬化、脾大、门静脉海绵样变性。
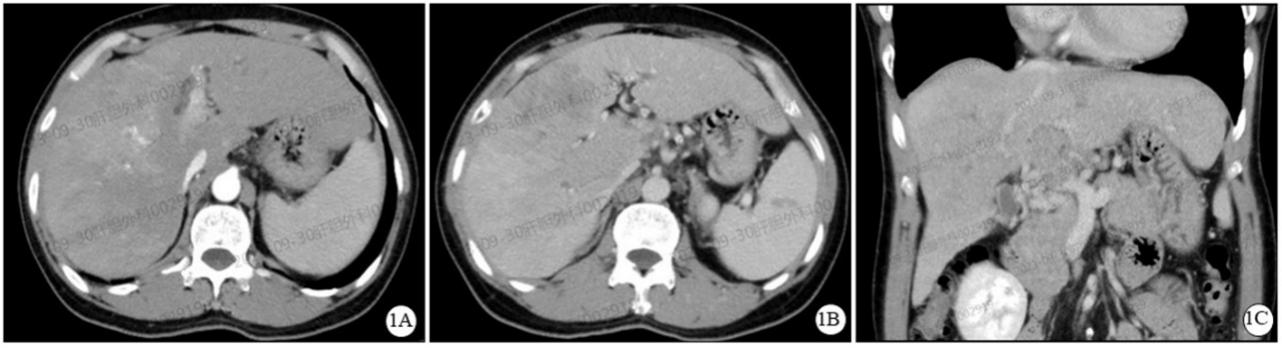
入院时腹部增强CT图像,A:动脉期;B:静脉期;C:门静脉主干、左右支癌栓
入院时肝脏MRI普美显示:肝右叶巨大肿块,并周围多发结节,结合普美显增强,考虑肝脏原发性肝癌,并门静脉左右分支及主干内癌栓形成,门静脉阻塞,门静脉海绵样变性。
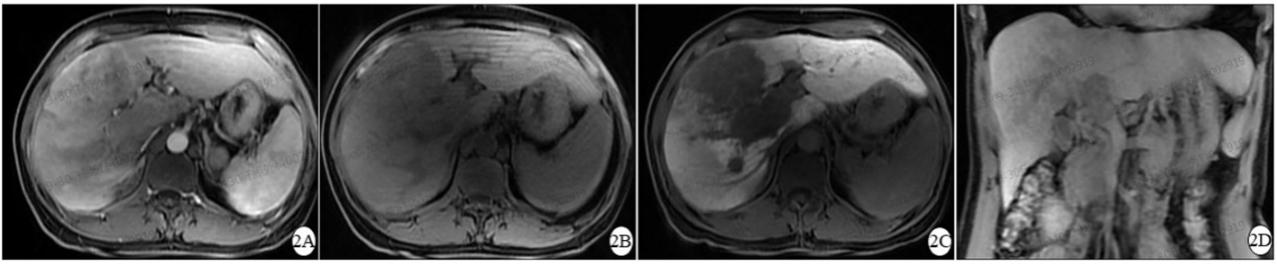
入院时肝脏普美显MRI图像,A:动脉期;B:静脉期;C:普美显期;D:门静脉主干、左右支癌栓
03临床诊断
肝右叶原发性肝癌伴门静脉癌栓(主干、左右支)
CNLC IIIa期,肝功能 Child-Pugh分级A级
乙肝肝硬化代偿期
04治疗经过
入院后给予恩替卡韦抗乙肝病毒治疗,考虑患者巨大肝癌合并门静脉主干、左右支癌栓,且侵犯肝中、肝右静脉,病灶周围多发结节卫星灶,无法立即行根治性手术切除,经我科手术切除小组、介入组、射频组、肿瘤内科、放疗、感染科、影像科行多学科会诊(MDT)讨论后,建议先行降期转化治疗,争取实现根治性切除,然后通过术后辅助治疗降低复发风险。
1、转化治疗
2023-01-10行第一次肝动脉栓塞(TAE)联合动脉置管化疗灌注术(HAIC),术中用500-700um栓塞微球栓塞肿瘤供血动脉,灌注药物为奥沙利铂,亚叶酸钙和氟尿嘧啶(FolFox4方案)。
同期开始免疫治疗联合靶向治疗,具体用药为:替雷利珠单抗200mg ivgtt q3w+多纳非尼200mg po bid。
于2023-04-07应用6MV-X线治疗,采用VMAT技术,给予DT50Gy/25f。靶区仅包括门静脉癌栓,剂量分布尽可能保护正常肝脏。
转化治疗3个半月后(2023-04-26)复查肝脏普美显MRI示:肝右叶肝癌,门静脉右支内癌栓形成并分布区域的干细胞受损,信号减低,肝门部门静脉海绵样变性,较前病灶缩小,门静脉癌栓缩小。
于2023-05-11行第2次TAE+HAIC,介入操作过程顺利;继续维持原靶免方案不变。
转化治疗半年后(2023-07-18)复查普美显MRI示:肝右叶肝癌,肿瘤较前范围减小;门静脉右支内癌栓形成,门静脉海绵样变性。
转化治疗期间患者肿瘤标志物水平急剧下降并持续维持在较低水平。
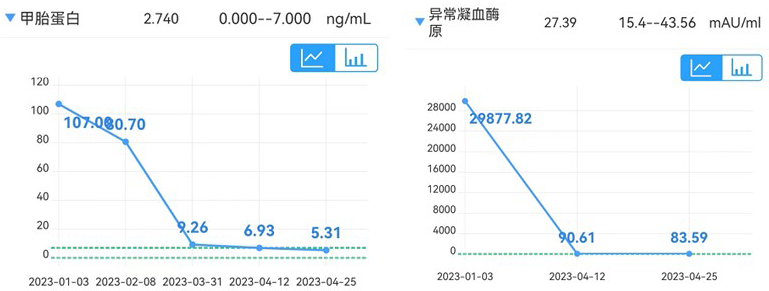 转化治疗期间患者甲胎蛋白和异常凝血酶原水平变化趋势
转化治疗期间患者甲胎蛋白和异常凝血酶原水平变化趋势
2、手术及术后辅助治疗
考虑患者转化治疗达到了显著缩瘤的预期,拟安排择期手术,术前行CT血管成像(2023-07)进行手术评估,结果示:肝右前叶下段恶性肿块影,考虑肝癌,肝右动脉分支进入病灶内;残余肝体积/标准肝体积>40%。

术前CT血管成像(2023-07)见肝右前叶下段恶性肿块影,门静脉右支癌栓形成
予完善术前准备后,于2023-07-24行右半肝切除术,手术过程顺利,术后继续抗乙肝病毒治疗。
术后病理学检查结果(右肝)示:“右叶”肝切除标本肝局限性间质纤维组织增生玻变及慢性炎细胞浸润背景中小灶状中分化肝细胞癌残存,未累及肝被膜,符合治疗后改变(TRG:1级),肝切缘未见癌组织。其余肝组织呈结节性肝硬化改变,胆囊慢性炎。门静脉未见癌栓(图5)。提示达R0切除和MPR。
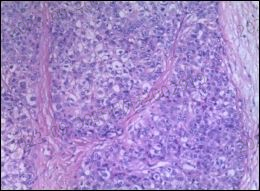
术后病理学检查结果(镜下观)
患者术后无出血、肝衰等并发症,术后5d拔除腹腔引流管,术后10d顺利出院。
为尽可能降低肿瘤复发风险,决定施行术后辅助治疗,具体用药仍选择先前转化治疗中的靶免方案,即:替雷利珠单抗200mg ivgtt q3w+多纳非尼200mg po bid。
出院后多次复查甲胎蛋白,结果均在正常范围内。
最近一次复查(2023-10-24)腹部增强CT示:肝脏右叶缺如,肝左叶体积增大,残余肝内密度均匀,增强扫描未见异常强化。肝内外胆管无扩张,腹膜后未见肿大淋巴结。提示无肿瘤复发转移。
疗效评估:“替雷利珠单抗+多纳非尼”联合TAE、HAIC、放疗成功转化治疗IIIa期HCC实现R0切除且达到MPR,并在术后辅助治疗中使患者持续获益。
不良反应:整个治疗期间患者未出现任何明显的药物相关不良反应。
病例总结
转化治疗能减少晚期HCC患者的肿瘤负荷以提高 R0切除率并降低手术风险,或使肿瘤降期后切除,从而使患者获得比其他治疗更好的生存获益[3]。本例HCC患者肝功能 Child-Pugh分级A级,但其初诊就已是晚期(CNLC IIIa期),属于外科学可切除、生物学不可切除的HCC。对此,《肝癌转化治疗中国专家共识(2021版)》推荐采用较为积极的转化策略,包括高强度、多种治疗模式联合(比如系统治疗与局部治疗的结合)等,以争取在短期内获得肿瘤缩小和降期,或使剩余肝脏体积增大,最终获得根治性治疗机会[3]。基于此,我们经MDT讨论后,为本例患者实施了“靶向药物+免疫治疗”系统治疗联合TAE、HAIC、放疗等局部治疗的多模式、综合性转化治疗方案。
手术切除并不是抗肿瘤治疗的终点,患者的长期生存才是最终目的。因此,在转化成功后我们决定给予术后辅助治疗尽可能降低肿瘤复发风险,从而延长患者术后无瘤生存期。尽管目前尚无公认有效预防HCC术后复发转移的辅助治疗方案,但现有的研究证据显示:靶向药物、免疫检查点抑制剂单药或联合应用,有望改善合并高危复发因素HCC患者的预后[4]。其中,国产PD-1免疫检查点抑制剂替雷利珠单抗因疗效突出、安全性可靠、可及性高等多种优势而成为临床医生优选的免疫治疗药物。
在RATIONALE-301研究中,替雷利珠单抗单药治疗组患者的中位总生存期(mOS)达15.9个月,客观缓解率(ORR)为14.3%,其中完全缓解(CR)率是索拉非尼组的10倍(2.9% VS 0.3%);替雷利珠单抗组持续缓解时间(DoR)高达36.1个月,是索拉非尼组(11.0个月)的3倍之多[5]。另外,BGB-A317-211研究表明:替雷利珠单抗联合靶向药物治疗下,不可切除HCC患者的ORR约38.7%,疾病控制率高达90.3%,中位无进展生存期(mPFS)达9.6个月;且两药联合≥3级治疗相关不良事件(TRAEs)发生率仅为28.1%[6]。以上诸多数据体现了在中晚期HCC患者治疗中,替雷利珠单抗单药及与靶向药物联合治疗的重要价值:不仅具有强劲而持久的缩瘤抗癌能力,而且药物安全性可靠。
基于以上证据和相关指南、共识推荐,本例患者采用了“替雷利珠单抗+多纳非尼”联合TAE、HAIC以及放疗的综合性转化治疗方案,经治疗,患者实现肿瘤体积缩小、门静脉癌栓消退、肿瘤指标降至正常,最后顺利实施根治性手术,获得MPR。术后采用原靶免方案治疗至今,未见任何肿瘤复发转移征象,且迄今为止的整个治疗期间未发现明显的药物相关不良反应。本例典型案例提示,免疫联合靶向、局部治疗、放疗可能是晚期HCC患者有效的转化治疗方式,这种多模式联合的综合性治疗方案能使患者获益更多,且安全性可控。期待后续见证该患者更远期的生存获益,同时也希望替雷利珠单抗能够助力我国更多的中晚期HCC患者,通过转化治疗获得根治性切除机会,并在术后辅助治疗中达到长期无瘤生存的目的。
[1]中华人民共和国国家卫生健康委员会医政医管局. 原发性肝癌诊疗指南(2022年版)[J]. 中华肝脏病杂志, 2022, 30(4):367-388.
[2]国家科技部传染病防治重大专项课题《病毒性肝炎相关肝癌外科综合治疗的个体化和新策略研究》专家组, 陈孝平, 沈锋,等. 肝细胞癌肝切除术后复发预防和治疗中国专家共识(2020版)[J]. 中国实用外科杂志, 2021,41(1):20-30.
[3]中国抗癌协会肝癌专业委员会转化治疗协作组, 樊嘉. 肝癌转化治疗中国专家共识(2021版)[J]. 中华消化外科杂志, 2021, 20(6):600-616.
[4]肝癌术后辅助治疗中国专家共识协作组, 中国医师协会外科医师分会, 中国抗癌协会肝癌专业委员会, 等. 肝癌术后辅助治疗中国专家共识(2023版)[J]. 中华消化外科杂志, 2023, 22(4):437-448.
[5]Masatoshi Kudo, et al. Final analysis of RATIONALE-301: Randomized, phase III study of tislelizumab versus sorafenib as first-line treatment for unresectable hepatocellular carcinoma. 2022 ESMO.LBA36.
[6]Minshan Chen, et al. Efficacy and safety of tislelizumab (TIS) plus lenvatinib (LEN) as first-line treatment in patients (pts) with unresectable hepatocellular carcinoma (uHCC): a single-arm, multicenter, phase II trial. 2022 ESMO IO Abstract 165P.
排版编辑:肿瘤资讯-小瑜











 苏公网安备32059002004080号
苏公网安备32059002004080号


