近年来,免疫联合治疗在肝细胞癌 (HCC) 治疗领域「展露锋芒」,多项临床研究均证实其在晚期 HCC 治疗中具有良好的疗效与耐受性 [1-3] ,目前国内外权威指南均推荐免疫联合治疗作为晚期 HCC 治疗新一线选择 [4-6] 。
真实世界中 HCC 患者的情况较临床研究中更为复杂,尤其是在 HCC「独具特色」的中国,具有乙型肝炎病毒(HBV)感染率高、肿瘤分期晚、肝功能差等特点。面对错综复杂的真实世界,临床研究中免疫联合治疗的「锋芒」能否照进现实,在真实世界的临床实践中继续「大放异彩」?
免疫联合治疗在晚期 HCC 一线治疗中的临床研究捷报频传
近 10 余年,免疫治疗在 HCC 领域飞速发展,打破了酪氨酸激酶抑制剂(TKI)靶向治疗在晚期 HCC 一线治疗的主导地位,使晚期 HCC 一线治疗步入了免疫治疗时代,相关临床研究捷报频传。
尤其是在今年 Lancent 最新发表的 CARES-310 研究 [3] ,卡瑞利珠单抗+阿帕替尼一线治疗更是将不可切除 HCC(uHCC)患者的中位 OS 延长至 22.1 个月 ,直逼两年,成为首个获得无进展生存期(PFS)及 OS 双终点阳性的免疫联合 TKI 的研究,确立了免疫联合 TKI 在 HCC 治疗的新一线地位。
免疫联合方案的临床研究不断刷新 OS 数据,为晚期 HCC 患者的长期生存带来希望。当面对复杂的真实世界临床实践时,免疫联合治疗能否禁得住考验?
免疫联合治疗在复杂的临床实践中表现依然亮眼,但需根据患者谨慎选择方案
真实世界中,中国 HCC 患者的较为复杂,一定程度上限制了肝癌临床治疗方法的选择,进而影响疗效。面对中国复杂 HCC 人群,免疫联合治疗的应答如何?通过目前的临床研究结果,我们来一探究竟。
合并 HBV 感染
我国 90% 的 HCC 患者伴有 HBV 感染,HBV 相关 HCC 易发生远处转移,预后较差。
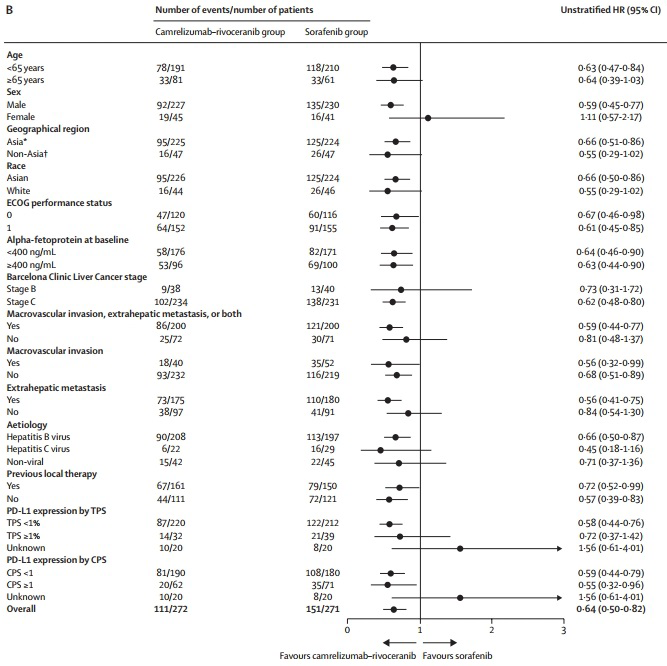
CARES-310 研究 [3]中卡瑞利珠单抗联合阿帕替尼队列合并 HBV 感染的患者比例高达 76%(208/272 例),亚组分析显示,与索拉非尼相比,HBV 相关 HCC 患者接受卡瑞利珠单抗+阿帕替尼治疗死亡风险降低 34%(图 1)。
此外,一项纳入了 86 例患者的回顾性研究发现,卡瑞利珠单抗+阿帕替尼治疗 HBV 相关 HCC 的疗效不受 HBV DNA 水平的影响,无论基线 HBV-DNA 水平(< 2000 IU/mL vs. ≥ 2000 IU/mL),客观有效率(ORRs)(34.5% vs. 32.2%, p= 0.829)和疾病控制率(DCRs)(67.3% vs. 80.6%, p=0.184)均无显著差异 [7]。另一项纳入了 2205 例 HCC 患者的回顾性研究发现,在合并病毒感染(HBV,HCV)的患者中,与仑伐替尼相比,T+A 可显著延长 OS(HR 0.76; p= 0.024) [8]。
从目前的研究结果来看,对于合并 HBV 感染的 HCC 患者,卡瑞利珠单抗+阿帕替尼或 T+A 治疗均可获益。
肿瘤分期晚
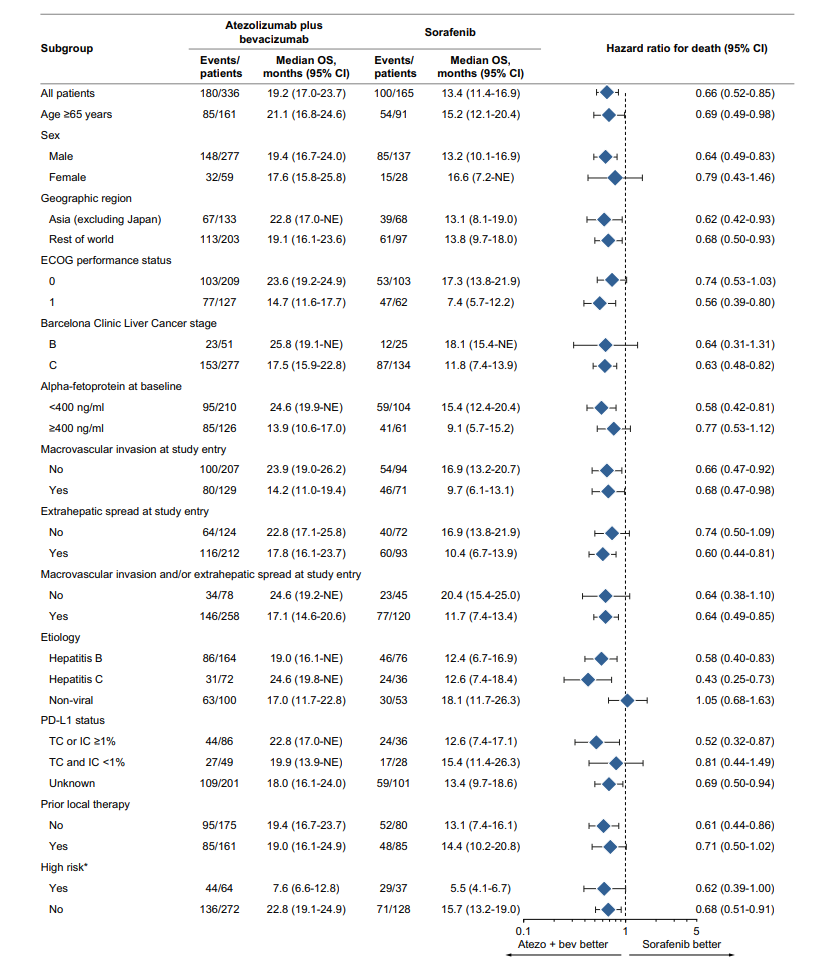
我国 HCC 患者分期较晚, 血管侵犯和(或)肝外转移的 BCLC C 期患者占比较高。CARES-310 研究 [3]卡瑞利珠单抗+阿帕替尼队列 BCLC C 期患者占比高达 86%(234/272 例),亚组分析显示,与索拉非尼相比,该部分患者接受卡瑞利珠单抗+阿帕替尼治疗可降低 38% 的死亡风险(图 1)。IMbrave150 研究 [9]T+A 队列中 82%(276/336 例)的患者为 BCLC C 期,亚组分析显示,与索拉非尼相比,该部分患者接受 T+A 治疗可降低 37% 的死亡风险 [1](图 2)。
合并门静脉主干或分支有癌栓(PVTT)的患者,相较于其他患者往往预后更差。CARES-310 研究 [3]和 IMbrave 150 研究 [1]结果显示,合并大血管侵犯的患者接受卡瑞利珠单抗+阿帕替尼治疗可降低 44% 的死亡风险(图 1),接受 T+A 治疗可降低 32% 的死亡风险(图 2)。
对于合并 PVTT 的 HCC 患者,一项单中心随机研究入组了 60 例合并 PVTT II/III/IV 型的患者,结果表明,与卡瑞利珠单抗+阿帕替尼组相比,卡瑞利珠单抗+阿帕替尼联合放疗可进一步提高疗效,中位 OS 由 8.6 个月延长至 12.7 个月 [10]。一项入组了 69 例患者的多中心前瞻性研究发现,对于预后更差的 PVTT III/IV 型的患者,予以卡瑞利珠单抗+仑伐替尼+肝动脉化疗栓塞(TACE)联合治疗中位 OS 达 18.2 个月,与 PVTT I/II 型患者(23.9 个月)无显著差异( p= 0.83) [11]。
左右滑动查看(点击查看大图)
综上,对于 BCLC C 期 HCC 患者,T+A 或免疫+TKI 治疗均可降低死亡风险。而对于预后更差的合并 PVTT 的患者,免疫+TKI 基础上联合放疗或 TACE 等局部治疗可提高临床获益。
肝功能差
我国 Child-Pugh B 级 HCC 患者比例高,且往往预后较差,而该部分人群在临床研究中常被排除在外。
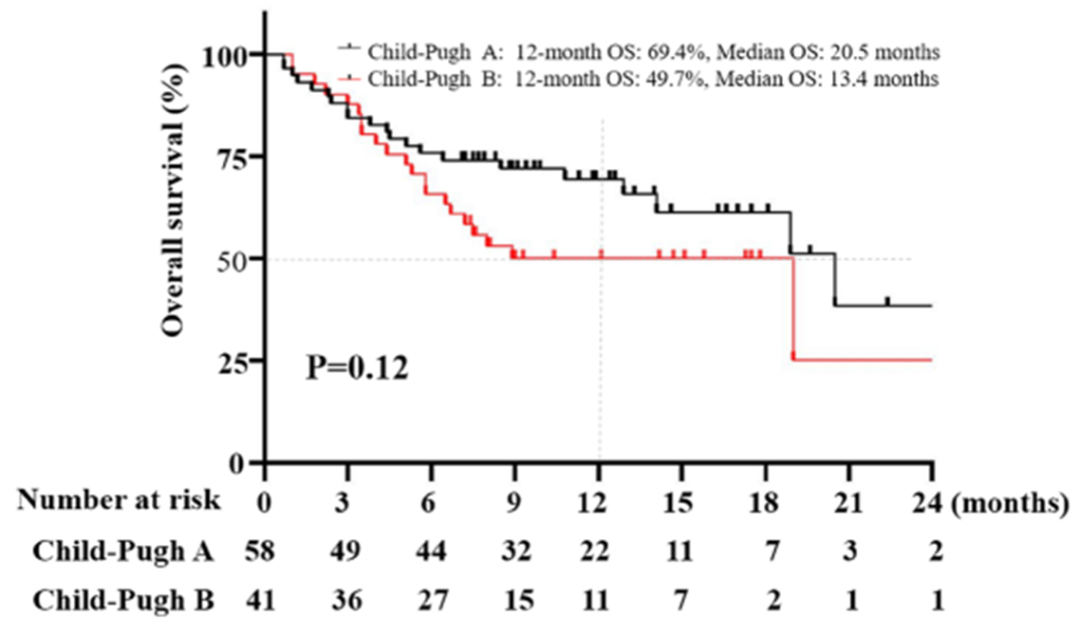
真实世界研究中,接受 T+A 治疗的 Child-Pugh B 级 HCC 患者的中位 OS 约为 6.7~7.7 个月,显著低于 Child-Pugh A 级的患者 [12, 13]。来自中国的一项多中心回顾性研究发现,卡瑞利珠单抗联合 TKI 治疗 Child-Pugh B 级 HCC 患者的中位 OS 可长达 13.4 个月,与 Child-Pugh A 级患者(20.5 个月)OS 无显著差异,且安全性相似 [14](图 3)。 目前 Child-Pugh B 级 HCC 患者接受免靶治疗的研究数据有限,仍有待进一步探索。
图 3. 根据 Child-Pugh 分级卡瑞利珠单抗治疗 uHCC 的 OS
从上述研究数据可见,面对真实世界中 HBV 感染率高、分期晚、肝功能更差的 HCC 患者,免靶联合治疗仍然具有获益。但是面对不同的患者,免靶方案的疗效还是有所差别,应谨慎选择。
免疫联合治疗探索不止,不断拓展应用空间,丰富实践经验
在 HCC 免疫联合治疗的临床实践中,除面对上述病情复杂的患者,还需面对许多悬而未解的问题,如免疫联合治疗用于围手术期治疗的疗效?免疫联合基础上,增加其他治疗是否可进一步提高疗效?可喜的是,免疫联合治疗对于上述问题也已经展开探索。
围手术期新治疗模式的探索
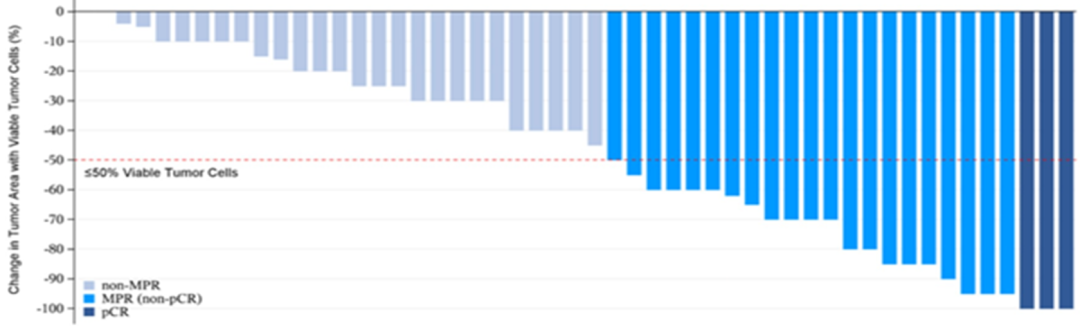
免疫联合靶向治疗因具有缓解率高、起效较快、长时间缓解等优点,成为临床上围手术期治疗探索的优选方案。2023 年美国临床肿瘤学会(ASCO)年会报道了卡瑞利珠单抗+阿帕替尼用于 HCC 围手术期治疗的 2/3 期研究 [15] ,结果显示,在意向治疗人群中,卡瑞利珠单抗+阿帕替尼治疗组主要病理缓解(MPR)率为 40%(24/60),52 例接受手术的患者中 MPR 率为 46.2%(24/52),更是有 5.8%(3/52)的患者实现了病理完全缓解(图 4)。卡瑞利珠单抗+ 阿帕替尼显示出的高抗肿瘤活性,有望使其阵线继续前移,布局 HCC 的围手术期治疗。
图 4. 接受卡瑞利珠单抗联合阿帕替尼围手术期治疗的 HCC 患者的病理学缓解情况
免靶联合局部新治疗方法的探索
研究发现,在免靶联合的基础上,再辅以局部治疗手段,还可进一步提升疗效。TRIPLET 研究中 [16] ,卡瑞利珠单抗+阿帕替尼联合肝动脉灌注化疗(HAIC)治疗 BCLC C 期 HCC 患者的 ORR 达 76.92%,DCR 达 92.31%。
结 语
面对 HBV 感染率高、肿瘤分期晚、患者肝功能较差的更加复杂的 HCC 真实世界的临床实践,免疫联合治疗表现依然亮眼,相较于传统的 TKI 治疗,免疫联合治疗可显著延长复杂 HCC 患者的生存。同时临床实践中免疫联合治疗在围手术期治疗、免疫联合局部治疗领域持续探索,进一步拓展了免疫联合治疗的受益人群,为 HCC 临床实践再添新证据。
参考文献
本文仅供医疗卫生等专业人士参考
内容策划:慧慧
内容审核:蔡静
题图来源:图虫创意












 苏公网安备32059002004080号
苏公网安备32059002004080号


