伯基特淋巴瘤(BL)是一种具有高度侵袭性的B细胞淋巴瘤。其常见于儿童和青少年,但仅占成人非霍奇金淋巴瘤的1%~2%。BL累及部位广泛,尤其是结外部位包括骨髓、中枢神经系统(CNS)等。大部分BL患者可通过多药联合的免疫化疗手段获得缓解,但高危患者经过治疗后的生存结果仍较差。一项由来自阿姆斯特丹大学医学中心的Martine E D Chamuleau教授等人报告的研究显示,DA-EPOCH-R 治疗方案或可改善高危BL患者的预后。【肿瘤资讯】特此整理,以供学习
研究背景
BL是一种罕见的侵袭性 B 细胞肿瘤,与 MYC 致癌基因易位到免疫球蛋白启动子有关。在成人低风险BL且无如乳酸脱氢酶过高、WHO表现状态评分为2或以上、III 期或 IV 期、肿块大小 10 厘米或以上等风险因素的患者中,其 2 年总生存率(OS)可达 100%。相比之下,具有高危风险因素的患者 2 年OS仅为 70%~75%。 既往一项对比DA-EPOCH-R(剂量调整的依托泊苷、泼尼松、长春新碱[oncovin]、环磷酰胺、多柔比星[羟基柔红霉素]和利妥昔单抗)和高强度化疗方案的研究显示,在接受 DA-EPOCH-R 治疗的高危患者中,其 3 年无进展生存(PFS)率为95%(95% CI,75%~99%)。而在后续的多中心随访研究中,患者4年无事件生存(EFS)率为 82%(95% CI,73%~89%)。目前研究尚未进行比较不同化疗方案的随机对照试验。
HOVON/SAKK 127试验是一项在高危BL患者中对比高强度的R-CODOX-M/R-IVAC方案和低强度的DA-EPOCH-R方案疗效和安全性的试验。该试验旨在验证既往报告的DAEPOCH-R方案在随机环境中是否同样具有PFS优势。由于DA-EPOCH-R疗法不含大剂量CNS渗透性药物(如甲氨蝶呤和阿糖胞苷),因此研究者排除了CNS受累的患者。此外,研究者延用了在 R-CODOXM/R-IVAC 组首次前瞻性试验中使用到的对高危疾病的定义。
研究方法
本研究为研究者发起的多中心、开放标签、随机3期研究。研究纳入的患者年龄为18~75岁的新诊断高危BL且未累及CNS。患者被随机分配至R-CODOX-M/R-IVAC治疗组(2个周期)或DA -EPOCH-R 治疗组(6个周期)。65 岁以上的患者将接受剂量调整后的 R-CODOX-M/R-IVAC治疗。除泼尼松龙为口服药物外,其他药物均为静脉注射。患者还接受了4次CNS鞘内注射的阿糖胞苷(70mg)和4次甲氨蝶呤(15mg)。研究者按中心、白血病情况和HIV阳性率对患者进行分层。研究主要终点是PFS。所有分析均遵循改良的意向治疗原则,但这其中不包括随机分配的且在研究开始时发现有CNS受累或被诊断为非BL的患者(EudraCT2013-004394-27)。
研究结果
患者情况
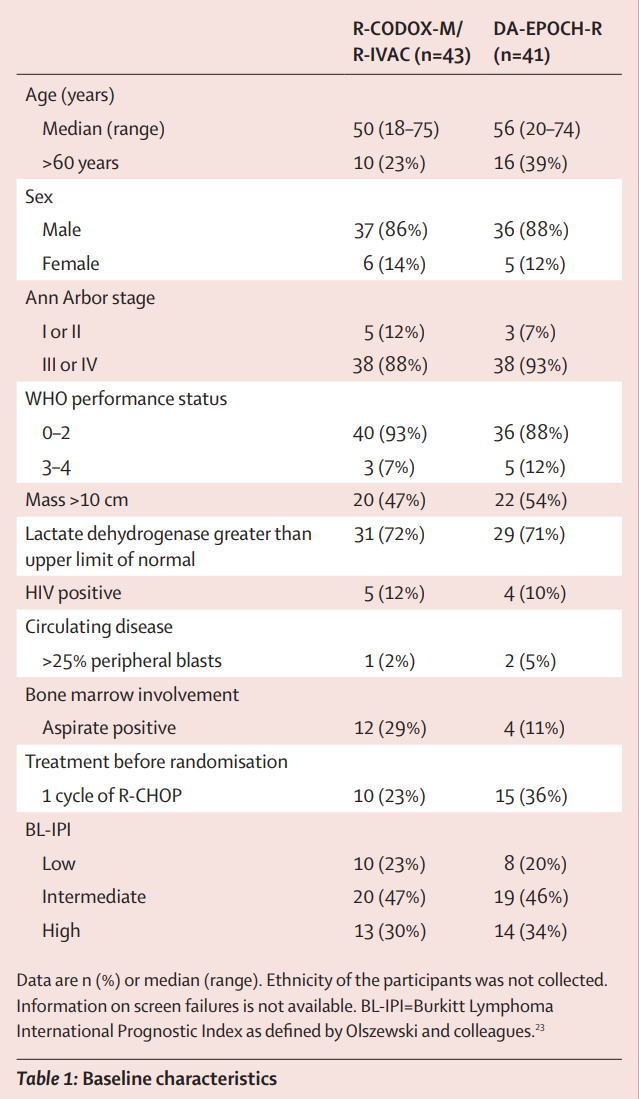
2014年8月4日至2021年9月17日,研究共有89例患者入组。其中有84 例患者进行了修改后的意向治疗分析,患者基线特征见表1。在所有纳入分析的患者中,87%(73 例)为男性,患者中位年龄为52岁(IQR 37~64),90%(76 例)为 III 期或 IV 期患者,11%(9例)为HIV 阳性BL患者。根据拟议的伯基特淋巴瘤国际预后指数(BL-IPI)对患者进行分类,21%(18例)为低危患者,46%(39例)为中危患者,32%(27例)为高危患者。在研究方案修订后,R-CODOX-M/R-IVAC组的10例患者和DA-EPOCH-R组的15例患者均在进行随机分配前接受了1个周期的R-CHOP治疗,其中有12例患者在1个周期的R-CHOP治疗后完成了6个周期的DA-EPOCH-R治疗。
在R-CODOX-M/R-IVAC组中,1例患者在治疗开始前拒绝治疗,还有9例患者因病情进展(4例)、毒性反应(4例)和败血症(1例)而中止治疗。有2例患者在治疗期间死亡(1例因病情进展,1例因败血症)。在DA-EPOCH-R组中,有4例患者因病情进展(3例)或感染COVID-19(1例)而中止治疗。R-CODOX-M/R-IVAC组的33例患者和DA-EPOCH-R组的37例患者完成了治疗。
表1.患者基线特征
疗效结果
中位随访时间为28.5个月(IQR13.2~43.7)。R-CODOXM/R-IVAC 组患者的1年和2年PFS率均为76%(95% CI 60%~86%)。而DA-EPOCH-R 组患者的1年和2年PFS率分别为 73%(95% CI,57%~84%)和70%(95% CI,54%~82%)(图 1)。主要结果的预估 HR(未调整)为 1.47(95% CI,0.66~3.28;P=0.34)。在调整了白血病负担和 HIV 阳性率后,患者PFS的预估 HR 为 1.42(95% CI 0.63~3.18,P=0.40)。
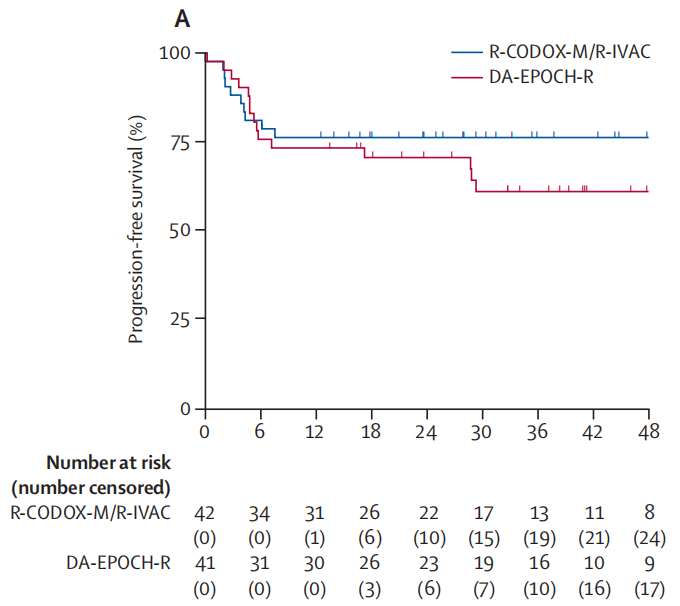
图1. 两组患者PFS Kaplan-Meier 生存曲线
在患者的1年OS率方面,R-CODOX-M/R-IVAC组 vs DA-EPOCH-R组为78%(95% CI,62%~88%)vs 80%(95% CI,65%~86%)(图2);2年OS率方面,R-CODOX-M/R-IVAC组 vs DA-EPOCH-R组为76%(95% CI,60%~86%) vs 75%(95% CI,59%~86)(HR 1.21, 95%CI, 0.53~2.76; P=0.65)。
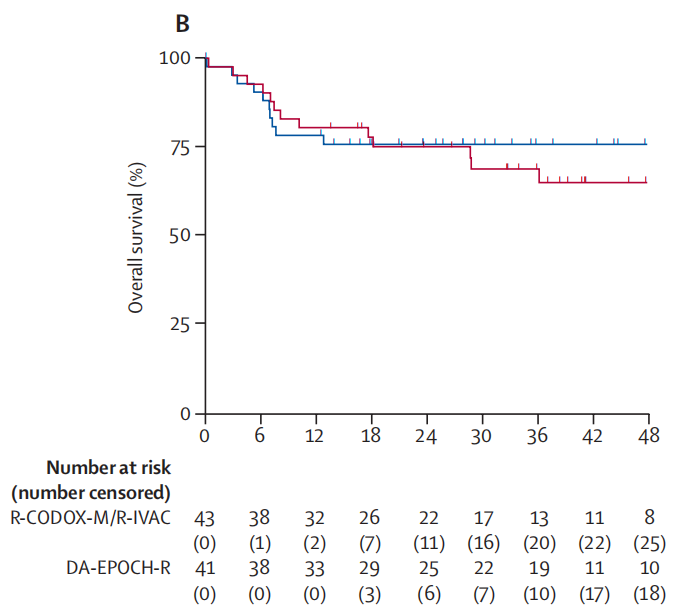
图2.两组患者OS Kaplan-Meier 生存曲线
两组患者的1年疾病特异性生存率类似,R-CODOX-M/R-IVAC组84%[95% CI,67%~93%] vs DA-EPOCH-R组83%[95% CI,67%~91%]。此外,两组患者2年疾病特异性生存率也较为相似,R-CODOX-M/R-IVAC组82%[95% CI,65%~91%] vs DA-EPOCH-R组80%[95% CI,64%~90%](HR 1.10, 0.40~3.02;P=0.86,图3)。
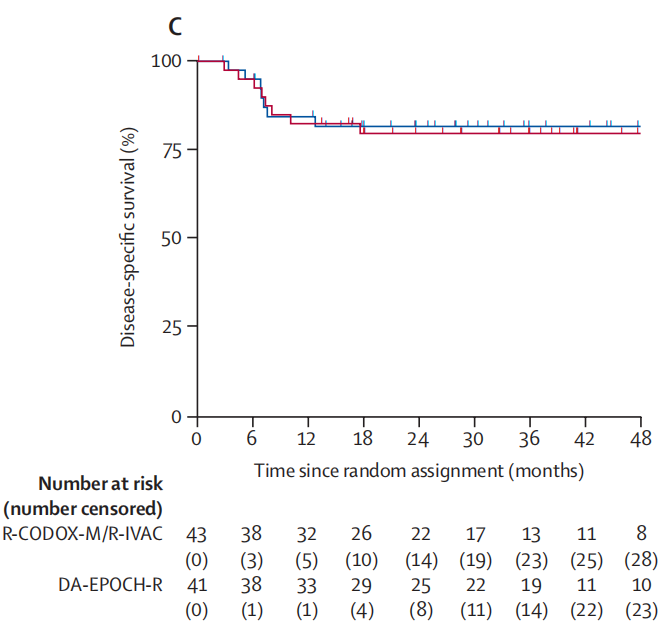
图3.两组患者疾病特异性生存曲线
相对于R-CODOX-M/R-IVAC组,DA-EPOCH-R组患者的1年EFS率更高,为66%(R-CODOX-M/R-IVAC组62%;HR 0.84,0.41~1.79;P=0.64])。治疗结束时,R-CODOXM/R-IVAC组和DA-EPOCH-R组分别有34例(79%)和37例(90%)患者进行了PET-CT缓解评估,结果显示两组分别有28例(65%)和27例(66%)患者获得完全代谢缓解(P=0.94)。
安全性结果
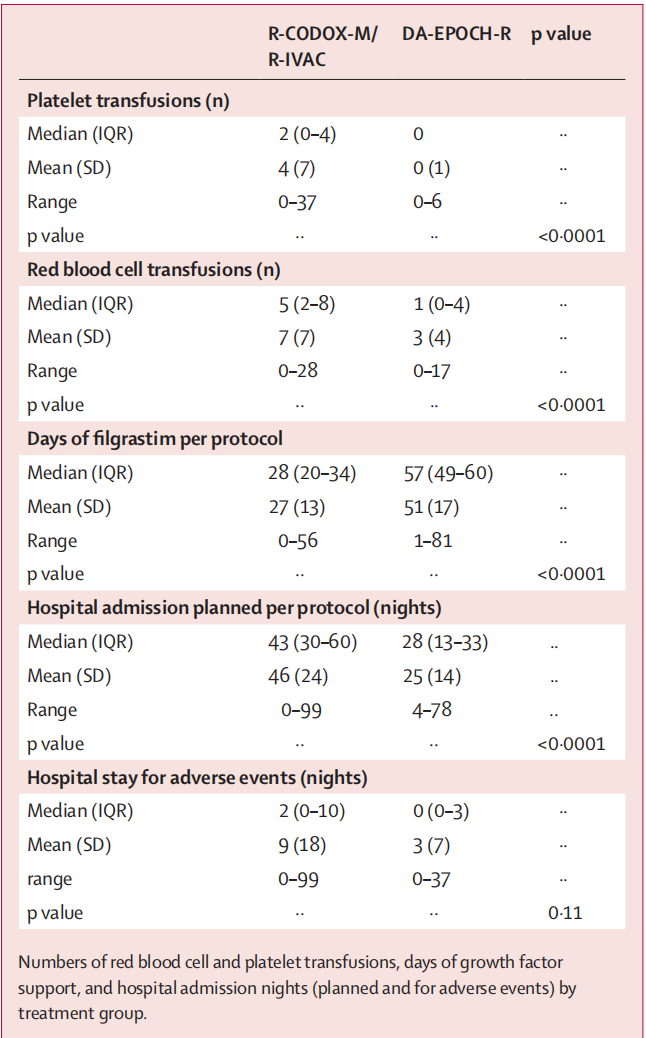
在R-CODOX-M/R-IVAC组的34例患者中,共出现了129起3~5级不良事件(AEs)。而在DA-EPOCH-R组的30例患者中,共出现了83起AEs。与DA-EPOCH-R组相比,R-CODOXM/R IVAC组患者似乎出现了更多的感染性AEs(56% vs 34%)。在60岁以上的患者中,接受R-CODOX-M/R-IVAC治疗的患者发生过≥1次3~5级AEs的比例更高(90%[9例] vs 75%[12例])。大多数严重AEs都是感染性的(包括发热性中性粒细胞减少症),而且大多数都发生在 R-CODOX-M/R-IVAC 组(R-CODOX-M/R-IVAC 组n=22 vs DA-EPOCH-R 组n=13 )。相比于DA-EPOCH-R组,R-CODOX-M/R-IVAC组患者接受红细胞输血的中位次数更高(5次 vs 1次;P<0.0001;表2])。同时,R-CODOX-M/R-IVAC组患者输注血小板的中位次数也更高(2 次 vs 0 次 ;P<0.0001])。R-CODOX-M/R-IVAC组有2例患者死亡(1例死于感染[与治疗相关],1例死于疾病进展[与治疗无关]),DA-EPOCH-R 组有1例死亡(COVID-19 感染[与治疗有关])。
表2.患者在治疗期间需要的支持性护理
结论
本研究为多中心随机研究,旨在探索两种不同的免疫化疗方案(高强度的R-CODOX-M/ R-IVAC 与低强度的DA-EPOCH-R)治疗高危BL患者的疗效差异。结果表明,与R-CODOX-M/R-IVAC相比,DA-EPOCH-R治疗并不能带来更好的完全代谢缓解和生存率。但患者接受DA-EPOCH-R治疗后的毒性反应更小,对支持治疗的需求也更少。DA-EPOCH-R治疗组的缓解率和生存结果与R-CODOX-M/R-IVAC组相似。但由于研究结束过早,试验的效力较小,这一结果尚未最终确定。
虽然研究者无法证明 DA-EPOCH-R 治疗的优越性,但这项研究仍旧提供了宝贵的信息。首先,两种治疗方案都是可行的。在 91% 的治疗周期中,R-CODOX-M/R-IVAC 为全剂量给药,而DA-EPOCH-R 的剂量递增也与之前公布的数据相似,这反映了实际治疗方案与计划治疗方案基本保持一致。其次,与 DA-EPOCH-R 组相比,R-CODOX-M/R-IVAC 组患者出现了更多的毒性反应。 最后,与接受 DA-EPOCH-R 治疗的患者相比,接受 R-CODOX-M/R-IVAC 治疗的患者需要更多的支持性护理,住院时间也明显更长。
结合两个治疗组,WHO 表现状态评分为 0 与患者更好的OS和PFS显著相关(Kruskal Wallis 的 P=0·02 和 P=0·01)。两组60岁以上患者的OS无差异。根据 BL-IPI 评分界定的高危疾病在2个治疗组中均无预后价值,这可能是由于研究纳入人数较少。在高危 BL-IPI 患者中,两种治疗方案的结果没有显着差异。
除了过早结束治疗和用于亚组分析的人数较少之外,这项研究还存在一定的局限性。虽然所有完成治疗的患者的中位随访时间超过24个月,总随访时间超过12个月,但随访时间仍然太短,无法评估治疗的长期毒性。
总之,虽然现有的数据未体现出DA-EPOCH-R 方案疗效方面的显著优势,但其毒性作用较小,患者需要的支持治疗也明显较少。对于无CNS受累的高危BL患者来说,DA-EPOCH-R 治疗是一种有效且毒性较小的治疗选择。
R-CODOX-M/R-IVAC versus DA-EPOCH-R in patients with newly diagnosed Burkitt lymphoma (HOVON/SAKK): final results of a multicentre, phase 3, open-label, randomised trialChamuleau, Martine E D et al.The Lancet Haematology, Volume 10, Issue 12, e966 - e975
排版编辑:cherry











 苏公网安备32059002004080号
苏公网安备32059002004080号


