边缘区淋巴瘤(MZL)是一类临床异质性较大的B细胞淋巴瘤,发生发展与BCR信号传导异常激活、NF-κB等通路激活密切相关。一线化疗免疫疗法效果较佳但易复发,二线治疗缺乏标准方案。BTK抑制剂在边缘区淋巴瘤治疗中显示出一定疗效。近日,Blood Advances杂志上发表了一项研究,利用全外显子测序和循环肿瘤DNA技术,评估基因突变对BTK抑制剂泽布替尼疗效的预测作用,以及监测获得性耐药相关突变,旨在阐明BTK抑制剂在MZL治疗中的分子机制、耐药因素及个体化治疗策略选择[1] 。特邀浙江大学附属第一医院俞文娟教授对该研究进行点评,详情如下。
研究目的
边缘区淋巴瘤(MZL)是一种异质性的B细胞淋巴瘤,常依赖B细胞受体(BCR)信号传导途径。MZL包含多种临床亚型,发生与进展涉及多条关键信号通路及驱动基因的突变。一线化疗免疫疗法反应较好,但易复发且缺乏标准二线治疗。BTK抑制剂伊布替尼和zanubrutinib在MZL中显示出抗肿瘤活性。临床试验提示NOTCH、TP53、KMT2D等基因突变可能影响BTKi疗效。本研究利用全外显子测序评估基线样本对zanubrutinib的预测作用,以及通过循环肿瘤DNA监测耐药相关突变,旨在进一步阐明BTKi在MZL治疗中的分子机制、耐药因素及个体化治疗策略。MZL是一类临床异质性较大的B细胞淋巴瘤,包括黏膜相关淋巴组织型、脾边缘区型、淋巴结边缘区型和原发性皮肤型,发生发展与BCR信号传导异常激活、NF-κB和相关通路激活等密切相关。典型突变基因涉及NOTCH、NF-κB、BCR等关键信号通路。一线化疗免疫疗法效果较佳但易复发,二线治疗缺乏标准方案。BTKi在MZL治疗中显示出一定疗效。本研究利用全外显子测序和循环肿瘤DNA技术,进一步解析zanubrutinib治疗MZL患者的敏感性预测标志物及获得性耐药机制,为BTKi在MZL个体化治疗中提供依据。
研究方法
本研究探讨了MZL患者zanubrutinib治疗响应的基因组学特征。选取18例接受MAGNOLIA II期临床试验治疗的MZL患者。从原发肿瘤、口腔粘膜和血液中提取DNA,进行全外显子组测序。生物信息分析集中在48个候选基因,这些基因涉及NF-kB、NOTCH、BCR通路,也是MZL常见的致病突变。此外,设计了针对这48个基因的定制化芯片,对cfDNA进行目标测序。数据分析采用生物信息分析流程,包括去杂合、变异检测和拷贝数分析。仅保留对蛋白功能有影响的非同义突变。运用公共数据库评估突变的致病性。对有原发肿瘤样本(17例)的患者,分析基因组学特征与zanubrutinib的疗效相关性。方法包括Fisher精确检验和Kaplan-Meier分析。
研究结果
复发/难治性MZL中NF-κB、NOTCH和BCR通路突变较为常见
对18例患者中的19个原发肿瘤样本于zanubrutinib治疗前进行了全外显子组测序。17例患者在研究过程中接受了zanubrutinib治疗,1例未通过筛选但仍符合肿瘤分子特征分析条件。 4例患者进行了与体细胞对比。患者中位数年龄为71岁(范围37-86岁),以男性居多(67%)。所有患者至少接受过1次化学免疫治疗(中位数:1.5次;范围:1-4次)。
共检测到90个突变,19个肿瘤样本中7个(37%)检测到同一基因的多个突变。48个候选基因中有33个(69%)受到影响(图1)。每个肿瘤样本的中位突变数为5个(范围:0-12个),错义突变占主导地位(76%;图1)。1例患者(MZ17)对比分析了淋巴结和胃组织样本:NOTCH1、NOTCH2和KMT2D突变检测于两样本中,而TNFAIP3和FAS突变仅检测于淋巴结。1例肿瘤组织样本量有限的患者,未检测到任何变异。
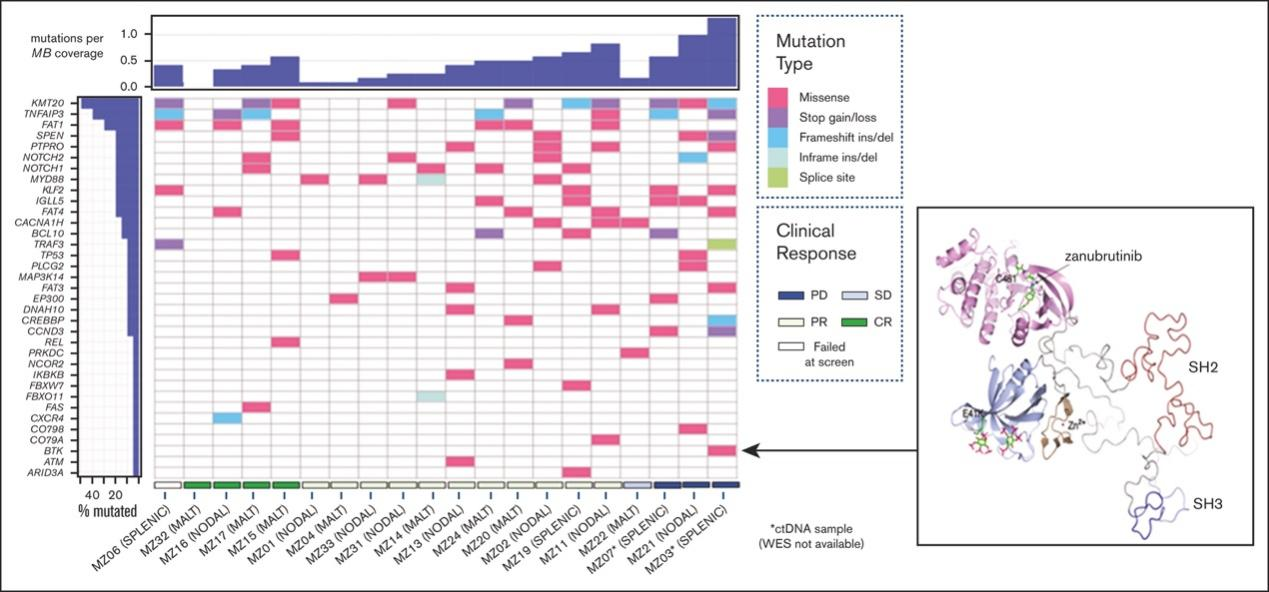 图1 入组时检测到的变异共突变图
图1 入组时检测到的变异共突变图
NF-κB通路基因突变可能预测MZL对泽布替尼的治疗反应
对17例接受泽布替尼治疗的MZL患者的肿瘤进行了全外显子组测序,探讨了基因组学特征与疗效的相关性。结果显示,NF-κB通路基因MYD88和TNFAIP3的突变可能预测疗效。4例MYD88突变(包括1例非热点L265P突变)和4例TNFAIP3突变的患者,均达到客观缓解且无进展生存期显著延长。提示这些突变激活NF-κB通路,可能导致对BTK抑制剂泽布替尼更敏感。
NOTCH通路在MZL中也发生突变,但本研究中NOTCH1和NOTCH2突变与疗效无相关性。未检测到导致BTK抑制剂耐药的CARD11突变。KMT2D是本研究中最常见的突变基因,但其突变却与较短的无进展生存期相关。推测KMT2D可能通过精确的表观遗传调控参与MZL发生。TP53、FAT家族等其他基因突变频率较低,无法进行有意义的统计分析。但TP53突变定位于DNA结合区或无DNA结合区可能会影响其功能效应。
综上,NF-κB通路基因突变可作为MZL对BTK抑制剂泽布替尼敏感性的预测生物标志物,有助于患者的个体化治疗选择。更大样本量的研究还需验证这些发现。
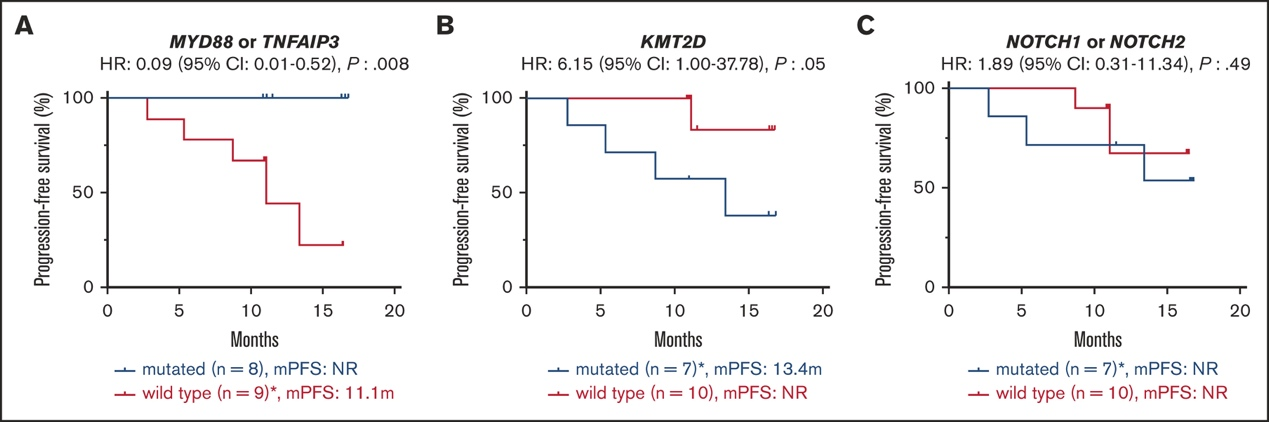 图2 泽布替尼治疗反应的分子预测标志物
图2 泽布替尼治疗反应的分子预测标志物
ctDNA可用于追踪和检测导致BTKi耐药的获得性新发突变
为了纵向监测获得性耐药突变的产生,在7例患者中多个时间点采用从血浆中分离的cfDNA与对照体细胞DNA进行了比较;其中4例有基线石蜡切片肿瘤样本进行WES;另外3例没有基线肿瘤样本进行WES分析。cfDNA的平均和中位产量分别为10.6 ng/mL和6.9 ng/mL(范围:2.5-105 ng/mL),在疾病进展时水平升高。也对7例患者的多个样本进行了ctDNA分析:3例有反应的患者(MZ01、MZ02和MZ04)、3例有疾病进展的患者(MZ03、MZ05和MZ07)以及1例在WES中检测到多个突变(n=5)但未接受泽布替尼治疗的患者(MZ06)。
治疗期间ctDNA疾病负荷的变化
在有反应的患者中,MZ01和MZ02的肿瘤样本WES检测出MYD88 L265P突变;两位患者均达PR,治疗期间ctDNA中的突变负荷下降(图3A-B)。两位患者的基线ctDNA中也检测到筛查时WES未检出的突变:MZ01检出KMT2D Q2416H突变(VAF下降),MZ02检出TP53 R248W突变(VAF稳定)。在这组患者中,未观察到与BTKi耐药相关的获得性突变。
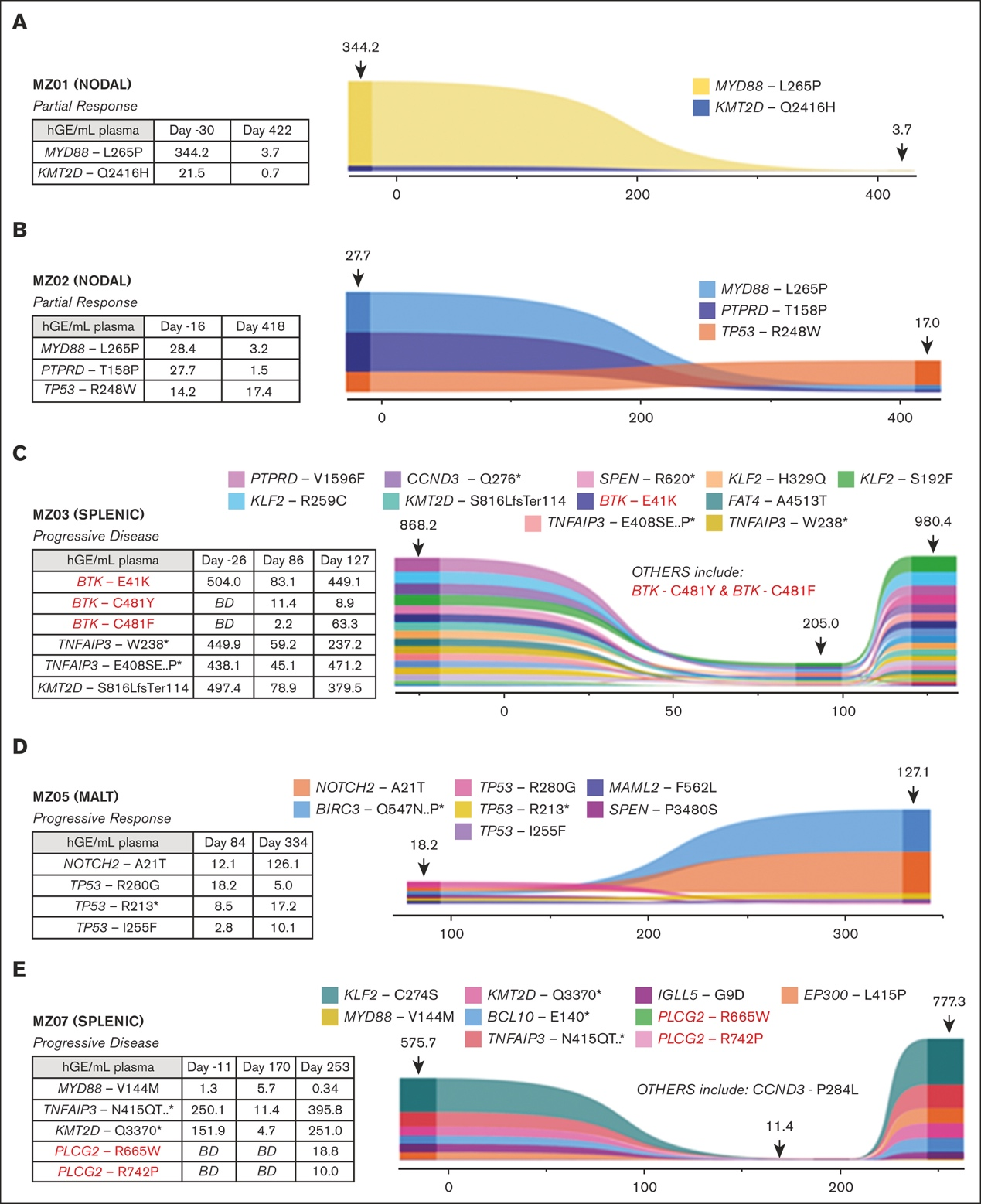 图3 5例患者泽布替尼治疗过程中ctDNA突变的检测和演变
图3 5例患者泽布替尼治疗过程中ctDNA突变的检测和演变
治疗过程中ctDNA中获得性耐药相关突变
3例在泽布替尼治疗后疾病进展的患者,没有基线肿瘤样本进行WES。MZ03和MZ07的ctDNA样本显示,获得了与BTKi耐药相关的新突变。MZ07初期达PR,第253天疾病进展,ctDNA检测到基线未见的PLCG2 R665W和L742P突变。MZ03的ctDNA治疗前检测到BTK E41K突变,第86天疾病进展,ctDNA检测到新的BTK C481F、C481Y突变和持续存在的BTK E41K突变。MZ05没有基线肿瘤组织或ctDNA样本,但最早和疾病进展的ctDNA样本检测到影响BIRC3的突变和3个TP53突变。以上结果表明,这些患者在BTKi治疗过程中ctDNA中出现了与获得性耐药相关的新突变。监测ctDNA的变化,可以检测到获得性耐药相关突变的产生,为后续治疗选择提供参考。
ctDNA与基线组织WES的差异
有3例患者(MZ01、MZ02和MZ06)同时进行了肿瘤组织WES测序和筛查时ctDNA检测。比较结果发现,在这3例患者WES检出的13个突变中,有8个(62%)在ctDNA检测中也被检出。然而,筛查ctDNA检出的2个突变未在WES中检出。筛选失败患者(MZ06)肿瘤样本的5个突变(包括KMT2D和TNFAIP3)在ctDNA检测中可被检出。另有4个突变(CACNA1H、EP300和2个TBL1XR1)仅在ctDNA中检出而不在WES中。MZ02肿瘤WES检出但ctDNA未检出的突变有1个(PLCG2 H244R)。
研究结论
本研究描述的相关性研究证明,MYD88和TNFAIP3的突变与PFS的改善相关,而KMT2D的突变可能与减少的PFS相关,这是针对用泽布替尼治疗的复发/难治性MZL患者。我们队列中发现的非催化域BTK E41K突变也描述了一种潜在的BTKi治疗的原发耐药机制。我们假设可以通过非侵入性取样(如在ctDNA中检测MYD88 L265P突变)检测与反应相关的突变,这一点得到了验证。此外,我们的假说即BTKi获得性耐药是通过获得性BTK和PLCG2突变介导的,也得到了支持,这可能预示着临床进展。这些研究对BTKi用于复发性MZL方面提供了预测原发反应或耐药以及演示获得性耐药机制的信息。应该进行更大样本的队列研究,以提供验证我们观察结果的依据,以期优化选择可能从BTK抑制治疗中获益的复发/难治性MZL患者。
浙江大学医学院附属第一医院科室副主任
中国抗癌协会血液肿瘤青委会副主任委员
中华医学会血液学分会第十一届委员会淋巴细胞疾病学组组员
CSCO抗白血病联盟&抗淋巴瘤联盟青年委员会委员
中国女医师协会血液淋巴专委会委员、白求恩基金会血液病专家委员会委员
中国老年血液病淋巴瘤学组委员
浙江省医师协会血液科分会委员兼秘书
浙江省医学会血液病学分会第十届委员会青年委员
中华血液学杂志编委会通讯编委
以通讯及第一作者在Journal of Hematology & Oncology, British Journal of Hematology, Annals of Hematology, Leukemia & Lymphoma , Leukemia research及中华血液学杂志发 表 论文16篇,主持2项国家自然科学基金
俞文娟教授:边缘区淋巴瘤(MZL)是一组异质性疾病,约占非霍奇金淋巴瘤的7%~8%。复发/难治性MZL(rrMZL)对化疗敏感性差,预后不佳。近年BTK抑制剂(BTKi)用于rrMZL治疗取得一定疗效。本研究针对rrMZL使用BTKi泽布替尼的治疗进行相关性分析和机制研究,主要发现:
1. MYD88和TNFAIP3突变可能是BTKi治疗反应的良好预测标志物。
2. 发现BTK基因非催化域E41K突变可能是BTKi治疗原发耐药的新机制。
3. 可通过非侵入性ctDNA检测监测BTKi治疗过程中耐药相关突变。
4. BTK和PLCG2突变可能介导BTKi获得性耐药。
上述发现可为rrMZL使用BTKi治疗选择提供预测指标,监测耐药提供方法,并揭示获得性耐药的潜在机制。尽管研究样本量较小,但其对指导rrMZL精准用药具有一定价值。后续若能扩大样本验证研究结论,并深入探究分子机制,将为rrMZL的BTKi治疗选择和监测提供重要依据。本研究表明,结合疾病生物学特征来指导BTKi用药是rrMZL精准治疗的重要方向。
[1] M Tatarczuch et al. Blood Adv. 2023 Jul 25;7(14):3531-3539. DOI: 10.1182/bloodadvances.2022009412
排版编辑:guangli











 苏公网安备32059002004080号
苏公网安备32059002004080号


