血浆循环肿瘤DNA(ctDNA)分析可用于晚期非小细胞肺癌(NSCLC)的基因分型,动态监测ctDNA的变化或可预测治疗结局。在一项基于两项III期临床研究(AURA3研究和FLAURA研究)的回顾性探索性分析中,所有患者均明确为EGFR敏感突变阳性(19外显子缺失突变或21外显子L858R突变)的晚期NSCLC,AURA3研究还包括T790M突变阳性的NSCLC患者,这些患者均接受奥希替尼(FLAURA研究,AURA3研究)或对照EGFR-TKI(吉非替尼或厄洛替尼,FLAURA研究)或含铂双药化疗(AURA3研究)治疗。使用数字微滴聚合酶链式反应(ddPCR)对基线、第3周和第6周时的血浆EGFR突变状态进行分析,并基于基线可检测到或不可检测到血浆EGFR突变以及第3周和第6周血浆EGFR突变清除(血浆EGFR突变不可检测)进行评估。
FLAURA:基于基线血浆EGFR突变检测状态分层的临床结果
FLAURA研究共纳入556例患者,其中90%的患者具有有效的基线血浆ddPCR结果并被纳入ctDNA可评估人群(奥希替尼组247例,吉非替尼或厄洛替尼组252例)。在基线可评估ctDNA的499例患者中,352例(71%)基线血浆EGFR突变可检测,147例(29%)基线血浆EGFR突变不可检测。两个治疗组的基线血浆EGFR突变可检测患者比例相似,奥希替尼组和吉非替尼或厄洛替尼组分别为69%(171/247)和72%(181/252)。与AURA3研究一致,基于ddPCR和NGS技术检测的基线EGFR突变和变异等位基因频率(VAF)有高度的一致性。
表1:FLAURA研究的患者人口学和基线临床特征(ctDNA可评估人群)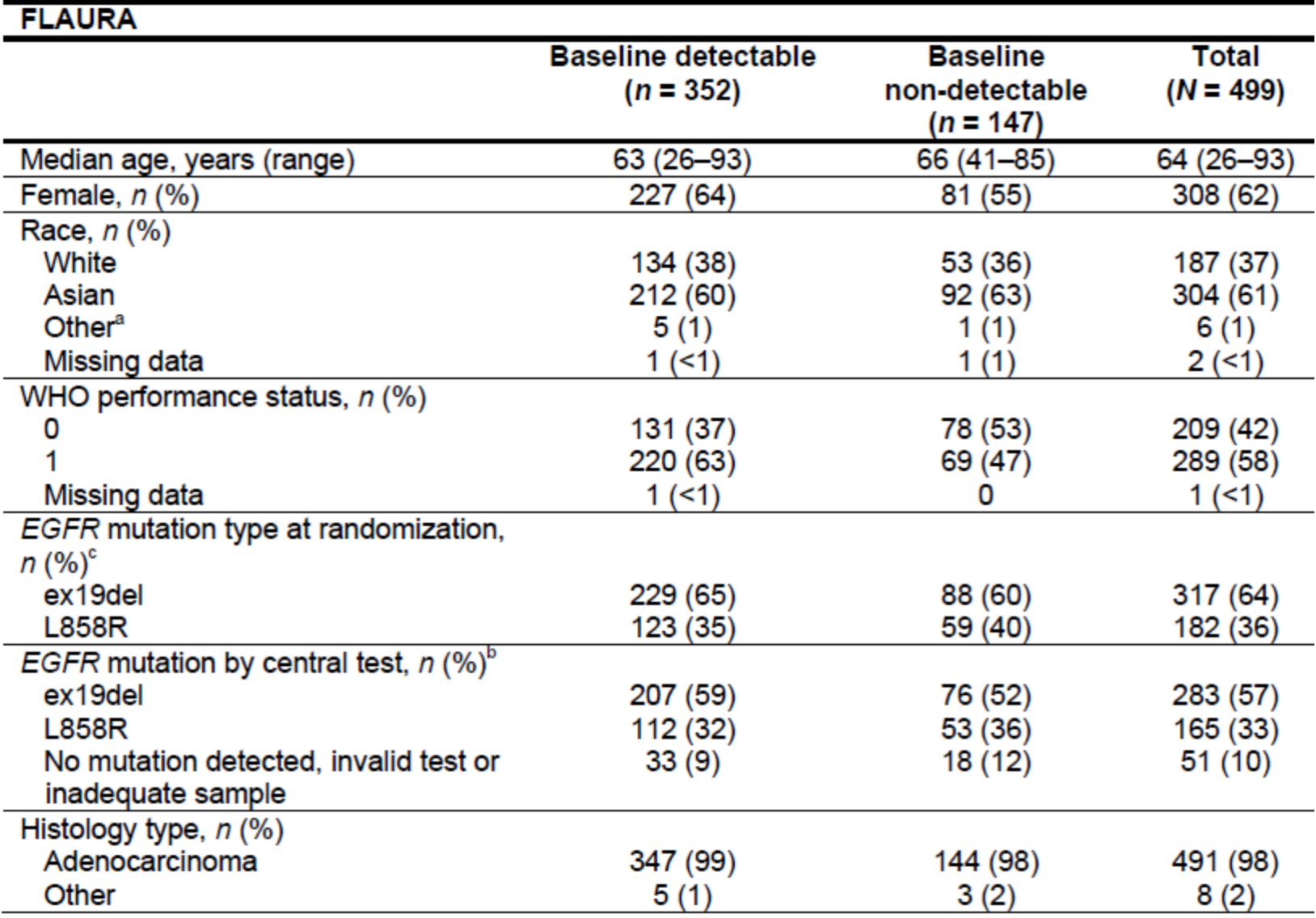
基线血浆EGFR突变不可检测相比可检测患者的中位PFS分别为19.1个月和11.1个月,HR 0.54,95% CI 0.41-0.70,P<0.0001(图1A)。在奥希替尼组中,基线血浆EGFR突变不可检测相比可检测患者的中位PFS分别为23.5个月和15.2个月,在吉非替尼或厄洛替尼组中,基线血浆EGFR突变不可检测相比可检测患者的中位PFS分别为15.3个月和9.6个月(图1B),两个治疗组有一致的趋势。基线血浆EGFR突变不可检测相比可检测患者的中位OS分别为NC(无法计算)和29.7个月(HR 0.34,95% CI 0.25-0.45,P<0.0001)。
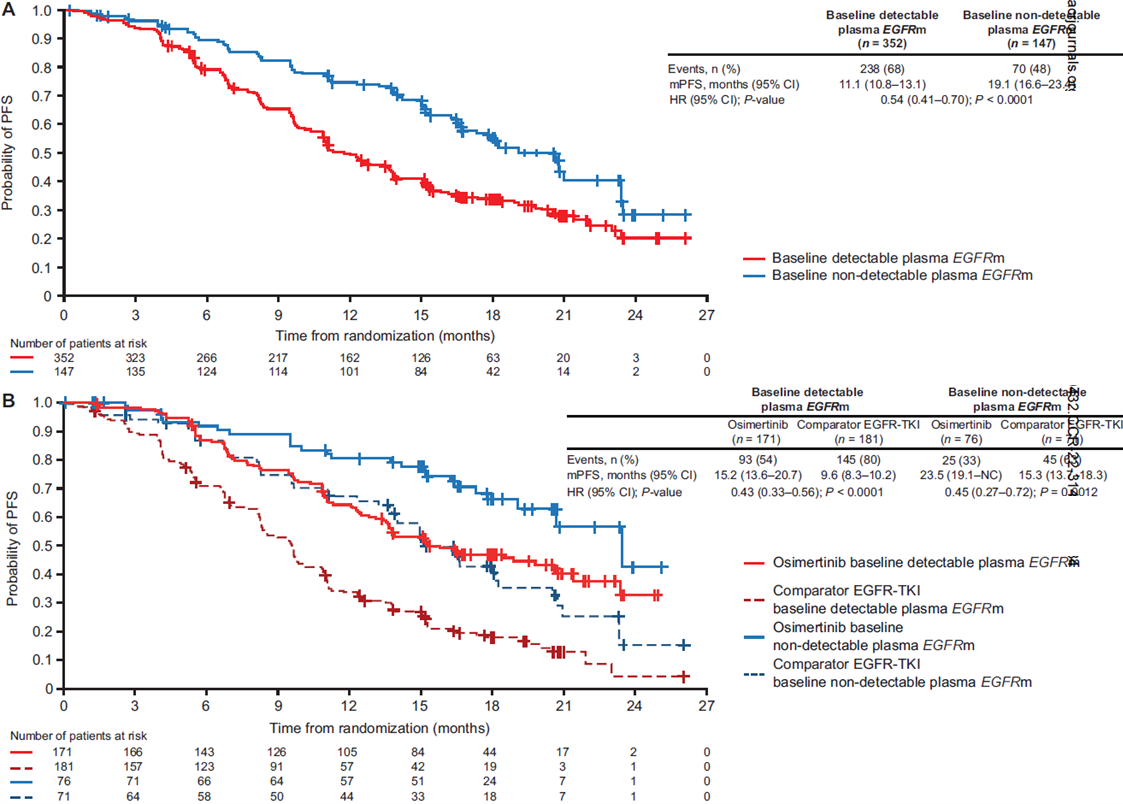 图1:研究者基于有效的基线血浆ctDNA结果评估的PFS生存曲线(FLAURA研究),A)所有基线有有效血浆ctDNA结果的患者(可检测352例,不可检测147例),B)基于治疗组分层的所有基线有有效血浆ctDNA结果的患者(可检测352例,不可检测147例)。
图1:研究者基于有效的基线血浆ctDNA结果评估的PFS生存曲线(FLAURA研究),A)所有基线有有效血浆ctDNA结果的患者(可检测352例,不可检测147例),B)基于治疗组分层的所有基线有有效血浆ctDNA结果的患者(可检测352例,不可检测147例)。
FLAURA:基于血浆EGFR突变清除分层的临床结局
在奥希替尼组中,238例患者同时具有有效的基线血浆EGFR突变检测状态(可检测或不可检测)和第3周时的ddPCR结果,106例(45%)患者基线血浆EGFR突变可检测变成不可检测(清除)。240例患者同时具有有效的基线血浆EGFR突变检测状态(可检测或不可检测)和第6周时的ddPCR结果,134例(56%)患者基线血浆EGFR突变可检测变成不可检测(清除)(图2A)。在吉非替尼或厄洛替尼组中,243例患者有有效的基线血浆EGFR突变检测状态和第3周时的ddPCR结果,102例(42%)基线血浆EGFR突变可检测的患者变成清除患者,235例患者具有有效的基线血浆EGFR突变检测状态和第6周时的ddPCR结果,124例(53%)基线血浆EGFR突变可检测的患者变成清除患者(图2A)。在基线血浆EGFR突变状态可检测的患者中,第3周时清除的患者,奥希替尼组和吉非替尼或厄洛替尼组分别有65%和59%(OR 1.3,95% CI 0.8-2.1,P=0.3)(Fisher检验)。相似的趋势:第6周时清除的患者,奥希替尼组和吉非替尼或厄洛替尼组分别有82%和76%(OR 1.4,95% CI 0.8-2.6,P=0.2)。
在接受奥希替尼治疗的基线血浆EGFR突变可检测患者中,第3周时不可检测(清除)患者(n=106)和可检测患者(n=56)的中位PFS分别为19.8个月和11.3个月(图2B),第6周时不可检测(清除)患者(n=134)和可检测患者(n=30)的中位PFS分别为19.8个月和11.1个月(图2C)。在接受吉非替尼或厄洛替尼治疗的基线血浆EGFR突变可检测患者中,第3周时不可检测(清除)患者(n=102)和可检测患者(n=70)的中位PFS分别为10.8个月和7.0个月(图2B),第6周时不可检测(清除)患者(n=124)和可检测患者(n=40)的中位PFS分别为10.2个月和8.2个月(图2C)。
在第3周血浆EGFR突变未清除的患者中,奥希替尼相比吉非替尼或厄洛替尼组有显著的PFS获益(11.3个月 vs 7.0个月,HR 0.50,95% CI 0.33-0.76,P=0.001,图2B),然而,在第6周血浆EGFR突变未清除的患者中,奥希替尼相比吉非替尼或厄洛替尼组没有显著的PFS获益(11.1个月 vs 8.2个月,HR 0.69,95% CI 0.40-1.17,P=0.164,图2C)。在血浆EGFR突变清除的患者中,无论第3周还是第6周,奥希替尼相比吉非替尼或厄洛替尼组均有显著的PFS获益(第3周,19.8个月 vs 10.8个月,HR 0.41,95% CI 0.29-0.58,P<0.0001,图2B;第6周,19.8个月 vs 10.2个月,HR 0.40,95% CI 0.29-0.55,P<0.001,图2C)。基线血浆EGFR突变检测状态以及第3周清除和第6周清除均是PFS的强效预测因子,且无论患者接受何种治疗。
在第3周血浆EGFR突变未清除的患者中,奥希替尼组和吉非替尼或厄洛替尼组的ORR相似(80% vs 76%,OR 1.31,95% CI 0.56-3.16,P=0.5319),在第6周血浆EGFR突变未清除的患者中,奥希替尼组和吉非替尼或厄洛替尼组的ORR相似(73% vs 73%,OR 1.04,95% CI 0.36-3.11,P=0.9381),在第3周血浆EGFR突变清除的患者中,奥希替尼组和吉非替尼或厄洛替尼组的ORR相似(86% vs 88%,OR 0.81,95% CI 0.35-1.82,P=0.6083),在第6周血浆EGFR突变清除的患者中,奥希替尼组和吉非替尼或厄洛替尼组的ORR相似(86% vs 90%,OR 0.65,95% CI 0.29-1.38,P=0.2643)。
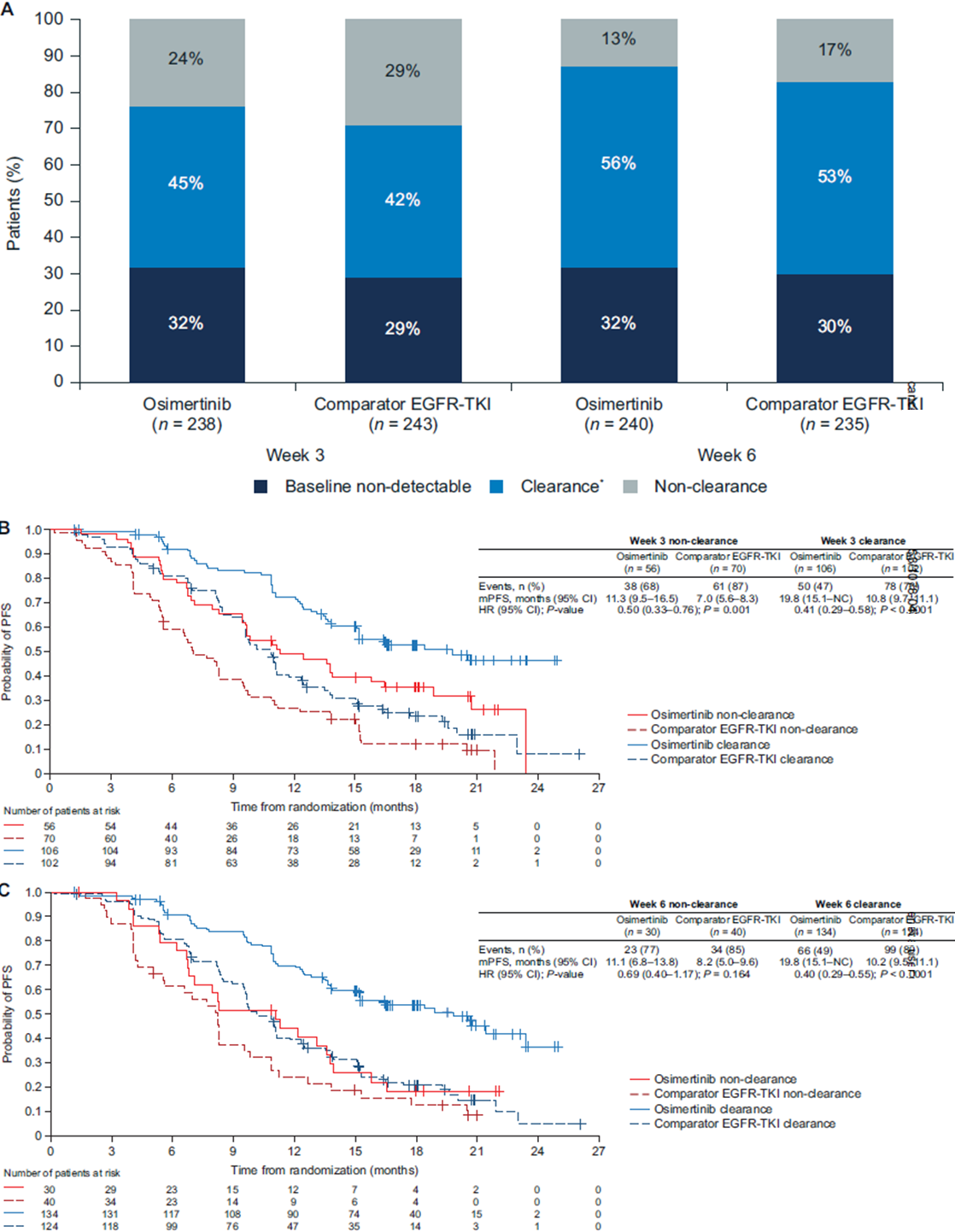 图2:FLAURA研究第3周和第6周血浆EGFR突变未清除和清除患者的分析。A)基线和第3周(n=481)和或第6周(n=475)具有有效血浆ddPCR结果(可检测或不可检测)的患者,B)基线血浆EGFR突变可检测且第3周血浆EGFR突变未清除(n=126)或清除(n=208)患者的研究者评估的PFS分析,C)基线血浆EGFR突变可检测且第6周血浆EGFR突变未清除(n=70)或清除(n=258)患者经研究者评估的PFS。清除指代基线血浆EGFR突变可检测但后续血浆EGFR突变不可检测。
图2:FLAURA研究第3周和第6周血浆EGFR突变未清除和清除患者的分析。A)基线和第3周(n=481)和或第6周(n=475)具有有效血浆ddPCR结果(可检测或不可检测)的患者,B)基线血浆EGFR突变可检测且第3周血浆EGFR突变未清除(n=126)或清除(n=208)患者的研究者评估的PFS分析,C)基线血浆EGFR突变可检测且第6周血浆EGFR突变未清除(n=70)或清除(n=258)患者经研究者评估的PFS。清除指代基线血浆EGFR突变可检测但后续血浆EGFR突变不可检测。
研究讨论
基线肿瘤释放可检测的ctDNA代表预后不佳,因此基线评估血浆ctDNA是否可检测或是一种有价值的预后指标。此外,进一步监测血浆ctDNA随着时间的变化可能为EGFR敏感突变阳性NSCLC患者获得更好疗效提供指引。
在FLAURA研究中,两个治疗组的汇总分析均显示基线血浆EGFR突变不可检测的患者相比可检测的患者有更长的PFS和OS。血浆ctDNA水平是变化的且可反应肿瘤负荷和肿瘤进展,其他研究也提示ctDNA可检测是预后不佳的预测因子。一项多瘤种的大型回顾性研究提示,循环肿瘤片段(治疗开始前)是晚期NSCLC患者独立的OS预测因子。但基线ctDNA的预测效力尚不清楚,我们的分析意外发现了,EGFR突变VAF和PFS没有相关性。以上结果表明,当基线EGFR突变可检测时,等位基因频率并不是预测PFS的关键,并且EGFR扩增对EGFR突变等位基因频率的可变影响可能是与PFS相关性的混杂因素。以上数据提示可能还存在其他潜在的生物学差异,而且这些差异比仅仅因为整体肿瘤负荷对ctDNA是否可检测的影响更为复杂。此外,靶病灶的总径和并不纳入所有已知的病灶,ctDNA信号是否可检测也受到无法扫描到的微转移病灶的影响。有研究正在探索ctDNA检测与更具侵袭性的疾病临床特征之间的相关性。有识别预后不良患者和进展风险增加患者的潜力或有助于进一步支持基线ctDNA分析作为风险分层的临床工具。
在FLAURA研究中,基线血浆EGFR突变可检测患者接受一代或三代EGFR-TKI治疗后早期血浆EGFR突变清除(相比未清除)与更好的PFS获益有相关性。相似的结果在AURA3和FLAURA研究中均可观察到,这提示血浆EGFR突变清除不受治疗线数的影响,且对所有接受EGFR-TKI治疗的EGFR敏感突变阳性NSCLC患者均适用。在其他研究中也观察到一致的结果,无论一线还是二线奥希替尼治疗亦或是其他EGFR-TKI治疗。值得注意的是,在血浆EGFR突变未清除的亚组患者中,相比吉非替尼或厄洛替尼治疗,奥希替尼治疗与PFS获益存在相关性。因此,在血浆EGFR突变未清除的患者中,并不支持停止奥希替尼的治疗,但可能提示这类患者需要更为积极的治疗策略。
有趣的是,在FLAURA研究中,奥希替尼组相比吉非替尼或厄洛替尼组,第3周和第6周血浆EGFR突变清除的比例相似(第3周,45%和42%,第6周,56%和53%)。两个治疗组相似的ORR也反映出已有的这些化合物的治疗潜力。更有趣的是,虽然ORR相似,但在血浆EGFR突变清除的患者中,奥希替尼组相比吉非替尼或厄洛替尼组有更好的PFS获益。这可能与奥希替尼的缓解持续时间和缓解深度有关,还可能与延缓耐药有关。因此,早期ctDNA动态可能是一种潜在的药效学生物标志物,它可以反映一种药物的初始活性,而不能反映长期受益。
研究结论
早在治疗开始后的3周时,血浆EGFR突变检测状态分析就有预测EGFR-TKI治疗EGFR敏感突变阳性晚期NSCLC患者治疗结果的潜力。
Jhanelle E Gray, et al. Clin Cancer Res. 2023 Jun 28;CCR-22-3146.
排版编辑:肿瘤资讯-olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


