抗体偶联药物(ADC)被誉为“抗癌精准导弹”,近年来在非小细胞肺癌(NSCLC)领域的探索如火如荼,研究成果也层出不穷。ADC药物已然成为继靶向和免疫治疗之后掀起的又一个浪潮。在今年ESMO大会上,作为ADC对比化疗的首个III期TROPION-Lung01研究取得了主要终点阳性结果,为临床带来诸多启示。本期肿瘤资讯特邀解放军总医院胡毅教授解读研究结果,并展望Dato-DXd未来研究布局。
解放军总医院肿瘤医学部主任
国家教育部重点实验室、全军肿瘤学重点实验室主任
解放军总医院临床试验药理基地肿瘤专业组负责人
呼吸肿瘤及内镜介入科主任
军队优秀专业技术人才一类岗位津贴
中央保健委员会会诊专家, 中央保健先进个人
中央军委保健委员会会诊专家
解放军医学杂志副主编
中国临床肿瘤学会(CSCO)老年肿瘤防治专业委员会主任委员
中国研究型医院学会分子肿瘤与免疫治疗专业委员会主任委员
北京医学会肿瘤学分会 副主任委员
中国临床肿瘤学会(CSCO)理事
中国临床肿瘤学会(CSCO)非小细胞肺癌专委会 常务委员
中国临床肿瘤学会(CSCO)小细胞肺癌专委会常务委员
中国临床肿瘤学会(CSCO)肉瘤和黑色素瘤专委会 常务委员
世界内镜协会呼吸内镜协会常务委员
中国医师协会肿瘤多学科诊疗专业委员会常务委员
迎难而上,TROPION-Lung01研究为NSCLC后线治疗带来新希望
在中国,肺癌是发病率和死亡率均在首位的恶性肿瘤,每年有超过80万的患者被诊断出来,其中80%左右都是NSCLC患者。虽然靶向治疗和免疫治疗显著改善了NSCLC患者的生存期,然而大多数患者仍会出现疾病进展并需要进行化疗。数十年以来,尚无其他创新药物有疗效及安全性的突破,在缺乏其他治疗选择的情况下,尽管疗效有限且伴有已知副作用,但化疗一直是晚期NSCLC患者可用的最后的治疗方式[1]。
TROP2是一种跨膜糖蛋白,在NSCLC中高表达,且与NSCLC预后不良相关[2]。Datopotamab deruxtecan(Dato-DXd/DS-1062)是TROP2 ADC的代表药物之一,目前在NSCLC临床布局最为丰富。TROPION-PanTumor01研究提示,Dato-DXd单药治疗对标准治疗无应答或治疗后复发的晚期NSCLC患者ORR为26%,展现出有希望的抗肿瘤疗效[3]。
在2023年10月23日的ESMO年会上,来自 Dato-DXd 的首个 III 期临床项目 TROPION-Lung01研究重磅亮相,这是近年来ADC药物在经靶向/免疫及化疗治疗后进展的NSCLC患者中首个且唯一取得阳性结果的III期临床研究。该研究入组人群更广泛,同时纳入了经靶向/免疫和化疗治疗进展的患者。
TROPION-Lung01研究[4]是一项全球性、随机、多中心、开放标签的III期临床试验(图1),旨在评估Dato-DXd对比多西他赛在既往至少接受过一次治疗、伴或不伴有可靶向基因组改变(AGA)的局部晚期或转移性NSCLC患者的有效性和安全性。AGA患者既往接受过针对EGFR、ALK、ROS1、NTRK、BRAF、METex14或RET的1-2线经批准的靶向治疗和含铂化疗,接受过不超过一次的免疫治疗。无AGA患者既往接受过1-2线含铂化疗和免疫治疗。主要研究终点为经盲态独立中心审查(BICR)评估的无进展生存期(PFS)和总生存期(OS),次要研究终点包括客观缓解率(ORR)、缓解持续时间(DOR)和安全性。
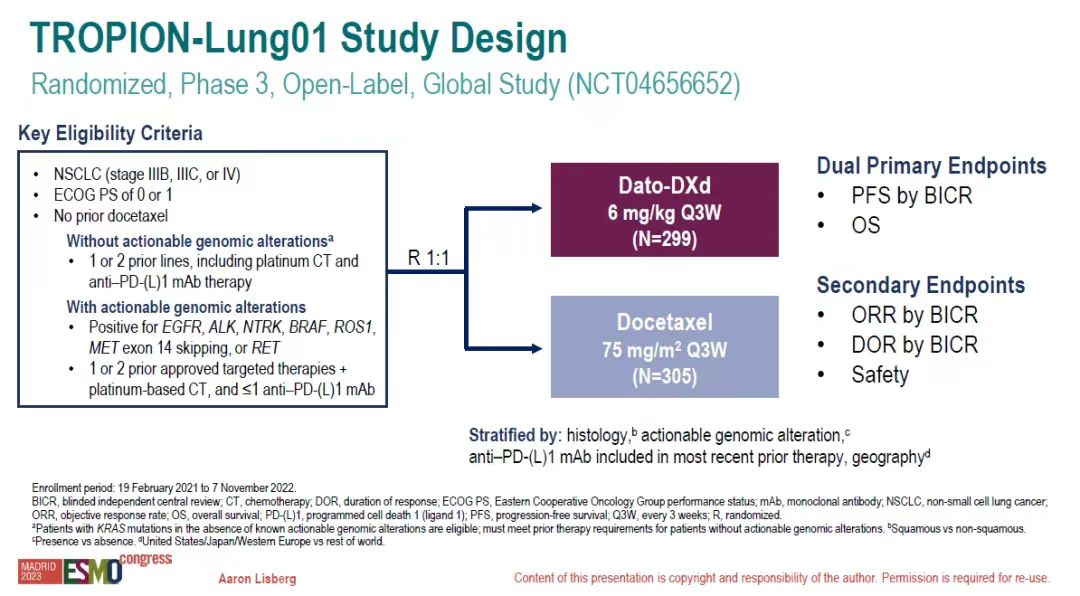 图1 TROPION-Lung01研究设计
图1 TROPION-Lung01研究设计
数据分析截至2023年3月29日,Dato-DXd组和多西他赛组纳入了经靶向和免疫治疗进展后的患者,入组人群广泛。基线特征显示,Dato-DXd组和多西他赛组患者分别有43%和42%既往接受过≥2线全身治疗;非鳞NSCLC(nsq-NSCLC)患者占比分别为78%和77%;两组患者均有17%携带AGA。组间患者基线特征基本一致。
研究结果显示,在意向治疗人群(ITT)中,Dato-DXd对比多西他赛在全人群中显示出有统计学意义的PFS获益(BICR评估的mPFS分别为4.4个月 vs 3.7个月),Dato-DXd组疾病进展或死亡风险降低25%,HR=0.75(95%Cl 0.62-0.91;P=0.004)(图2)。Dato-DXd组ORR为26.4%,而多西他赛组仅12.8%。两组DOR分别为7.1个月和5.6个月。
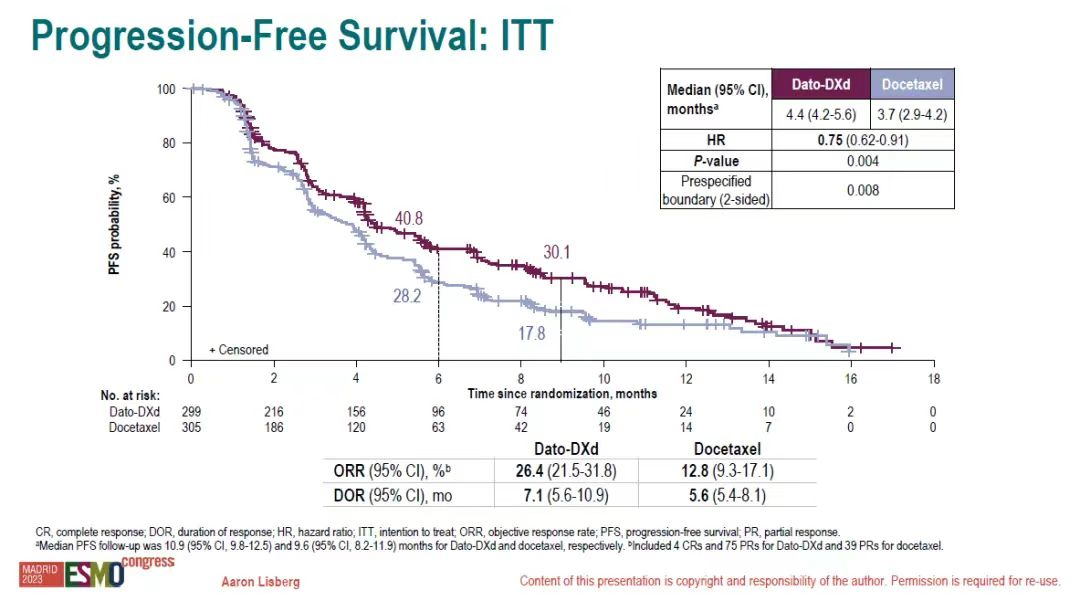 图2 TROPION-Lung01研究ITT人群PFS结果
图2 TROPION-Lung01研究ITT人群PFS结果
在预先指定的非鳞癌亚组中,患者PFS获益更佳,Dato-DXd组mPFS延长近2个月(5.6个月 vs. 3.7个月),疾病进展或死亡风险降低37%(HR=0.63;95% CI 0.51-0.78)。OS数据尚不成熟。Dato-DXd组与多西他赛的中位治疗持续时间分别为4.2个月和2.8个月。安全性方面,Dato-DXd≥3级治疗相关不良反应(TRAEs)为25%,远低于多西他赛组的41%(图3)。最常见的任何级别TRAEs包括口腔炎(47%)和恶心(34%),多数为1-2级,且未观察到新的安全性信号。Dato-DXd组药物相关间质性肺病(ILD)发生率为8%,但大多数为1-2级,整体安全性可耐受。
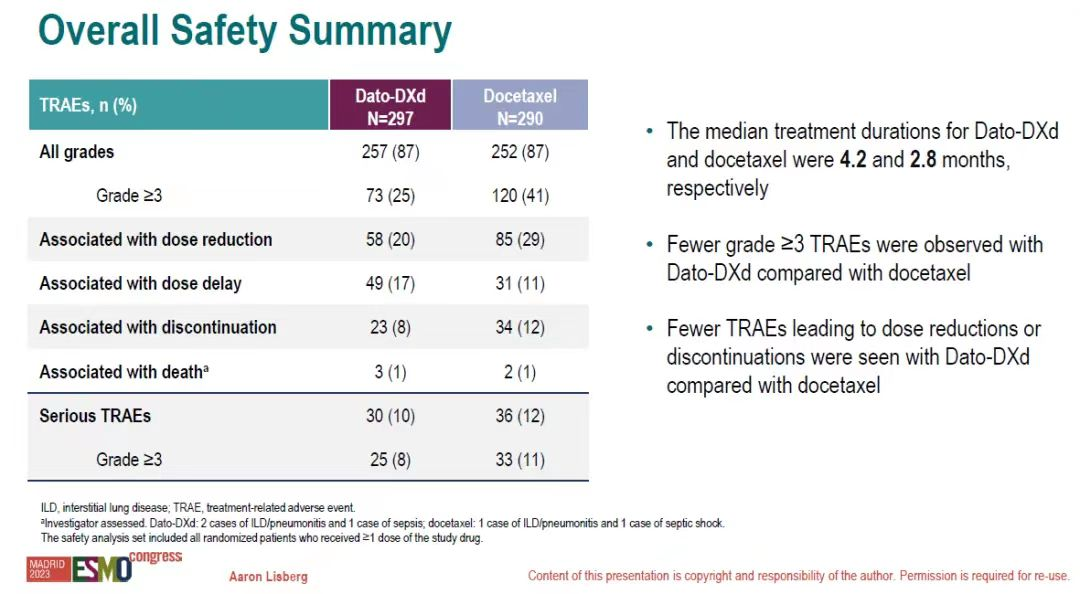 图3 TROPION-Lung01研究安全性结果
图3 TROPION-Lung01研究安全性结果
TROPION-Lung01研究可以看到,Dato-DXd单药对比化疗治疗既往接受过免疫治疗的NSCLC后线人群中取得了鼓舞人心的疗效,为这类患者提供了传统化疗手段之外的新选择。
一线布局,Dato-DXd领跑NSCLC领域ADC临床研发
Dato-DXd率先通过III期研究证实其单药在晚期经治NSCLC患者中的疗效,一系列临床前研究证明,Dato-DXd与免疫治疗联合具有机制协同作用,可促进免疫应答,或产生更强的抗肿瘤活性[5]。目前数项早期临床研究包括TROPION-Lung02以及TROPION-Lung04研究已在Dato-DXd联合免疫治疗NSCLC患者中表现了有潜力的结果,为后续开展更大样本量的试验打下了坚实的基础。
TROPION-Lung02研究是首个评估Dato-DXd联合免疫和(或)化疗治疗NSCLC患者的临床研究[6]。这是一项全球性、开放性、六队列Ib期研究,旨在评价两种给药剂量(4mg/kg和6mg/kg)的Dato-DXd与帕博利珠单抗(200 mg)联合治疗伴或不伴四个周期的铂类化疗(卡铂或顺铂)在初治或经治晚期或转移性NSCLC患者中的安全性和疗效。结果显示,Dato-DXd+帕博利珠单抗±化疗在1L及2L+NSCLC患者中具有良好的疗效和安全性,Dato-DXd+帕博利珠单抗(双联组)ORR为38%,三联组ORR(Dato-DXd+帕博利珠单抗+化疗)为49%。两组疾病控制率(DCR)分别为84%和87%。亚组分析显示,一线治疗人群的疗效更为突出,双联组的ORR为50%,三联组的ORR为57%,两组的DCR均为91%。Dato-DXd双联和三联方案均显示出了可耐受的安全性,且未发生新的安全性信号。
TROPION-Lung02研究结果证实和支持了Dato-DXd联合帕博利珠单抗伴或不伴铂类化疗的疗效和可耐受的安全性,凸显了Dato-DXd联合免疫治疗方案在晚期NSCLC一线治疗中的价值。目前,Dato-DXd联合免疫治疗对比标准治疗(SOC)在晚期NSCLC一线治疗中的两项关键研究TROPION-Lung07、TROPION-Lung08已在中国启动,挑战NSCLC治疗一线标准治疗方案(图4)。
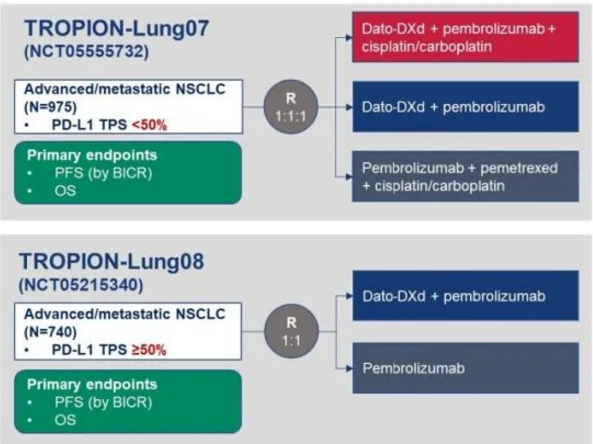 图4 TROPION-Lung07以及TROPION-Lung 08研究设计
图4 TROPION-Lung07以及TROPION-Lung 08研究设计
另一项在无AGA的NSCLC患者中探索Dato-DXd更优联合治疗模式的研究TROPION-Lung04正在进行中。TROPION-Lung04是一项多中心、开放标签的Ib临床试验,旨在探索Dato-DXd与免疫检查点抑制剂联合治疗NSCLC的应用前景。在今年的WCLC大会上首次公布了队列2和4的数据[7],纳入了初治或放疗后出现进展或既往接受过一线化疗且未使用过免疫治疗的晚期/转移性NSCLC患者,这些患者接受了Dato-DXd+度伐利尤单抗±卡铂的治疗。该研究主要终点为剂量限制性毒性(DLTs)、治疗期间不良事件(TEAEs)等;次要终点包括ORR、DOR、DCR、PFS、OS等(图5)。
 图5 TROPION-Lung04研究设计
图5 TROPION-Lung04研究设计
结果显示,在初治患者中(1L),队列2双联组(Dato-DXd+度伐利尤单抗)ORR为50.0%,DCR为92.9%,队列4三联组(Dato-DXd+度伐利尤单抗+化疗)ORR为76.9%,DCR为92.3%;在总人群中(1L/2L+),双联组ORR为47.4%,三联组ORR为71.4%。三联组的ORR获益整体上高于双联组,并且在所有PD-L1表达水平的患者中均观察到缓解。常见TEAEs为便秘、口腔炎、脱发、恶心和贫血等,未发生与治疗相关的死亡事件,未发现新的安全信号。
TROPION-Lung04研究公布的结果证明,Dato-DXd+度伐利尤单抗±卡铂在晚期NSCLC,尤其是一线治疗中表现出可控的安全性和可期待的抗肿瘤活性,也与TROPION-Lung02研究的结果互相印证。因此非常期待探索Dato-DXd联合度伐利尤单抗的III期AVANZAR研究。
未来已来,AVANZAR研究值得期待
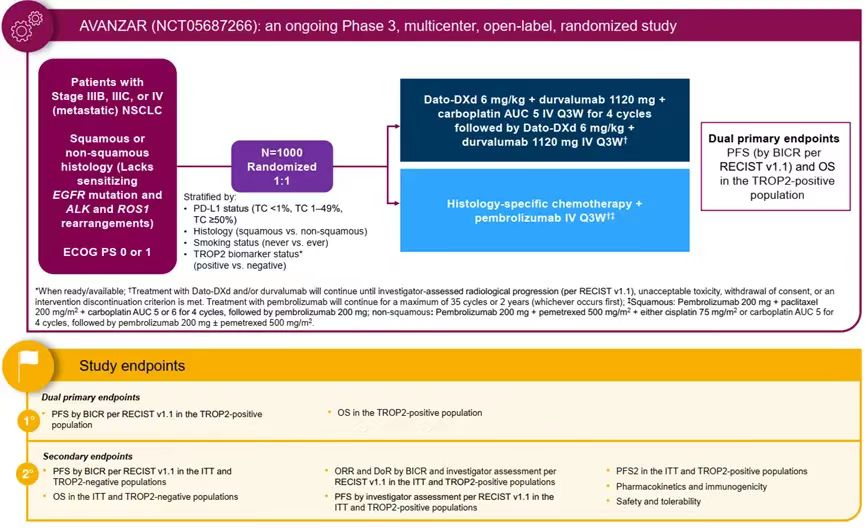
AVANZAR(NCT05687266)是一项III期、随机、开放标签、国际多中心研究[8],拟入组1000例初治的鳞状或非鳞状(EGFR敏感突变/ALK融合/ROS1融合阴性、无其他已知肿瘤基因组改变包括NTRK/BRAF/RET/MET、无其他已获批靶向疗法的AGA)的局部晚期/转移性NSCLC患者,1:1随机分配至Dato-DXd+度伐利尤单抗+化疗组或帕博利珠单抗联合化疗组。其中,治疗组给药方式为前4个周期IV输注Dato-DXd(6.0 mg/kg)+度伐利尤单抗(1120 mg)+卡铂(AUC 5),Q3W,随后Dato-DXd+度伐利尤单抗维持治疗;对照组化疗方案根据组织学分型选择的化疗方案与帕博利珠单抗的联合治疗。主要终点是BICR评估的TROP2阳性人群的PFS和OS。次要终点包括ITT人群中TROP2阴性患者的PFS和OS;ITT人群中TROP2阳性患者的PFS、PFS2、ORR和DOR,药代动力学和免疫原性,安全性和耐受性。研究目前正在进行中,期待未来结果的更新报道。
作为AVANZAR研究的中国主要研究者,非常欣喜的看到Dato-DXd如此丰富的临床证据以及全面的临床布局。TROPION-Lung01研究证实Dato-DXd为NSCLC后线治疗患者带来了超越经典多西他赛的治疗选择,未来可能改变NSCLC尤其是非鳞NSCLC后线治疗格局。期待未来TROPION-Lung07、TROPION-Lung08以及AVANZAR研究结果公布,为NSCLC一线治疗带来更多希望。
排版编辑:肿瘤资讯-olivia
[1] Majeed U, et al. J Hematol Oncol. 2021;14(1):108.
[2]Mito R, et al. Pathol Int. 2020;70(5):287-294.
[3]Shimizu T, et al. J Clin Oncol. 2023 Oct 10;41(29):4678-4687.
[4]Ahn M-J, et al. ESMO Congress 2023, LBA12.
[5]Drago JZ, et al. Nat Rev Clin Oncol. 2021 Jun;18(6):327-344.
[6]Goto Y, et al.2023 ASCO. 9004.
[7]Papadopoulos KP, et al. 2023 WCLC. OA05.06.
[8]Aggarwal C , et al.2023 WCLC.P2.04-02











 苏公网安备32059002004080号
苏公网安备32059002004080号


