Datopotamab deruxtecan(Dato-DXd)是一种新型的靶向TROP2的抗体-药物偶联物(ADC),正在多种肿瘤类型中进行临床研究。2023 ESMO大会上,Dato-DXd在乳腺癌和肺癌领域共有2项Ⅲ研究和2项Ⅱ期报道结果,其中Ⅲ期的TROPION-Breast01和 TROPION-Lung01入选重磅的LBA,Ⅱ期的BEGONIA和TROPION-Lung05入选Mini Oral。

乳腺癌
TROPION-Breast01:Dato-DXd vs 化疗用于经治的不可切除/转移性HR+/HER2-乳腺癌,双终点之一PFS达到
研究分期:Ⅲ期
摘要号:LBA11
Datopotamab deruxtecan (Dato-DXd) vs chemotherapy in previously-treated inoperable or metastatic hormone receptor-positive, HER2-negative (HR+/HER2e) breast cancer (BC): Primary results from the randomised phase III TROPION-Breast01 trial
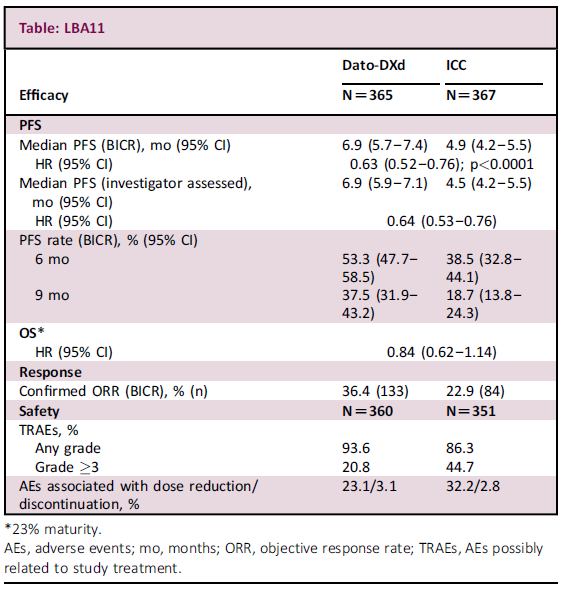
TROPION-Breast01是全球性的Ⅲ期临床试验,纳入不可手术/转移性HR+/HER2-乳腺癌患者,患者在既往的内分泌治疗期间发生进展或内分泌治疗不适用,且既往接受过1~2线全身化疗。入组患者按1∶1随机接受Dato-DXd或研究者选择的化疗(ICC)直至疾病进展或出现不可接受的毒性。设双主要终点:盲法独立中心评审(BICR)评估的无进展生存期(PFS)和总生存期(OS)。
共733例患者被随机分组:Dato-DXd组365例,ICC组367例。数据截止到2023年7月17日的结果显示,Dato-DXd较ICC显著改善PFS(HR=0.63,P<0.0001),PFS的改善兼具统计学和临床意义。OS数据尚不成熟,但观察到Dato-DXd组有改善的趋势。Dato-DXd的安全性也更好,Dato-DXd组较ICC组发生≥3级治疗相关不良事件(TRAE)的比例以及药物减量的比例更低。结果支持Dato-DXd作为既往接受过1~2线化疗的不可手术或转移性HR+/HER 2-乳腺癌患者的新型治疗选择。
BEGONIA:Dato-DXd +度伐利尤单抗一线治疗不可切除局部晚期/转移性三阴性乳腺癌,缓解率高且缓解持久
研究分期:Ⅱ期
摘要号:379MO
Datopotamab deruxtecan (Dato-DXd) + durvalumab (D) as first-line (1L) treatment for unresectable locally advanced/metastatic triple-negative breast cancer (a/mTNBC): Updated results from BEGONIA, a phase Ib/II study
BEGONIA是一项正在进行中的Ⅱ期、开放标签的平台研究,在局部晚期/转移性三阴性乳腺癌(TNBC)的一线治疗中评价在PD-L1抑制剂度伐利尤单抗(D)的基础上加用新型疗法(包括Dato-DXd)的安全性和疗效。主要终点是安全性和耐受性,次要终点包括研究者评估的客观缓解率(ORR)、PFS和缓解持续时间(DOR)。BEGONIA的第7组采用的是Dato-DXd + D方案,该组的早期数据显示出了有希望的肿瘤缓解结果。本次报告的是包括DOR在内的更新结果。
截至2023年2月2日,共62例患者接受了Dato-DXd + D方案,其中29例仍在治疗中。中位随访时间11.7个月。60%的患者有内脏转移,87%的患者PD-L1低表达(PD-L1高表达定义为表达PD-L1的肿瘤细胞和免疫细胞占肿瘤面积≥10%)。
结果显示,确认的ORR为79%,其中6例(10%)完全缓解,43例(69%)部分缓解。治疗反应与PD-L1表达水平无关。中位DOR为15.5个月。中位PFS为13.8个月。
安全性方面,最常见的不良事件是恶心和口腔炎。未报告新的安全性信号。
总体而言,Dato-DXd + D用于局部晚期/转移性TNBC安全性可管理,缓解率高且缓解持久。
肺癌
TROPION-Lung01:Dato-DXd vs 多西他赛用于经治的晚期/转移性非小细胞肺癌,双终点之一——PFS达到
研究分期:Ⅲ期
摘要号:LBA12
Datopotamab deruxtecan (Dato-DXd) vs docetaxel in previously treated advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC): Results of the randomized phase III study TROPION-Lung01
TROPION-Lung01是一项全球性、开放标签的Ⅲ期随机临床试验,在有/无可靶向基因突变的经治晚期/转移性非小细胞肺癌患者中比较Dato-DXd与多西他赛的疗效和安全性。双主要终点是BICR评估的PFS和OS,次要终点包括客观缓解率(ORR)、缓解持续时间(DOR)和安全性。
共604例患者纳入全分析集(FAS),43.1%既往接受过≥2线治疗。结果显示:Dato-DXd较多西他赛显著改善PFS(HR=0.75,P=0.004),中位PFS分别为4.4个月和3.7个月。两组确认的ORR分别为26.4%和12.8%,中位DOR分别为7.1个月和5.6个月。在预先设定的非鳞亚组中,Dato-DXd较多西他赛的PFS也更长(5.6个月 vs 3.7个月)。
安全性方面,Dato-DXd组最常见的治疗期间不良事件(TEAE)是口腔炎(49.2%,大多为1/2级)和恶心(37%)。判定的≥3级药物相关间质性肺病发生率在Dato-DXd组为3.4%,DTX组为1.4%。与多西他赛组相比,Dato-DXd组≥3级药物相关性TEAE发生率更低,导致剂量降低或停药的AE也更少。
这是TROPION-Lung01首次报告结果。

TROPION-Lung05:Dato-DXd用于有可靶向基因变异的经治非小细胞肺癌
研究分期:Ⅱ期
摘要号:1314MO
TROPION-Lung05: Datopotamab deruxtecan (Dato-DXd) in previously treated non-small cell lung cancer (NSCLC) with actionable genomic alterations (AGAs)
TROPION-Lung05是一项全球性、开放标签的Ⅱ期研究,评价Dato-DXd在伴有可靶向基因变异的(AGA)、经≥1种AGA特异性治疗后进展的局部晚期/转移性非小细胞肺癌患者中的应用。
入组的患者体力状态较好,ECOG评分0或1分。EGFR、ALK、ROS1、NTRK、BRAF、MET外显子14跳跃或RET这些基因中有≥1个AGA。主要终点为BICR确认的ORR(cORR)。次要终点包括BICR评估的DOR和疾病控制率,以及安全性。
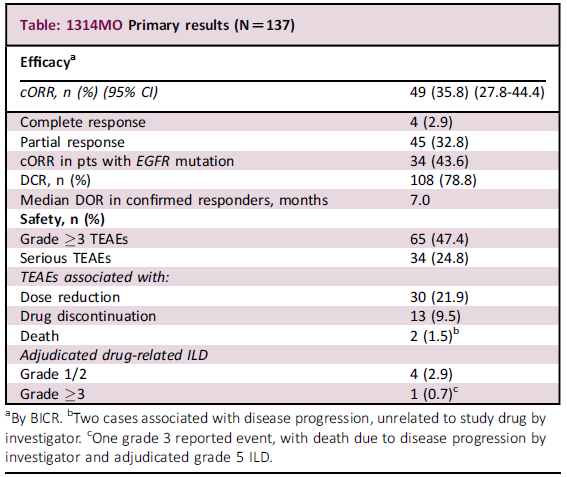
共137例患者接受了至少1剂Dato-DXd。71.5%的患者既往接受过≥3线治疗,56.9%有EGFR突变。截至2022年12月14日的数据显示,cORR为35.8%,DCR为78.8%,中位DOR 7.0个月。EGFR突变患者的cORR为43.6%。
最常见的≥3级TEAE为口腔炎、贫血和淀粉酶升高。
以上结果表明,Dato-DXd用于接受过大量治疗的AGA非小细胞肺癌患者抗肿瘤活性令人鼓舞,缓解时间持久,安全性可管理。
此外,本届大会上,Dato-DXd还有一项尚在进行中的研究Ⅲ期研究TROPION-Lung07报道了方案设计(摘要号:1505TiP)。这是一项全球性的、开放标签、Ⅲ期随机研究,探讨Dato-DXd+帕博利珠单抗±铂类 vs 培美曲塞+帕博利珠单抗+铂类一线治疗无AGA、PD-L1表达<50%晚期/转移性非鳞非小细胞肺癌,计划入组975例患者。期待该研究的结果。
排版编辑:Linda












 苏公网安备32059002004080号
苏公网安备32059002004080号


