开疆拓土:免疫疗法开启肺癌治疗新时代
肺癌的发病率与死亡率在各种恶性肿瘤中位居榜首,对全球人民的生命健康造成了巨大威胁。其中,非小细胞肺癌(NSCLC)约占肺癌总数的80%~85%。自20世纪90年代以来,以铂类为基础的化疗在NSCLC中确立了重要地位,配合手术及放射治疗,能够延缓患者疾病复发与进展,为患者带来更长生存。随着对肺癌分子生物学特征的进一步了解,针对多种特定突变的精准疗法开花结果。自第一代靶向表皮生长因子受体(EGFR)的酪氨酸激酶抑制剂(TKI)问世以来,靶向治疗已成为临床晚期肺癌的标准治疗方案。步入精准治疗时代后,肿瘤治疗有效率大幅提高,同时治疗相关毒副反应减少,大大改善了患者生存及生活质量。然而,对于突变阴性NSCLC人群,仍然亟需更好的治疗方式。
1992年,免疫学家本庶佑教授发现了PD-1蛋白,并证明PD-1具有免疫抑制功能,PD-1/PD-L1随即被开发用于肿瘤的免疫治疗。1996年,Allison证实用抗CTLA-4阻断可使肿瘤缩小,2011年,伊匹木单抗成为全球首个获批的免疫检查点抑制剂。2014年,纳武利尤单抗在日本获批,成为全球首个上市的PD-1抑制剂。2015年4月,纳武利尤单抗获美国FDA批准,成为全球首个获批NSCLC适应症的药物。自此,免疫治疗彻底改变了肺癌乃至其他恶性肿瘤的治疗方式,是人类肿瘤治疗发展史上的一个重大突破。随着免疫治疗的蓬勃发展,Allison教授和本庶佑教授也因此获得2018年的诺贝尔生理学和医学奖。
通幽洞微:探究早期肿瘤微环境,免疫治疗可带来更多获益
免疫治疗在晚期肺癌中发展得如火如荼的同时,也在逐渐向更早期探索。对于可手术的非转移性肺癌患者,根治性手术是潜在治愈性手段和首选治疗方法。但即使进行根治性手术,IB-IIIB期患者5年生存率仅68%~26%,即使是I~II期NSCLC患者,接受根治术后早期复发风险也较高[1,2]。既往研究表明,传统新辅助或辅助化疗对患者总生存期(OS)影响有限,5年OS率仅提升5%左右[3],因此,接受手术治疗的NSCLC患者依然存在较大未被满足的治疗需求。
在肿瘤发生的早期阶段,T细胞通过分泌Th-1细胞因子(IFN-γ、IL-2和IL-12)、募集NK细胞以及抗原特异性CTLs清除免疫原性肿瘤细胞。随着肿瘤进展,肿瘤细胞发生免疫逃逸。这些逃逸肿瘤细胞通过多种机制诱导调节性CD4+T细胞(Tregs)的募集,从而对抗抗肿瘤免疫细胞,Tregs高浸润的肿瘤患者预后较差[4]。因此,早期的肿瘤微环境对免疫治疗更为有利。近年来,对可手术NSCLC患者进行免疫新辅助治疗成为肺癌治疗的热点话题。有别于传统治疗模式,免疫新辅助治疗由于术前抗原的存在、完整的淋巴系统,以及患者良好的身体状态,能够更好地激活抗肿瘤免疫活性、控制远处微转移,从而延缓疾病复发。
三登顶刊:纳武利尤单抗在新辅助免疫治疗领域强势开局
CheckMate-159研究是纳武利尤单抗在新辅助治疗领域带来的开篇之作,于2018年发表于The New England Journal of Medicine。研究纳入21例Ⅰ-ⅢA期NSCLC患者,术前接受2个周期的纳武利尤单抗单药新辅助治疗。研究结果显示,纳武利尤单抗单药治疗达到45%的主要病理学缓解(MPR)(图1)[5]。作为全球首个NSCLC新辅助免疫治疗的临床研究,CheckMate-159具有里程碑式意义。
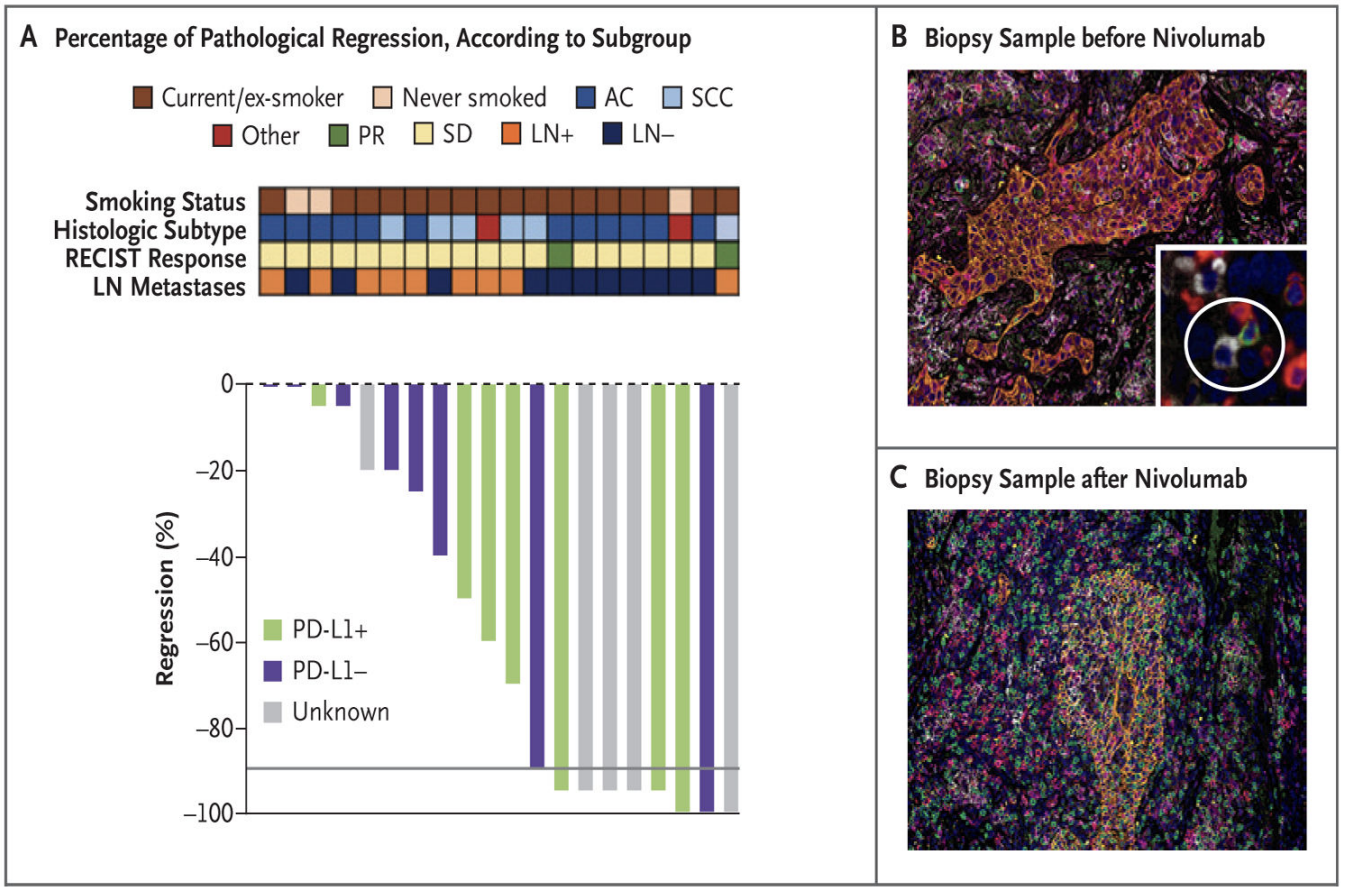
图1. 对PD-1抑制剂新辅助治疗响应的病理学评估
既往研究表明,在化疗诱导免疫原性细胞死亡和抗肿瘤T细胞启动、增强NK细胞介导的细胞毒性以及通过抑制MDSCs减少免疫抑制的基础上,协同免疫治疗恢复抗肿瘤T细胞功能,能够进一步增强疗效[6]。2020年,NADIM研究登上The Lancet Oncology,开启了新辅助免疫联合化疗的治疗探索。NADIM研究是一项开放标签、多中心、单臂II期临床试验,评估了患者接受紫杉醇、卡铂联合纳武利尤单抗用于可切除IIIA期NSCLC患者新辅助治疗的可行性、安全性、抗肿瘤活性和生存结局。研究提示纳武利尤单抗+化疗的新辅助模式疗效或优于免疫单药[7]。2022年,首个大型Ⅲ期CheckMate-816研究结果于The New England Journal of Medicine惊艳亮相。至此,纳武利尤单抗三登顶刊,再次开启了肺癌新辅助免疫治疗之路。
推陈出新:CheckMate-816研究建立NSCLC治疗新标准
作为全球首个免疫新辅助治疗取得阳性结果的多中心III期临床研究,CheckMate-816研究旨在对比术前应用纳武利尤单抗+化疗和单纯化疗的疗效与安全性。研究纳入358例患者,按1:1比例随机分配接受术前纳武利尤单抗(360mg)+化疗(3周期/q3w)或化疗(3周期/q3w)治疗;主要终点为病理学完全缓解(pCR)和无事件生存期(EFS),次要终点为MPR,OS,患者死亡或发生远处转移时间。结果显示,新辅助免疫+化疗组患者pCR率达24%,单纯化疗组仅2.2%(图2);新辅助免疫+化疗组患者中位EFS为31.6个月,单纯化疗组为20.8个月,HR 0.63(图3);研究达到pCR和EFS双终点。初步分析显示OS尚未成熟,新辅助免疫+化疗显示明显获益趋势(HR 0.57,99.67% CI,0.30~1.07)(图4)。在安全性方面,新辅助治疗组和单独化疗组分别有33.5%和36.9%的患者发生3~4级治疗相关不良事件,相较化疗未增加患者严重不良事件发生率[8]。
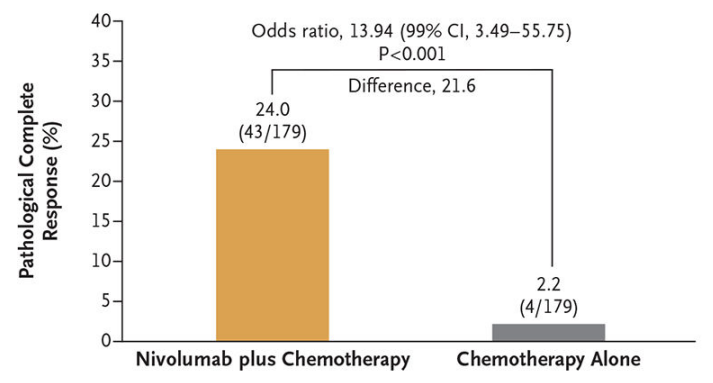
图2. 主要分析人群中的pCR率
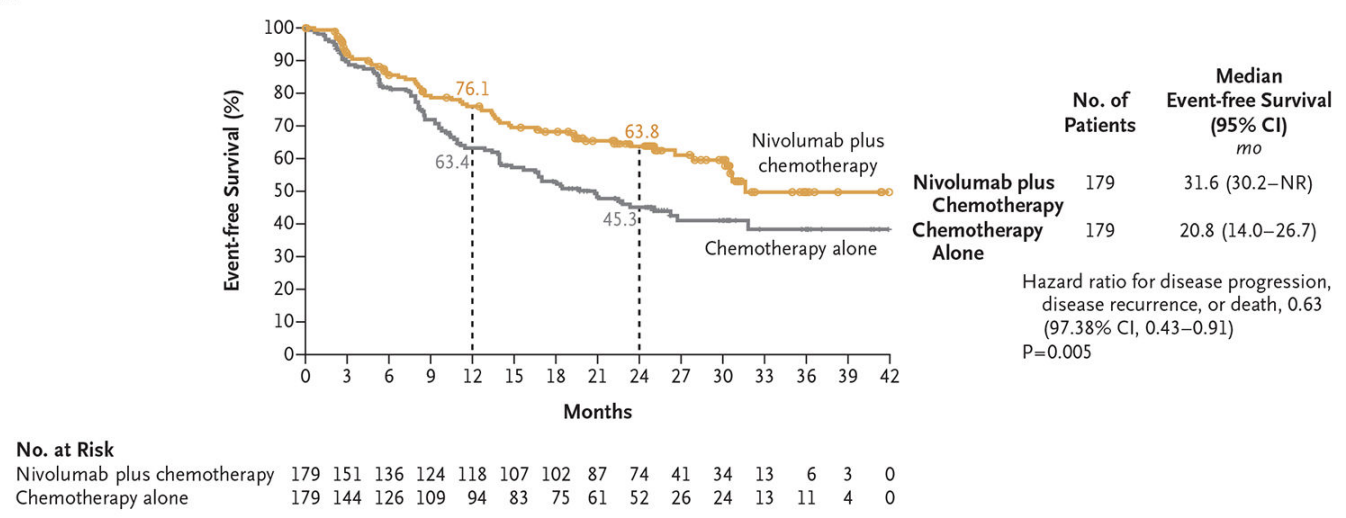
图3. 同时接受随机化患者的EFS
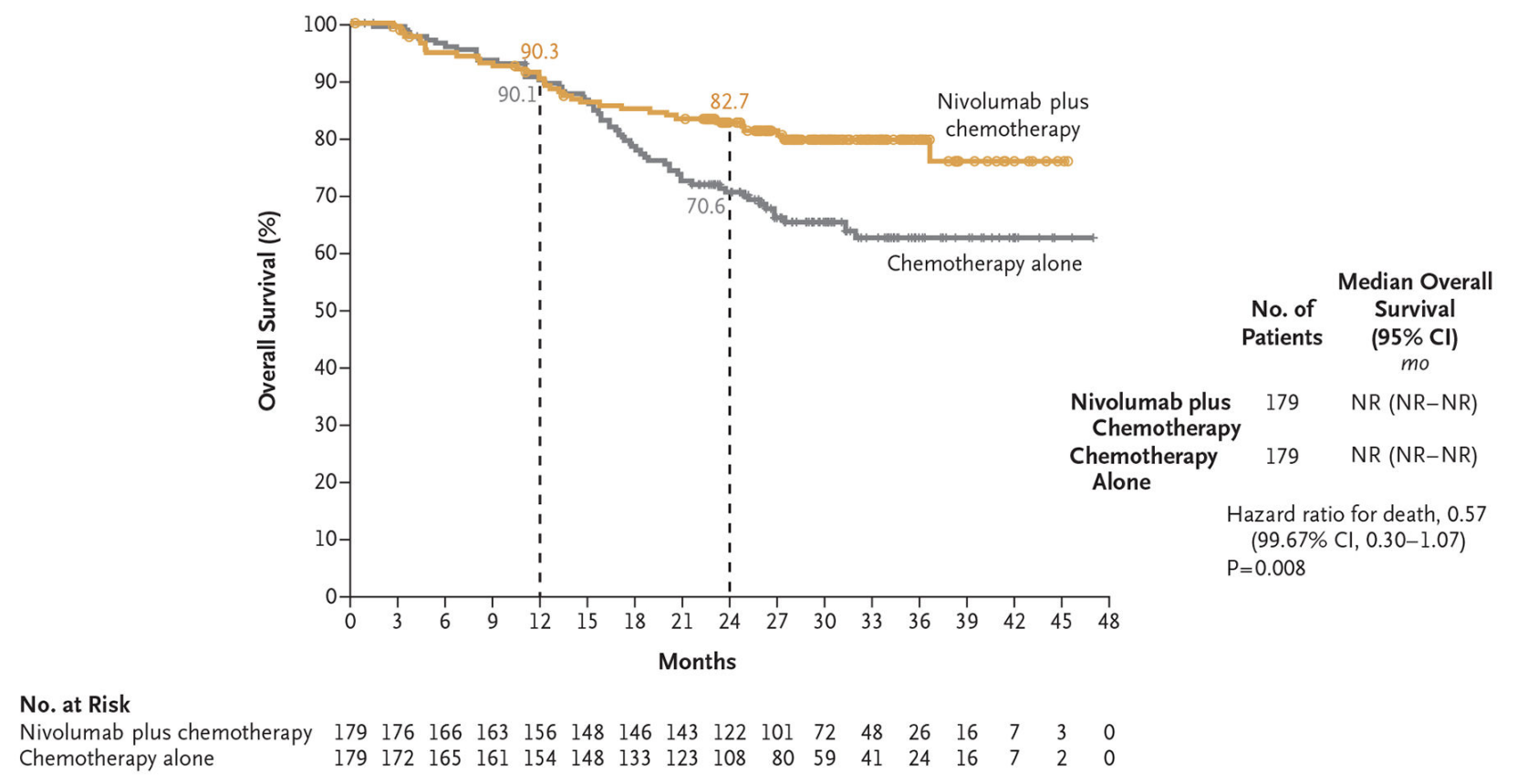
图4. 总生存期
CheckMate-816研究结果一经公布,便建立了可手术NSCLC新辅助治疗新标准:FDA批准纳武利尤单抗+含铂双药化疗用于肿瘤≥4cm或淋巴结阳性的可切除NSCLC新辅助治疗,无论患者PD-L1表达水平如何。2023年,国家药品监督管理局(NMPA)批准纳武利尤单抗+含铂双药化疗用于肿瘤≥4cm或淋巴结阳性的可切除NSCLC新辅助治疗。指南推荐意见纷纷跟进:2023年NCCN NSCLC指南强烈推荐对肿瘤≥4cm或淋巴结阳性且无ICI禁忌证的患者,应考虑纳武利尤单抗+化疗新辅助治疗。同年,CSCO指南也将纳武利尤单抗+化疗新辅助治疗列为I级推荐。可手术NSCLC患者的治疗迎来重大变革,新辅助免疫治疗时代正式展开。
回顾肺癌治疗领域传奇之路,不到十年,从二线到一线治疗,从远处转移到局部晚期再到早期应用,从不可切除到可切除患者,纳武利尤单抗不仅证实了自身在肺癌治疗中的实力,并且引领了免疫治疗的“前移”发展,开创了早期可手术NSCLC治疗全面步入免疫时代的崭新篇章。
1. Lou F, Sima CS, Rusch VW, et al. Differences in patterns of recurrence in early-stage versus locally advanced non-small cell lung cancer. Ann Thorac Surg. 2014 Nov;98(5):1755-60; discussion 1760-1. doi: 10.1016/j.athoracsur.2014.05.070. Epub 2014 Aug 7. PMID: 25110337; PMCID: PMC4256682.
2. Ekeke CN, Mitchell C, Schuchert M, et al. Early Distant Recurrence in Patients With Resected Stage I Lung Cancer: A Case Series of "Blast Metastasis". Clin Lung Cancer. 2021 Jan;22(1):e132-e135. doi: 10.1016/j.cllc.2020.09.002. Epub 2020 Sep 18. PMID: 33144072; PMCID: PMC8669737.
3. NSCLC Meta-analysis Collaborative Group. Preoperative chemotherapy for non-small-cell lung cancer: a systematic review and meta-analysis of individual participant data. Lancet. 2014 May 3;383(9928):1561-71. doi: 10.1016/S0140-6736(13)62159-5. Epub 2014 Feb 25. PMID: 24576776; PMCID: PMC4022989.
4. Gonzalez H, Hagerling C, Werb Z. Roles of the immune system in cancer: from tumor initiation to metastatic progression. Genes Dev. 2018 Oct 1;32(19-20):1267-1284. doi: 10.1101/gad.314617.118. PMID: 30275043; PMCID: PMC6169832.
5. Forde PM, Chaft JE, Smith KN, et al. Neoadjuvant PD-1 Blockade in Resectable Lung Cancer. N Engl J Med. 2018 May 24;378(21):1976-1986. doi: 10.1056/NEJMoa1716078. Epub 2018 Apr 16. Erratum in: N Engl J Med. 2018 Nov 29;379(22):2185. PMID: 29658848; PMCID: PMC6223617.
6. Topalian SL, Taube JM, Pardoll DM. Neoadjuvant checkpoint blockade for cancer immunotherapy. Science. 2020 Jan 31;367(6477):eaax0182. doi: 10.1126/science.aax0182. PMID: 32001626; PMCID: PMC7789854.
7. Provencio M, Nadal E, Insa A, et al. Neoadjuvant chemotherapy and nivolumab in resectable non-small-cell lung cancer (NADIM): an open-label, multicentre, single-arm, phase 2 trial. Lancet Oncol. 2020 Nov;21(11):1413-1422. doi: 10.1016/S1470-2045(20)30453-8. Epub 2020 Sep 24. PMID: 32979984.
8. Forde PM, Spicer J, Lu S, et al; CheckMate 816 Investigators. Neoadjuvant Nivolumab plus Chemotherapy in Resectable Lung Cancer. N Engl J Med. 2022 May 26;386(21):1973-1985. doi: 10.1056/NEJMoa2202170. Epub 2022 Apr 11. PMID: 35403841; PMCID: PMC9844511.
图文:1506-CN-2301145
问答:1506-CN-2301140
排版编辑:肿瘤资讯-Mia











 苏公网安备32059002004080号
苏公网安备32059002004080号


