专家简介
主要学术任职:
国际保肢协会(ISOLS)会员
中华医学会骨科学分会青委会骨肿瘤学组副组长
中国医师协会骨科医师分会青委会骨肿瘤学组委员
中国医药教育协会骨与软组织肿瘤青年委员会副主任委员
CACA肉瘤专业委员会智能骨科与精准诊疗学组组长、基础研究及转化学组副组长
CACA骨肿瘤与骨转移癌专委会青年学组副组长
CACA肉瘤专业委员会委员&脊柱学组委员
CACA骨肿瘤与骨转移瘤专委会药物与精准治疗学组委员
CSCO肉瘤专家委员会委员
CSCO黑色素瘤专家委员会常务委员&青委会副主委
主持并参与北京市自然科学基金、北京市医管中心、北京市科委、首发基金、国家自然科学基金、科技部国家重点研发计划等多项国家及省部级项目;
发表论文106篇,其中第一或通讯作者42篇;
参与专著编写出版14部,参与全国指南编写出版5部;发明专利1项,实用新型专利5项。
骨与软组织肉瘤,尤其骨肉瘤的主要发病人群为儿童与青少年,但其在所有年龄段人群中都有可能发生,目前的主要治疗模式为多学科综合治疗模式,包括外科手术治疗、化学药物治疗、放射治疗、靶向及免疫治疗等。但在面对难治性的复发及转移性肉瘤患者时,目前的治疗手段较难获得良好的预后。ASCO(美国临床肿瘤学会)作为全球最大的肿瘤专业学术组织,每年6月定期召开年会,汇聚了全球临床肿瘤学研究的精英,介绍了各个瘤肿的最新研究及进展,尽管是小瘤肿,骨与软组织肉瘤也被囊括在其中,这为肉瘤的治疗发展提供了极大的帮助。本文旨在盘点2023 ASCO年会中有关肉瘤治疗相关的新进展,其中不乏来自中国的研究之声。
(一)骨源性肿瘤方面
1.骨肉瘤
1.1 骨肉瘤新辅助化疗及辅助化疗已获认可,在围手术期治疗中,除标准的的一线四大药物之外无有潜力的新药出现。中山大学肿瘤中心团队探索了在骨肉瘤新辅助治疗的新方案,将一线化疗与免疫进行组合进行了一项单臂、探索性的2期试验,应用卡瑞利珠单抗联合阿霉素、顺铂、异环磷酰胺以及甲氨蝶呤对75例骨肉瘤患者进行了新辅助治疗,主要研究终点为肿瘤坏死率,次要研究终点OS、PFS及安全性。尽管不如肺癌等其他实体瘤研究中那样,新辅助化疗联合免疫治疗明显增加了患者的病理完全缓解率,骨肉瘤新辅助化疗联合免疫的这项尝试,肿瘤坏死率、2年OS率与既往报道结果相似约48.4%和86.7%,3级及以上AE的发生率为62.3%,多数为化疗所致的AE(45.3%血小板减少,36.0%白细胞减少,30.7%中性粒细胞减少、13.3%口腔黏膜炎,12.0%谷丙转氨酶升高,10.7%谷草转氨酶升高)。在骨肉瘤患者中,如何优选免疫治疗人群和加用免疫治疗的合适时机,仍需要进一步摸索。
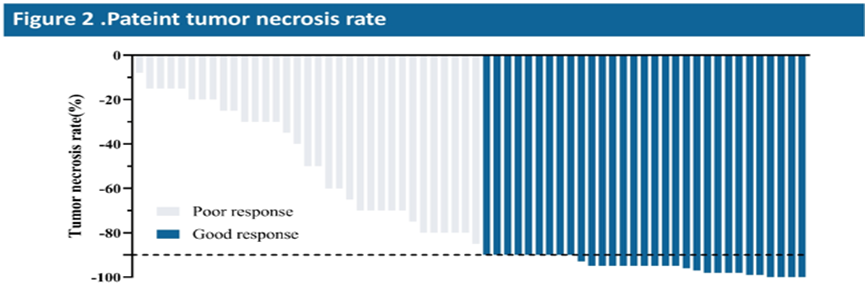
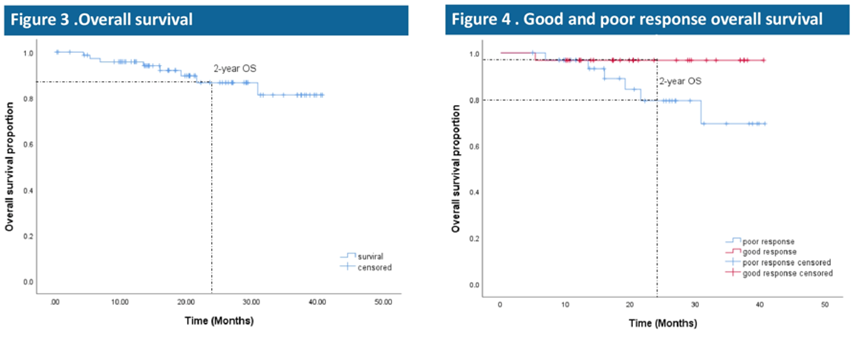
1.2 标准化疗后的转移性或不可切除性骨肉瘤的治疗仍然是一个巨大的临床挑战。此次大会既有对老药IFO新用法的探索,也有对新治疗靶向的尝试。
1.2.1 意大利儿童肿瘤血液学协会的五个中心以及意大利肉瘤小组回顾了14天连续灌注大剂量异环磷酰胺(IFO 1g/m2/day x 14 d,q21d)治疗复发性或难治性高级别骨肉瘤的多中心队列研究,26名患者(约57%患者既往用过IFO)纳入了研究,其中16例患者(61%)经历了至少4个疗程,评估了共101个疗程的毒性,4级血液学毒性报告如下:7%白细胞减少; 8%中性粒细胞减少; 2%血小板减少,未见3-4级非血液学毒性,整组患者的DCR为57.5%,mPFS为4.1个月,mOS为13.7个月。尽管患者数量较少,但与其他治疗相比,14IFO治疗活性并不低,因此可将14IFO作为R/R HOS患者的一个治疗选择,尤其是它良好的可耐受毒性以及提升了患者生活质量的家庭管理,此外还可以显著减少患者的肿瘤护理费用。
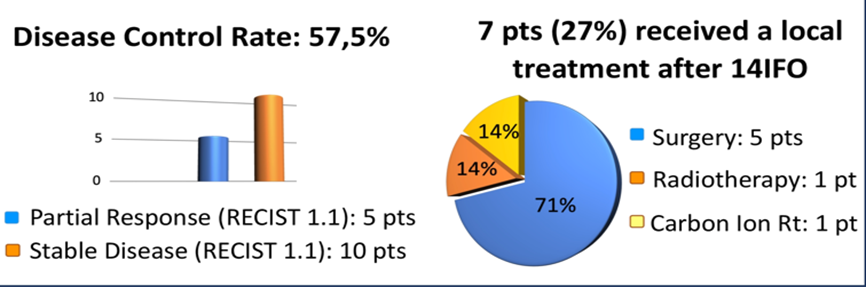
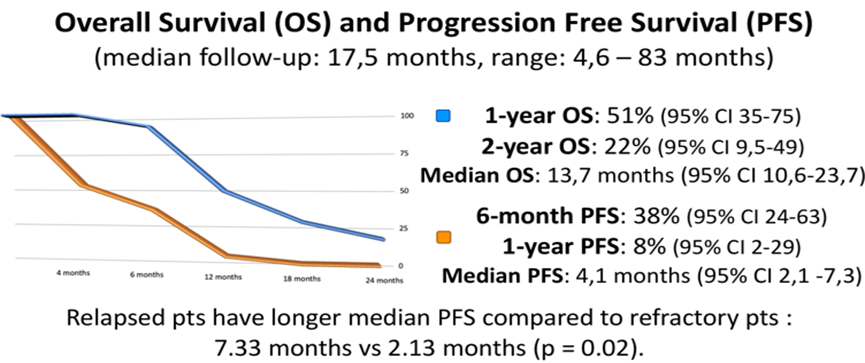
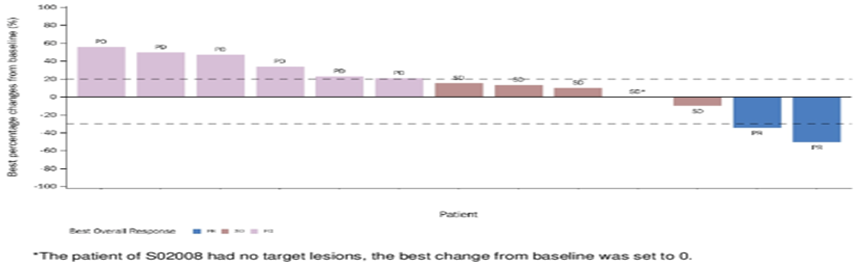
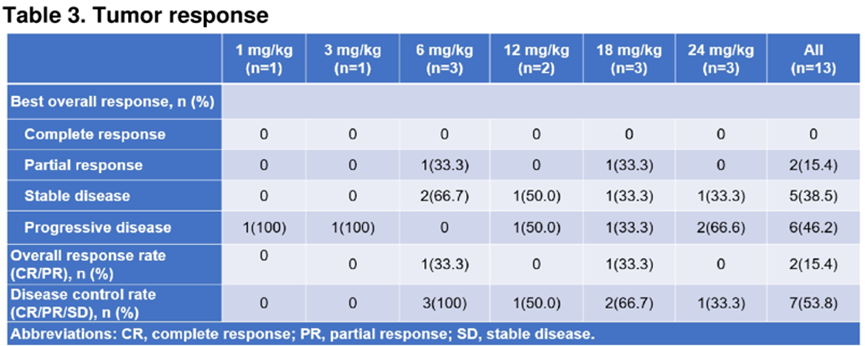
1.2.2 Cx43半通道被认为是骨内环境稳定的一个关键调节因子,ALMB-0168是针对Cx半通道的一线治疗性抗体激动剂,其在临床前研究中已表现出对骨肉瘤细胞的抑制活性。中山大学第一附属医院以及北京大学人民医院联合国内多家医院,针对ALMB-0168治疗标准化疗后转移性或不可切除性骨肉瘤患者进行了一项多中心、开放、单臂I期临床试验,在1期剂量递增试验中提示ALMB-0168在标准化疗后转移性或不可切除骨肉瘤患者中显示出令人鼓舞的疗效和可耐受的安全性,共有13例患者可评估肿瘤治疗反应,ORR为15.4% (2/13,95% CI: 1.9-45.5%), 包括2例PR (6 mg/kg和18 mg/kg各1例);DCR为53.8% (7/13,95% CI: 25.1-80.8%)。没有剂量限制性毒性(DLT)的报告。10例(71.4%)患者发生任何级别的TRAEs, 其中1例(感染性肺炎)为3级;常见>10%TRAEs为:蛋白尿(21.4%)、贫血(21.4%)、血尿(14.3%)和天冬氨酸转氨酶升高(14.3%),未观察到Cx43相关的心脏或严重的肝脏事件。剂量递增和剂量扩展的II期临床研究即将开展。
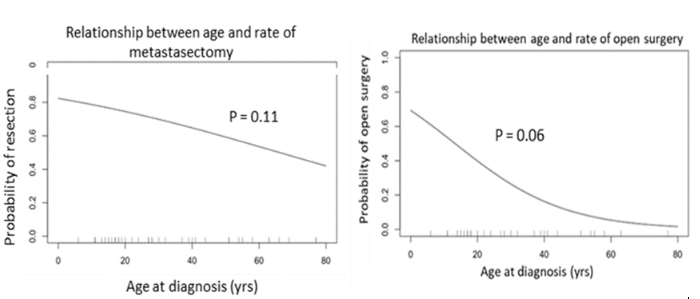
1.2.3 骨肉瘤最常见的转移为肺转移,而肺转移的外科手术干预效果已获多项临床研究证实,但关注儿童和成人骨肉瘤肺转移之间差异的研究并不多,从Victoria A Wytiaz等报道了单中心研究中可以了解到儿童与成年患者的肺转移时间、模式与数量是相似的;在儿童与成人患者中转移灶切除术后的无复发生存期是相似的;但是年轻患者更有可能接受开放手术,但随着年龄的增长,患者接受转移灶切除术的概率也逐渐降低。当然我们需要更大规模的研究去进一步了解患者的治疗选择决定以及治疗的预后。
2. 软骨肉瘤:
软骨肉瘤(cCS)是第二常见的原发性骨肿瘤,85%的CS为经典型,并且对化疗与放疗均存在抵抗性,目前尚无批准的全身治疗方法。免疫和表观遗传学方面治疗在软骨肉瘤中异军突起。
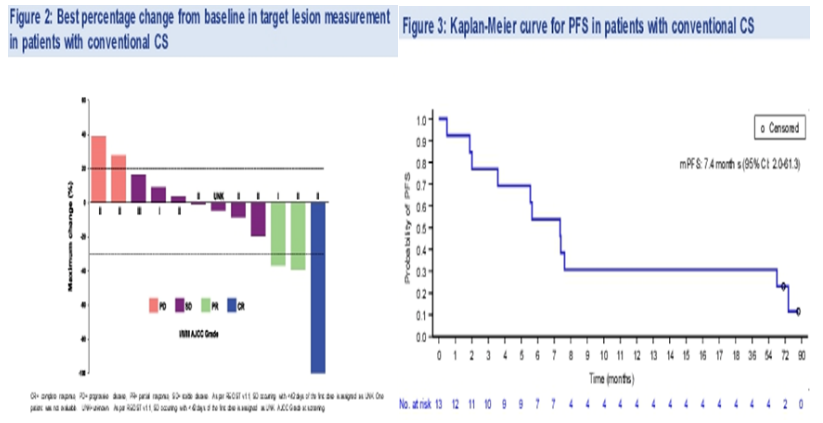
2.1 异柠檬酸脱氢酶1 (IDH1)基因突变发生在约50%的常规CS中。在IDH1突变晚期实体瘤患者的I期研究中,艾伏尼布(IVO),一种口服的IDH1突变抑制剂,显示出可控的毒性(没有剂量限制毒性DLT),在300 mg/天的剂量水平下可以抑制肿瘤代谢物2-羟基戊二酸(2-HG,有致癌性)。一项I期研究提示:突变型IDH1抑制剂艾伏尼布(IVO)用于晚期经典型软骨肉瘤(CS)患者,ORR为23.1%,mPFS为7.4个月,最常见的TEAE(>4例, 大多为1/2级):腹泻(n = 5)和恶心(n = 5)。6名患者经历了≥3级AE,3例患者出现SAEs(与治疗无关),没有因不良反应而停药、减少剂量或死亡的病例。
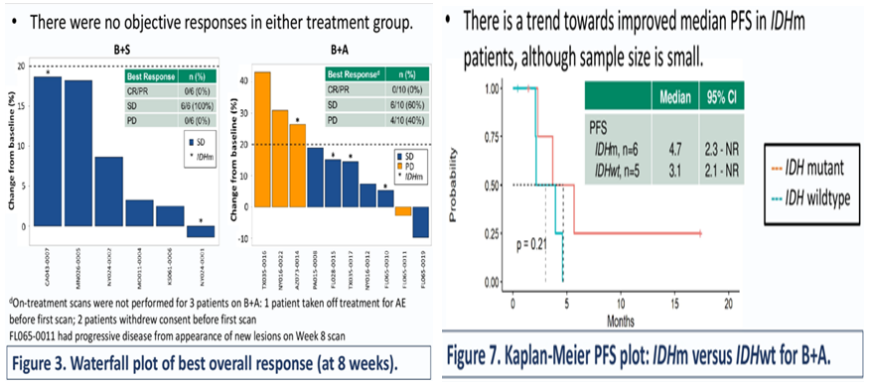
2.2 IDH突变型与野生型的软骨肉瘤都存在表观遗传调节紊乱,在临床前模型中,HDACi(贝利司他)与DNMTi(瓜地西他或地西他滨/西达尿苷)的联合使用,通过逆转超甲基化状态以及诱导肿瘤抑制因子、干扰素反应基因以及细胞凋亡抑制了肿瘤在体内外的生长。Kristine Peregrino Lacuna等人针对贝利司他与SGI-110(瓜地西他钠)或者ASTX727(地西他滨/西达尿苷)联合治疗16例(6例B+S,10例B+A)不可切除性以及转移性常规软骨肉瘤进行了研究分析提示了此种联合治疗耐受性良好,但没有ORR病例,B+S组100%获得了SD的疗效,而B+A组获得了60%的SD,可分析IDH1突变状况的11例患者中,IDH1突变组的中位PFS为4.7月,IDH1野生组的中位PFS为3.1月。软骨肉瘤在IDH基因参与下,是否在表观遗传学治疗通路中能获得突破需进一步深入探讨。
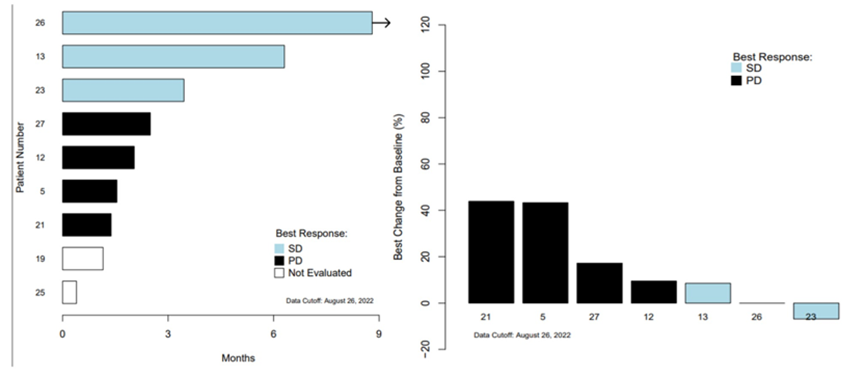
2.3 与低级别软骨肉瘤的惰性相反,去分化亚型(Dcs)具有侵袭性、切除后高复发性以及预后差的特征,约占所有软骨肉瘤的5-10%。PD-L1的表达已经在去分化亚型标本中被证实,并且与大量的肿瘤浸润淋巴细胞有关,均提示晚期去分化软骨肉瘤患者可能是免疫治疗获益人群,但尚未有过对此病种对抗PD1治疗反应的前瞻性评估结果,而今年Mohamad Adham Salkeni等报道了去分化软骨肉瘤患者接受抗PD-L1药物(阿替利珠单抗)治疗的II期临床研究结果,共纳入9例患者,7例患者进行最佳反应评估,没有观察到客观缓解的患者,但可见到3例(42.9%)为SD。该治疗队列因无效而关闭。但1/3的患者中获得疾病稳定,未来在去分化软骨肉瘤患者中的免疫药效学结果,可能至关重要的是在去分化亚型队列中摸索出阿替利珠单抗抵抗性的决定因素以及确定联合治疗的可能搭档。
2.4 INBRX-109 是一种四价死亡受体 5 (DR5) 激动剂抗体,旨在利用 DR5激活引起的肿瘤偏向性细胞死亡。DR5 是肿瘤坏死因子相关凋亡诱导配体 (TRAIL) 的受体。DR5 激活自然地消除了受损和/或肿瘤细胞,而正常细胞对 DR5 介导的细胞死亡不太敏感。目前正在进行INBRX-109治疗晚期或不可切除的软骨肉瘤患者的随机、安慰剂对照的II期研究 (NCT04950075),主要终点是与安慰剂对比,INBRX-109的无进展生存期,对此我们期待该研究的最终结果。
(二)软组织肉瘤方面
软组织肉瘤的进展聚焦在联合治疗上。软组织肉瘤通常被认为是突变负荷低、新抗原相对匮乏的非免疫原性肿瘤,由于大部分STS属于免疫“冷”肿瘤,免疫治疗单药用于肉瘤往往疗效不佳,但免疫联合靶向或者放化疗往往可以协同增效。今年的ASCO也有不少这方面的新进展:
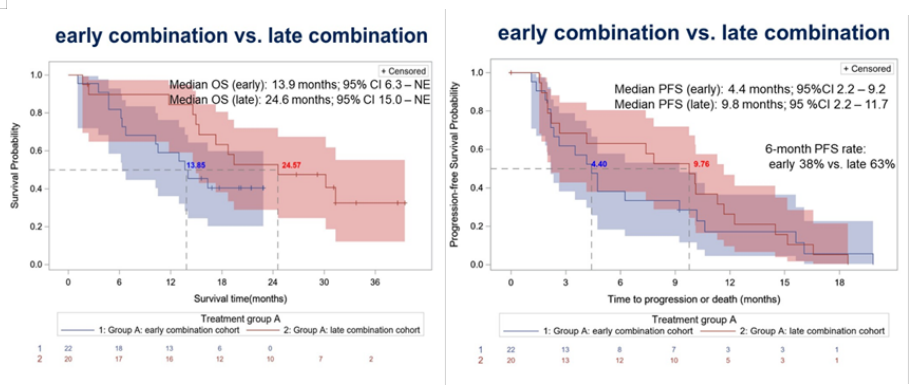
2.1 曲贝替定是国内外常用的L型软组织肉瘤的二线药物,但药物有效性仍有限, Peter Reichardt等人对纳武单抗与曲贝替定联合使用在经预治疗的晚期软组织肉瘤患者中的疗效与安全性进行一项II期临床研究(GISG-15,NitraSarc)。研究对象的准入标准:(1)局限性晚期/不可切除性或者转移性软组织肉瘤;(2)年龄≥18岁;(3)先前接受过≥1项针对肉瘤的全身治疗,包括辅助性全身治疗(蒽环类药物治疗方案)。同时将研究对象分为两组,即Group A(病人必须患有组织学证实的脂肪肉瘤或者平滑肌肉瘤)与Group B(病人必须患有组织学证实的除脂肪肉瘤与平滑肌肉瘤之外的软组织肉瘤)。另外在试验设计过程中,作者将研究对象分为早期联合用药队列(ECC,单药曲贝替定1个周期后联合纳武利尤单抗)与晚期联合用药队列(LCC,在单药曲贝替定3个周期后联合纳武利尤单抗)。研究结果提示:B组mPFS 2.3个月,mOS 5.6个月,A组mPFS 5.5个月,mOS 18.7个月;6个月PFSR6A组PFSR6为47.6% (LCC 60% vs. ECC 36.4%), B组为14.6%;mPFS: A组高于B组(5.5 vs 2.3个月),且A组LCC比ECC的mPFS更长(9.8 vs 4.4个月);mOS: A组比B组的mOS长3倍多(18.7 vs. 5.6个月),LCC比ECC的mOS长(24.6个月比13.9个月)。本研究证实了曲贝替定和纳武利尤单抗联合使用的疗效,特别是在脂肪瘤(LPS)或平滑肌肉瘤(LMS)患者中ECC和LCC在PFSR6、mPFS和mOS方面存在显著差异;而非L型肉瘤患者的结果不能证明进一步研究这种组合的合理性。
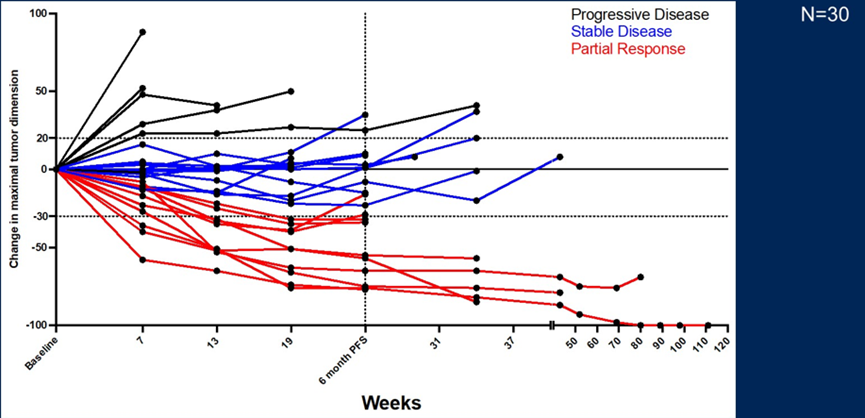
2.2 软组织肉瘤中经典的化疗药物多柔比星(阿霉素)在多个临床前模型中它诱导了免疫原性细胞的死亡,会提升软组织肉瘤的免疫原性,可以增强免疫检查点抑制剂的疗效,今年ASCO上也报道了阿霉素与免疫治疗联合治疗研究结果。Breelyn A等进行了关于阿霉素联合泽福利单抗(CTLA-4抑制剂)、巴替利单抗(PD-1抑制剂)治疗晚期/转移性软组织肉瘤患者的单臂、开放性II期试验。试验结果显示PFS6mo为52%(95%CI 31-72),mPFS为25.6 wks(24.0-44.9),ORR为36%(19-56),DCR为86%(67-96),mDOR为12.8 wks(range 6-105)。与stage 2的病人相比,在stage 1的病人中可以观察到一些治疗结果的提升,包括PFS6mo(56.3%v.25.0%),mPFS(31.7v.25.3 wks),ORR(56%v.8.3%)以及DCR(94%v.75%)。毒性与预期一致,在31个可评估的患者中48%的患者发生了3/4级与治疗相关的不良事件,主要是与阿霉素相关的血液学不良事件,同时在19%的患者中出现了需要类固醇治疗的免疫学相关不良事件。作者得出最终结论,DOX/ZAL/BAL的联合使用产生了有意义的疗效,并且在几个软组织肉瘤的亚型中产生了单用DOX或者ICI不能产生的效果,例如较好的PFS6mo和缓解。另外,一个探索下一代CTLA-4抑制剂Botensilimab与DOX+/-BAL联合使用的队列研究也正在进行中。
2.3 阿霉素联合帕博利珠单抗(PD-1抑制剂)在一项治疗转移性/不可切除性肉瘤患者的1/2期试验中取得了优于历史对照的疗效,mPFS为8.1月;在此基础上加入另一种PD-1抗体(纳武单抗),可能会增强药物的抗肿瘤活性。Javier Martin-Broto等对阿霉素联合达卡巴嗪与纳武单抗作为晚期平滑肌肉瘤的一线治疗进行了1b期试验。经过1期试验,作者称DOX/DAC/NIV的联合使用是一个可行并且耐受性良好的治疗方案,II期试验将进一步开展。
2.4 在不增加毒性的情况下加强化疗以改善治疗结果是一个值得关注的领域。临床前与临床证据表明,同时使用抗血管生成剂与化疗药物会产生协同效应。Midwest Sarcoma Trials Partnership进行了一项关于卡博替尼CAB联合替莫唑胺TMZ治疗不可切除性或转移性平滑肌肉瘤患者以及其他软组织肉瘤患者的多中心II期试验,提示CAB/TMZ的联合使用在治疗不可切除性/转移性平滑肌肉瘤患者时超过了它的主要终点,12周的PFR大于39%。试验中队列1的6.4个月的无进展生存期超过了LMS患者二线治疗方案酪氨酸激酶抑制剂与烷基化剂比率,值得在平滑肌肉瘤的治疗中进一步探索。
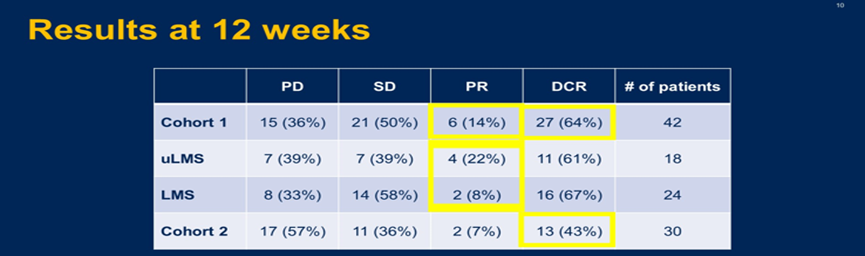
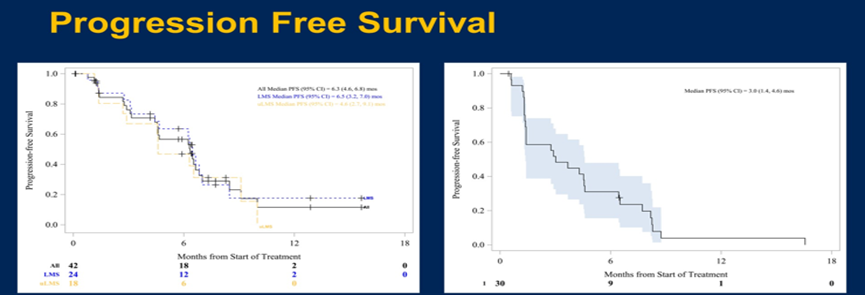
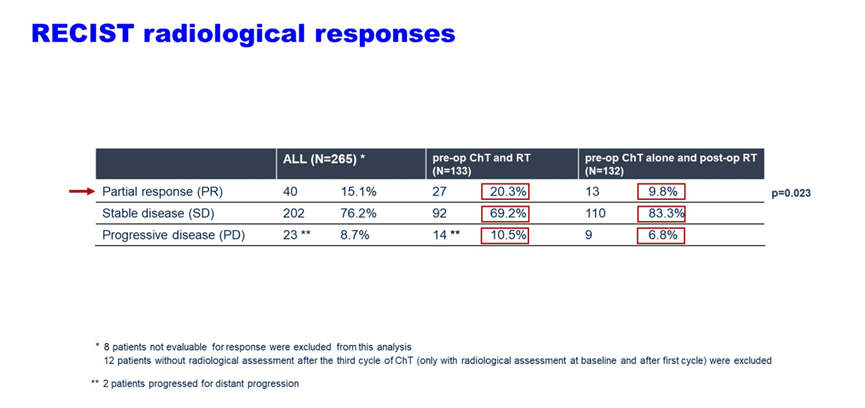
2.5 2023年ASCO也关注了同步放化疗的可行性与疗效。ISG-STS1001是一项关于局部、高风险软组织肉瘤的国际性、随机的3期临床试验,在综合多模式策略的背景下,将表柔比星E与异环磷酰胺I构成的标准新辅助化疗方案与五种组织学类型的组织学定制方案进行比较。与组织学定制方案相比,在总共生存期方面,该试验的最终结果支持EI。在该文中,无论是在试验标准组还是在平行组,还是单独使用新辅助化疗时还是与RT共同使用时,作者都分析了由EI构成的新辅助化疗方案的耐受性与疗效,证实了EI与RT的同时使用是可行且安全的,并且这种组合导致了部分缓解患者的数量增加。根据这项随机试验的最终结果,当肿瘤处于可切除边缘或功能保存成为目标时,这种联合使用可能会有所帮助。
2.6 TTI-621是一个将人类IG-1的Fc区域与SIRPα的一个片段相结合的重组融合蛋白,作为肿瘤细胞上CD47的诱惑性受体它可以阻断CD47-SIRPα的信号传导,并且可以促进巨噬细胞介导的肿瘤细胞吞噬作用以及NK细胞的激活。临床前研究提示TTI-621可能会增强表达CD47且富含巨噬细胞的肿瘤对阿霉素的反应,例如平滑肌肉瘤。Sujana Movva等对TTI-621联合阿霉素治疗不可切除性或转移性高级别平滑肌肉瘤患者的安全临床研究,该文展示了来自低剂量扩展队列的试验结果,在晚期平滑肌肉瘤患者中,包括那些长期暴露于TTI-621的患者,在阿霉素的基础上加入TTI-621表现出了良好的临床活性与安全性,需要进行额外的研究,以证明疗效并进一步评估安全性,以及确定阿霉素的用药周期次数和与抗CD47相关的给药时间。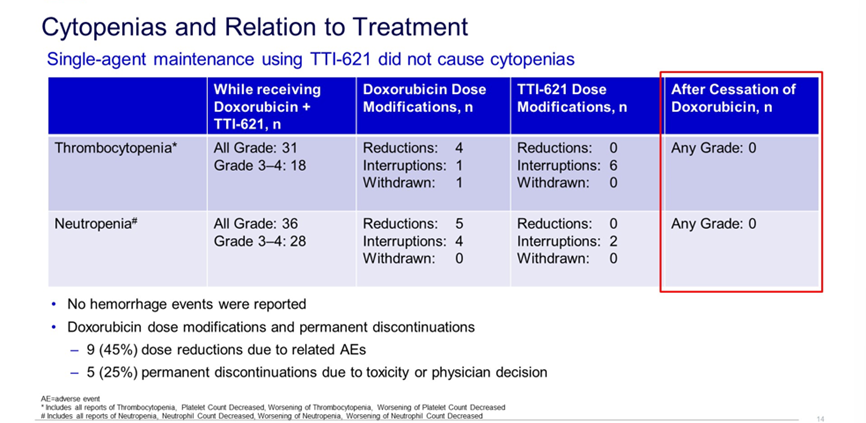
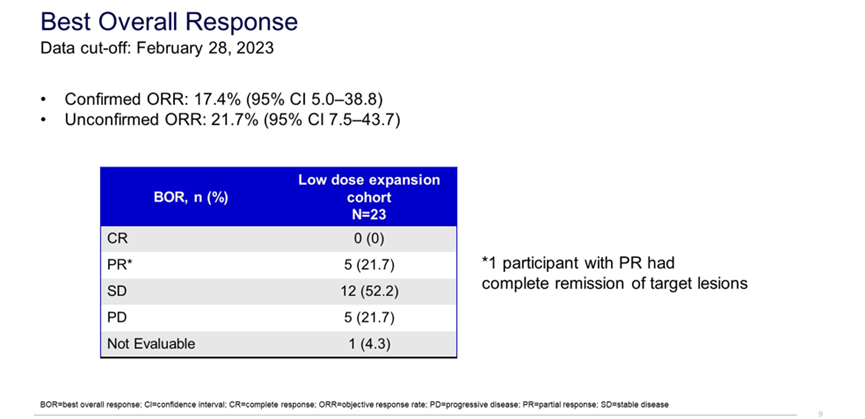
2.7 联合HT-RT与抗PD-L1可能会增强转移性软组织肉瘤患者局部与远处肿瘤的控制。Shane H Zaidi等进行了一项阿维单抗联合低分割胸部放射(HT-RT)治疗转移性软组织肉瘤患者的安全性、耐受性与疗效的1期临床研究,研究没有观察到剂量限制性毒性或者治疗相关的死亡,1年PFS率15%,1年生存率67%,2年生存率53%。在一定程度上显示了阿维单抗联合胸部放射治疗对转移性肉瘤患者是安全的,同时具有较好的抗肿瘤活性,其分子生物标志分析正在进行中。
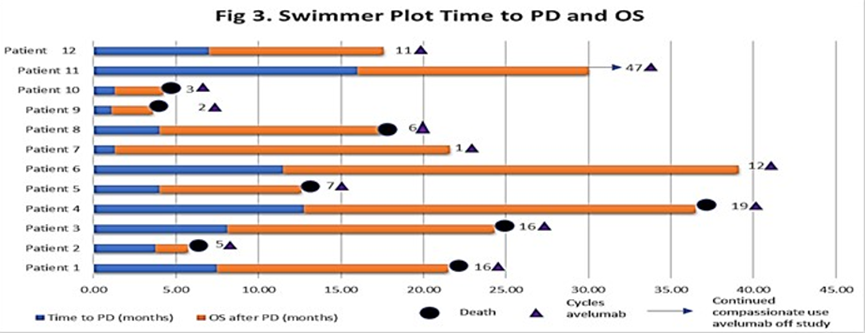
2.8 肉瘤需要新的治疗方案,乐伐替尼是一种口服多酪氨酸激酶抑制剂,它具有抑制VEFGR1-3、FGFR1-3、KIT、PDGFRα/β和RET的显著活性。实验室模型表明乐伐替尼可以有利的改变肿瘤的免疫环境,并且乐伐替尼与帕博利珠单抗的联合使用已经被证明在多个实体瘤类别中具有协同性与有效性。Sujana Movva等进行了一项乐伐替尼联合帕博利珠单抗治疗晚期肉瘤患者(5个队列,A为平滑肌肉瘤,B为未分化多形性肉瘤,C为血管肉瘤和血管内皮瘤,D为滑膜肉瘤和恶性周围神经鞘瘤,E为骨肉瘤和软骨肉瘤)的临床研究,研究结果提示mPFS≥20周,A组ORR为0,SD 60%,中位PFS17.9月,B组ORR 20%,SD 60%,中位PFS 25.3月C组ORR 0%,SD 75%,中位PFS4 0.9月,D组ORR 33.3%,SD 44.4%,中位PFS 32月,E组10%,SD 70%,中位PFS 20.7月。在这项针对骨肉瘤、恶性周围神经鞘瘤、血管肉瘤和滑膜肉瘤患者的初步研究中,乐伐替尼联合帕博利珠单抗具有一定的疗效,但平滑肌肉瘤队列对此联合治疗无反应,PFS较差。
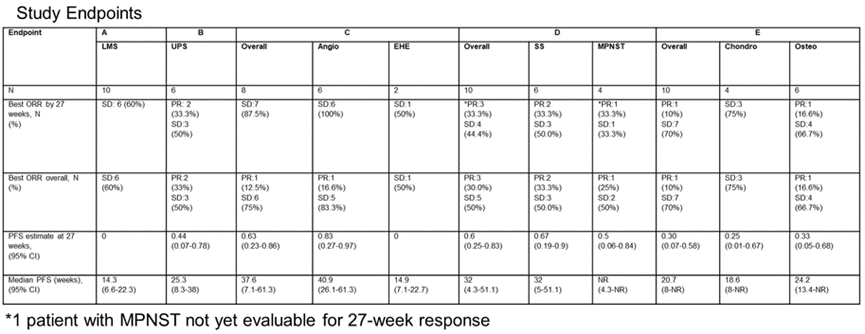
2.9 吉西他滨联合多西他赛(GD)方案是晚期软组织肉瘤较常见的二线治疗方案,在子宫平滑肌肉瘤中甚至可以用于一线化疗。PD-1抑制剂瑞弗利单抗联合GD治疗I期临床研究结果提示其耐受好。Rosenbaum等进行了瑞弗利单抗联合吉西他滨与多西他赛一线治疗晚期软组织肉瘤患者的II期试验,中期结果提示与历史对照相比R+GD显示较好的优势,中位无进展生存期31.3月,24周PFS率66.3%,ORR27.3%,但与单独使用GD相比,该联合用药有着更高的肺炎发病率。主要终点分析需要等待累积完成后才可进行,在最终疗效与安全分析完成之后,该联合用药的未来研究需要去仔细考虑其益处与风险。
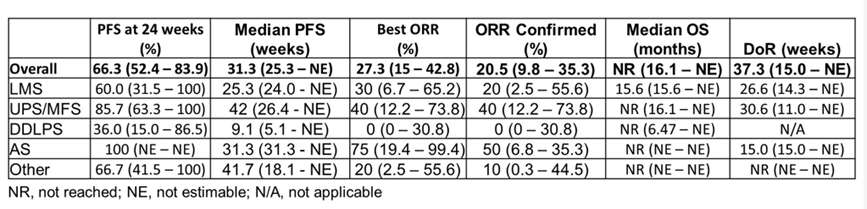
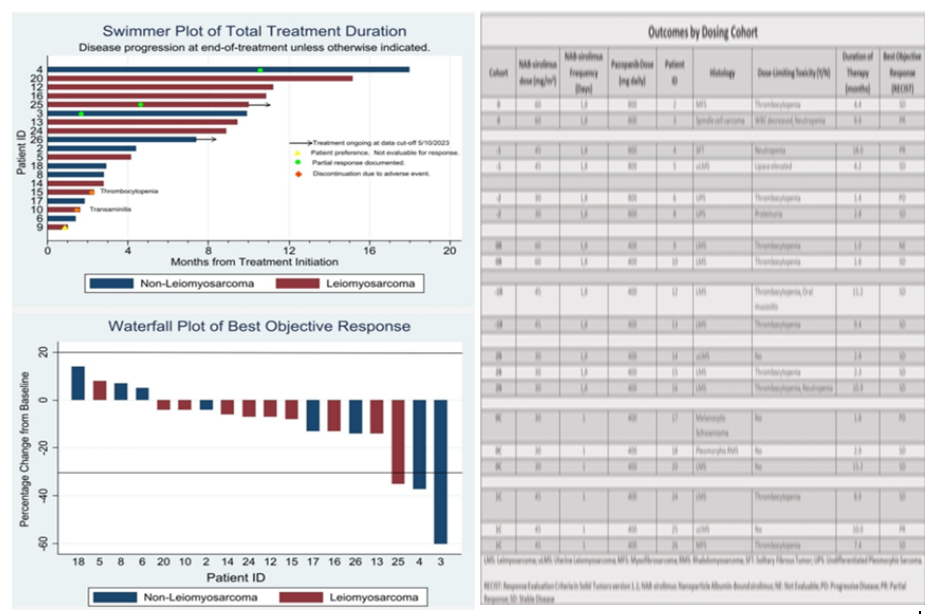
2.10 NAB-S被批准用来治疗患有不可切除性或转移性血管周围上皮样细胞肿瘤的成人。白蛋白结合可以提升西罗莫司的溶解度,并且可能将其靶向肿瘤细胞。mTOR抑制剂可能可以直接或通过克服抵抗力来增强帕唑帕尼的活性。Lee D.Cranmer等人评估了纳米颗粒白蛋白结合西罗莫司联合帕唑帕尼的可行性以及安全性。在研究NAB-S/PAZO组合时,血小板减少是最明显的剂量限制性毒性。19位病人中的3位病人由于不良事件没有继续治疗;剩下的16位病人在调整之后继续了治疗。最大耐受剂量与2期推荐剂量是NAB-S 30mg/m2 day1以及PAZO 400mg days1-21。已经观察到了这种组合具有活性的初步证据。
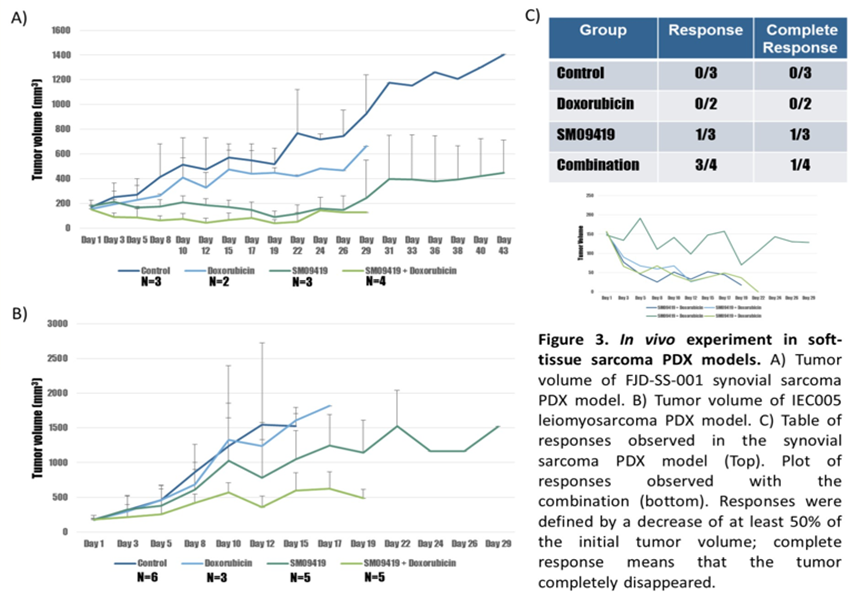
2.11 选择性剪接去调节与癌症的发生、进展与治疗抵抗有所关联。这种去调节可能由于突变或者不平衡的表达或者剪接因子的活性而发生。剪接因子的变化可能会改变数以千计的mRNA前体,增加细胞复杂性以及促进肿瘤发展。CDC样激酶可以磷酸化富含丝氨酸精氨酸的剪接因子,是选择性剪接的关键调节因子。SM09419是一种口服的泛CLK/DYRK抑制剂,已经被表明可以通过多种机制来抑制SRSF磷酸化、选择性修饰剪接体活性以及减慢肿瘤生长,这些机制包括下调Wnt/β连环素的信号。David Silva Moura等人针对选择性剪接调节作为软组织肉瘤的一个新的治疗性靶点进行了相关研究验证了泛CLK/DYRK抑制剂对STS肿瘤细胞系和PDX模型的生长与生存的影响,SM09419与阿霉素的联合在临床前研究提示这些选择性剪接调节剂或许可以治疗STS。
2.12 p53抑癌基因的失活是促进肿瘤存活和增殖的关键机制。p53失活可能是由于TP53突变或关键负调控因子MDM2下调野生型(wt) p53所致。BI 907828是一种高效的MDM2-p53拮抗剂,在临床前研究中展现了抗肿瘤活性,特别是在TP53-wt MDM2扩增的DDLPS模型中。在这项I期研究(NCT03449381)中,BI 907828单药用于晚期实体瘤患者,包括DDLPS。在剂量递增(Ia期)期间,BI 907828具有可控的安全性,推荐扩展剂量(RDE)为45mg/3w。2023年ASCO报道了所有接受此RDE患者(n=140)的安全性数据,以及DDLPS亚组的有效性数据。10/69(14.5%)的DDLPS患者达到PR,47(68.1%)患者达到SD,DCR (PR+SD)为82.6%,初步预期mPFS为7.9月(95%CI 4.2-9.9)。在软组织肉瘤中P53突变和MDM突变的频率是较高的,因此BI 907828值得期待。
2.13 ADC类药物在乳腺癌等其他实体瘤中展现了不俗的实力。B7-H3 ADC药物HS-20093在晚期肿瘤患者中进行I期临床试验,剂量爬坡过程中纳入了数例软组织肉瘤患者,目前有观察到SD的病例,期待进一步研究数据。
(三)其他方面
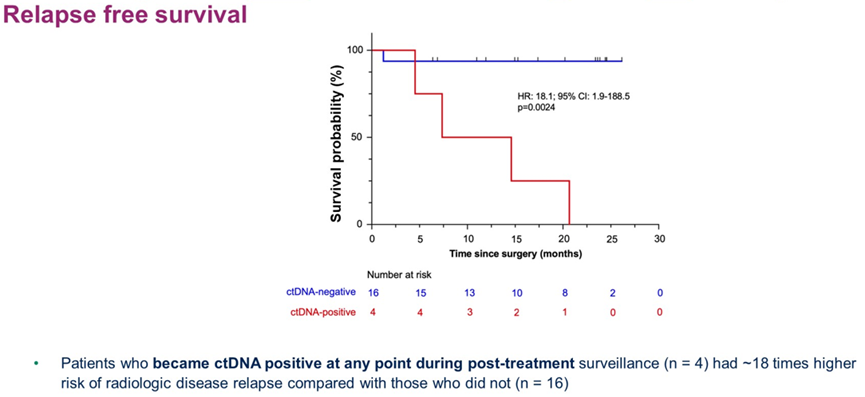
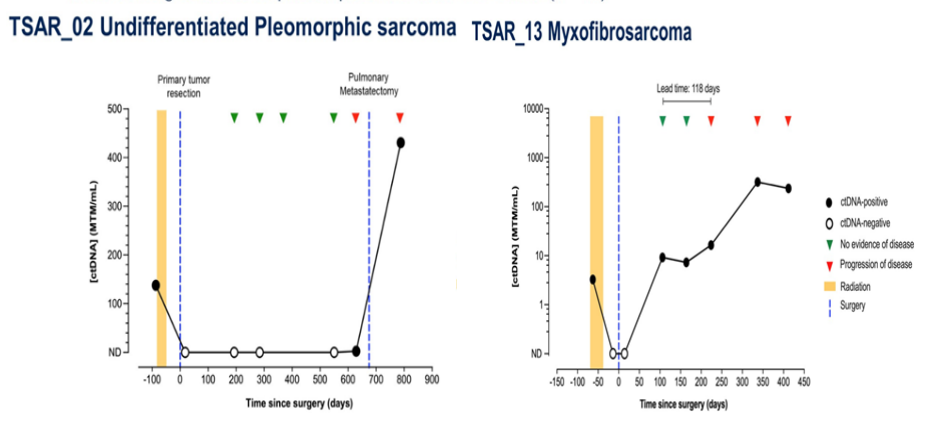
ctDNA :Abdulazeez Salawu等人针对使用定制循环肿瘤DNA(ctDNA)检测局部软组织肉瘤中的分子残留疾病(MRD)进行了研究分析。手术与(新)辅助放疗是局部软组织肉瘤的主要可治愈性治疗方案。但是尽管进行了治疗,依然有高达50%的软组织肉瘤患者经历了转移性复发,并且辅助全身治疗的常规使用存在争议。软组织肉瘤治疗后存在的ctDNA是分子残留疾病的一个潜在生物标志物,它或许可以识别出那些患者可以在辅助全身治疗中获得益处。根据软组织肉瘤的基因组学异质性,在该人群中采用一种ctDNA检测的组织学不可知性方法是可取的。
总结
骨与软组织肉瘤的发病率较较低,较低的发病率导致了人们对肉瘤的忽视,患者往往在早期得不到正确诊断,延误了治疗时机,进而导致肿瘤向晚期进展。骨与软组织肿瘤的发病原因和机制至今尚未被完全阐明,这也给患者的治疗带来一些困难。针对以上两点,在研究肉瘤的发病机制与新治疗策略的同时,做好骨肉瘤的健康科普也是极为重要的一环。通过增强公众对骨肉瘤的认知来提升患者的早期诊断率,做到早发现、早诊断、早治疗,以此来延长患者的生存时间。
在骨与软组织肉瘤治疗领域,外科治疗仍然是主要治疗手段,但其他治疗方式的不断进步也为手术治疗提供了条件与契机。相比于传统放化疗,免疫及靶向治疗在减少患者不良事件的同时提升了治疗效果延长了患者的生存期;新辅助化疗的使用为晚期患者带来新的治疗策略;放疗配合靶向治疗也取得了不错的疗效。但目前趋势倾向与不同作用机制的治疗手段结合,多中心随机对照临床研究对临床治疗策略的制定提供了极大的帮助,ctDNA检测在肿瘤复发方面也提供了不错的预测价值。随着外科治疗、放疗、化疗、免疫及靶向治疗的综合运用以及治疗规范化、标准化、个体化的提升,骨与软组织肉瘤患者的临床治疗效果与生活质量也会随之不断进步。
排版编辑:肿瘤资讯-Amber











 苏公网安备32059002004080号
苏公网安备32059002004080号


