
我国肝细胞癌(以下简称“肝癌”)患者的总体生存较差,重要原因是首诊时中晚期肝癌患者的比例很高。以往肝癌的药物治疗效果有限,而随着近年来靶向治疗、免疫治疗等系统治疗的进步,中晚期肝癌的疗效已显著改善,部分患者可能通过手术切除而获根治[1]。此外,系统治疗与局部治疗的结合,能够进一步提高肿瘤缩小、降期的机会[1]。转化切除只是中晚期肝癌治疗的阶段性目标,实现长期生存才是最终的目标,而肿瘤复发转移是影响肝癌患者术后长期生存的最主要原因[2],因此,以遏制复发为主要目的的术后辅助治疗对肝癌患者而言至关重要。本期由山东省肿瘤医院介入一病区李金鹏医生为大家分享并解读一则病例,该病例为“替雷利珠单抗+仑伐替尼”转化治疗Ⅲa期肝癌患者实现R0切除,且术后辅助治疗使该患者长期获益的真实案例,目前患者无复发生存(RFS)时间已超26个月,患者总生存期(OS)长达37个月。
专家介绍
山东省肿瘤医院
介入一病区主治医师 医学博士
山东省肿瘤医院介入一病区 医学博士
山东省医学会放射学分会介入诊疗学组委员
山东省医师协会介入放射学专业委员会首届委员会委员
中国医药教育协会肿瘤内照射专委会委员
山东省老年医学学会肿瘤多学科诊疗专业委员会委员
山东省抗癌协会神经肿瘤专业委员会青年委员
山东省抗癌协会放射肿瘤学分会青年委员
山东省健康管理协会综合介入专业委员会委员
山东省临床肿瘤学会放射介入治疗专家委员会委员
世界华人肿瘤医师协会微创介入治疗诊疗会青年委员
第一作者发表论文北大核心期刊7篇,SCI 8篇
第一作者被全球肿瘤学大会(ESMO TAT、ASCO、SIR、GEST、ET、ECIO、SIR、CIRSE)收录研究摘要多篇,其中8 篇被选为Oral Presentation.
Scientific Reports、Journal of Hepatocellular Carcinoma等杂志审稿人.
参与和主持多项临床科研课题.
病例详情
01基本情况
患者男性,52岁。
主诉:腹部不适1月余,查体发现肝占位7天。
现病史:患者约1月余前无明显诱因出现腹部不适,当时未在意。因症状持续存在呈加重趋势遂于7天前来院就诊,行腹部强化CT示:肝右后叶肝癌并局部卫星灶形成,门静脉右支癌栓形成,肝硬化,脾大。为求进一步诊治,今来我院,遂以“肝占位”为诊断收入院。
既往史:有“乙型肝炎”病史10年,间断服用抗病毒药物治疗。
个人史:长期抽烟半包/天,偶尔饮酒。
家族史:家族中无肝炎及肿瘤患者。
体格检查:EGOG 0分;黄疸征(-),肝肋下未及,质中,无压痛反跳痛,移动性浊音(-)。
02辅助检查
实验室检查:
肿瘤标志物:甲胎蛋白(AFP):>60500ng/mL;糖类抗原19-9(CA19-9):96.35U/mL;癌胚抗原(CEA):2.12ng/mL。
乙肝相关检查:乙肝表面抗原:6906.0COI;乙肝e抗体:0.09COI;乙肝核心抗体:0.006COI;乙肝病毒DNA定量:6.49x103IU/mL。
血常规检查:各指标未见明显异常。
2020-03-16胸腹盆CT增强扫描检查示:肝右后叶可见不规则低密度肿块影,分叶状,周围可见卫星灶,局部与肿块相连,大小约7.3cmx10.3cm,肝右后静脉略示受压移位,门脉右支主干可见低密度充盈缺损;胸部未见明显异常。
 2020-03-16(基线)胸腹盆CT增强检查影像
2020-03-16(基线)胸腹盆CT增强检查影像
03临床诊断
肝右后叶占位病变伴门脉右支瘤栓(肝功能Child-Pugh A级、ECOG 0分);
乙型病毒性肝炎。
04治疗经过
根据患者影像学检查、肿瘤标志物检查等资料,经多学科会诊(MDT)讨论,认为患者为晚期肝细胞癌(CNCL-Ⅲa期)可能性大。考虑瘤体巨大(约7.3cmx10.3cm)、合并门脉右支癌栓,不宜首选手术,遂采取治疗方案为:在积极抗病毒治疗基础上,先积极转化治疗来获取行根治性手术的机会,然后给予术后辅助治疗来长期遏制复发。
1、转化治疗
2020-03-17给予首次载药微球肝动脉化疗栓塞术(D-TACE):DSA示肝右后叶肿瘤染色。腹腔动脉、肝右动脉灌注洛铂50mg。微导管超选至肿瘤供血动脉,缓推300~500μm载药栓塞微球1瓶(载表柔比星50mg),碘化油6ml栓塞。栓塞后造影肿瘤染色消失。
 首次(2020-03-17)D-TACE术中情况
首次(2020-03-17)D-TACE术中情况
同时启动靶向药物治疗,具体用药为:仑伐替尼,8mg PO qd。
首次D-TACE术后1月(2020-04-17)实验室检查结果:
肿瘤标志物:AFP:>60500ng/mL;CA19-9:159.07U/mL;CEA:2.12ng/mL。
乙肝病毒DNA定量:25IU/mL。
首次D-TACE术后1月(2020-04-17)影像学(CT)检查结果:肝右后叶可见不规则低密度肿块影(7.3cm×10.5cm),分叶状,周围可见卫星灶,呈不均匀强化,内见多发片状液性密度区,门静脉右支主干可见低密度充缺;内示多发片状液性低密度区,mRECIST疗效评价:病情稳定(SD)。

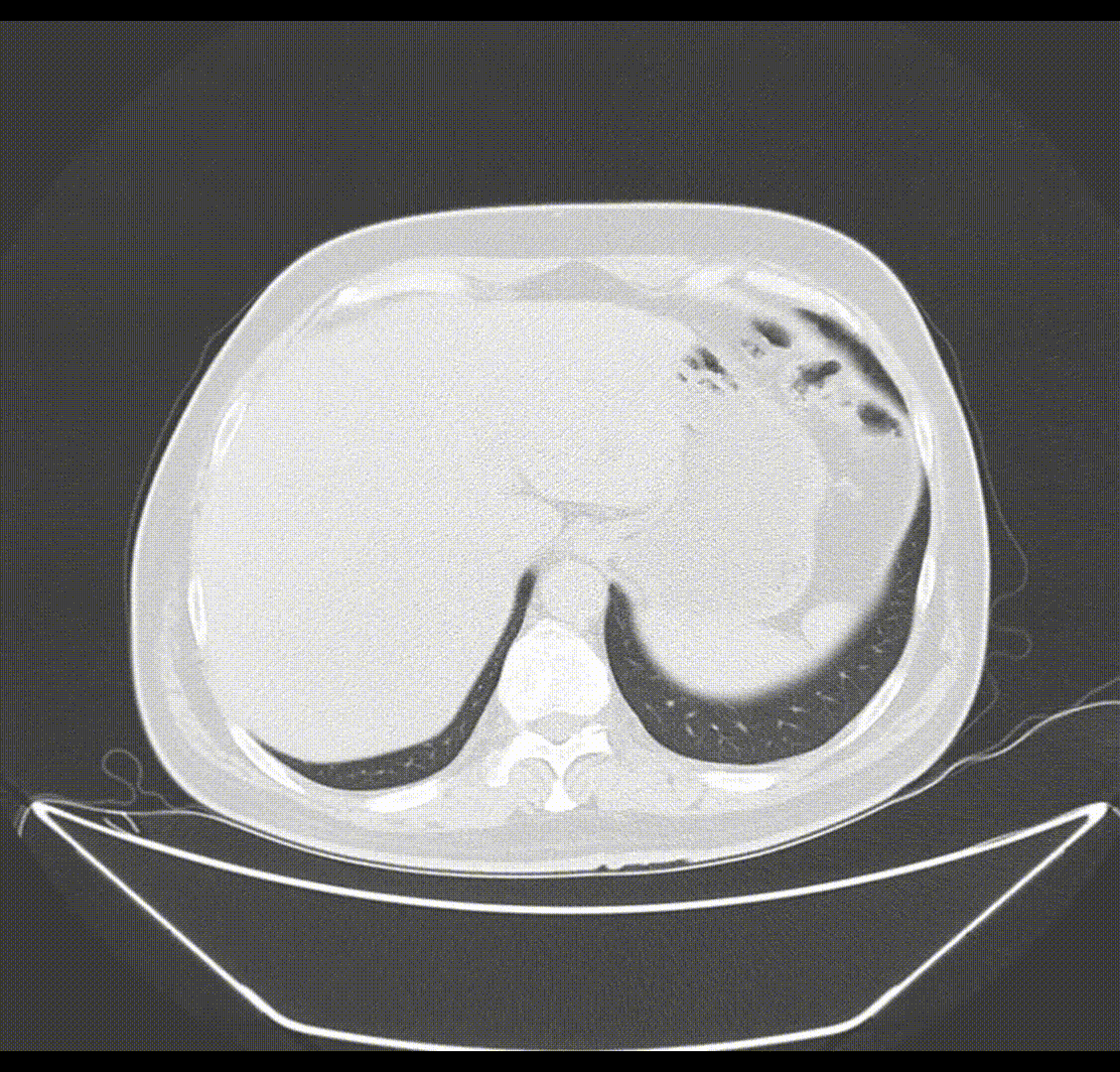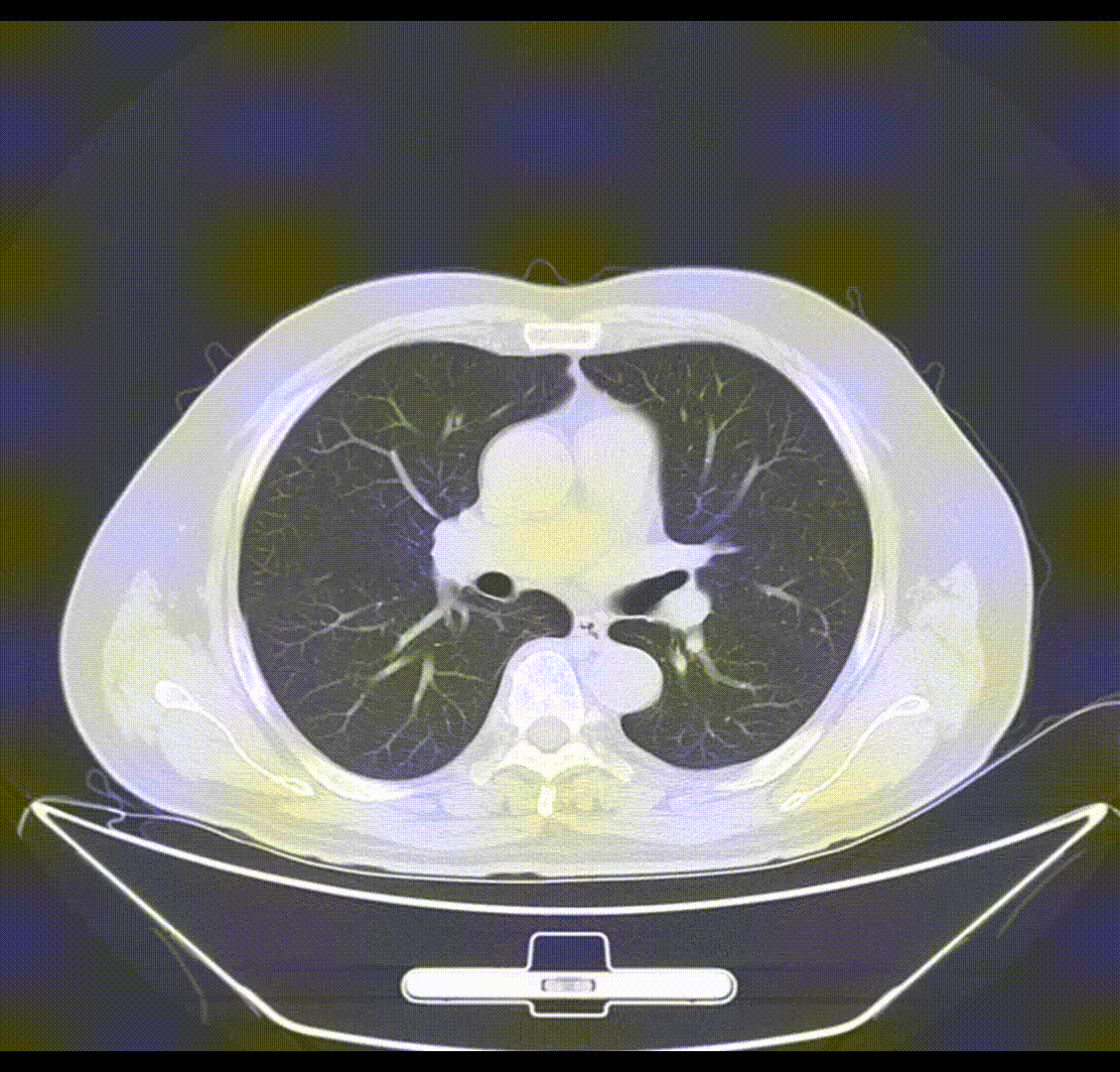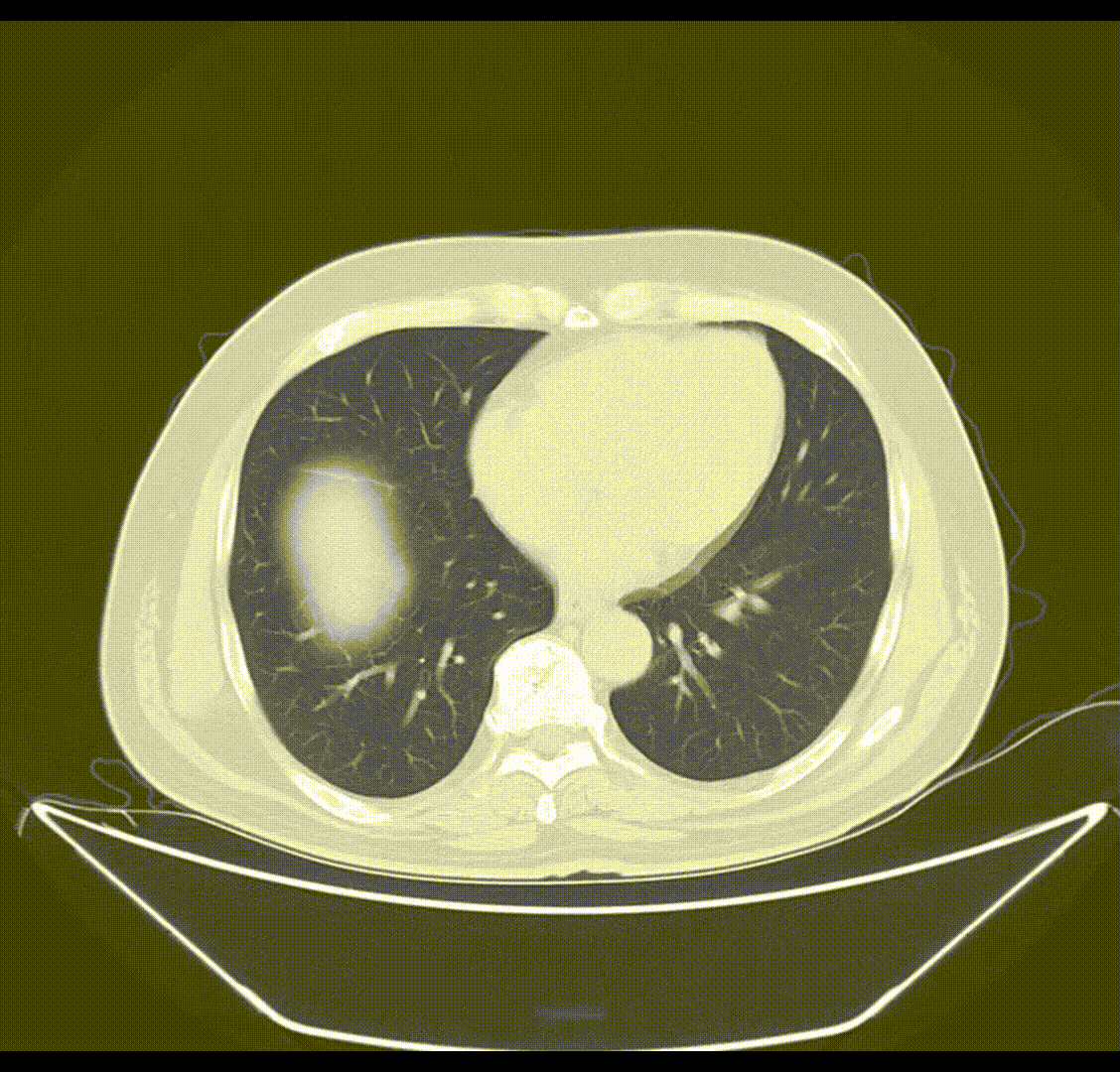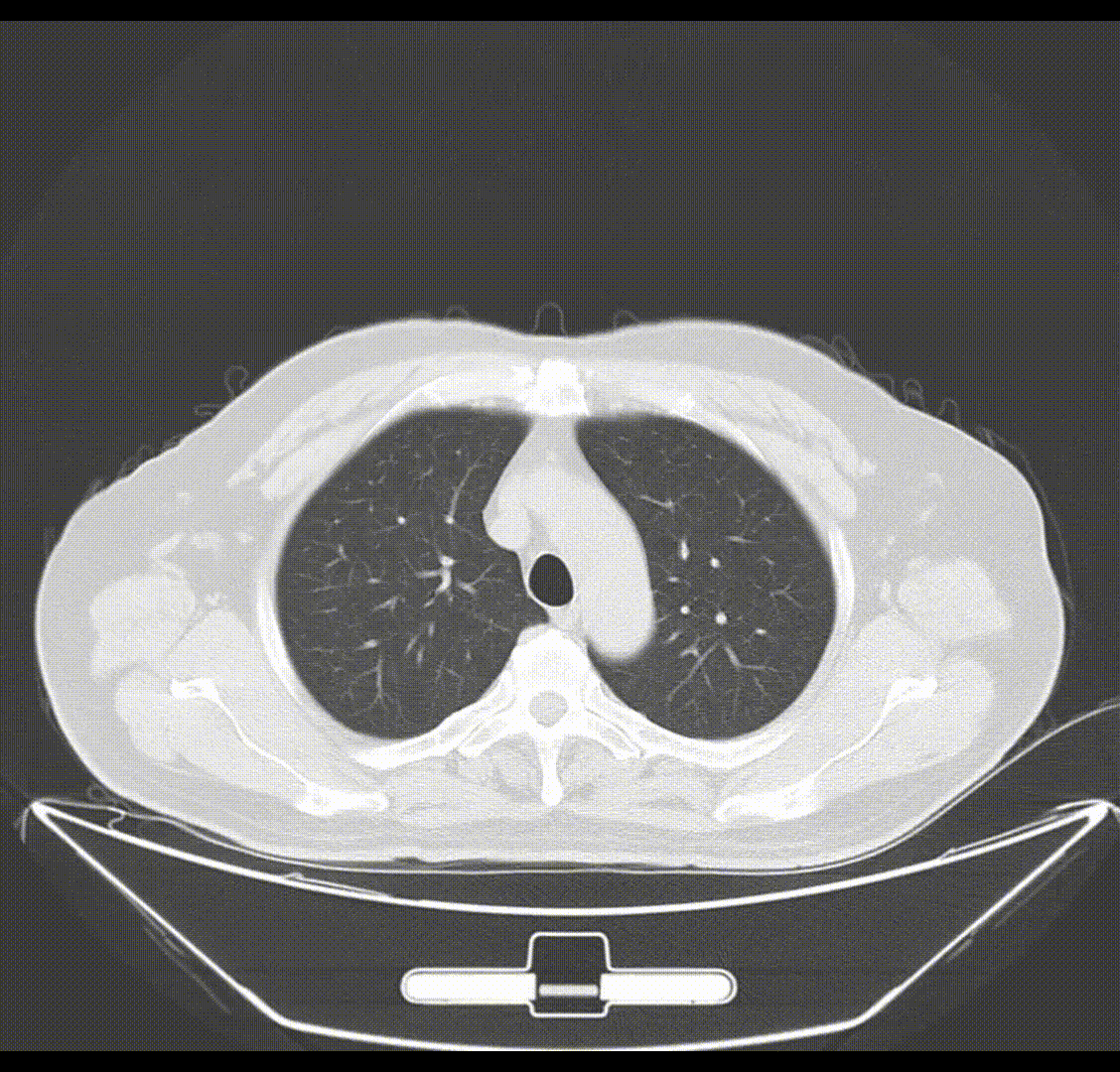 2020-04-17(首次D-TACE术后1月)腹部CT增强检查影像
2020-04-17(首次D-TACE术后1月)腹部CT增强检查影像
经治疗,患者疗效评估为SD,拟继续在抗病毒治疗基础上,给予D-TACE+仑伐替尼靶向药物治疗,并加用免疫治疗药物来加强转化治疗效果,具体用药为:替雷利珠单抗 200mg IV q3w。
第2次D-TACE术后50天(2020-06-07)实验室检查结果:
肿瘤标志物:AFP:34263ng/mL;CA19-9:91.09U/mL;CEA:3.12ng/mL。
第2次TACE术后50天(2020-06-07)影像学(CT)检查结果:肝右后叶可见不规则低密度肿块影(4.3cm×8.5cm),分叶状,呈不均匀强化,内见低密度坏死区及高密度碘油沉积影,门静脉右支可见低密度充缺,mRECIST疗效评价:部分缓解(PR)。
2020-06-07(第2次TACE术后50天)腹部CT增强检查影像
考虑目前患者瘤灶较前明显缩小(从7.3cmx10.3cm缩小到4.3cm×8.5cm),疗效评价为PR;尽管加用替雷利珠单抗治疗3个周期后,出现了甲状腺功能减退的副反应,但症状轻微(I级),且在给予小剂量优甲乐口服后缓解,整体安全性可控。综上,经MDT讨论,决定继续采取“仑伐替尼+替雷利珠单抗”这一靶免治疗方案。
2020-07-08实验室检查结果:
肿瘤标志物:AFP:85.62ng/mL;CA19-9:37.09U/mL;CEA:2.19ng/mL。
与此前相比,AFP呈断崖式下降,遂继续目前靶免方案治疗,分别于2020-10-28、2021-02-18、2021-04-10复查腹部影像学检查,结果示肿瘤完全坏死,mRECIST 影像学评价为持续完全缓解(CR)。
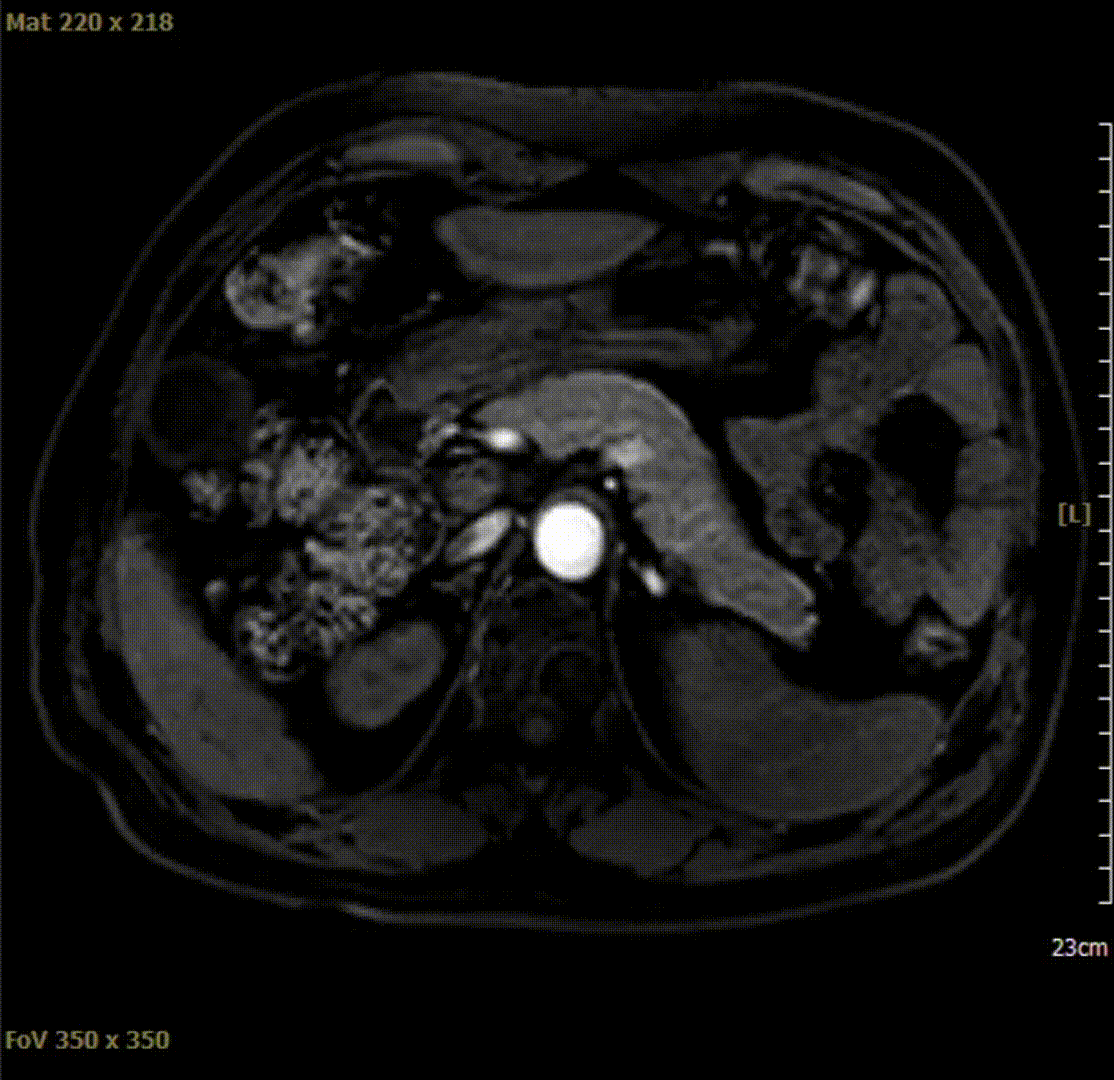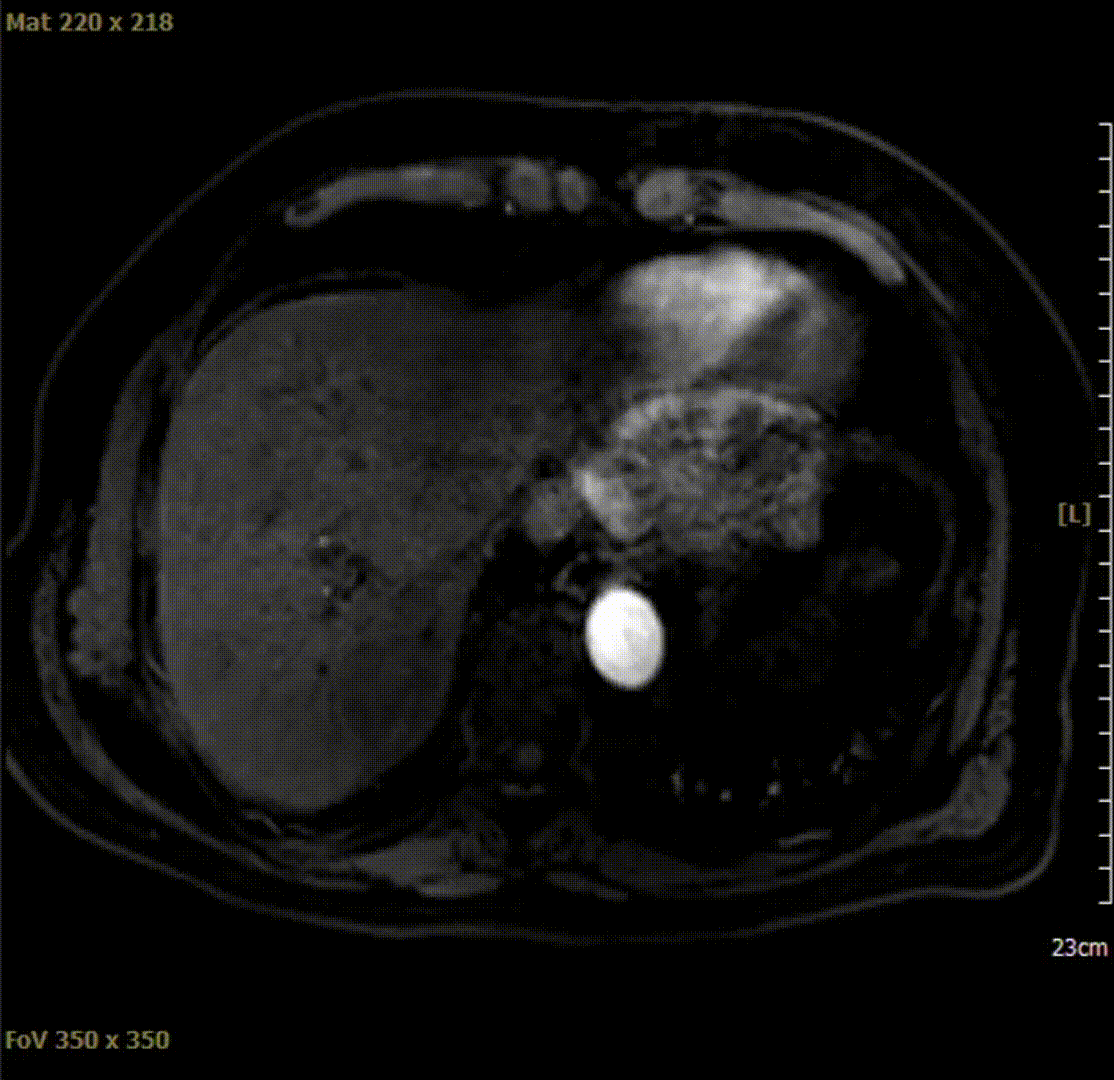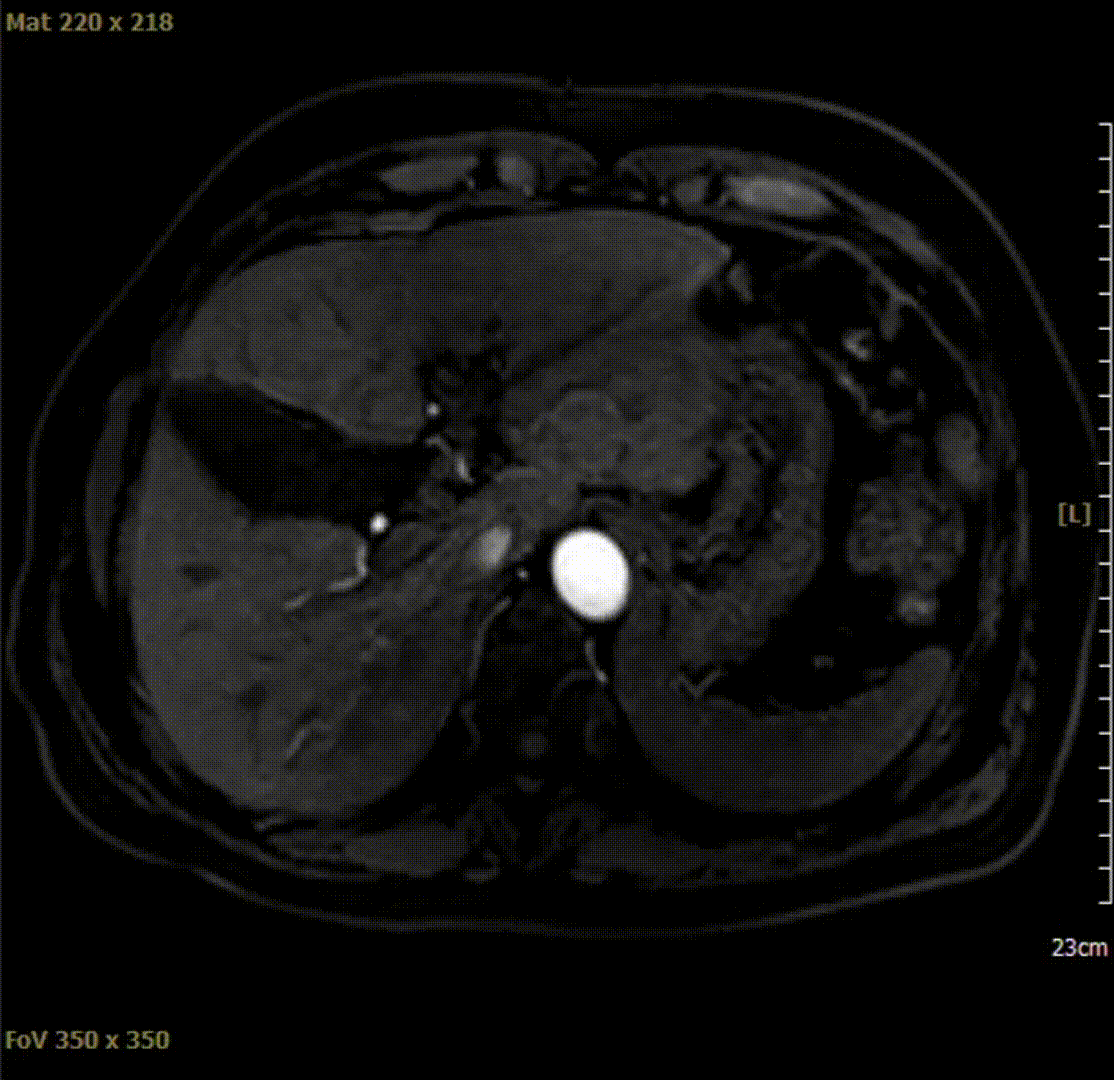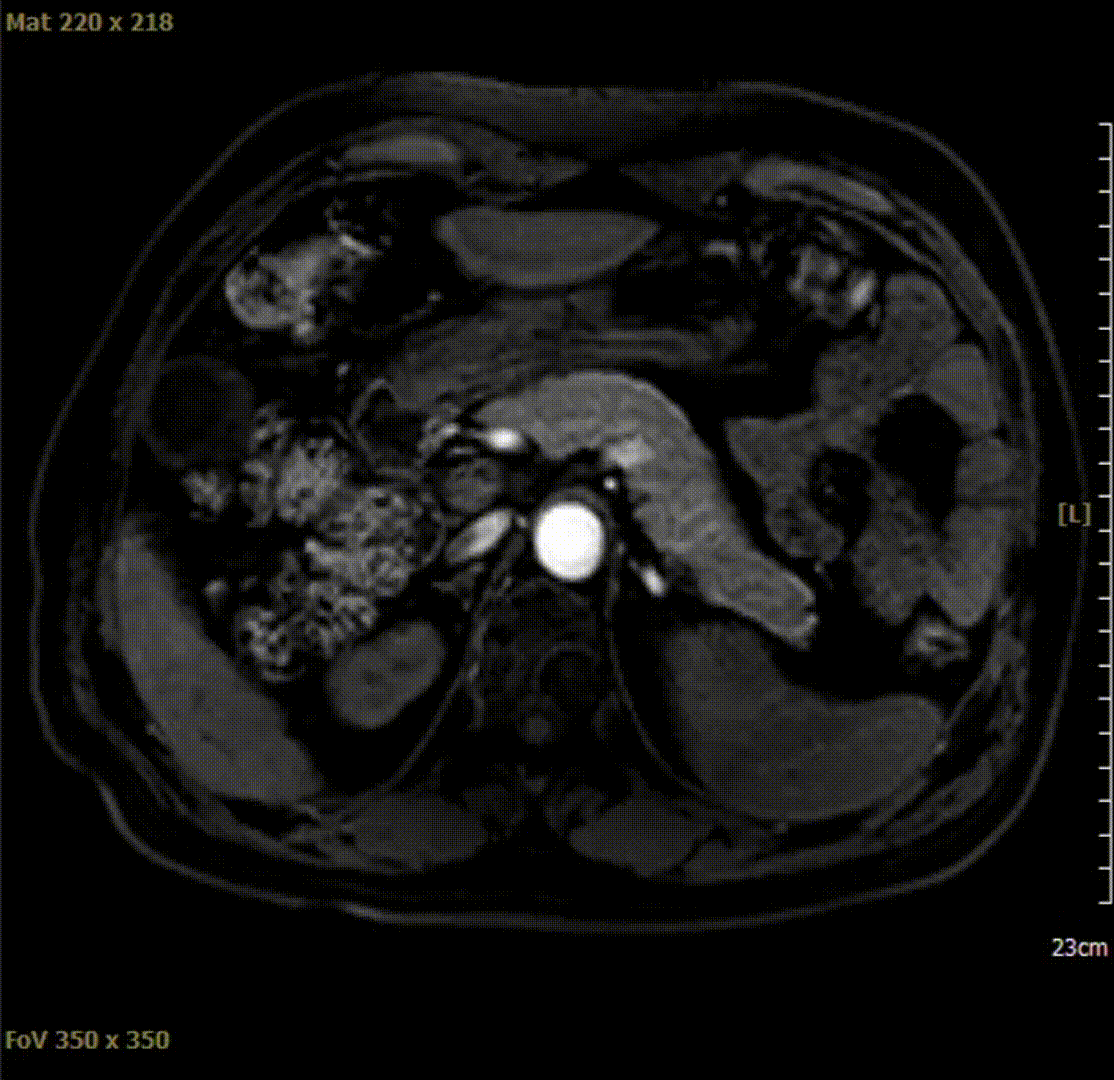
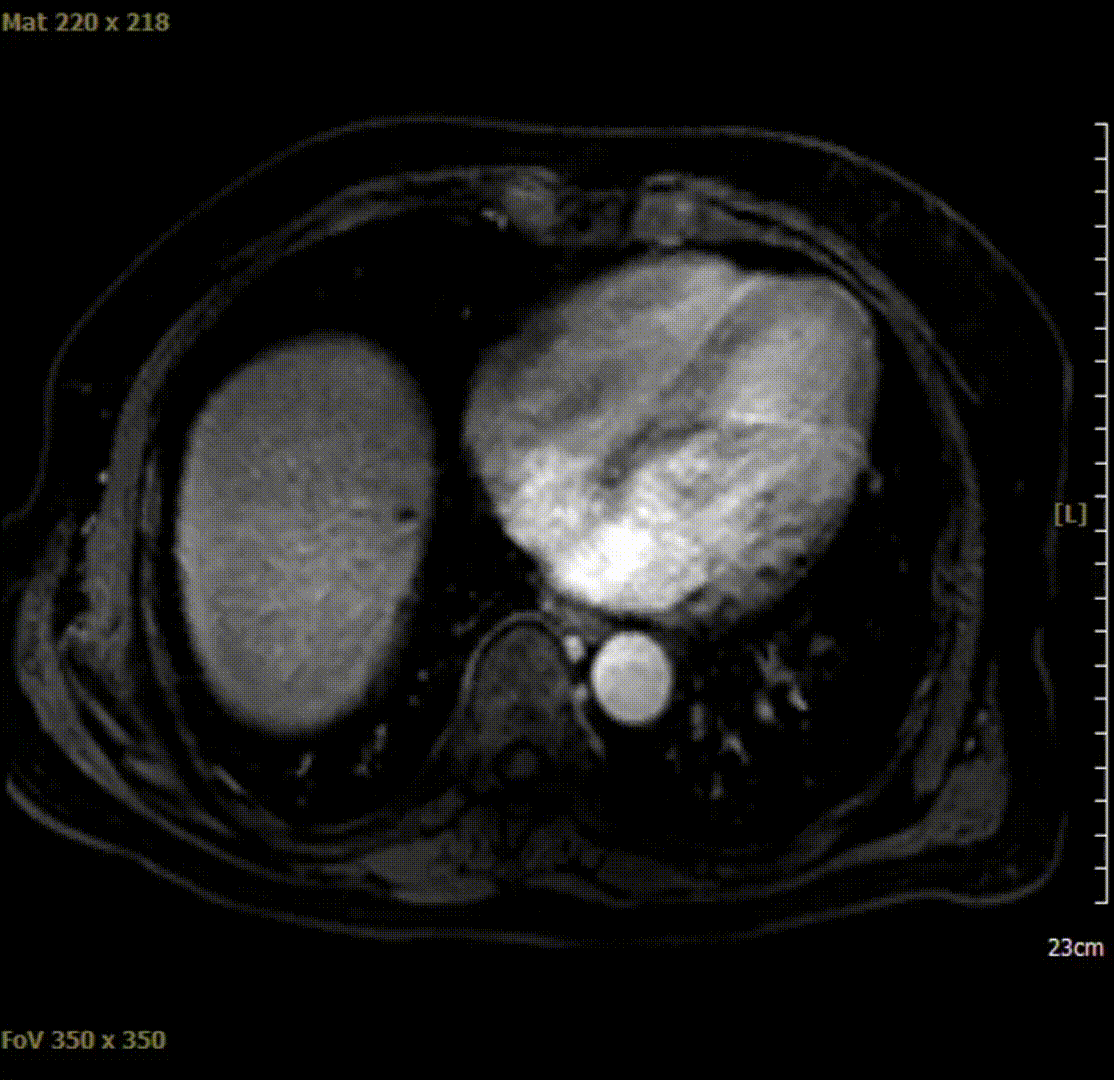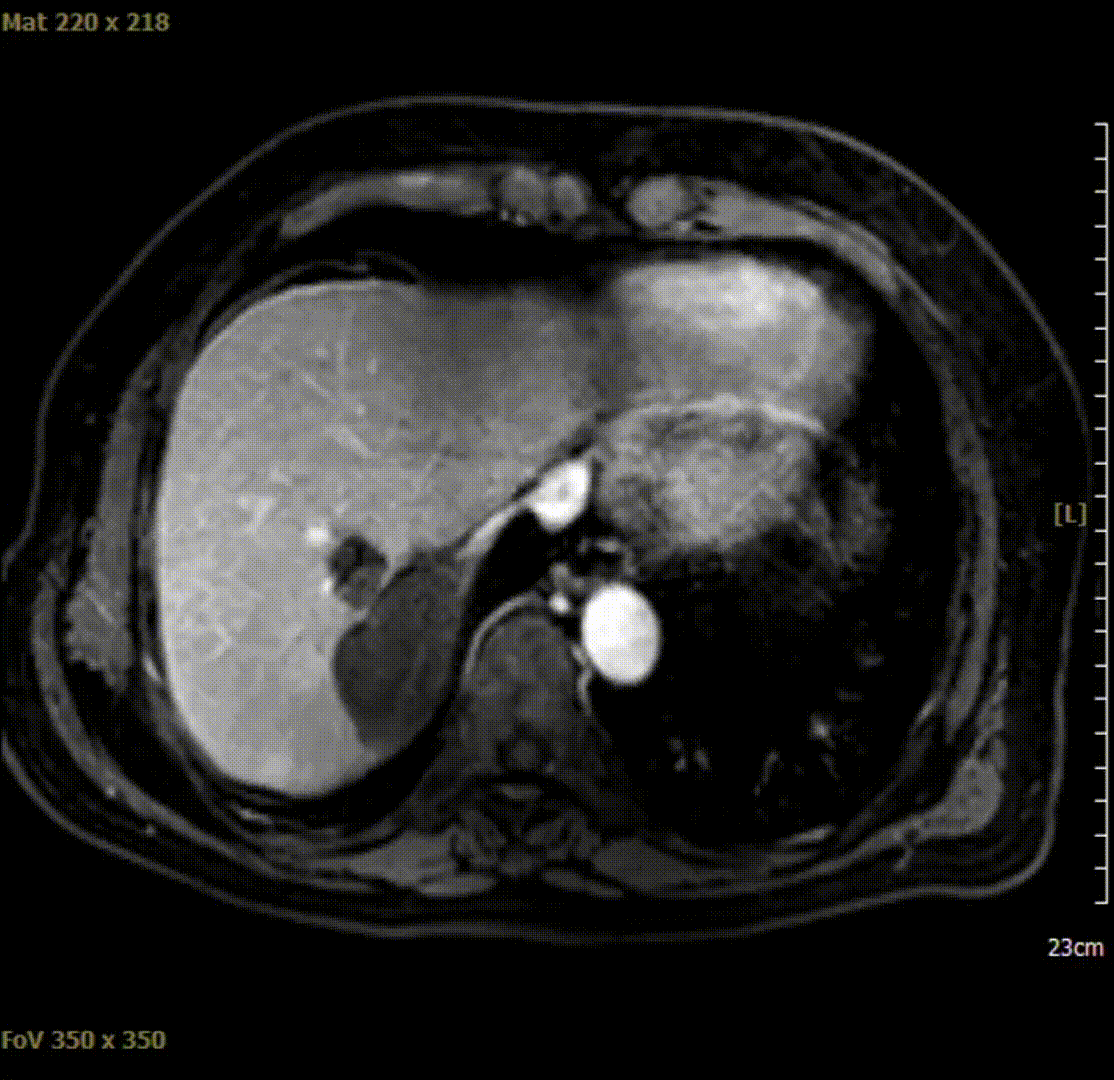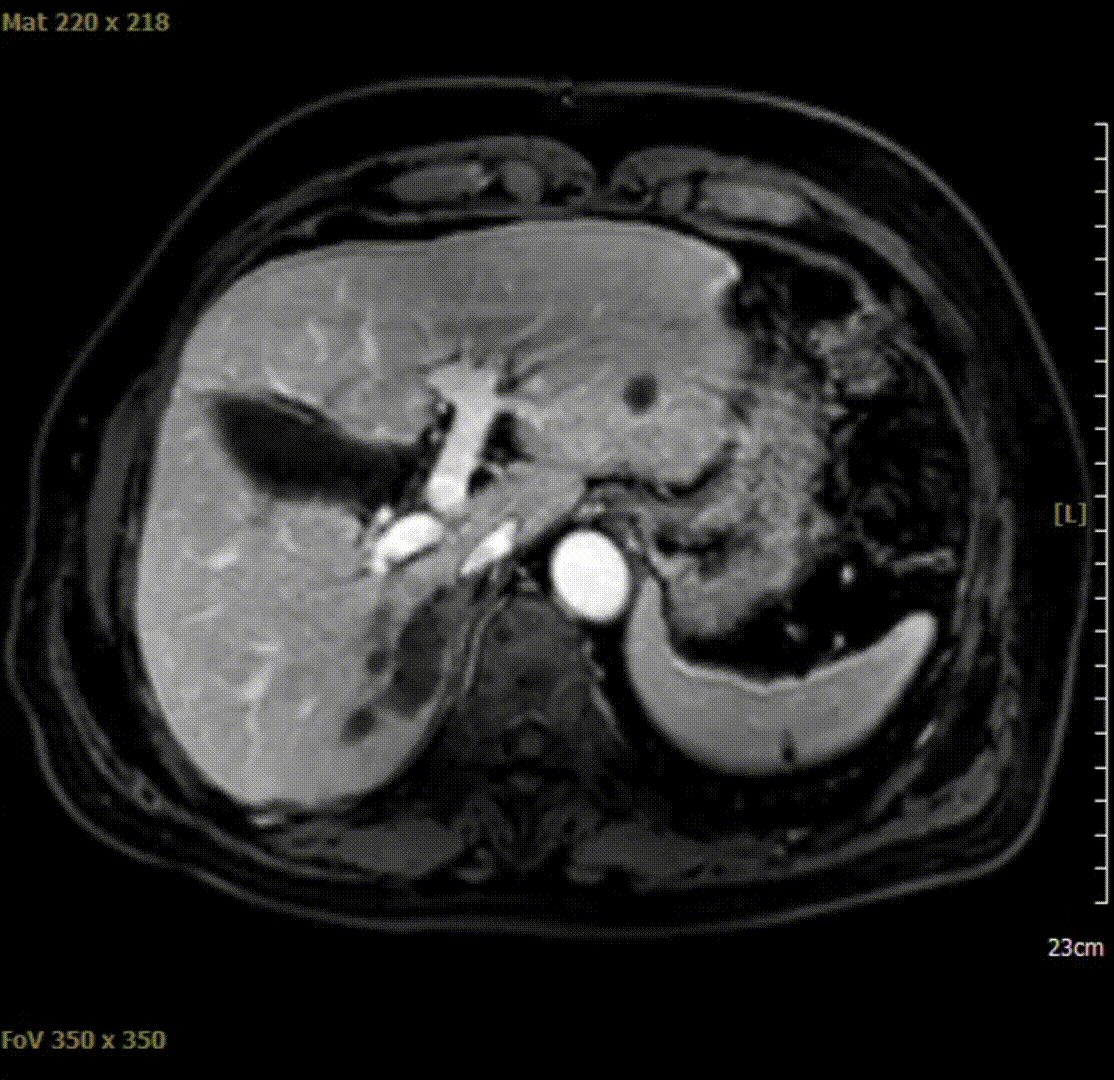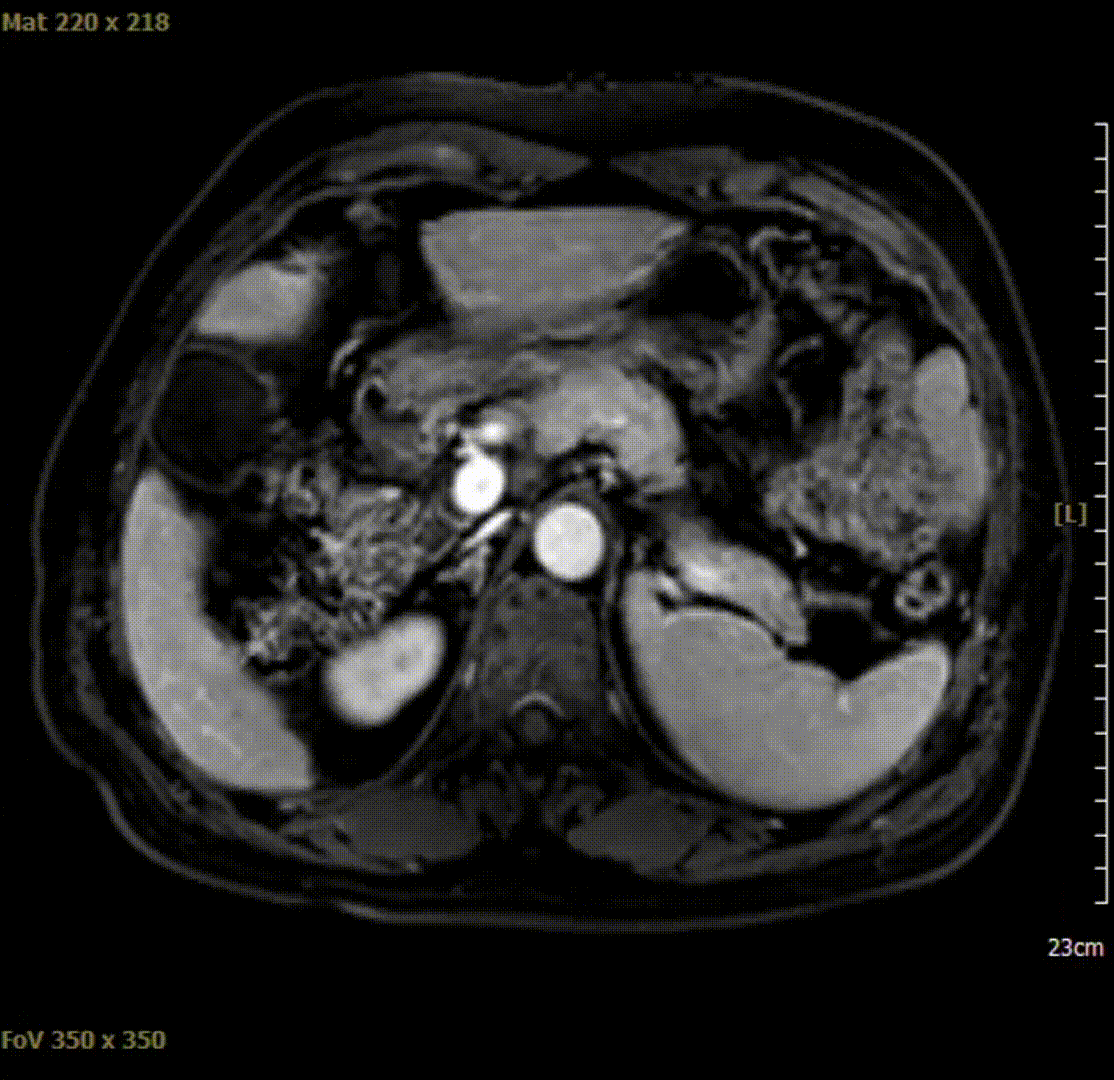 2021-04-10腹部MRI检查影像
2021-04-10腹部MRI检查影像
转化治疗期间肿瘤标志物AFP的变化趋势:
 在靶免治疗启动后,患者AFP由高水平骤然下降,然后一直维持在极低水平
在靶免治疗启动后,患者AFP由高水平骤然下降,然后一直维持在极低水平
2、手术及术后辅助治疗和随访
考虑患者近期为持续完全缓解(CR)状态,且评估ICGR15:2.3%、FLR:50%,满足采取根治性手术治疗的要求。遂于2021-04-15行“右半肝切除+右尾叶切除+胆囊切除术”。
 2021-04-15术中情况
2021-04-15术中情况
手术标本及病理结果(2021-04-19)示:术中可见大部分呈坏死状态,无病灶残存活;瘤组织全部为坏死组织,周围伴大量纤维组织增生,炎细胞浸润,组织细胞及多核巨细胞反应。表明达到了R0切除、病理学pCR。
 2021-04-19手术标本及病理结果
2021-04-19手术标本及病理结果
后续分别于2021-05-20、2021-08-18、2023-04-25复查影像学检查,结果均未见复发迹象。
 2023-04-25腹部MRI检查影像
2023-04-25腹部MRI检查影像
最近一次(2023-04-25)实验室检查结果亦未见复发迹象:
肿瘤标志物:甲胎蛋白:1.03ng/mL;糖类抗原CA19-9:24U/mL;癌胚抗原:2.12ng/mL。
疾病历程:

疗效评估:经转化治疗患者实现了R0切除、病理学pCR;术后辅助治疗使患者进一步获益,迄今其 RFS 已超26个月,患者OS长达37个月。
不良反应:除了轻度(I级)甲减(给予小剂量优甲乐口服后缓解)外,在整个治疗期间,患者未出现其它明显的药物相关不良反应。
讲堂点金
原发性肝癌是目前我国第 4 位常见恶性肿瘤及第 2 位肿瘤致死病因,其中肝细胞癌(hepatocellular carcinoma, HCC)占比高达75%~85%[3]。由于起病隐匿、进展迅速、侵袭性高,我国大多数HCC患者首诊时已处于中晚期[1],失去了根治性手术治疗的机会,故整体生存较差。而转化治疗有望帮助这些中晚期HCC患者重获根治性手术切除的机会,并赢得与早期HCC手术治疗相当的生存获益[1]。目前认为,在转化治疗方案中,系统治疗(比如靶向治疗、免疫治疗)与局部治疗(比如TACE)相结合的方式更有利于减瘤降期、提升转化成功率,这种多模式的综合治疗策略已成为中晚期HCC获得长期生存的主要途径[1]。本例HCC患者首诊时就已处于CNLC Ⅲa期,其瘤体巨大(约7.3cmx10.3cm),且合并门脉右支癌栓。经慎重MDT讨论,决定先行转化治疗,待减瘤降期后寻求实施根治性手术的机会。
然而,转化切除只是中晚期HCC治疗的阶段性目标,实现长期生存才是最终的目标,而肿瘤复发转移被认为是影响HCC患者术后长期生存的最主要原因[2]。有数据显示,HCC的术后5年复发率>70%[4],故以遏制复发为主要目的的术后辅助治疗对HCC患者而言至关重要。尤其是对于合并高危复发因素的HCC患者(比如本例中的合并门脉右支癌栓),相关指南、共识的一致推荐积极采取术后辅助治疗[2-5]。《肝癌术后辅助治疗中国专家共识(2023版)》指出,靶向药物、免疫检查点抑制剂单药或联合应用,有望改善合并高危复发因素HCC患者的预后[2]。由于PD-1免疫检查点抑制剂替雷利珠单抗近年来在HCC的治疗中屡创佳绩,其已经成为HCC患者免疫治疗的优选药物。
以采用替雷利珠单抗单药治疗不可切除HCC的RATIONALE 301研究为例,其结果表明:替雷利珠单抗治疗组患者的中位总生存期(mOS)为15.9个月,客观缓解率(ORR)为14.3%,其中完全缓解(CR)率为2.9%,是索拉非尼组(0.3%)的10倍;替雷利珠单抗组持续缓解时间(DoR)高达36.1个月,是索拉非尼组(11.0个月)的3倍之多;不仅如此,替雷利珠单抗≥3级的治疗相关不良事件(TRAEs)发生率约22.2%,明显低于索拉非尼相的53.4%[6];这些数据有力证明了替雷利珠单抗在不可切除HCC治疗中的强力减瘤和持久抗癌能力,以及可控的安全性。至于替雷利珠单抗联合靶向药物治疗不可切除HCC的价值,从BGB-A317-211研究中便可窥见:替雷利珠单抗联合靶向药物治疗下,不可切除HCC患者的ORR约38.7%,疾病控制率高达90.3%,中位无进展生存期(mPFS)达9.6个月;且两药联合≥3级TRAEs发生率仅为28.1%[7]。这些数据再一次证实了替雷利珠单抗治疗中晚期HCC患者不仅疗效非凡,而且安全性良好,是值得信赖的能够长期使用的免疫治疗药物。
基于以上证据和相关指南、共识推荐,我们选择了“替雷利珠单抗+仑伐替尼”作为靶免治疗方案的药物,在联合应用2次TACE后成功转化治疗患者实现了R0切除、病理学pCR;术后辅助治疗方案为继续采用“替雷利珠单抗+仑伐替尼”的靶免治疗方案,目前患者RFS 已超过26个月,患者OS更是达到了37个月之久。值得一提的是,除了轻度(I级)甲减(给予小剂量优甲乐口服后缓解)外,在整个治疗期间,患者未出现其它明显的药物毒副作用,整体安全性可控。期待后续见证该患者更远期的生存获益,同时也希望替雷利珠单抗联合靶向药物的方案能帮助我国更多中晚期HCC患者实现更长期的生存。
[1]中国抗癌协会肝癌专业委员会转化治疗协作组, 樊嘉. 肝癌转化治疗中国专家共识(2021版)[J]. 中华消化外科杂志, 2021, 20(6):600-616.
[2]肝癌术后辅助治疗中国专家共识协作组, 中国医师协会外科医师分会, 中国抗癌协会肝癌专业委员会, 等. 肝癌术后辅助治疗中国专家共识(2023版)[J]. 中华消化外科杂志, 2023, 22(4):437-448.
[3]中华人民共和国国家卫生健康委员会医政医管局. 原发性肝癌诊疗指南(2022年版)[J]. 中华肝脏病杂志, 2022, 30(4):367-388.
[4]国家科技部传染病防治重大专项课题《病毒性肝炎相关肝癌外科综合治疗的个体化和新策略研究》专家组, 陈孝平, 沈锋,等. 肝细胞癌肝切除术后复发预防和治疗中国专家共识(2020版)[J]. 中国实用外科杂志, 2021,41(1):20-30.
[5]海峡两岸医药卫生交流协会肿瘤防治专家委员会, 吴健雄, 许建萍,等. 肝癌肝切除围手术期管理中国专家共识(2021年版)[J]. 中华肿瘤杂志, 2021, 43(4):414-430.
[6]Masatoshi Kudo, et al. Final analysis of RATIONALE-301: Randomized, phase III study of tislelizumab versus sorafenib as fifirst-line treatment for unresectable hepatocellular carcinoma. 2022 ESMO.LBA36.
[7]Minshan Chen, et al. Efficacy and safety of tislelizumab (TIS) plus lenvatinib (LEN) as first-line treatment in patients (pts) with unresectable hepatocellular carcinoma (uHCC): a single-arm, multicenter, phase II trial. 2022 ESMO IO Abstract 165P.
排版编辑:肿瘤资讯- Olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


